6.2 金属的化学性质(第一课时)-2022-2023学年九年级化学下册精品课件(21页)(科粤版2012)
文档属性
| 名称 | 6.2 金属的化学性质(第一课时)-2022-2023学年九年级化学下册精品课件(21页)(科粤版2012) |

|
|
| 格式 | pptx | ||
| 文件大小 | 280.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-24 00:00:00 | ||
图片预览








文档简介
第一课时
6.2 金属的化学性质
第六章 金属
科粤版九年级下册
01 金属与氧气的反应
02 金属与酸的反应
03 置换反应
CONTENTS
目 录
课堂导入
人类文明背后的推手—金属材料(市微课二等奖)
一、金属与氧气的反应
【知识回顾】哪些金属可以与氧气发生反应?
2Mg + O2 2MgO
2Mg + O2 2MgO
镁在常温下可与氧气反应
一、金属与氧气的反应
4Al + 3O2 2Al2O3
4Al + 3O2 2Al2O3
注意
铝在空气中与氧气反应,其表面生成一层致密的氧化膜
具有很好的抗腐蚀性
白色
一、金属与氧气的反应
1、铝在常温下能与氧气反应,那么我们用的铝制餐具是怎么回事呢?为什么却很耐腐蚀?
金属在常温下发生缓慢氧化:4Al+3O2=2Al2O3 , 形成一层致密的氧化膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性
2、为何不宜用钢丝球来擦洗铝制餐具吗?
若用钢刷擦洗铝制品,容易把氧化膜除掉,从而起不到保护作用
一、金属与氧气的反应
3Fe + 2O2 Fe3O4 纯氧
2Cu + O2 2CuO
红色固体变为黑色
一、金属与氧气的反应
注意
“真金不怕火炼”说明金即使在高温时也不与氧气反应
镁、铝比较活泼,铁、铜次之,金最不活泼
Mg、Al、Fe、Cu、Au
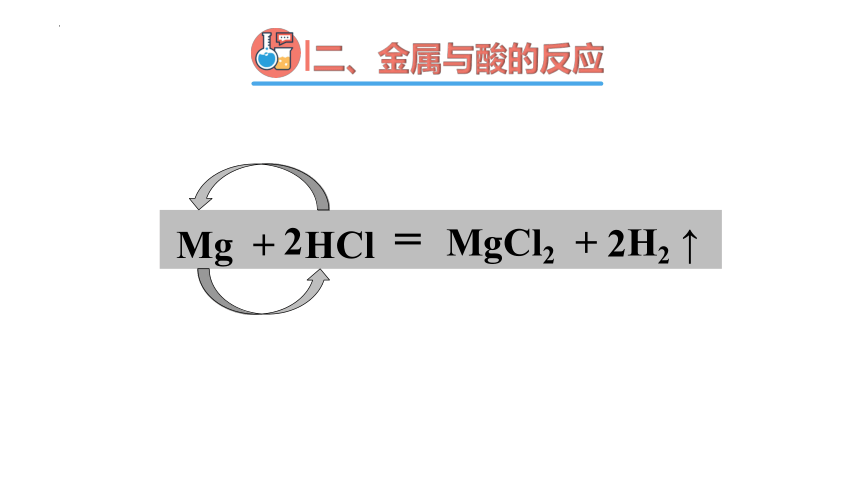
二、金属与酸的反应
Mg + HCl
= MgCl2 + H2 ↑
2
2
二、金属与酸的反应
二、金属与酸的反应
镁、锌、铁都能与稀盐酸反应,放出氢气,而铜不反应
反应越剧烈,说明金属越活泼
二、金属与酸的反应
铁、镁、锌能和稀盐酸或稀硫酸反应时剧烈程度不同。______反应最剧烈,其次是 ______,然后是______
镁
锌
铁
由此推出 ,金属活动性顺序____________
Mg> Zn>Fe>Cu
二、金属与酸的反应
{5940675A-B579-460E-94D1-54222C63F5DA}金属
现 象
稀盐酸
稀硫酸
镁
锌
铁
铜
剧烈反应,产生大量气泡
反应较剧烈,产生大量气泡
反应缓慢,产生少量气泡,溶液的颜色由无色变为浅绿色
无明显现象
二、金属与酸的反应
金属
反应的化学方程式
稀盐酸
稀硫酸
镁
锌
铁
铜
Mg + 2HCl = MgCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
二、金属与酸的反应
已知:铝的活动性比锌强,也可以与盐酸和稀硫酸反应,试写出方程式
2Al + 6HCl = 2AlCl3 + 3H2↑
Al + 3H2SO4 = 2Al2(SO4)3 + 3H2↑
未经打磨的铝条与盐酸和稀硫酸反应,产生气泡的速度非常缓慢,你知道是什么原因吗?
未打磨的铝条表面有致密的氧化膜,等氧化膜被除去之后金属铝才会和盐酸反应产生气泡
二、金属与酸的反应
假黄金的主要成分是黄铜(即铜锌合金),现在你知道为什么可用稀盐酸浸泡的方法来鉴别真伪了吧?
假黄金中含有锌,它会与盐酸发生反应,放出气体
三、置换反应
金属与盐酸反应
金属与稀硫酸反应
Mg + 2HCl = MgCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
观察这些反应,它们有什么共同点?
三、置换反应
置换反应:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应
单质换单质
特点
A+BC=B+AC
表达式
镁、锌、铁都能与稀盐酸或稀硫酸发生置换反应,置换出酸中的氢
化合反应
分解反应
特点:多变一
特点:一变多
四、课堂练习
1、下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )
A、金属的活动性 B、金属的导电性
C、金属的延展性 D、地壳中金属元素的含量
A
四、课堂练习
2、下列物质中,不能用金属和稀硫酸直接反应制得的是( )
A、硫酸镁 B、硫酸锌 C、硫酸铝 D、硫酸铜
D
3、下列反应中,不属于置换反应的是( )
A、Mg+2HCl = MgCl2+H2↑
B、CO+CuO = Cu+CO2
C、C+2CuO = 2Cu+CO2↑
D、Cu+2AgNO3 = 2Ag+Cu(NO3)2
B
第一课时
6.2 金属的化学性质
第六章 金属
科粤版九年级下册
6.2 金属的化学性质
第六章 金属
科粤版九年级下册
01 金属与氧气的反应
02 金属与酸的反应
03 置换反应
CONTENTS
目 录
课堂导入
人类文明背后的推手—金属材料(市微课二等奖)
一、金属与氧气的反应
【知识回顾】哪些金属可以与氧气发生反应?
2Mg + O2 2MgO
2Mg + O2 2MgO
镁在常温下可与氧气反应
一、金属与氧气的反应
4Al + 3O2 2Al2O3
4Al + 3O2 2Al2O3
注意
铝在空气中与氧气反应,其表面生成一层致密的氧化膜
具有很好的抗腐蚀性
白色
一、金属与氧气的反应
1、铝在常温下能与氧气反应,那么我们用的铝制餐具是怎么回事呢?为什么却很耐腐蚀?
金属在常温下发生缓慢氧化:4Al+3O2=2Al2O3 , 形成一层致密的氧化膜,从而阻止铝的进一步氧化,因而铝具有较好的抗腐蚀性
2、为何不宜用钢丝球来擦洗铝制餐具吗?
若用钢刷擦洗铝制品,容易把氧化膜除掉,从而起不到保护作用
一、金属与氧气的反应
3Fe + 2O2 Fe3O4 纯氧
2Cu + O2 2CuO
红色固体变为黑色
一、金属与氧气的反应
注意
“真金不怕火炼”说明金即使在高温时也不与氧气反应
镁、铝比较活泼,铁、铜次之,金最不活泼
Mg、Al、Fe、Cu、Au
二、金属与酸的反应
Mg + HCl
= MgCl2 + H2 ↑
2
2
二、金属与酸的反应
二、金属与酸的反应
镁、锌、铁都能与稀盐酸反应,放出氢气,而铜不反应
反应越剧烈,说明金属越活泼
二、金属与酸的反应
铁、镁、锌能和稀盐酸或稀硫酸反应时剧烈程度不同。______反应最剧烈,其次是 ______,然后是______
镁
锌
铁
由此推出 ,金属活动性顺序____________
Mg> Zn>Fe>Cu
二、金属与酸的反应
{5940675A-B579-460E-94D1-54222C63F5DA}金属
现 象
稀盐酸
稀硫酸
镁
锌
铁
铜
剧烈反应,产生大量气泡
反应较剧烈,产生大量气泡
反应缓慢,产生少量气泡,溶液的颜色由无色变为浅绿色
无明显现象
二、金属与酸的反应
金属
反应的化学方程式
稀盐酸
稀硫酸
镁
锌
铁
铜
Mg + 2HCl = MgCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
二、金属与酸的反应
已知:铝的活动性比锌强,也可以与盐酸和稀硫酸反应,试写出方程式
2Al + 6HCl = 2AlCl3 + 3H2↑
Al + 3H2SO4 = 2Al2(SO4)3 + 3H2↑
未经打磨的铝条与盐酸和稀硫酸反应,产生气泡的速度非常缓慢,你知道是什么原因吗?
未打磨的铝条表面有致密的氧化膜,等氧化膜被除去之后金属铝才会和盐酸反应产生气泡
二、金属与酸的反应
假黄金的主要成分是黄铜(即铜锌合金),现在你知道为什么可用稀盐酸浸泡的方法来鉴别真伪了吧?
假黄金中含有锌,它会与盐酸发生反应,放出气体
三、置换反应
金属与盐酸反应
金属与稀硫酸反应
Mg + 2HCl = MgCl2 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Zn + 2HCl = ZnCl2 + H2↑
Zn + H2SO4 = ZnSO4 + H2↑
Fe + 2HCl = FeCl2 + H2↑
Fe + H2SO4 = FeSO4 + H2↑
观察这些反应,它们有什么共同点?
三、置换反应
置换反应:由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应
单质换单质
特点
A+BC=B+AC
表达式
镁、锌、铁都能与稀盐酸或稀硫酸发生置换反应,置换出酸中的氢
化合反应
分解反应
特点:多变一
特点:一变多
四、课堂练习
1、下表中不同的金属被开发和利用的年代不同,从化学反应的角度看,决定这一年代先后顺序的关键因素是( )
A、金属的活动性 B、金属的导电性
C、金属的延展性 D、地壳中金属元素的含量
A
四、课堂练习
2、下列物质中,不能用金属和稀硫酸直接反应制得的是( )
A、硫酸镁 B、硫酸锌 C、硫酸铝 D、硫酸铜
D
3、下列反应中,不属于置换反应的是( )
A、Mg+2HCl = MgCl2+H2↑
B、CO+CuO = Cu+CO2
C、C+2CuO = 2Cu+CO2↑
D、Cu+2AgNO3 = 2Ag+Cu(NO3)2
B
第一课时
6.2 金属的化学性质
第六章 金属
科粤版九年级下册
