第四节 化学式(第二课时)
图片预览








文档简介
课件27张PPT。化学式(第二课时)化学式书写原则:
(1)以客观事实为基础,不可臆造
(2)遵守化合价规则和化合物中正负化合价代数和为零的原则化合价的一般规律(1)在化合物里氢元素通常显+1价、氧元素-2价。(2)金属元素在化合物中通常显正价。(3)非金属元素与氢元素和金属结合形成化合物时显负价、与氧元素结合时显正价。(4)单质里元素的化合价为零。 化学式的书写方法:1)单质化学式的写法:
如Fe、Al
②由分子构成的单质,如气态或液态非金属单质,用元素符号及其右下角的数字表示,如O2、N2、H2、Br2 。
①由原子构成的单质,直接用元素符号表示金属单质稀有气体单质某些固态非金属如He、Ne、Ar
如P 、 C
2) 化合物化学式的写法:
①氧化物化学式写法:
一般氧元素写在右边, 另一元素写在左边.如: H2O , CO2 , HgO 氧右, 非氧左.
②金属和非金属组成的化合物:
一般金属元素排在左边,非金属元素排在右边.如: NaCl , KCl , ZnS. 金左, 非金右
化学式的读法单质: 读元素的名称。
Fe:铁,Al :铝化合物:一般从右往左读作某化某。
NaCl:氯化钠有时还要读出各种元素原子的个数.
CO:一氧化碳,SO2:二氧化硫,
Fe3O4 :四氧化三铁
若是气体在元素名称后加“ 气 ”。
O2:氧气,N2 :氮气化学式的读法:从右往左读两种元素组成的物质读为“某化某”
如 :CaCl2 MgO
由非金属元素和氧元素组成的物质,读为“几氧化几某”
如: P2O5 SO2
金属元素和原子团组成的物质,读为“某酸某”
如: CaCO 3 CuSO4 NaNO 3
氢原子和原子团组成的物质,读为“某酸”。
如:H2CO3 H2SO4
金属元素和氢氧根组成的物质,读为“氢氧化某’’
如: NaOH Ca(OH) 2 Cu(OH) 2 Fe(OH) 2某化某:指该物质中含两种元素
某酸某:指该物质中含“某酸根”原子团
氢氧化某:指该物质中含“氢氧根”原子团
某化亚某:
某酸亚某:
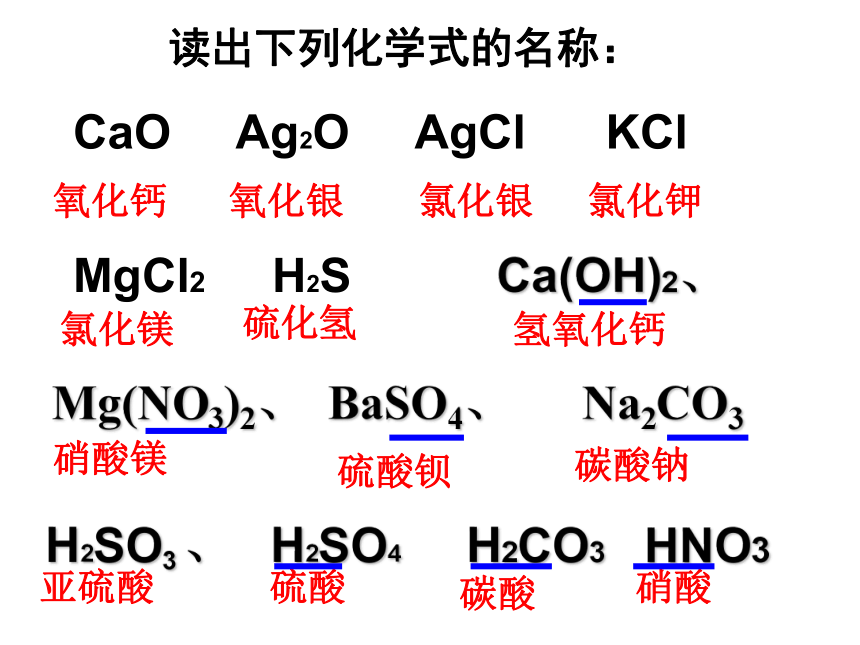
氢氧化亚某:化学式读法规律:指该物质中某正价元素有两种化合价,且取该元素较低的化合价。当一种元素在不同的化合物中有两种变价时,低价读作“某化亚某”,高价读作“某化某”.如:FeO读作氧化亚铁,Fe2O3读作氧化铁.读出下列化学式的名称:Mg(NO3)2、 BaSO4、 Na2CO3CaO Ag2O AgCl KCl
MgCl2 H2S Ca(OH)2、 H2SO3 、 H2SO4 H2CO3 HNO3 氧化钙氧化银氯化银氯化钾氯化镁硫化氢氢氧化钙硝酸镁硫酸钡碳酸钠亚硫酸硫酸碳酸硝酸例题:已知O为-2价,求Fe2O3中铁元素的化合价.
解:设Fe2O3中铁元素的化合价为X
2X+(-2)×3=0练习:已知SO4为-2价,求FeSO4中铁元素的化合价.(依据:化合物里正负化合价代数和为0.)可变价元素的化合价必须根据计算才能确定。
X=+3
化合价的应用(1)根据化学式,确定元素或原子团的化合价。(2)根据化合价,写出化合物的化学式。
方法:十字交叉法“排 标 叉 查”排列元素
正价在前
负价在后标出元素
的化合价交叉价数检查代数和是否为零化合价的应用已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式【思路】(1)先写元素符号(正前负后)(2)标出各元素的化合价(正上)(3)把化合价数值化为最简(4)把化简后的数字交叉写在
相应元素符号的右下角(1省略不写)P OP O+ 3 -2P O+ 3 -2P2 O 3P OP O+ 5 -2P O+ 5 -2省略+ 3 -2+ 3 -2P2 O 5+ 5 -2一排顺序二标价. 价数交叉写右下.
约简价数作角码. 总价为零去检查.
步骤:注意:1.写化学式时正价元素或原子团在前,负价元素或原子团在后。
2.化学式中各原子间个数一般要最简整数比,但也有特例,如:H2O2的化学式中原子个数不能化简。
3.若同一个根有两个或多个时,应先用括号括起,再在右下方标上数字,若为一个时,括号和数字“1”都省略。已知元素M的氧化物化学式为M2On,则M的氯化物的化学式为____。 MCln判断下列化学式是否正确,错则更正。
MgO2、NaO、Ba2O2、K(OH)2、 NaCO3、
CaCl、 AgCl2MgONa2OBaOKOHNa2CO3CaCl2AgCl练习:水由什么构成的?水有质量吗?水分子有质量吗? 原子的质量很小,分子的质量也很小,原子可以用相对原子质量来表示它的质量,那么分子呢?问题? 水分子的质量是否可以用氢原子的质量和氧原子的质量来表示呢?如何理解相对分子质量1、是化学式中各原子的相对原子质量的总和2、是分子的相对质量3、它的单位也是 1相对分子质量概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。【说明】每种纯净物的组成是固定不变的,所以,每种纯净物的相对分子质量也是固定不变的。
如:H2:2 O2:32 H2O:18 CO2:44 有关化学式的计算1、计算物质的相对分子质量书写格式:O2的相对分子质量= 16×2=32(NH4)2CO3的相对分子质量=96H2O的相对分子质量=1×2 + 16=18例题1:计算02、H2O、(NH4)2CO3的相对分子质量=(14+1×4)×2 + 12 + 16 ×3相对分子质量=(相对原子质量×原子个数)之和1、计算下列物质的相对分子质量 。
N2 的相对分子质量=
H2SO4的相对分子质量=
Cu(OH)2的相对分子质量=
NH4NO3的相对分子质量=
CuSO4·5H2O的相对分子质量=
HmSO2n+1的相对分子质量= 14× 2 = 281× 2 + 32 + 16 × 4= 9864 +(16+1)×2 = 9814+1× 4 + 14 + 16 × 3= 8064+32+16× 4+ 5 ×(1 ×2 + 16 )= 250m+32n+48练习:2、已知化合物R2O3 的相对分子质量是160,求 R的相对原子质量。设R的相对原子质量为XX×2+16×3=160X=56解:答: R的相对原子质量为56练习:2、计算化合物分子中原子个数比例:求二氧化锰(MnO2)中锰原子和氧原子的个数比。 MnO2中Mn和O的原子个数比为1∶2 求CuSO4·5H2O中铜原子、硫原子、氧原子和氢原子的个数比。 CuSO4·5H2O中Cu、S、O和H的原子个数比为 1 ∶ 1 ∶ 9 ∶ 10 练习:计算下列化合物分子中原子的个数比
(NH4)2SO4、FeSO4·7H2O一般按化学式中原子的顺序例题2:计算硝酸铵中各元素的质量比m(N) : m(H) : m( O ) = 14×2 : 1×4 : 16×3在NH4NO3中= 28 : 4 : 48= 7 : 1 : 123、计算物质组成元素的质量比元素质量比=(相对原子质量×原子个数)之比解: 3、已知某氮氧元素组成的氧化物中,氮与氧的
质量比是 7 :16,该化合物的化学式为 。解: 设化学式为 NX OY,∴该化合物的化学式是 NO2练习:物质的相对分子质量元素的质量分数4、计算物质中某一元素的质量分数=注意事项:①质量分数——用百分数来表示②意义:每100克物质中含有某元素的质量例题3:计算硝酸铵中氮元素的质量分数。解 : 在NH4NO3中N%=2N×100%=35%答:硝酸铵中氮元素的质量分数为35%(意义:每100克硝酸铵中氮元素的质量为35克。)NH4NO31、150千克的硝酸铵中有多少氮元素?解 : 在NH4NO3中∴150千克的硝酸铵中含有的N元素的质量为150千克×35% = 52.5 千克答:150千克的硝酸铵中有52.5千克氮元素。练习:例:多少kg尿素【CO(NH2)2】中含有5kg氮元素?答:需要10.7kg的尿素。含有5kg氮元素的尿素的质量为:CO(NH2)2的相对分子质量=12+16+(14+1×2)×2=60解:化合物的质量=某元素的质量÷某元素的质量分数1、相同质量的SO2和SO3中氧元素的质量比是( )
A、2:3 B、3:2 C、5:6 D、6:5
解析:设SO2和SO3的质量均为m,则:
—— 化学式计算的应用所以, SO2和SO3中的O的质量比是5:6
(1)以客观事实为基础,不可臆造
(2)遵守化合价规则和化合物中正负化合价代数和为零的原则化合价的一般规律(1)在化合物里氢元素通常显+1价、氧元素-2价。(2)金属元素在化合物中通常显正价。(3)非金属元素与氢元素和金属结合形成化合物时显负价、与氧元素结合时显正价。(4)单质里元素的化合价为零。 化学式的书写方法:1)单质化学式的写法:
如Fe、Al
②由分子构成的单质,如气态或液态非金属单质,用元素符号及其右下角的数字表示,如O2、N2、H2、Br2 。
①由原子构成的单质,直接用元素符号表示金属单质稀有气体单质某些固态非金属如He、Ne、Ar
如P 、 C
2) 化合物化学式的写法:
①氧化物化学式写法:
一般氧元素写在右边, 另一元素写在左边.如: H2O , CO2 , HgO 氧右, 非氧左.
②金属和非金属组成的化合物:
一般金属元素排在左边,非金属元素排在右边.如: NaCl , KCl , ZnS. 金左, 非金右
化学式的读法单质: 读元素的名称。
Fe:铁,Al :铝化合物:一般从右往左读作某化某。
NaCl:氯化钠有时还要读出各种元素原子的个数.
CO:一氧化碳,SO2:二氧化硫,
Fe3O4 :四氧化三铁
若是气体在元素名称后加“ 气 ”。
O2:氧气,N2 :氮气化学式的读法:从右往左读两种元素组成的物质读为“某化某”
如 :CaCl2 MgO
由非金属元素和氧元素组成的物质,读为“几氧化几某”
如: P2O5 SO2
金属元素和原子团组成的物质,读为“某酸某”
如: CaCO 3 CuSO4 NaNO 3
氢原子和原子团组成的物质,读为“某酸”。
如:H2CO3 H2SO4
金属元素和氢氧根组成的物质,读为“氢氧化某’’
如: NaOH Ca(OH) 2 Cu(OH) 2 Fe(OH) 2某化某:指该物质中含两种元素
某酸某:指该物质中含“某酸根”原子团
氢氧化某:指该物质中含“氢氧根”原子团
某化亚某:
某酸亚某:
氢氧化亚某:化学式读法规律:指该物质中某正价元素有两种化合价,且取该元素较低的化合价。当一种元素在不同的化合物中有两种变价时,低价读作“某化亚某”,高价读作“某化某”.如:FeO读作氧化亚铁,Fe2O3读作氧化铁.读出下列化学式的名称:Mg(NO3)2、 BaSO4、 Na2CO3CaO Ag2O AgCl KCl
MgCl2 H2S Ca(OH)2、 H2SO3 、 H2SO4 H2CO3 HNO3 氧化钙氧化银氯化银氯化钾氯化镁硫化氢氢氧化钙硝酸镁硫酸钡碳酸钠亚硫酸硫酸碳酸硝酸例题:已知O为-2价,求Fe2O3中铁元素的化合价.
解:设Fe2O3中铁元素的化合价为X
2X+(-2)×3=0练习:已知SO4为-2价,求FeSO4中铁元素的化合价.(依据:化合物里正负化合价代数和为0.)可变价元素的化合价必须根据计算才能确定。
X=+3
化合价的应用(1)根据化学式,确定元素或原子团的化合价。(2)根据化合价,写出化合物的化学式。
方法:十字交叉法“排 标 叉 查”排列元素
正价在前
负价在后标出元素
的化合价交叉价数检查代数和是否为零化合价的应用已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式【思路】(1)先写元素符号(正前负后)(2)标出各元素的化合价(正上)(3)把化合价数值化为最简(4)把化简后的数字交叉写在
相应元素符号的右下角(1省略不写)P OP O+ 3 -2P O+ 3 -2P2 O 3P OP O+ 5 -2P O+ 5 -2省略+ 3 -2+ 3 -2P2 O 5+ 5 -2一排顺序二标价. 价数交叉写右下.
约简价数作角码. 总价为零去检查.
步骤:注意:1.写化学式时正价元素或原子团在前,负价元素或原子团在后。
2.化学式中各原子间个数一般要最简整数比,但也有特例,如:H2O2的化学式中原子个数不能化简。
3.若同一个根有两个或多个时,应先用括号括起,再在右下方标上数字,若为一个时,括号和数字“1”都省略。已知元素M的氧化物化学式为M2On,则M的氯化物的化学式为____。 MCln判断下列化学式是否正确,错则更正。
MgO2、NaO、Ba2O2、K(OH)2、 NaCO3、
CaCl、 AgCl2MgONa2OBaOKOHNa2CO3CaCl2AgCl练习:水由什么构成的?水有质量吗?水分子有质量吗? 原子的质量很小,分子的质量也很小,原子可以用相对原子质量来表示它的质量,那么分子呢?问题? 水分子的质量是否可以用氢原子的质量和氧原子的质量来表示呢?如何理解相对分子质量1、是化学式中各原子的相对原子质量的总和2、是分子的相对质量3、它的单位也是 1相对分子质量概念:化学式中各原子的相对原子质量的总和,就是相对分子质量。【说明】每种纯净物的组成是固定不变的,所以,每种纯净物的相对分子质量也是固定不变的。
如:H2:2 O2:32 H2O:18 CO2:44 有关化学式的计算1、计算物质的相对分子质量书写格式:O2的相对分子质量= 16×2=32(NH4)2CO3的相对分子质量=96H2O的相对分子质量=1×2 + 16=18例题1:计算02、H2O、(NH4)2CO3的相对分子质量=(14+1×4)×2 + 12 + 16 ×3相对分子质量=(相对原子质量×原子个数)之和1、计算下列物质的相对分子质量 。
N2 的相对分子质量=
H2SO4的相对分子质量=
Cu(OH)2的相对分子质量=
NH4NO3的相对分子质量=
CuSO4·5H2O的相对分子质量=
HmSO2n+1的相对分子质量= 14× 2 = 281× 2 + 32 + 16 × 4= 9864 +(16+1)×2 = 9814+1× 4 + 14 + 16 × 3= 8064+32+16× 4+ 5 ×(1 ×2 + 16 )= 250m+32n+48练习:2、已知化合物R2O3 的相对分子质量是160,求 R的相对原子质量。设R的相对原子质量为XX×2+16×3=160X=56解:答: R的相对原子质量为56练习:2、计算化合物分子中原子个数比例:求二氧化锰(MnO2)中锰原子和氧原子的个数比。 MnO2中Mn和O的原子个数比为1∶2 求CuSO4·5H2O中铜原子、硫原子、氧原子和氢原子的个数比。 CuSO4·5H2O中Cu、S、O和H的原子个数比为 1 ∶ 1 ∶ 9 ∶ 10 练习:计算下列化合物分子中原子的个数比
(NH4)2SO4、FeSO4·7H2O一般按化学式中原子的顺序例题2:计算硝酸铵中各元素的质量比m(N) : m(H) : m( O ) = 14×2 : 1×4 : 16×3在NH4NO3中= 28 : 4 : 48= 7 : 1 : 123、计算物质组成元素的质量比元素质量比=(相对原子质量×原子个数)之比解: 3、已知某氮氧元素组成的氧化物中,氮与氧的
质量比是 7 :16,该化合物的化学式为 。解: 设化学式为 NX OY,∴该化合物的化学式是 NO2练习:物质的相对分子质量元素的质量分数4、计算物质中某一元素的质量分数=注意事项:①质量分数——用百分数来表示②意义:每100克物质中含有某元素的质量例题3:计算硝酸铵中氮元素的质量分数。解 : 在NH4NO3中N%=2N×100%=35%答:硝酸铵中氮元素的质量分数为35%(意义:每100克硝酸铵中氮元素的质量为35克。)NH4NO31、150千克的硝酸铵中有多少氮元素?解 : 在NH4NO3中∴150千克的硝酸铵中含有的N元素的质量为150千克×35% = 52.5 千克答:150千克的硝酸铵中有52.5千克氮元素。练习:例:多少kg尿素【CO(NH2)2】中含有5kg氮元素?答:需要10.7kg的尿素。含有5kg氮元素的尿素的质量为:CO(NH2)2的相对分子质量=12+16+(14+1×2)×2=60解:化合物的质量=某元素的质量÷某元素的质量分数1、相同质量的SO2和SO3中氧元素的质量比是( )
A、2:3 B、3:2 C、5:6 D、6:5
解析:设SO2和SO3的质量均为m,则:
—— 化学式计算的应用所以, SO2和SO3中的O的质量比是5:6
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
