人教版(2019)化学必修第一册1.1.1物质的分类及转化导学案(Word含答案)
文档属性
| 名称 | 人教版(2019)化学必修第一册1.1.1物质的分类及转化导学案(Word含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 496.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-24 00:00:00 | ||
图片预览


文档简介
物质的分类与转化导学案
【知识目标】
1、了解物质分类方法和依据
2、认识分类方法的应用
3、感受分类方法对化学学科研究和化学学习的重要应用
【预习学案】
一、物质的分类
1.根据物质的组成和性质分类
(1)同一种可以组成不同的单质,由同一种元素组成的不同单质之间互称为 ;不同元素可以组成化合物,100多种元素可以能成种类繁多的物质。我们可以采用树状分类法和交叉分类法来认识和研究物质的组成、性质、用途、制备等。
(2)树状分类法和交叉分类法
A.交叉分类法
(1)含义:根据________的分类标准,对同一事物进行多种分类的一种分类方法。
(2)举例:
Na2CO3
B.树状分类法
(1)含义:对________事物按照某种属性进行________的分类法。
(2)举例:
(3)根据物质的性质也可以对物质进行分类
根据氧化物质的性质可对氧化物进行分类,能与酸反应生成盐和水的氧化物叫 ,如 ;能与碱反应生成盐和水的氧化物叫 ,如 ;既能与酸反应生成盐和水又能与碱反应生成盐和水的氧化物叫 ,如 ;既不能与酸反应生成盐和水又不能与碱反应生成盐和水的氧化物叫 ,如 ;
大多数非金属氧化物是 ,大多数金属氧化物是 。
二、物质的转化
1.酸、碱、盐的性质
同类物质的性质具有相似的性质,酸、碱、盐都各自有自己的化学通性。
(1)酸:酸溶液中都含有
①酸与活泼金属单质反应,生成 : Fe+2HCl=
②酸与金属氧化物反应,生成 : Fe2O3+6HCl=
③酸与碱反应,生成 :HCl+NaOH=
④酸与盐反应,生成 :HCl+AgNO3=
(2)碱:碱溶液中都含有
①碱与非金属氧化物反应,生成 :2NaOH+CO2=
②碱与酸反应,生成 :2NaOH+H2SO4=
③碱与盐反应,生成 :2NaOH+CuSO4=
(3)盐:同类盐含有相同的 或
①盐与某些金属单质反应:Fe+CuSO4=
②盐与酸反应:BaCl2+H2SO4=
③盐与碱反应:CuCl2+2NaOH=
2、反应类型
根据反应物和生成物的类别和种类可分为 、 、 和
,金属与酸的反应一般属于 ,酸与碱、盐与酸、盐与碱、盐与盐的反应一般属于 。
3、物质间的转化
(1)物质间的转化:金属单质、非金属单质、氧化物、酸、碱、盐之间有如下转化关系:
我们总结出如下两条转化路线:
金属单质 碱盐
非金属单质 酸盐
(2)物质间转化的应用
1)物质的制备:从上述转化关系我们可以找到制备某种物质的可能方法。
①酸的制备:酸性氧化物与水反应、盐与另一种酸反应
②碱的制备:碱性氧化物与水反应、盐与另一种碱反应
③盐的制备:金属单质与非金属单质反应、酸性氧化物与碱性氧化物反应、盐与盐反应、酸与盐反应、碱与盐反应
2)工业上物质的制备方法选择因素:要从反应的可能性、原料来源、成本高低、 等方面来选择物质制备的适宜方法。
【知识讲解】
一.物质分类
物质的分类
常用分类方法:树状分类法和交叉分类法
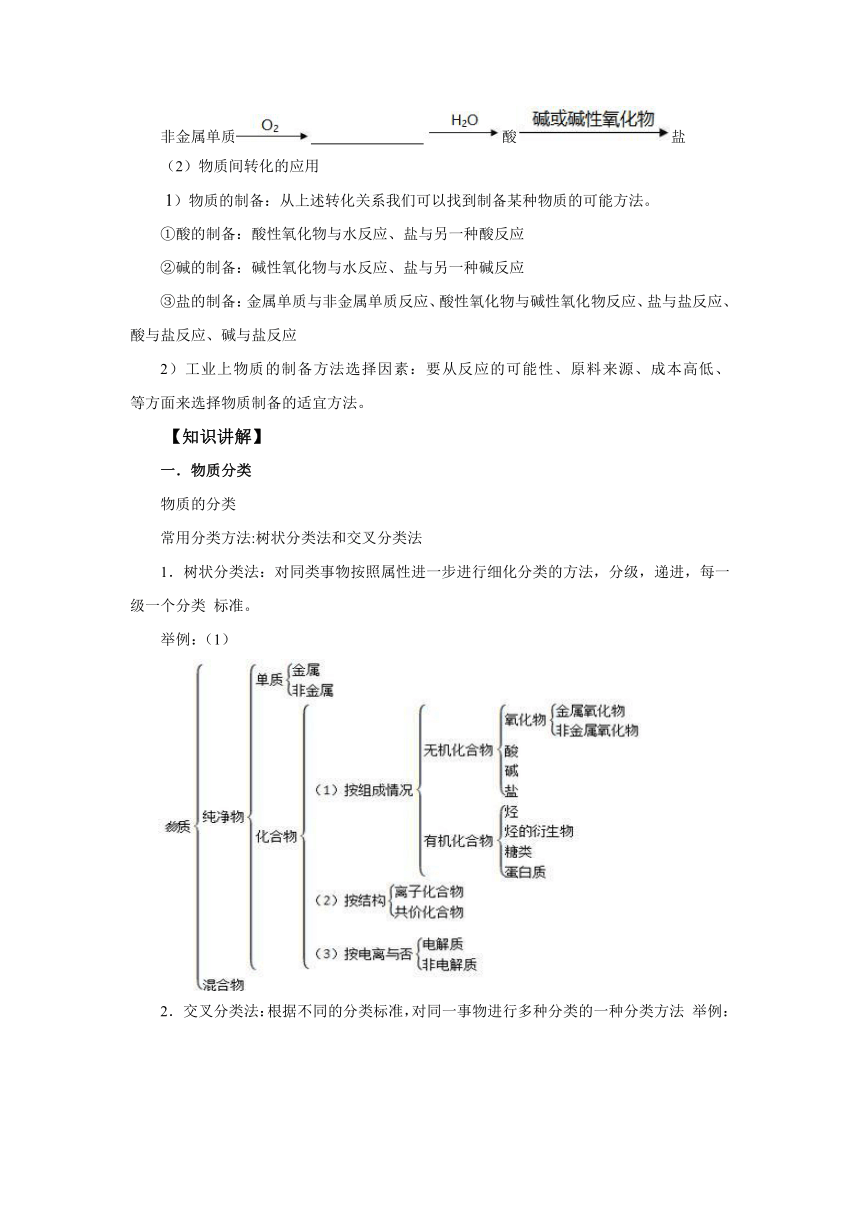
1.树状分类法:对同类事物按照属性进一步进行细化分类的方法,分级,递进,每一级一个分类 标准。
举例:(1)
交叉分类法:根据不同的分类标准,对同一事物进行多种分类的一种分类方法 举例:
3.氧化物的分类
4.酸和碱的分类
5.盐的分类
6.交叉分类法和树状分类法的区别
(1)交叉分类法中的类别之间存在交叉关系,如Na2SO4、K2SO4分别属于钠盐、钾盐,但它们又都属于硫酸盐;
(2)树状分类法中的物质类别间存在从属关系,如盐属于化合物,而化合物又属于纯净物等。
7.物质分类的几点注意事项
(1)根据不同标准可以对化学物质和化学反应进行不同的分类,因此没有固定的分类标准,就不会有正确的分类。如:把物质分为混合物、纯净物、化合物,就是分类标准不统一导致的错误。混合物和纯净物是并列关系,而纯净物包含化合物。
(2)概念间的关系——“并列”与“包含”。
①并列关系:纯净物与混合物,单质与化合物,酸与碱、盐;
②包含关系:纯净物>化合物>氧化物。
(3)酸的元数是酸电离出H+的个数,而不是分子中氢原子的个数,如CH3COOH是一元酸而不是四元酸。
8.氧化物的分类中的特殊物质
(1)碱性氧化物指能与酸反应生成盐和水的氧化物。碱性氧化物都是金属氧化物,但金属氧化物不一定都是碱性氧化物,如Mn2O7为酸性氧化物。
(2)酸性氧化物指能与碱反应生成盐和水的氧化物。非金属氧化物不一定都是酸性氧化物,如CO、H2O等;酸性氧化物也不一定都是非金属氧化物,如Mn2O7。
(3)CO、NO等不能与碱反应生成盐,故属于不成盐氧化物。
(4)Na2O2、Na2O都能与酸反应,如:Na2O+2HCl===2NaCl+H2O;2Na2O2+4HCl===4NaCl+2H2O+O2↑,Na2O2和Na2O不都是碱性氧化物。与酸反应生成盐和水的氧化物属于碱性氧化物,Na2O符合概念,Na2O2与酸反应不仅生成盐和水,还生成了O2,故Na2O2不属于碱性氧化物。
例题:
1.对下列物质的分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱:①④ B.纯净物:③④⑤ C.盐:①⑥ D.混合物:②⑤
2.碳酸钠俗名纯碱,采用不同的分类法对纯碱进行分类,其中正确的是( )
①碱 ②含氧酸盐 ③钠盐 ④碳酸盐
A.①②③ B.①③④ C.①②④ D.②③④
3.下列物质分类的组合中,正确的是( )
选项 碱 酸 盐 酸性氧化物
A 纯碱 盐酸 烧碱 二氧化硫
B 烧碱 硫酸 食盐 一氧化碳
C 苛性钠 醋酸 小苏打 水
D 苛性钾 碳酸 苏打 三氧化硫
4.碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
5.某同学在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型有( )
A.复分解反应 B.分解反应 C.化合反应 D.置换反应
6.对于化学反应A+B===C+D,下列说法中正确的是( )
A.若生成物C、D中有一种为单质,则该反应一定是置换反应
B.若C和D分别为两种沉淀,A、B有可能为盐和碱
C.若C、D是盐和水,则A、B一定是酸和碱
D.若C、D是两种化合物,则A、B一定是化合物
7.现有下列八种物质:①纯碱溶液;②盐酸;③稀硫酸;④氯化钙溶液;⑤烧碱溶液;⑥二氧化硫;⑦氧化铁;⑧氢氧化铁。按照下列要求书写反应的化学方程式。
(1)无氧酸和钠盐________________________________________________。
(2)碱与无氧酸__________________________________________________。
(3)两种盐溶液__________________________________________________。
(4)酸性氧化物与可溶性碱________________________________________。
(5)含氧酸与不溶性碱_____________________________________________。
参考答案
1-5CDDCB 6、B
7、(1)Na2CO3+2HCl===2NaCl+CO2↑+H2O
(2)NaOH+HCl===NaCl+H2O[或Fe(OH)3+3HCl===FeCl3+3H2O]
(3)Na2CO3+CaCl2===CaCO3↓+2NaCl
(4)SO2+2NaOH===Na2SO3+H2O
(5)3H2SO4+2Fe(OH)3===Fe2(SO4)3+6H2O
【知识目标】
1、了解物质分类方法和依据
2、认识分类方法的应用
3、感受分类方法对化学学科研究和化学学习的重要应用
【预习学案】
一、物质的分类
1.根据物质的组成和性质分类
(1)同一种可以组成不同的单质,由同一种元素组成的不同单质之间互称为 ;不同元素可以组成化合物,100多种元素可以能成种类繁多的物质。我们可以采用树状分类法和交叉分类法来认识和研究物质的组成、性质、用途、制备等。
(2)树状分类法和交叉分类法
A.交叉分类法
(1)含义:根据________的分类标准,对同一事物进行多种分类的一种分类方法。
(2)举例:
Na2CO3
B.树状分类法
(1)含义:对________事物按照某种属性进行________的分类法。
(2)举例:
(3)根据物质的性质也可以对物质进行分类
根据氧化物质的性质可对氧化物进行分类,能与酸反应生成盐和水的氧化物叫 ,如 ;能与碱反应生成盐和水的氧化物叫 ,如 ;既能与酸反应生成盐和水又能与碱反应生成盐和水的氧化物叫 ,如 ;既不能与酸反应生成盐和水又不能与碱反应生成盐和水的氧化物叫 ,如 ;
大多数非金属氧化物是 ,大多数金属氧化物是 。
二、物质的转化
1.酸、碱、盐的性质
同类物质的性质具有相似的性质,酸、碱、盐都各自有自己的化学通性。
(1)酸:酸溶液中都含有
①酸与活泼金属单质反应,生成 : Fe+2HCl=
②酸与金属氧化物反应,生成 : Fe2O3+6HCl=
③酸与碱反应,生成 :HCl+NaOH=
④酸与盐反应,生成 :HCl+AgNO3=
(2)碱:碱溶液中都含有
①碱与非金属氧化物反应,生成 :2NaOH+CO2=
②碱与酸反应,生成 :2NaOH+H2SO4=
③碱与盐反应,生成 :2NaOH+CuSO4=
(3)盐:同类盐含有相同的 或
①盐与某些金属单质反应:Fe+CuSO4=
②盐与酸反应:BaCl2+H2SO4=
③盐与碱反应:CuCl2+2NaOH=
2、反应类型
根据反应物和生成物的类别和种类可分为 、 、 和
,金属与酸的反应一般属于 ,酸与碱、盐与酸、盐与碱、盐与盐的反应一般属于 。
3、物质间的转化
(1)物质间的转化:金属单质、非金属单质、氧化物、酸、碱、盐之间有如下转化关系:
我们总结出如下两条转化路线:
金属单质 碱盐
非金属单质 酸盐
(2)物质间转化的应用
1)物质的制备:从上述转化关系我们可以找到制备某种物质的可能方法。
①酸的制备:酸性氧化物与水反应、盐与另一种酸反应
②碱的制备:碱性氧化物与水反应、盐与另一种碱反应
③盐的制备:金属单质与非金属单质反应、酸性氧化物与碱性氧化物反应、盐与盐反应、酸与盐反应、碱与盐反应
2)工业上物质的制备方法选择因素:要从反应的可能性、原料来源、成本高低、 等方面来选择物质制备的适宜方法。
【知识讲解】
一.物质分类
物质的分类
常用分类方法:树状分类法和交叉分类法
1.树状分类法:对同类事物按照属性进一步进行细化分类的方法,分级,递进,每一级一个分类 标准。
举例:(1)
交叉分类法:根据不同的分类标准,对同一事物进行多种分类的一种分类方法 举例:
3.氧化物的分类
4.酸和碱的分类
5.盐的分类
6.交叉分类法和树状分类法的区别
(1)交叉分类法中的类别之间存在交叉关系,如Na2SO4、K2SO4分别属于钠盐、钾盐,但它们又都属于硫酸盐;
(2)树状分类法中的物质类别间存在从属关系,如盐属于化合物,而化合物又属于纯净物等。
7.物质分类的几点注意事项
(1)根据不同标准可以对化学物质和化学反应进行不同的分类,因此没有固定的分类标准,就不会有正确的分类。如:把物质分为混合物、纯净物、化合物,就是分类标准不统一导致的错误。混合物和纯净物是并列关系,而纯净物包含化合物。
(2)概念间的关系——“并列”与“包含”。
①并列关系:纯净物与混合物,单质与化合物,酸与碱、盐;
②包含关系:纯净物>化合物>氧化物。
(3)酸的元数是酸电离出H+的个数,而不是分子中氢原子的个数,如CH3COOH是一元酸而不是四元酸。
8.氧化物的分类中的特殊物质
(1)碱性氧化物指能与酸反应生成盐和水的氧化物。碱性氧化物都是金属氧化物,但金属氧化物不一定都是碱性氧化物,如Mn2O7为酸性氧化物。
(2)酸性氧化物指能与碱反应生成盐和水的氧化物。非金属氧化物不一定都是酸性氧化物,如CO、H2O等;酸性氧化物也不一定都是非金属氧化物,如Mn2O7。
(3)CO、NO等不能与碱反应生成盐,故属于不成盐氧化物。
(4)Na2O2、Na2O都能与酸反应,如:Na2O+2HCl===2NaCl+H2O;2Na2O2+4HCl===4NaCl+2H2O+O2↑,Na2O2和Na2O不都是碱性氧化物。与酸反应生成盐和水的氧化物属于碱性氧化物,Na2O符合概念,Na2O2与酸反应不仅生成盐和水,还生成了O2,故Na2O2不属于碱性氧化物。
例题:
1.对下列物质的分类全部正确的是( )
①纯碱 ②食盐水 ③石灰水 ④NaOH ⑤液态氧 ⑥KClO3
A.碱:①④ B.纯净物:③④⑤ C.盐:①⑥ D.混合物:②⑤
2.碳酸钠俗名纯碱,采用不同的分类法对纯碱进行分类,其中正确的是( )
①碱 ②含氧酸盐 ③钠盐 ④碳酸盐
A.①②③ B.①③④ C.①②④ D.②③④
3.下列物质分类的组合中,正确的是( )
选项 碱 酸 盐 酸性氧化物
A 纯碱 盐酸 烧碱 二氧化硫
B 烧碱 硫酸 食盐 一氧化碳
C 苛性钠 醋酸 小苏打 水
D 苛性钾 碳酸 苏打 三氧化硫
4.碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba(OH)2性质的描述中不属于碱的共同性质的是( )
A.能使紫色石蕊溶液变蓝色
B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
5.某同学在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型有( )
A.复分解反应 B.分解反应 C.化合反应 D.置换反应
6.对于化学反应A+B===C+D,下列说法中正确的是( )
A.若生成物C、D中有一种为单质,则该反应一定是置换反应
B.若C和D分别为两种沉淀,A、B有可能为盐和碱
C.若C、D是盐和水,则A、B一定是酸和碱
D.若C、D是两种化合物,则A、B一定是化合物
7.现有下列八种物质:①纯碱溶液;②盐酸;③稀硫酸;④氯化钙溶液;⑤烧碱溶液;⑥二氧化硫;⑦氧化铁;⑧氢氧化铁。按照下列要求书写反应的化学方程式。
(1)无氧酸和钠盐________________________________________________。
(2)碱与无氧酸__________________________________________________。
(3)两种盐溶液__________________________________________________。
(4)酸性氧化物与可溶性碱________________________________________。
(5)含氧酸与不溶性碱_____________________________________________。
参考答案
1-5CDDCB 6、B
7、(1)Na2CO3+2HCl===2NaCl+CO2↑+H2O
(2)NaOH+HCl===NaCl+H2O[或Fe(OH)3+3HCl===FeCl3+3H2O]
(3)Na2CO3+CaCl2===CaCO3↓+2NaCl
(4)SO2+2NaOH===Na2SO3+H2O
(5)3H2SO4+2Fe(OH)3===Fe2(SO4)3+6H2O
