2022-2023学年九年级化学人教版下册 9.2 溶解度 第2课时 课件(共17张PPT)
文档属性
| 名称 | 2022-2023学年九年级化学人教版下册 9.2 溶解度 第2课时 课件(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-24 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
课题2 溶解度
U9 溶液
1.掌握饱和溶液、不饱和溶液的含义及相互转化的方法。
2.能举例说明结晶现象。掌握常用的两种结晶方法(降温结晶、蒸发结晶),认识海水晒盐的原理。
3. 掌握溶解度的含义和影响因素(固体、气体)。
4.掌握溶解度曲线的含义(点、面、变化趋势等)。
5.掌握溶解度曲线的应用。
6.了解气体溶解度概念及影响因素。
1.溶解度是表示在一定 ,某固体物质在 g溶剂里达到 状态时所溶解的 。如果没指明溶剂,通常所说的溶解度是指物质在 的溶解度。
4.根据物质在室温(20℃)时的溶解度不同,可将物质分为 、 、 、 四个等次。
2.20℃时,100g水最多能溶解36g氯化钠。我们就说20℃时,氯化钠
的溶解度是 ;50℃时,氯化钾的溶解度是42.6g。其含义是
时,在 水中最多能溶解 氯化钾,这时溶液达到 状态。
3.20℃时硝酸钾溶解度为31.6g。根据这句话信息填表。
温度 溶质质量 溶剂质量 溶液质量
温度
100
饱和
质量
水里
36g
50℃
100g
42.6g
饱和
20℃
31.6g
100g
131.6g
难溶
微溶
可溶
易溶
2.溶解度
20℃时,100g水最多能溶解NaCl 36.0 g
20℃时,200g水最多能溶解KNO3 73.2 g
40℃时,100g水最多能溶解NaCl 36.6 g
20℃时,100g水最多能溶解KNO3 31.6 g
KNO3 能溶解的更多
溶剂的量不同
NaCl能溶解的更多
温度不同
20℃时,100g水溶解了30.0 g NaCl
20℃时,100g水最多能溶解KNO3 31.6 g
KNO3 能溶解的更多
NaCl溶解不是最大量
2.溶解度
下列情景的氯化钠和硝酸钾谁的溶解能力比较强?理由?
思考:
x
x
x
只有在温度确定、溶剂的量确定、饱和状态的条件下才能作出比较。
20℃时,100g水最多能溶解NaCl 36.0 g
20℃时,100g水最多能溶解KNO3 31.6g
条件 ——
标准 ——
状态 ——
单位 ——
在_________下,某固态物质在_________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。
用“S”表示。
一定温度
饱和状态
100g溶剂
质量
溶解度4要素
一定温度
100克溶剂(水)
饱和
g
2.固态物质的溶解度
定义:
1.判断下列说法是否正确,并指明错误原因。
①把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的溶解度就是20克。
②20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠的溶解度是10克。
③20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。
④20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。
一定温度
标准:100g溶剂
状态:饱和
单位:g
×
×
×
×
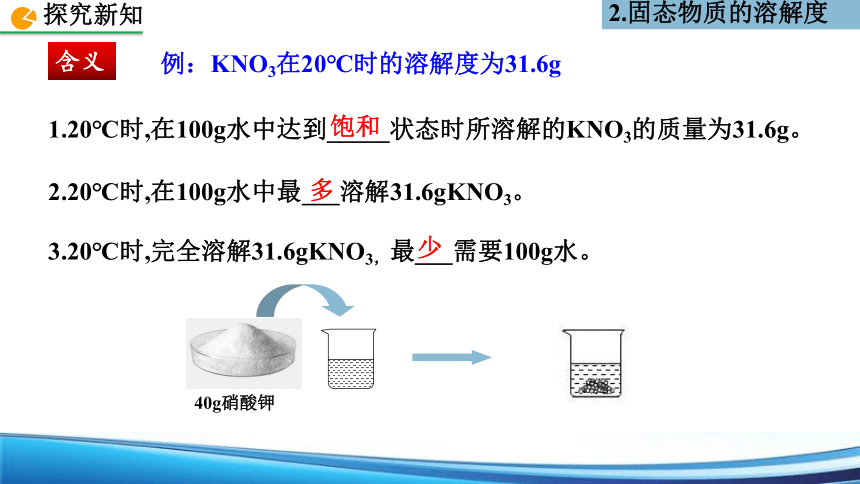
例:KNO3在20℃时的溶解度为31.6g
1.20℃时,在100g水中达到_____状态时所溶解的KNO3的质量为31.6g。
2.20℃时,在100g水中最___溶解31.6gKNO3。
3.20℃时,完全溶解31.6gKNO3,最___需要100g水。
二、溶解度
含义
饱和
多
少
2.溶解度
2.固态物质的溶解度
40g硝酸钾
温度 溶质的质量 溶剂的质量 饱和溶液的质量
硝酸钾 20℃
氯化钠 20℃
31.6g
100g
131.6g
1.20℃时氯化钠的溶解度是36.0g,这句话的含义是什么?将其关系代入下表:
m溶质:m溶剂:m溶液=S:100g:(S+100g)
当某物质在一定温度下溶解度为S时,饱和溶液中有以下关系:
2.溶解度
2.固态物质的溶解度
36.0g
100g
136.0g
例1.20℃时,氯化钠的溶解度为36g,对这句话理解错误的是( )
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,该饱和溶液中水与氯化钠质量比100:36
D.20℃时,将36g氯化钠溶解于100g水中,可得到该温度下氯化钠的饱和溶液136g
B
2.溶解度
例2. 20℃时将某固态物质5g加入40g水中搅拌,刚好达到饱和状态,求该物质在20℃的溶解度。
解:该物质在20℃的溶解度为
答:该物质在20℃的溶解度为12.5g
2.固态物质的溶解度
S=
影响溶解度的因素
①溶质的性质
(或种类)
②溶剂的性质
(或种类)
③温度
20℃时,NaCl的溶解度是 36.0 g
20℃时,KNO3 的溶解度是31.6g
高锰酸钾能溶于水,不能溶于汽油
20℃时,KNO3的溶解度是 31.6 g
40℃时,KNO3 的溶解度是63.9g
内因
外因
2.溶解度
2.固态物质的溶解度
大多数固体物质的溶解度随温度的升高而_____,如_______;少数物质的溶解度随温度变化升高变化不大,如_______;
极少数物质的溶解度随温度的升高而____,如________。
1.溶解度与溶质、溶剂的质量无关
2.与是否搅拌无关
1.内部因素:______和_____的性质
2.外部因素:_____。
温度
溶剂
溶质
二、溶解度
例.要使KNO3溶解度增大,采用的方法是( )
A.加水 B.增加KNO3 C.搅拌 D.升温
D
增大
KNO3
NaCl
减小
Ca(OH)2
2.溶解度
2.固态物质的溶解度
注意:
影响溶解度的因素
二、溶解度
固体物质溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度(20℃/g) s>10 1<s<10 0.1<s<1 s<0.01
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
溶解是绝对的,不溶是相对的,绝对不溶的物质是不存在的
20℃的溶解度/g
2.溶解度
2.固态物质的溶解度
例.①20 ℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是_____溶物质。
②20℃时氯化钠的溶解度是36 g,则氯化钠属于( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质
难
A
条件 ——
标准 ——
状态 ——
单位 ——
某气体的______为101kPa和________时,在________里达到_________时所溶解的________。
气体溶解度4要素
101kPa
1体积水
饱和
1
3.气态物质的溶解度
定义:
一定温度
饱和状态
1体积水
气体体积
压强
0℃时,氧气的溶解度为0.049的含义是什么?
思考:
在0℃,氧气压强为101kPa时,1体积水最多能溶解0. 049体积氧气
3.气态物质的溶解度
1.打开汽水盖时,汽水会自动喷出来,为什么?
思考:
打开汽水瓶盖,瓶内压强变小,二氧化碳的溶解度减小,所以汽水会自动喷出来。
2.喝了汽水后,常常会打嗝,为什么?
气体的溶解度受温度的影响,温度升高,气体的溶解度变小。
3.雷阵雨前鱼常浮头,说明了什么?
雷雨前,大气压强减少,氧气在水中的溶解度降低,水中缺少氧气。
4.加热煮沸为什么可以除去水中溶解的氧气?
温度升高,氧气在水中的溶解度降低。
①温度 ②压强
影响因素:
3.气态物质的溶解度
1.冬季养鱼池的冰面上总要打很多洞,为什么?
思考:
增大空气与水的接触面积,增加水中氧气的溶解量。
2.家里用鱼缸养鱼,如何增加水中的含氧量?
1.用空气泵向鱼缸中通空气
2.尽量选用开口大的鱼缸,可增大水与空气的接触面积
3.定期地更换新水
4.适量在鱼缸中种些水草,利用植物光合作用提供氧气
1.定义:在_________下,某固态物质在_________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。用“S”表示。
2.影响因素:内部:______和______的性质
外部:_____。大部分随温度升高而______,极少数随温度升高而_____,如________。
3.固体物质溶解度曲线
陡升_______,缓升_______,下降__________。
一定温度
饱和状态
100g溶剂
质量
固态物质的溶解度
溶剂
溶质
温度
KNO3
NaCl
Ca(OH)2
增大
减小
Ca(OH)2
2.溶解度
气体的溶解度
1.定义:某气体的______为101kPa和________时,在________里达到_________时所溶解的________。
一定温度
饱和状态
1体积水
气体体积
压强
2.影响气体溶解度的因素
2.溶解度
①压强增大,S气体变____。
②温度升高,S气体变____。
大
小
课题2 溶解度
U9 溶液
1.掌握饱和溶液、不饱和溶液的含义及相互转化的方法。
2.能举例说明结晶现象。掌握常用的两种结晶方法(降温结晶、蒸发结晶),认识海水晒盐的原理。
3. 掌握溶解度的含义和影响因素(固体、气体)。
4.掌握溶解度曲线的含义(点、面、变化趋势等)。
5.掌握溶解度曲线的应用。
6.了解气体溶解度概念及影响因素。
1.溶解度是表示在一定 ,某固体物质在 g溶剂里达到 状态时所溶解的 。如果没指明溶剂,通常所说的溶解度是指物质在 的溶解度。
4.根据物质在室温(20℃)时的溶解度不同,可将物质分为 、 、 、 四个等次。
2.20℃时,100g水最多能溶解36g氯化钠。我们就说20℃时,氯化钠
的溶解度是 ;50℃时,氯化钾的溶解度是42.6g。其含义是
时,在 水中最多能溶解 氯化钾,这时溶液达到 状态。
3.20℃时硝酸钾溶解度为31.6g。根据这句话信息填表。
温度 溶质质量 溶剂质量 溶液质量
温度
100
饱和
质量
水里
36g
50℃
100g
42.6g
饱和
20℃
31.6g
100g
131.6g
难溶
微溶
可溶
易溶
2.溶解度
20℃时,100g水最多能溶解NaCl 36.0 g
20℃时,200g水最多能溶解KNO3 73.2 g
40℃时,100g水最多能溶解NaCl 36.6 g
20℃时,100g水最多能溶解KNO3 31.6 g
KNO3 能溶解的更多
溶剂的量不同
NaCl能溶解的更多
温度不同
20℃时,100g水溶解了30.0 g NaCl
20℃时,100g水最多能溶解KNO3 31.6 g
KNO3 能溶解的更多
NaCl溶解不是最大量
2.溶解度
下列情景的氯化钠和硝酸钾谁的溶解能力比较强?理由?
思考:
x
x
x
只有在温度确定、溶剂的量确定、饱和状态的条件下才能作出比较。
20℃时,100g水最多能溶解NaCl 36.0 g
20℃时,100g水最多能溶解KNO3 31.6g
条件 ——
标准 ——
状态 ——
单位 ——
在_________下,某固态物质在_________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。
用“S”表示。
一定温度
饱和状态
100g溶剂
质量
溶解度4要素
一定温度
100克溶剂(水)
饱和
g
2.固态物质的溶解度
定义:
1.判断下列说法是否正确,并指明错误原因。
①把20克某物质溶解在100克水里恰好制成饱和溶液,这种物质的溶解度就是20克。
②20℃时10克氯化钠溶解在水里制成饱和溶液,故20℃时氯化钠的溶解度是10克。
③20℃时10克氯化钠可溶解在100克水里,故20℃时氯化钠的溶解度是10克。
④20℃时36克食盐溶解在100克水中恰好饱和,故20℃时食盐的溶解度是36。
一定温度
标准:100g溶剂
状态:饱和
单位:g
×
×
×
×
例:KNO3在20℃时的溶解度为31.6g
1.20℃时,在100g水中达到_____状态时所溶解的KNO3的质量为31.6g。
2.20℃时,在100g水中最___溶解31.6gKNO3。
3.20℃时,完全溶解31.6gKNO3,最___需要100g水。
二、溶解度
含义
饱和
多
少
2.溶解度
2.固态物质的溶解度
40g硝酸钾
温度 溶质的质量 溶剂的质量 饱和溶液的质量
硝酸钾 20℃
氯化钠 20℃
31.6g
100g
131.6g
1.20℃时氯化钠的溶解度是36.0g,这句话的含义是什么?将其关系代入下表:
m溶质:m溶剂:m溶液=S:100g:(S+100g)
当某物质在一定温度下溶解度为S时,饱和溶液中有以下关系:
2.溶解度
2.固态物质的溶解度
36.0g
100g
136.0g
例1.20℃时,氯化钠的溶解度为36g,对这句话理解错误的是( )
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,该饱和溶液中水与氯化钠质量比100:36
D.20℃时,将36g氯化钠溶解于100g水中,可得到该温度下氯化钠的饱和溶液136g
B
2.溶解度
例2. 20℃时将某固态物质5g加入40g水中搅拌,刚好达到饱和状态,求该物质在20℃的溶解度。
解:该物质在20℃的溶解度为
答:该物质在20℃的溶解度为12.5g
2.固态物质的溶解度
S=
影响溶解度的因素
①溶质的性质
(或种类)
②溶剂的性质
(或种类)
③温度
20℃时,NaCl的溶解度是 36.0 g
20℃时,KNO3 的溶解度是31.6g
高锰酸钾能溶于水,不能溶于汽油
20℃时,KNO3的溶解度是 31.6 g
40℃时,KNO3 的溶解度是63.9g
内因
外因
2.溶解度
2.固态物质的溶解度
大多数固体物质的溶解度随温度的升高而_____,如_______;少数物质的溶解度随温度变化升高变化不大,如_______;
极少数物质的溶解度随温度的升高而____,如________。
1.溶解度与溶质、溶剂的质量无关
2.与是否搅拌无关
1.内部因素:______和_____的性质
2.外部因素:_____。
温度
溶剂
溶质
二、溶解度
例.要使KNO3溶解度增大,采用的方法是( )
A.加水 B.增加KNO3 C.搅拌 D.升温
D
增大
KNO3
NaCl
减小
Ca(OH)2
2.溶解度
2.固态物质的溶解度
注意:
影响溶解度的因素
二、溶解度
固体物质溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度(20℃/g) s>10 1<s<10 0.1<s<1 s<0.01
.
.
.
0.01g
1g
10g
易溶
可溶
微溶
难(不)溶
溶解是绝对的,不溶是相对的,绝对不溶的物质是不存在的
20℃的溶解度/g
2.溶解度
2.固态物质的溶解度
例.①20 ℃时碳酸钙的溶解度是0.0013g,所以碳酸钙是_____溶物质。
②20℃时氯化钠的溶解度是36 g,则氯化钠属于( )
A.易溶物质 B.可溶物质 C.微溶物质 D.难溶物质
难
A
条件 ——
标准 ——
状态 ——
单位 ——
某气体的______为101kPa和________时,在________里达到_________时所溶解的________。
气体溶解度4要素
101kPa
1体积水
饱和
1
3.气态物质的溶解度
定义:
一定温度
饱和状态
1体积水
气体体积
压强
0℃时,氧气的溶解度为0.049的含义是什么?
思考:
在0℃,氧气压强为101kPa时,1体积水最多能溶解0. 049体积氧气
3.气态物质的溶解度
1.打开汽水盖时,汽水会自动喷出来,为什么?
思考:
打开汽水瓶盖,瓶内压强变小,二氧化碳的溶解度减小,所以汽水会自动喷出来。
2.喝了汽水后,常常会打嗝,为什么?
气体的溶解度受温度的影响,温度升高,气体的溶解度变小。
3.雷阵雨前鱼常浮头,说明了什么?
雷雨前,大气压强减少,氧气在水中的溶解度降低,水中缺少氧气。
4.加热煮沸为什么可以除去水中溶解的氧气?
温度升高,氧气在水中的溶解度降低。
①温度 ②压强
影响因素:
3.气态物质的溶解度
1.冬季养鱼池的冰面上总要打很多洞,为什么?
思考:
增大空气与水的接触面积,增加水中氧气的溶解量。
2.家里用鱼缸养鱼,如何增加水中的含氧量?
1.用空气泵向鱼缸中通空气
2.尽量选用开口大的鱼缸,可增大水与空气的接触面积
3.定期地更换新水
4.适量在鱼缸中种些水草,利用植物光合作用提供氧气
1.定义:在_________下,某固态物质在_________里达到__________时所溶解的_____,叫做这种物质在这种溶剂里的溶解度。用“S”表示。
2.影响因素:内部:______和______的性质
外部:_____。大部分随温度升高而______,极少数随温度升高而_____,如________。
3.固体物质溶解度曲线
陡升_______,缓升_______,下降__________。
一定温度
饱和状态
100g溶剂
质量
固态物质的溶解度
溶剂
溶质
温度
KNO3
NaCl
Ca(OH)2
增大
减小
Ca(OH)2
2.溶解度
气体的溶解度
1.定义:某气体的______为101kPa和________时,在________里达到_________时所溶解的________。
一定温度
饱和状态
1体积水
气体体积
压强
2.影响气体溶解度的因素
2.溶解度
①压强增大,S气体变____。
②温度升高,S气体变____。
大
小
同课章节目录
