科粤版(2012)化学 第二章---空气、物质的构成 单元练习 (含答案)
文档属性
| 名称 | 科粤版(2012)化学 第二章---空气、物质的构成 单元练习 (含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 145.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-25 00:00:00 | ||
图片预览


文档简介
第二章---空气、物质的构成
一、单选题
1.下列元素名称与其对应的元素符号完全正确的是( )
A.氯 B.氖 C.镁 D.铜
2.2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C18,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个( )
A.原子 B.质子 C.中子 D.电子
3.生活中的下列物质,属于纯净物的是
A.矿泉水 B.葡萄酒 C.蒸馏水 D.糖水
4.2020年6月23日长征三号乙运载火箭成功发射北斗三号卫星,在火箭的制造中使用了钛和钛合金。钛元素在元素周期表中的相关信息如下图所示。下列说法错误的是
A.钛原子的中子数为22
B.钛元素属于金属元素
C.钛的元素符号是Ti
D.钛元素的相对原子质量是47.87
5.有关空气中一些成分的说法错误的是
A.氮气可作保护气 B.稀有气体可用于制作霓虹灯
C.氧气可起助燃作用 D.二氧化碳是一种空气污染物
6.除去密闭容器内空气中的氧气,得到较纯净的氮气,下列物质中最好选用
A.木炭 B.红磷 C.铁丝 D.蜡烛
7.下列物质含有氢分子的是( )
A.H2 B.H2O2 C.H2CO3 D.H2O
8.下列各图中和分别表示不同元素的原子,则其中表示化合物的是( )
A. B.
C. D.
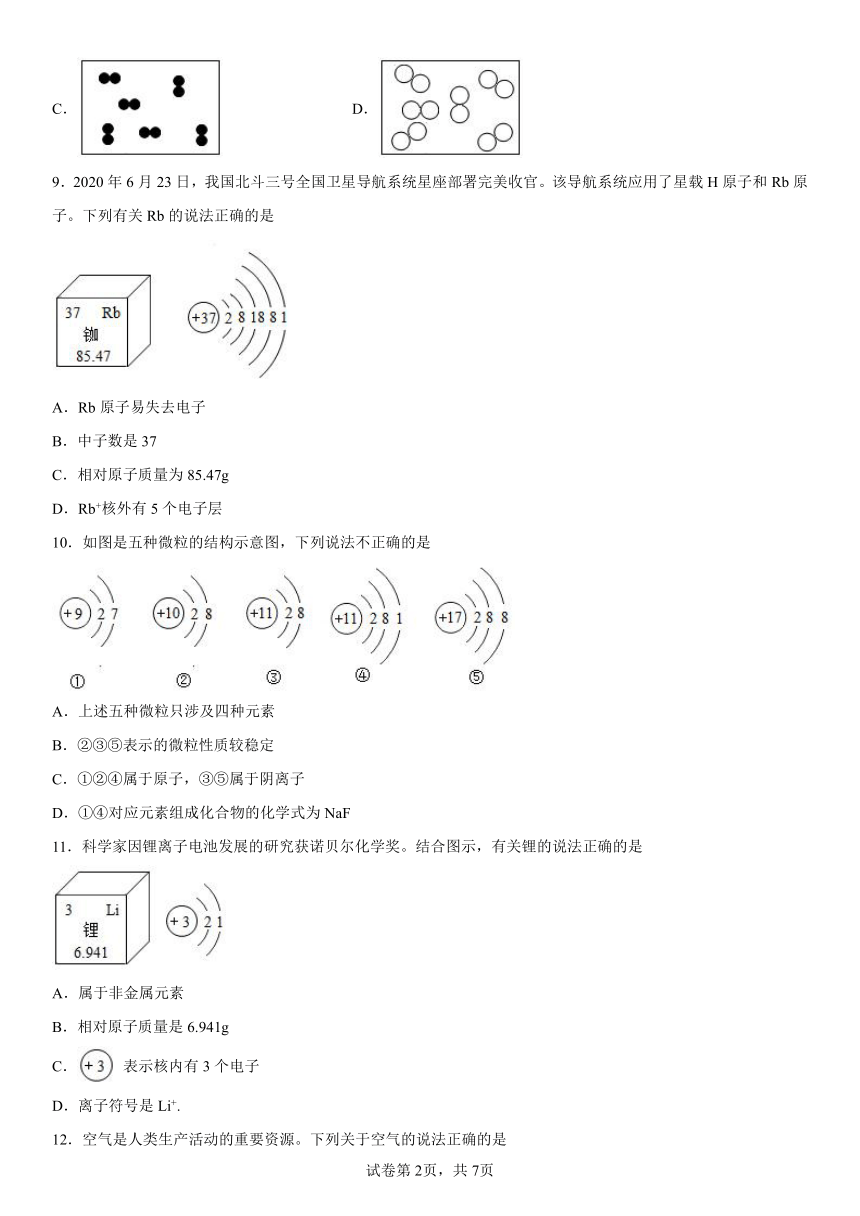
9.2020年6月23日,我国北斗三号全国卫星导航系统星座部署完美收官。该导航系统应用了星载H原子和Rb原子。下列有关Rb的说法正确的是
A.Rb原子易失去电子
B.中子数是37
C.相对原子质量为85.47g
D.Rb+核外有5个电子层
10.如图是五种微粒的结构示意图,下列说法不正确的是
A.上述五种微粒只涉及四种元素
B.②③⑤表示的微粒性质较稳定
C.①②④属于原子,③⑤属于阴离子
D.①④对应元素组成化合物的化学式为NaF
11.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
12.空气是人类生产活动的重要资源。下列关于空气的说法正确的是
A.洁净的空气是纯净物
B.空气中可分离出氧气用于医疗急救
C.空气中含量最多的气体是二氧化碳
D.空气中氮气的化学性质比氧气活泼
13.“分子机器”是指在分子尺寸上制造的一类分子器件,其长短仅相当于l纳米左右(1纳米=10-9米)。它的驱动方式是通过外部刺激(如电能、光照等)使分子结构发生改变,从而对外做功。下列关于分子机器的说法中,正确的是
A.肉眼能直接观察到分子机器
B.分子机器驱动过程中,发生了化学变化
C.分子机器的驱动不需要能量
D.分子机器“发动机”驱动方式与普通发动机相同
14.“青山绿水就是金山银山”,为了实现这一目标,我县已经开始实行电动公交出行,推广太阳能路灯,升级改造燃煤锅炉。你认为下列做法与这一理念不相符的是( )
A.使用无磷洗衣粉预防水体富营养化
B.淘汰黄标车减少汽车尾气污染
C.深埋废旧电池减少重金属污染
D.使用低毒、低残留农药减轻环境污染运用图示法可以帮助我们巧学化学
15.如图所示,将中间的玻璃片抽走,使两瓶口密合在一起,观察到甲中两瓶气体的颜色很快趋于一致,而乙中需很长时间才能达到相同效果(已知氢气与黄绿色的氯气在该实验中不反应)。下列说法错误的是
A.保持氢气化学性质的最小粒子是氢分子
B.该实验说明分子在不停地运动
C.该实验说明此条件下氯气的密度比氢气大
D.该实验证明在化学变化中,分子可以再分,原子不可再分
二、填空题
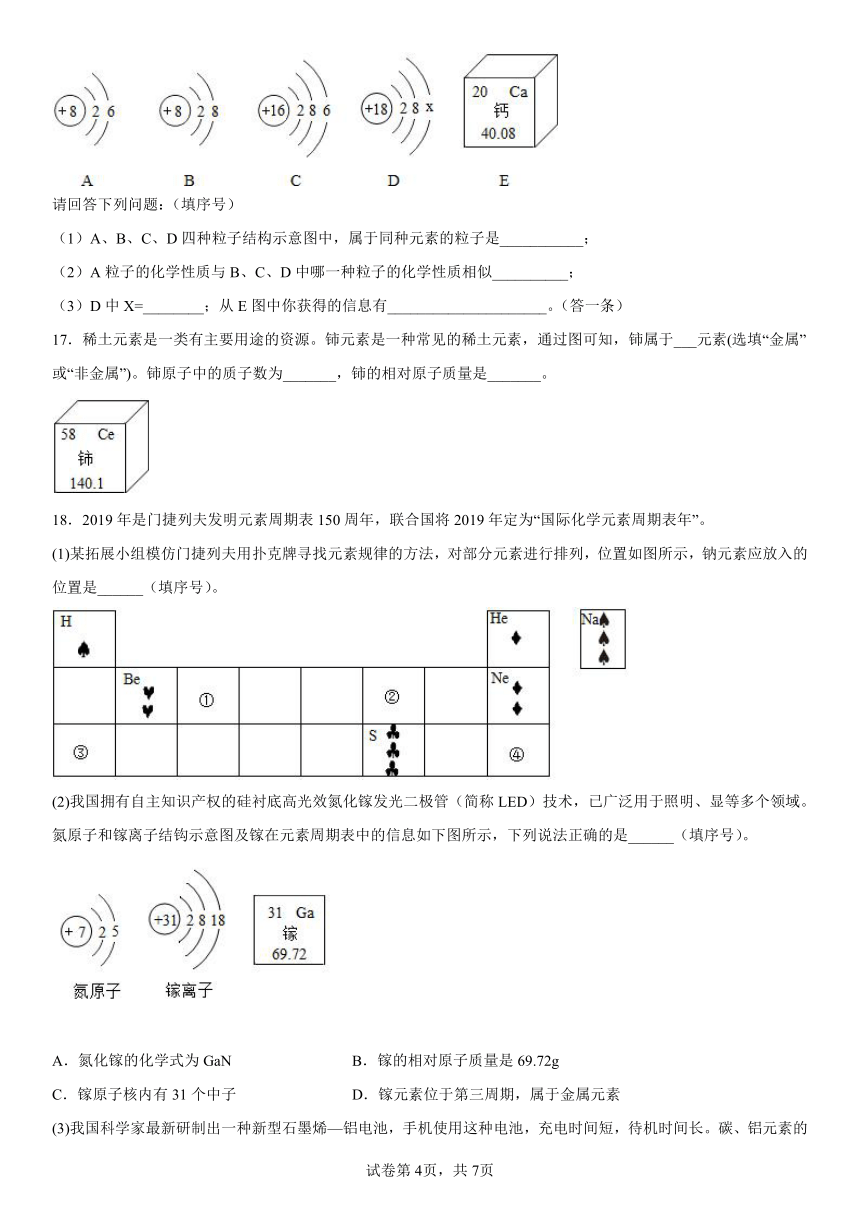
16.下图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息。
请回答下列问题:(填序号)
(1)A、B、C、D四种粒子结构示意图中,属于同种元素的粒子是___________;
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似__________;
(3)D中X=________;从E图中你获得的信息有_____________________。(答一条)
17.稀土元素是一类有主要用途的资源。铈元素是一种常见的稀土元素,通过图可知,铈属于___元素(选填“金属”或“非金属”)。铈原子中的质子数为_______,铈的相对原子质量是_______。
18.2019年是门捷列夫发明元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”。
(1)某拓展小组模仿门捷列夫用扑克牌寻找元素规律的方法,对部分元素进行排列,位置如图所示,钠元素应放入的位置是______(填序号)。
(2)我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显等多个领域。氮原子和镓离子结钩示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是______(填序号)。
A.氮化镓的化学式为GaN B.镓的相对原子质量是69.72g
C.镓原子核内有31个中子 D.镓元素位于第三周期,属于金属元素
(3)我国科学家最新研制出一种新型石墨烯—铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图所示,
它们的化学性质______(填“相似”或“不相似”)。在化学反应中,铝原子容易______(填“得到”或“失去”)电子。
(4)下列几种粒子的结构示意图中共有______种元素,表示阳离子的离子符号是______。
19.如图是氢分子(H2)和氧分子(O2)运动的示意图。根据图回答:
(1)仔细观察上述粒子运动的示意图,分子运动速率最快的是_____(填序号)。
(2)在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是_____(填序号)。
(3)从图中可见,影响分子运动速率的因素除温度外,还与_____有关。
(4)举一个能说明“温度升高,分子运动速率加快”的生活实例_____。
三、实验题
20.依据所学知识回答问题
(1)图1装置是用红磷燃烧来粗略测定空气中氧气含量。写出瓶中物质燃烧的符号表达式____。请仿照“图2实验后”的图示,画出“图1实验前”瓶中气体组成的微观示意图,水分子无需画出。已知金属镁会与空气中的氧气和氮气反应,如果用镁条代替红磷进行此实验,则进入集气瓶中的水会____瓶内空气总体积的五分之一(填写“ ”、“=”或“<”)。
(2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。用图3装置进行测定空气中氧气含量的实验。下表是有关数据:
所需要的时间 0 5 10 30 35 45
量筒中液面的刻度 50 35 27.5 19.7 19.7 19.7
①脱氧剂发生复杂的化学反应,首先是铁粉与氧气、水反应生成氢氧化亚铁【Fe(OH)2】固体,该反应符号表达式:_______,属于_______反应(填基本反应类型)。
②实验过程中量筒中的液面不断下降,水被吸入瓶中,出现该现象的原因是_______。
21.某同学设计了实验装置测定空气中氧气的含量。
实验过程:
①检查装置的气密性,气密性良好;
(1)②在集气瓶里装进适量a 体积的水,燃烧匙里放一块白磷(40℃即可燃烧),按图示装置连接仪器,然后在酒精灯上把玻璃棒下端加热,玻璃棒的作用为___________;(注:集气瓶内的长导管已接近瓶底)
③(注:白磷与红磷燃烧的产物、现象均相同)
(2)④待集气瓶完全冷却至室温,量出集气瓶中水的体积是b,整个集气瓶的体积是c. 从白磷开始燃烧到最后熄灭的过程中,集气瓶内水面的变化情况是___________ ;
(3)⑤根据a、b、c三个数据,计算出空气中氧气的体积分数。已知c=60mL,a=10mL,b=___________mL。
实验反思:
(4)组内成员小张对“实验前集气瓶里要装进适量a 体积的水”非常不理解。咨询了组长小明之后,他终于明白“a 体积的水”的作用,其一是为了加快④步骤中集气瓶的冷却速度;其二则主要是___________。
(5)在上述实验中,下列操作的实施和实验现象的出现,会导致实验最后产生的实际值大于理论值的是___________。
A.装置气密性不好 B.实验前集气瓶里没有装a 体积的水
C.集气瓶没有冷却到室温 D.用红磷代替白磷(红磷的着火点在240℃左右)
四、计算题
22.已知碳-12原子的质量为1.993×10-26kg,A原子的质量为5.146×10-26kg,若A原子核内中子数为16个。求:(写出对应的计算过程)
(1)A原子的相对原子质量______。(保留整数)
(2)A原子的核外电子数_______。
23.如图是某省生产的某加钙食盐包装标签上的部分文字,请仔细阅读后回答问题:
包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
为了测定此盐中的钙元素含量,取这种盐溶于水,加入足量的盐酸,生成二氧化碳,计算此加钙食盐中钙元素的质量分数.________
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.C
4.A
5.D
6.B
7.A
8.A
9.A
10.C
11.D
12.B
13.B
14.C
15.D
16.(1) A、B C 8 (2) 该元素的原子序数为20
17. (1) 金属 58 (2) 140.1
18.(1)③
(2)A
(3) 不相似 失去
(4) 3 Mg2+
19. (1) ① ②③ (2) 分子种类 (3) 湿衣服在阳光下比在阴凉处干得快
20.(1) >
(2) 化合 广口瓶中的氧气不断被消耗,压强不断减小
21.(1)点燃白磷
(2)先下降后上升
(3)20
(4)液封
(5)B
22.(1)解:A原子的相对原子质量为:
答:A的相对原子质量为31。
(2)解:因为相对原子质量=质子数+中子数
所以A的质子数为:31-16=15
因为在原子中质子数=核外电子数
所以A原子的核外电子数为15
答:A原子的核外电子数为15。
23.(1)钙元素(2)
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列元素名称与其对应的元素符号完全正确的是( )
A.氯 B.氖 C.镁 D.铜
2.2019年8月《Science》杂志报道,科学家合成了一种环状碳分子C18,这种分子具有广泛的应用前景。1个环状碳分子C18中共含有18个( )
A.原子 B.质子 C.中子 D.电子
3.生活中的下列物质,属于纯净物的是
A.矿泉水 B.葡萄酒 C.蒸馏水 D.糖水
4.2020年6月23日长征三号乙运载火箭成功发射北斗三号卫星,在火箭的制造中使用了钛和钛合金。钛元素在元素周期表中的相关信息如下图所示。下列说法错误的是
A.钛原子的中子数为22
B.钛元素属于金属元素
C.钛的元素符号是Ti
D.钛元素的相对原子质量是47.87
5.有关空气中一些成分的说法错误的是
A.氮气可作保护气 B.稀有气体可用于制作霓虹灯
C.氧气可起助燃作用 D.二氧化碳是一种空气污染物
6.除去密闭容器内空气中的氧气,得到较纯净的氮气,下列物质中最好选用
A.木炭 B.红磷 C.铁丝 D.蜡烛
7.下列物质含有氢分子的是( )
A.H2 B.H2O2 C.H2CO3 D.H2O
8.下列各图中和分别表示不同元素的原子,则其中表示化合物的是( )
A. B.
C. D.
9.2020年6月23日,我国北斗三号全国卫星导航系统星座部署完美收官。该导航系统应用了星载H原子和Rb原子。下列有关Rb的说法正确的是
A.Rb原子易失去电子
B.中子数是37
C.相对原子质量为85.47g
D.Rb+核外有5个电子层
10.如图是五种微粒的结构示意图,下列说法不正确的是
A.上述五种微粒只涉及四种元素
B.②③⑤表示的微粒性质较稳定
C.①②④属于原子,③⑤属于阴离子
D.①④对应元素组成化合物的化学式为NaF
11.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
12.空气是人类生产活动的重要资源。下列关于空气的说法正确的是
A.洁净的空气是纯净物
B.空气中可分离出氧气用于医疗急救
C.空气中含量最多的气体是二氧化碳
D.空气中氮气的化学性质比氧气活泼
13.“分子机器”是指在分子尺寸上制造的一类分子器件,其长短仅相当于l纳米左右(1纳米=10-9米)。它的驱动方式是通过外部刺激(如电能、光照等)使分子结构发生改变,从而对外做功。下列关于分子机器的说法中,正确的是
A.肉眼能直接观察到分子机器
B.分子机器驱动过程中,发生了化学变化
C.分子机器的驱动不需要能量
D.分子机器“发动机”驱动方式与普通发动机相同
14.“青山绿水就是金山银山”,为了实现这一目标,我县已经开始实行电动公交出行,推广太阳能路灯,升级改造燃煤锅炉。你认为下列做法与这一理念不相符的是( )
A.使用无磷洗衣粉预防水体富营养化
B.淘汰黄标车减少汽车尾气污染
C.深埋废旧电池减少重金属污染
D.使用低毒、低残留农药减轻环境污染运用图示法可以帮助我们巧学化学
15.如图所示,将中间的玻璃片抽走,使两瓶口密合在一起,观察到甲中两瓶气体的颜色很快趋于一致,而乙中需很长时间才能达到相同效果(已知氢气与黄绿色的氯气在该实验中不反应)。下列说法错误的是
A.保持氢气化学性质的最小粒子是氢分子
B.该实验说明分子在不停地运动
C.该实验说明此条件下氯气的密度比氢气大
D.该实验证明在化学变化中,分子可以再分,原子不可再分
二、填空题
16.下图中A、B、C、D是四种粒子的结构示意图,E是钙元素在元素周期表中的信息。
请回答下列问题:(填序号)
(1)A、B、C、D四种粒子结构示意图中,属于同种元素的粒子是___________;
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似__________;
(3)D中X=________;从E图中你获得的信息有_____________________。(答一条)
17.稀土元素是一类有主要用途的资源。铈元素是一种常见的稀土元素,通过图可知,铈属于___元素(选填“金属”或“非金属”)。铈原子中的质子数为_______,铈的相对原子质量是_______。
18.2019年是门捷列夫发明元素周期表150周年,联合国将2019年定为“国际化学元素周期表年”。
(1)某拓展小组模仿门捷列夫用扑克牌寻找元素规律的方法,对部分元素进行排列,位置如图所示,钠元素应放入的位置是______(填序号)。
(2)我国拥有自主知识产权的硅衬底高光效氮化镓发光二极管(简称LED)技术,已广泛用于照明、显等多个领域。氮原子和镓离子结钩示意图及镓在元素周期表中的信息如下图所示,下列说法正确的是______(填序号)。
A.氮化镓的化学式为GaN B.镓的相对原子质量是69.72g
C.镓原子核内有31个中子 D.镓元素位于第三周期,属于金属元素
(3)我国科学家最新研制出一种新型石墨烯—铝电池,手机使用这种电池,充电时间短,待机时间长。碳、铝元素的相关信息如图所示,
它们的化学性质______(填“相似”或“不相似”)。在化学反应中,铝原子容易______(填“得到”或“失去”)电子。
(4)下列几种粒子的结构示意图中共有______种元素,表示阳离子的离子符号是______。
19.如图是氢分子(H2)和氧分子(O2)运动的示意图。根据图回答:
(1)仔细观察上述粒子运动的示意图,分子运动速率最快的是_____(填序号)。
(2)在A、B和C中,能比较得出“温度越高,分子运动速率越快”的是_____(填序号)。
(3)从图中可见,影响分子运动速率的因素除温度外,还与_____有关。
(4)举一个能说明“温度升高,分子运动速率加快”的生活实例_____。
三、实验题
20.依据所学知识回答问题
(1)图1装置是用红磷燃烧来粗略测定空气中氧气含量。写出瓶中物质燃烧的符号表达式____。请仿照“图2实验后”的图示,画出“图1实验前”瓶中气体组成的微观示意图,水分子无需画出。已知金属镁会与空气中的氧气和氮气反应,如果用镁条代替红磷进行此实验,则进入集气瓶中的水会____瓶内空气总体积的五分之一(填写“ ”、“=”或“<”)。
(2)食品脱氧剂(以铁粉为主的物质组成)能通过化学反应除去密闭包装袋中的氧气,使食品处于无氧状态。用图3装置进行测定空气中氧气含量的实验。下表是有关数据:
所需要的时间 0 5 10 30 35 45
量筒中液面的刻度 50 35 27.5 19.7 19.7 19.7
①脱氧剂发生复杂的化学反应,首先是铁粉与氧气、水反应生成氢氧化亚铁【Fe(OH)2】固体,该反应符号表达式:_______,属于_______反应(填基本反应类型)。
②实验过程中量筒中的液面不断下降,水被吸入瓶中,出现该现象的原因是_______。
21.某同学设计了实验装置测定空气中氧气的含量。
实验过程:
①检查装置的气密性,气密性良好;
(1)②在集气瓶里装进适量a 体积的水,燃烧匙里放一块白磷(40℃即可燃烧),按图示装置连接仪器,然后在酒精灯上把玻璃棒下端加热,玻璃棒的作用为___________;(注:集气瓶内的长导管已接近瓶底)
③(注:白磷与红磷燃烧的产物、现象均相同)
(2)④待集气瓶完全冷却至室温,量出集气瓶中水的体积是b,整个集气瓶的体积是c. 从白磷开始燃烧到最后熄灭的过程中,集气瓶内水面的变化情况是___________ ;
(3)⑤根据a、b、c三个数据,计算出空气中氧气的体积分数。已知c=60mL,a=10mL,b=___________mL。
实验反思:
(4)组内成员小张对“实验前集气瓶里要装进适量a 体积的水”非常不理解。咨询了组长小明之后,他终于明白“a 体积的水”的作用,其一是为了加快④步骤中集气瓶的冷却速度;其二则主要是___________。
(5)在上述实验中,下列操作的实施和实验现象的出现,会导致实验最后产生的实际值大于理论值的是___________。
A.装置气密性不好 B.实验前集气瓶里没有装a 体积的水
C.集气瓶没有冷却到室温 D.用红磷代替白磷(红磷的着火点在240℃左右)
四、计算题
22.已知碳-12原子的质量为1.993×10-26kg,A原子的质量为5.146×10-26kg,若A原子核内中子数为16个。求:(写出对应的计算过程)
(1)A原子的相对原子质量______。(保留整数)
(2)A原子的核外电子数_______。
23.如图是某省生产的某加钙食盐包装标签上的部分文字,请仔细阅读后回答问题:
包装标签上的钙含量是指________(单质/碳酸钙/钙元素)
为了测定此盐中的钙元素含量,取这种盐溶于水,加入足量的盐酸,生成二氧化碳,计算此加钙食盐中钙元素的质量分数.________
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.C
4.A
5.D
6.B
7.A
8.A
9.A
10.C
11.D
12.B
13.B
14.C
15.D
16.(1) A、B C 8 (2) 该元素的原子序数为20
17. (1) 金属 58 (2) 140.1
18.(1)③
(2)A
(3) 不相似 失去
(4) 3 Mg2+
19. (1) ① ②③ (2) 分子种类 (3) 湿衣服在阳光下比在阴凉处干得快
20.(1) >
(2) 化合 广口瓶中的氧气不断被消耗,压强不断减小
21.(1)点燃白磷
(2)先下降后上升
(3)20
(4)液封
(5)B
22.(1)解:A原子的相对原子质量为:
答:A的相对原子质量为31。
(2)解:因为相对原子质量=质子数+中子数
所以A的质子数为:31-16=15
因为在原子中质子数=核外电子数
所以A原子的核外电子数为15
答:A原子的核外电子数为15。
23.(1)钙元素(2)
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
