洛阳市2022-2023学年第一学期期中考试高二化学试卷(PDF无答案)
文档属性
| 名称 | 洛阳市2022-2023学年第一学期期中考试高二化学试卷(PDF无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-26 00:00:00 | ||
图片预览


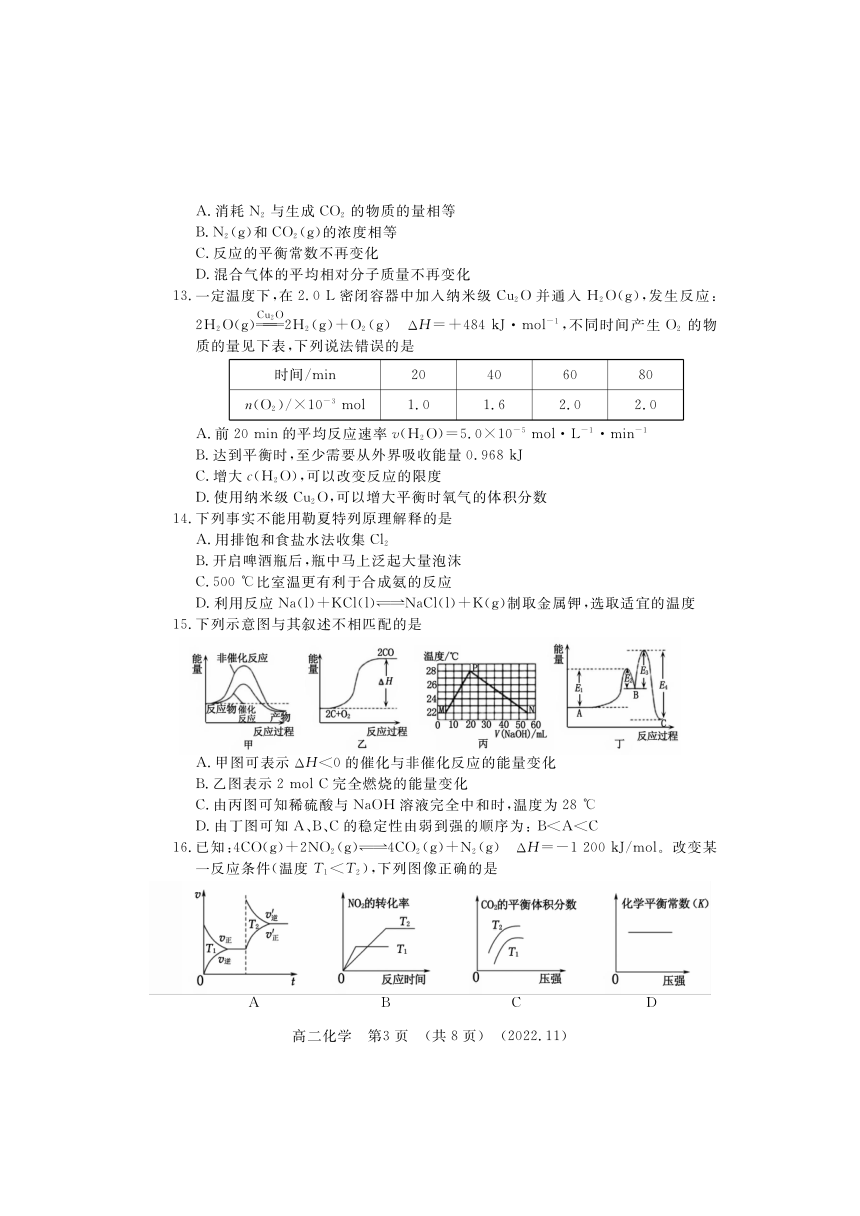
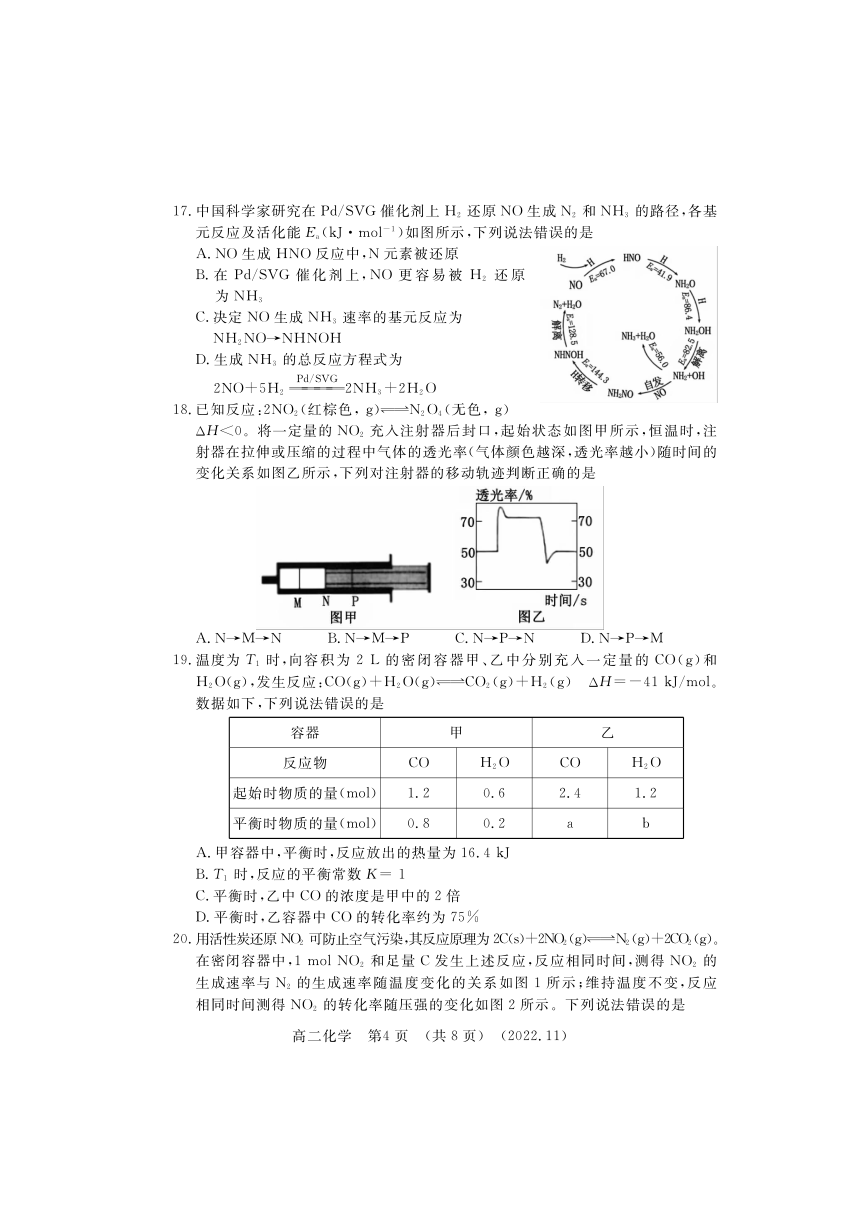
文档简介
洛阳市2022—2023学年第一学期期中考试
高二化学试卷
本试卷共100分,考试时间90分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考号填写在答题卡上。
2.考试结束,将答题卡交回。
本试卷可能用到的相对原子质量:H:1N:14
一、选择题(本题共10小题,每小题只有一个选项符合题意,每小题2分,共20分)
1.中国努力争取2060年前实现碳中和。下列做法不利于实现碳中和的是
A.大力开发和利用风能等清洁能源
B.加强二氧化碳的捕集和再利用
C.一定条件下将二氧化碳转为甲醇
D.用脱硫煤代替原料煤做燃料
2.下列做法的目的与改变化学反应速率无关的是
A.月饼包装内放置除氧剂
B.青香蕉和苹果放一起催熟
C.食盐中添加碘酸钾
D.红薯放在地窖中保存
3.下列反应的能量变化与示意图不相符的是
A.盐酸和碳酸氢钠的反应
B.灼热的炭与水蒸气的反应
液态水
C.生石灰与水的反应
化
D.工业上煅烧石灰石的反应
1g冰
4.下列热化学方程式正确的是
水的粲失状态变化时的烙变示意图
A.甲烷的燃烧热为△H=一890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:
CH (g)+202 (g)=CO2 (g)+2H2O(g)AH=-890.3 kJ/mol
B.500℃、30MPa下,将14gN2和3gH置于密闭容器中充分反应生成NH(g),
放热19.3kJ,其热化学方程式为N2(g)+3H2(g)一2NH(g》
△H=-38.6kJ/mol
C.已知H+(aq)+OH(ag)=H2O(1)△H=一57.3kJ/mol,则稀硫酸和稀
Ba(OH)2溶液反应的反应热△H=2×(-57.3)kJ/mol
D.25℃、101kPa下,1gH2燃烧生成液态水放热142.9kJ,其热化学方程式为
H,(g)+20.(g)=H,0)△H=-285.8k/mol
5.298K、l01kPa时,HCN(g)一HNC(g)异构化反应过程的能量变化如图所示。
下列说法正确的是
16s5
A.HNC比HCN稳定
B.正反应的活化能小于逆反应的活化能
,a3
C.该异构化反应的△H=+59.3kJ/mol
D.使用催化剂,可以改变反应的反应热
反应进和
高二化学第1页(共8页)(2022.11)
6.在气体反应中,能使反应物中活化分子数和活化分子百分数都增大的方法有
①增大反应物浓度②升高温度③增大压强④加入催化剂
A.①②③④
B.②④
C.②③
D.①②
7.在常温常压下,向FeCl溶液中滴入KSCN溶液,发生以下反应:FeCl+3KSCN
一Fe(SCN):+3KCI,所得溶液显红色。改变下列条件,能使平衡逆向移动的是
A.向溶液中加入少量NaC1晶体B.向溶液中加入少量水
C.向溶液中滴入数滴浓FeCl溶液D.向溶液中加入少量KCI固体
8.下列有关化学反应速率的说法中,正确的是
A.100mL2mol/L盐酸与锌反应时,加入少量NaC1溶液,生成氢气的速率不变
B.反应2CO+2NO一N2+2CO2,加入合适的催化剂,CO的生成速率和消耗速
率都加快
C.合成氨反应是一个放热反应,升高温度,正反应速率诚慢,逆反应速率加快
D.用铁片和稀硫酸反应制取氢气时,为加快反应速率可将稀硫酸改为浓硫酸
9.下列说法正确的是
A.自发进行的反应不需要任何条件,就可以发生反应
B.能够自发进行的反应一定是嫡增的过程
C.△H<0的反应均是自发进行的反应
D.△H<0、△S>0的反应在任何温度下都能自发进行
10.如下图所示为工业合成氨的流程图。下列说法错误的是
N2-
①净化N、H
②加压
③催化反应
④液化
NH
H2-
干燥
(2X10'Pa)
(500℃、催化剂)
分离
⑤N和H2
再循环
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.步骤③、④、⑤均有利于提高原料平衡的转化率
D.产品液氨除可生产化肥外,还可用作制冷剂
二、选择题(本题共10小题,每小题只有一个选项符合题意,每小题3分,共30分)
11.反应C→A十B(反应放热)分两步进行:①C→X(反应吸热);②X→A十B(反应放
热)。能正确表示总反应过程中能量变化的示意图是
能量个
能量个
能量
能量↑
A+B
A+B
A+B
反应过程
反应过程
反应过程
反应过程
A
B
C
D
12.利用活性炭涂层排气管处理NO气体:C(s)十2NO(g)=N2(g)十CO2(g)△H0
在绝热恒容密闭容器中,充人NO气体和适量碳粉,不能判断反应达到平衡状态的是
高二化学第2页(共8页)(2022.11)
高二化学试卷
本试卷共100分,考试时间90分钟。
注意事项:
1.答卷前,考生务必将自己的姓名、考号填写在答题卡上。
2.考试结束,将答题卡交回。
本试卷可能用到的相对原子质量:H:1N:14
一、选择题(本题共10小题,每小题只有一个选项符合题意,每小题2分,共20分)
1.中国努力争取2060年前实现碳中和。下列做法不利于实现碳中和的是
A.大力开发和利用风能等清洁能源
B.加强二氧化碳的捕集和再利用
C.一定条件下将二氧化碳转为甲醇
D.用脱硫煤代替原料煤做燃料
2.下列做法的目的与改变化学反应速率无关的是
A.月饼包装内放置除氧剂
B.青香蕉和苹果放一起催熟
C.食盐中添加碘酸钾
D.红薯放在地窖中保存
3.下列反应的能量变化与示意图不相符的是
A.盐酸和碳酸氢钠的反应
B.灼热的炭与水蒸气的反应
液态水
C.生石灰与水的反应
化
D.工业上煅烧石灰石的反应
1g冰
4.下列热化学方程式正确的是
水的粲失状态变化时的烙变示意图
A.甲烷的燃烧热为△H=一890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:
CH (g)+202 (g)=CO2 (g)+2H2O(g)AH=-890.3 kJ/mol
B.500℃、30MPa下,将14gN2和3gH置于密闭容器中充分反应生成NH(g),
放热19.3kJ,其热化学方程式为N2(g)+3H2(g)一2NH(g》
△H=-38.6kJ/mol
C.已知H+(aq)+OH(ag)=H2O(1)△H=一57.3kJ/mol,则稀硫酸和稀
Ba(OH)2溶液反应的反应热△H=2×(-57.3)kJ/mol
D.25℃、101kPa下,1gH2燃烧生成液态水放热142.9kJ,其热化学方程式为
H,(g)+20.(g)=H,0)△H=-285.8k/mol
5.298K、l01kPa时,HCN(g)一HNC(g)异构化反应过程的能量变化如图所示。
下列说法正确的是
16s5
A.HNC比HCN稳定
B.正反应的活化能小于逆反应的活化能
,a3
C.该异构化反应的△H=+59.3kJ/mol
D.使用催化剂,可以改变反应的反应热
反应进和
高二化学第1页(共8页)(2022.11)
6.在气体反应中,能使反应物中活化分子数和活化分子百分数都增大的方法有
①增大反应物浓度②升高温度③增大压强④加入催化剂
A.①②③④
B.②④
C.②③
D.①②
7.在常温常压下,向FeCl溶液中滴入KSCN溶液,发生以下反应:FeCl+3KSCN
一Fe(SCN):+3KCI,所得溶液显红色。改变下列条件,能使平衡逆向移动的是
A.向溶液中加入少量NaC1晶体B.向溶液中加入少量水
C.向溶液中滴入数滴浓FeCl溶液D.向溶液中加入少量KCI固体
8.下列有关化学反应速率的说法中,正确的是
A.100mL2mol/L盐酸与锌反应时,加入少量NaC1溶液,生成氢气的速率不变
B.反应2CO+2NO一N2+2CO2,加入合适的催化剂,CO的生成速率和消耗速
率都加快
C.合成氨反应是一个放热反应,升高温度,正反应速率诚慢,逆反应速率加快
D.用铁片和稀硫酸反应制取氢气时,为加快反应速率可将稀硫酸改为浓硫酸
9.下列说法正确的是
A.自发进行的反应不需要任何条件,就可以发生反应
B.能够自发进行的反应一定是嫡增的过程
C.△H<0的反应均是自发进行的反应
D.△H<0、△S>0的反应在任何温度下都能自发进行
10.如下图所示为工业合成氨的流程图。下列说法错误的是
N2-
①净化N、H
②加压
③催化反应
④液化
NH
H2-
干燥
(2X10'Pa)
(500℃、催化剂)
分离
⑤N和H2
再循环
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.步骤③、④、⑤均有利于提高原料平衡的转化率
D.产品液氨除可生产化肥外,还可用作制冷剂
二、选择题(本题共10小题,每小题只有一个选项符合题意,每小题3分,共30分)
11.反应C→A十B(反应放热)分两步进行:①C→X(反应吸热);②X→A十B(反应放
热)。能正确表示总反应过程中能量变化的示意图是
能量个
能量个
能量
能量↑
A+B
A+B
A+B
反应过程
反应过程
反应过程
反应过程
A
B
C
D
12.利用活性炭涂层排气管处理NO气体:C(s)十2NO(g)=N2(g)十CO2(g)△H0
在绝热恒容密闭容器中,充人NO气体和适量碳粉,不能判断反应达到平衡状态的是
高二化学第2页(共8页)(2022.11)
同课章节目录
