6.2 二氧化碳制取的研究(第2课时)课件--2022-2023学年九年级化学人教版上册(共17张PPT)
文档属性
| 名称 | 6.2 二氧化碳制取的研究(第2课时)课件--2022-2023学年九年级化学人教版上册(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-25 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
二氧化碳制取的研究
第2课时
01
了解常见固液常温型发生装置的优点
02
理解可以“控制反应发生和停止”装置的原理
学习目标
03
掌握多功能瓶的使用
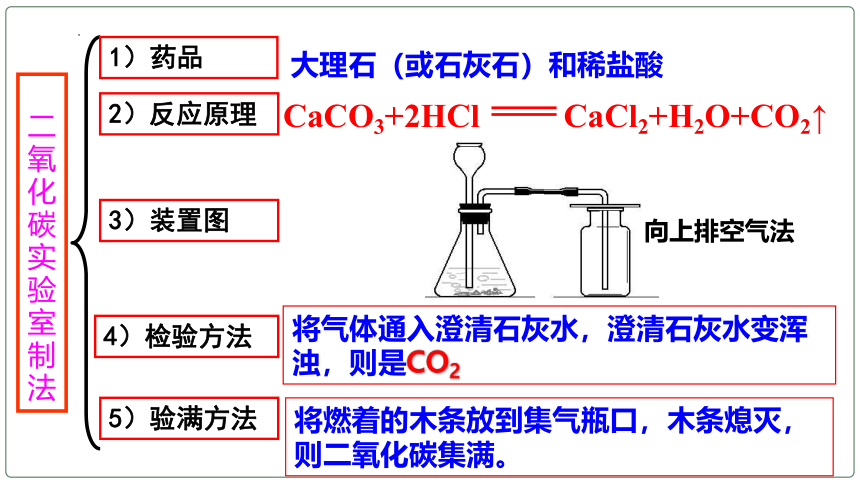
2)反应原理
3)装置图
4)检验方法
二氧化碳实验室制法
向上排空气法
将气体通入澄清石灰水,澄清石灰水变浑浊,则是CO2
5)验满方法
将燃着的木条放到集气瓶口,木条熄灭,则二氧化碳集满。
CaCO3+2HCl CaCl2+H2O+CO2↑
1)药品
大理石(或石灰石)和稀盐酸
五、实验室制取气体的思路
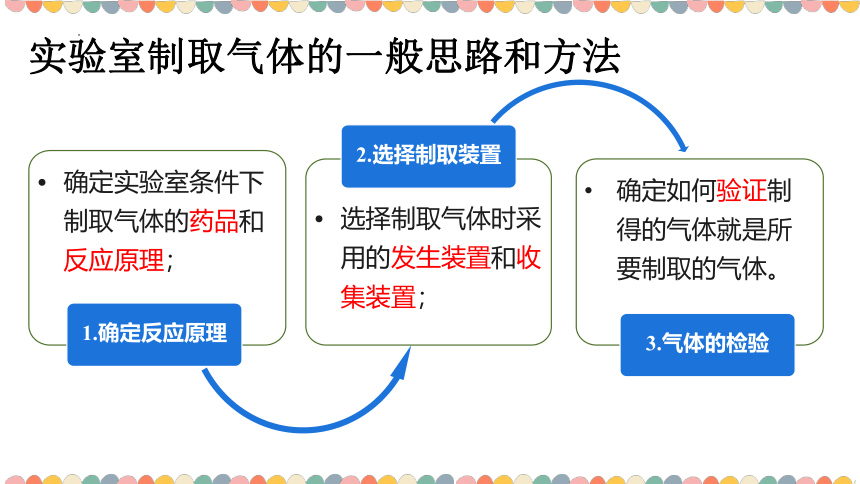
确定实验室条件下制取气体的药品和反应原理;
1.确定反应原理
选择制取气体时采用的发生装置和收集装置;
2.选择制取装置
确定如何验证制得的气体就是所要制取的气体。
3.气体的检验
实验室制取气体的一般思路和方法
工业制取CO2:
CaCO3高温CaO+CO2↑
工业上,煅烧石灰石可制得生石灰(CaO)和CO2。
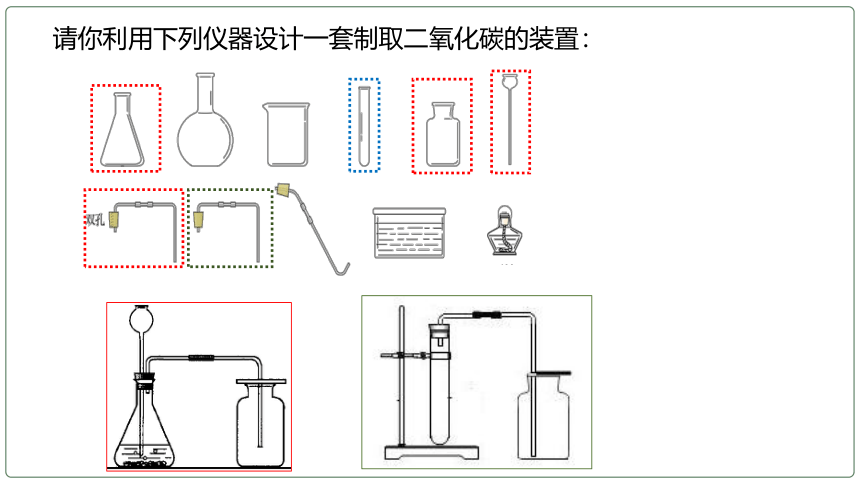
请你利用下列仪器设计一套制取二氧化碳的装置:
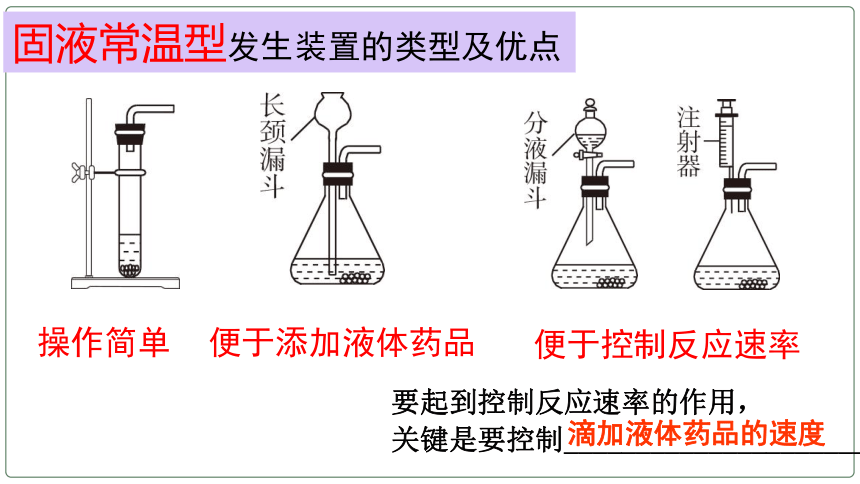
固液常温型发生装置的类型及优点
操作简单
便于添加液体药品
便于控制反应速率
要起到控制反应速率的作用,
关键是要控制________________________
滴加液体药品的速度
固液常温型发生装置的类型及优点
控制反应的发生和停止
关闭弹簧夹,观察到的现象是:
如果需要继续收集CO2,接下来的操作是:
长颈漏斗内液面 ,直至固体与液体 ,反应停止
上升
分离
打开弹簧夹
(放块状药品)
不能用铁制品,不能放粉末状固体
下列装置能否控制反应的发生和停止?
优点:便于控制反应的发生与停止
多功能瓶的应用
装置的用途
排空气法收集气体
排水法收集气体
洗气、干燥气体
如何才能将空气排出?
如何才能将水排出?
气体必须经过哪里才能办到?
1、排空气法收集气体
CO2
密度比空气大,如CO2 、O2
CO2
空气
密度比空气小,如NH3 、H2
H2
空气
如何才能将空气排出?
长进短出
短进长出
注意!
仪器变式:如果瓶子倒放,则在收集气体时,所有的进出气口也应该交换,
如CO2 、O2等气体应从短进长出;
而NH3 、H2等气体应从长进短出。
(或者下重上轻)
气体
水
气体(CO2、O2)
水
2.排水法收集气体(测量气体体积)
水的体积即为产生的气体体积。
待干燥气体
干燥后的气体
浓硫酸
试剂
3.洗气、干燥气体
A
B
D
1 . 实验室制取O2的发生装置应选____,收集装置应选_____。 2.氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应用 装置,收集氨气最好用 装置。
3.实验室制取CO2发生装置应选____,收集装置应选____。
A或B
D或E
F
A
B
D
E
F
考考你
C
甲烷(CH4)的实验室制法:用无水醋酸钠和碱石灰两种固体药品,经研磨均匀混合后装入装置中,加热后产生甲烷气体。甲烷是无色,无味,比空气轻,极难溶于水的气体。
①本实验的发生装置应选用____。
②甲烷气体可用________法收集。
4. 现有下列A、B、C、D、E五种实验装置:
A B C D E
A
C或E
二氧化碳制取的研究
第2课时
01
了解常见固液常温型发生装置的优点
02
理解可以“控制反应发生和停止”装置的原理
学习目标
03
掌握多功能瓶的使用
2)反应原理
3)装置图
4)检验方法
二氧化碳实验室制法
向上排空气法
将气体通入澄清石灰水,澄清石灰水变浑浊,则是CO2
5)验满方法
将燃着的木条放到集气瓶口,木条熄灭,则二氧化碳集满。
CaCO3+2HCl CaCl2+H2O+CO2↑
1)药品
大理石(或石灰石)和稀盐酸
五、实验室制取气体的思路
确定实验室条件下制取气体的药品和反应原理;
1.确定反应原理
选择制取气体时采用的发生装置和收集装置;
2.选择制取装置
确定如何验证制得的气体就是所要制取的气体。
3.气体的检验
实验室制取气体的一般思路和方法
工业制取CO2:
CaCO3高温CaO+CO2↑
工业上,煅烧石灰石可制得生石灰(CaO)和CO2。
请你利用下列仪器设计一套制取二氧化碳的装置:
固液常温型发生装置的类型及优点
操作简单
便于添加液体药品
便于控制反应速率
要起到控制反应速率的作用,
关键是要控制________________________
滴加液体药品的速度
固液常温型发生装置的类型及优点
控制反应的发生和停止
关闭弹簧夹,观察到的现象是:
如果需要继续收集CO2,接下来的操作是:
长颈漏斗内液面 ,直至固体与液体 ,反应停止
上升
分离
打开弹簧夹
(放块状药品)
不能用铁制品,不能放粉末状固体
下列装置能否控制反应的发生和停止?
优点:便于控制反应的发生与停止
多功能瓶的应用
装置的用途
排空气法收集气体
排水法收集气体
洗气、干燥气体
如何才能将空气排出?
如何才能将水排出?
气体必须经过哪里才能办到?
1、排空气法收集气体
CO2
密度比空气大,如CO2 、O2
CO2
空气
密度比空气小,如NH3 、H2
H2
空气
如何才能将空气排出?
长进短出
短进长出
注意!
仪器变式:如果瓶子倒放,则在收集气体时,所有的进出气口也应该交换,
如CO2 、O2等气体应从短进长出;
而NH3 、H2等气体应从长进短出。
(或者下重上轻)
气体
水
气体(CO2、O2)
水
2.排水法收集气体(测量气体体积)
水的体积即为产生的气体体积。
待干燥气体
干燥后的气体
浓硫酸
试剂
3.洗气、干燥气体
A
B
D
1 . 实验室制取O2的发生装置应选____,收集装置应选_____。 2.氨气极易溶于水,且密度比空气小,实验室常用加热固体硫酸铵和固体熟石灰的混合物来制取氨气,应用 装置,收集氨气最好用 装置。
3.实验室制取CO2发生装置应选____,收集装置应选____。
A或B
D或E
F
A
B
D
E
F
考考你
C
甲烷(CH4)的实验室制法:用无水醋酸钠和碱石灰两种固体药品,经研磨均匀混合后装入装置中,加热后产生甲烷气体。甲烷是无色,无味,比空气轻,极难溶于水的气体。
①本实验的发生装置应选用____。
②甲烷气体可用________法收集。
4. 现有下列A、B、C、D、E五种实验装置:
A B C D E
A
C或E
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
