人教版高中化学必修一《铝的氧化物和氢氧化物》课件(16张ppt)
文档属性
| 名称 | 人教版高中化学必修一《铝的氧化物和氢氧化物》课件(16张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 810.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2013-12-20 00:00:00 | ||
图片预览






文档简介
课件16张PPT。铝的氧化物和氢氧化物金属铝性质总结活泼金属通性:
1、与非金属反应:氧气、氯气
2、与酸反应:
3、与盐反应(置换反应)
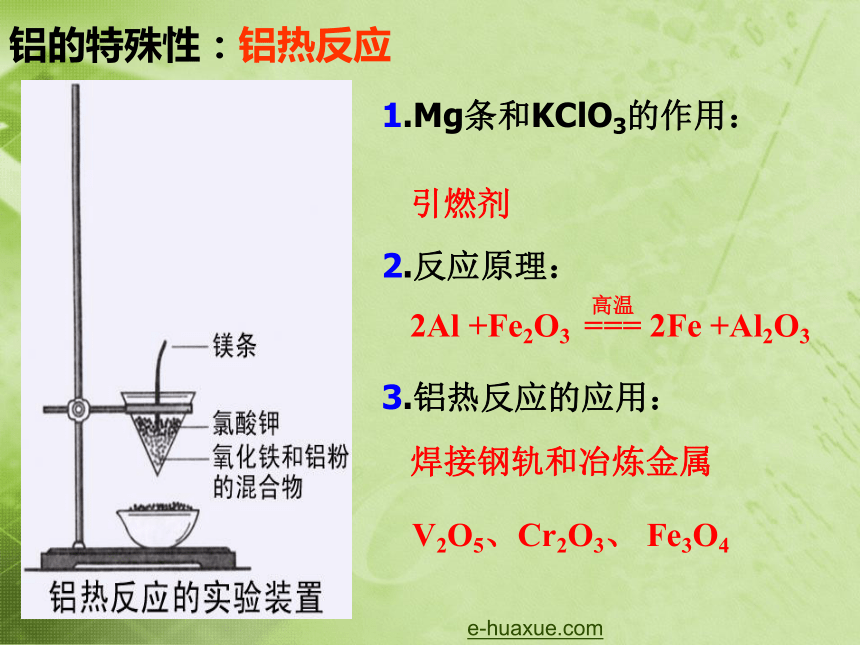
现象:发出耀眼的白光,放出大量的热用途:燃烧弹,信号弹,火箭推进剂2Al+6HCl = 2AlCl3+3H2↑2Al+3CuSO4=3Cu+Al2(SO4)3铝的特性:与碱反应取三支试管,分别加入相同长度的铁片,铝片,铜片(打磨后)。向试管中分别加入等量2mol/L的NaOH溶液,震荡,观察现象。1.Mg条和KClO3的作用:引燃剂3.铝热反应的应用:焊接钢轨和冶炼金属2.反应原理:铝的特殊性:铝热反应V2O5、Cr2O3、 Fe3O4e-huaxue.com 1.除去镁粉中混有的少量铝粉,可选
用下列溶液中的:
A 盐酸 B 硝酸
C 浓氢氧化钾溶液 D 氨水 A. Na+ B. Mg2+ C. S2- D.HCO3- 2.某无色透明的溶液,放入铝粉后有氢气
产生,则一定可以在该溶液中存在的离
子是:世界上最大的蓝宝石--“东方蓝巨人” 重达486.52克拉 估价为100到150万美元世界上最大的红宝石—卡门-露希娅 重达23.1克拉e-huaxue.com 蓝宝石中的极品--星光蓝宝石金色蓝宝石白色蓝宝石氧化铝(Al2O3)1.物理性质???
纯净氧化铝是白色无定形粉末,俗称矾土,密度3.9-4.0g/cm3,熔点2054℃,沸点2980℃,不溶于水 用途:电解法冶炼金属铝的原材料,可用作耐火材料,如:耐火坩埚、耐火管和耐高温实验仪器等。氧化铝难溶于水,却能溶于酸或强碱溶液,反应生成盐和水。与酸反应:Al2O3+6HCl=2AlCl3+3H2O与碱反应:Al2O3+2NaOH =2NaAlO2+H2O我们把Al2O3这样既能与酸反应又能与碱反应生成盐和水的氧化物称为两性氧化物思考桌面上有两堆白色粉末,已知它们分别是Al2O3和MgO,请问能用什么方法加以鉴别?操作:取两种白色粉末少量,分别放入两支小试管中,分别向试管中加入氢氧化钠(NaOH)溶液,观察现象现象、结论:白色固体溶解的是Al2O3,不能溶解的是MgO氢氧化铝 1.制备
2.物理性质
3.化学性质白色沉淀不断增多,而后沉淀逐渐溶解,最后完全消失白色沉淀不断增多,氨水过量沉淀不溶解Al2(SO4)3+6NaOH=
2Al(OH)3↓+3Na2SO4Al2(SO4)3+6NH3·H2O=
2Al(OH)3↓+3(NH4)2SO4Al(OH)3+NaOH=NaAlO2+H2O结论Al2(SO4)3与NaOH、NH3·H2O反应均能产生白色胶状沉淀Al(OH)3, Al(OH)3可溶于NaOH溶液,但不溶于氨水。2.实验室制Al(OH)3的方案(2)原理:(1)试剂:1.Al(OH)3的物理性质难溶于水的白色粉末实验总结 Al(OH)3既能溶于盐酸,又能溶于NaOH溶液,且产物均为盐和水,所以Al(OH)3是一种典型的两性氢氧化物。 既能与酸反应又能与碱反应且均能产生盐和水的氢氧化物,叫两性氢氧化物。白色沉淀消失白色沉淀消失Al(OH)3+3HCl=
AlCl3+3H2OAl(OH)3+NaOH=
NaAlO2+2H2O课堂练习下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②Al ③Al2O3 ④Al(OH)3
⑤AlCl3 ⑥CuO
A、②③④⑤ B、①③④⑥
C、①②③④ D、全部C
1、与非金属反应:氧气、氯气
2、与酸反应:
3、与盐反应(置换反应)
现象:发出耀眼的白光,放出大量的热用途:燃烧弹,信号弹,火箭推进剂2Al+6HCl = 2AlCl3+3H2↑2Al+3CuSO4=3Cu+Al2(SO4)3铝的特性:与碱反应取三支试管,分别加入相同长度的铁片,铝片,铜片(打磨后)。向试管中分别加入等量2mol/L的NaOH溶液,震荡,观察现象。1.Mg条和KClO3的作用:引燃剂3.铝热反应的应用:焊接钢轨和冶炼金属2.反应原理:铝的特殊性:铝热反应V2O5、Cr2O3、 Fe3O4e-huaxue.com 1.除去镁粉中混有的少量铝粉,可选
用下列溶液中的:
A 盐酸 B 硝酸
C 浓氢氧化钾溶液 D 氨水 A. Na+ B. Mg2+ C. S2- D.HCO3- 2.某无色透明的溶液,放入铝粉后有氢气
产生,则一定可以在该溶液中存在的离
子是:世界上最大的蓝宝石--“东方蓝巨人” 重达486.52克拉 估价为100到150万美元世界上最大的红宝石—卡门-露希娅 重达23.1克拉e-huaxue.com 蓝宝石中的极品--星光蓝宝石金色蓝宝石白色蓝宝石氧化铝(Al2O3)1.物理性质???
纯净氧化铝是白色无定形粉末,俗称矾土,密度3.9-4.0g/cm3,熔点2054℃,沸点2980℃,不溶于水 用途:电解法冶炼金属铝的原材料,可用作耐火材料,如:耐火坩埚、耐火管和耐高温实验仪器等。氧化铝难溶于水,却能溶于酸或强碱溶液,反应生成盐和水。与酸反应:Al2O3+6HCl=2AlCl3+3H2O与碱反应:Al2O3+2NaOH =2NaAlO2+H2O我们把Al2O3这样既能与酸反应又能与碱反应生成盐和水的氧化物称为两性氧化物思考桌面上有两堆白色粉末,已知它们分别是Al2O3和MgO,请问能用什么方法加以鉴别?操作:取两种白色粉末少量,分别放入两支小试管中,分别向试管中加入氢氧化钠(NaOH)溶液,观察现象现象、结论:白色固体溶解的是Al2O3,不能溶解的是MgO氢氧化铝 1.制备
2.物理性质
3.化学性质白色沉淀不断增多,而后沉淀逐渐溶解,最后完全消失白色沉淀不断增多,氨水过量沉淀不溶解Al2(SO4)3+6NaOH=
2Al(OH)3↓+3Na2SO4Al2(SO4)3+6NH3·H2O=
2Al(OH)3↓+3(NH4)2SO4Al(OH)3+NaOH=NaAlO2+H2O结论Al2(SO4)3与NaOH、NH3·H2O反应均能产生白色胶状沉淀Al(OH)3, Al(OH)3可溶于NaOH溶液,但不溶于氨水。2.实验室制Al(OH)3的方案(2)原理:(1)试剂:1.Al(OH)3的物理性质难溶于水的白色粉末实验总结 Al(OH)3既能溶于盐酸,又能溶于NaOH溶液,且产物均为盐和水,所以Al(OH)3是一种典型的两性氢氧化物。 既能与酸反应又能与碱反应且均能产生盐和水的氢氧化物,叫两性氢氧化物。白色沉淀消失白色沉淀消失Al(OH)3+3HCl=
AlCl3+3H2OAl(OH)3+NaOH=
NaAlO2+2H2O课堂练习下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②Al ③Al2O3 ④Al(OH)3
⑤AlCl3 ⑥CuO
A、②③④⑤ B、①③④⑥
C、①②③④ D、全部C
