【粤教版】化学九年级下册 7第7章溶液复习(课件共52页)
文档属性
| 名称 | 【粤教版】化学九年级下册 7第7章溶液复习(课件共52页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-29 00:00:00 | ||
图片预览










文档简介
(共52张PPT)
粤教版九年级下册
第七章 溶液
单元复习
1
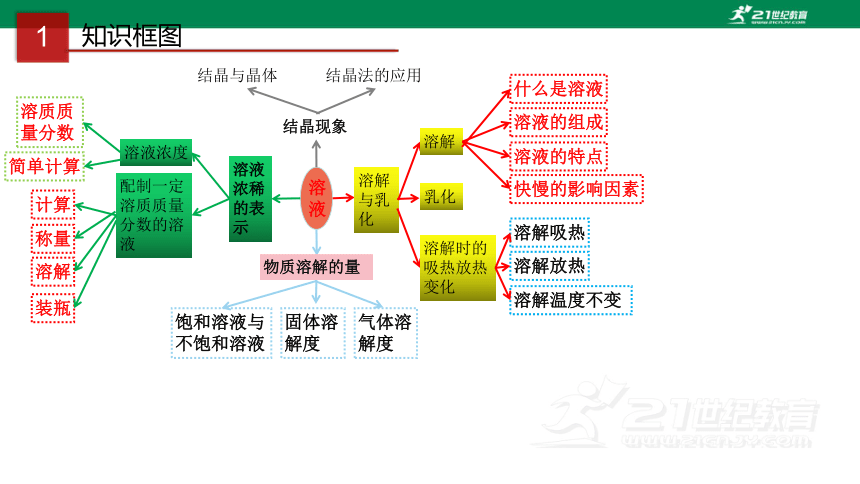
知识框图
溶液
溶解与乳化
溶解
溶解时的吸热放热变化
什么是溶液
溶液的组成
溶液的特点
快慢的影响因素
溶解吸热
溶解放热
溶解温度不变
物质溶解的量
溶液浓稀的表示
溶液浓度
配制一定溶质质量分数的溶液
溶质质量分数
简单计算
计算
称量
溶解
装瓶
结晶现象
结晶与晶体
结晶法的应用
乳化
饱和溶液与不饱和溶液
固体溶解度
气体溶解度
2
知识回顾
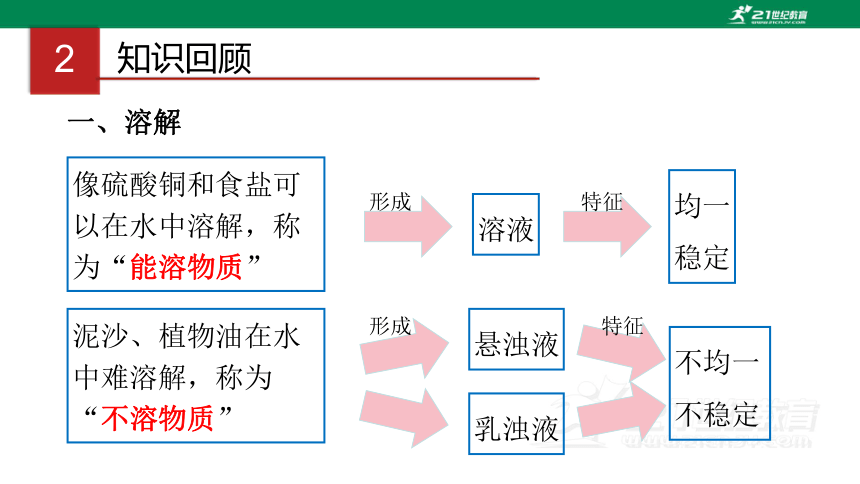
一、溶解
像硫酸铜和食盐可以在水中溶解,称为“能溶物质”
泥沙、植物油在水中难溶解,称为“不溶物质”
溶液
悬浊液
乳浊液
均一稳定
不均一不稳定
形成
形成
特征
特征
1.溶液
(1)概念:一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
(2)特点:
均一、稳定的混合物
颜色呢?
试举例?
含Cu2+的盐溶液:蓝色
含Fe2+的盐溶液:浅绿色
含Fe3+的盐溶液:黄色
体系 溶质 溶剂
气+液
固+液
液+液 无水
有水
气体
液体
固体
液体
量少
量多
非水物
水
溶液中溶质和溶剂的判断方法:
(3)组成:
溶质+溶剂
在通常情况下,水是最常用的溶剂。
(5)影响溶质溶解快慢的因素
_____________、 _____________________、 ____________能加快溶质在溶剂里的溶解。
温度升高
减小溶质颗粒
搅拌
(4)溶液命名:
XX 的 XX溶液
(溶质)
(溶剂)
如:蔗糖的水溶液或蔗糖溶液
像泥沙一样的不溶性固体小颗粒分散到水里形成的混浊液,称为悬浊液。
将油滴等不溶性小液滴分散到水里形成的混浊液,称为乳浊液。如牛奶、豆浆等。
悬浊液和乳浊液的共同特征:不均一、不稳定。
2.悬浊液和乳浊液
【典型例题1】下列溶液中,不是以水作溶剂的是( )
A.10g硝酸铵跟8g水组成的溶液
B.10g水跟8g硝酸铵组成的溶液
C.1g水跟9g酒精组成的溶液
D.100g酒精跟5g碘组成的溶液
考点一:溶解
D
【迁移训练1】下列关于溶液、悬浊液、乳浊液的说法:
①溶液一定是无色、均一、稳定、透明的液体;
②溶液中溶质可以有多种,但溶剂只有一种;
③溶液是纯净物,而浊液是混合物;
④酸溶液呈酸性,呈酸性的一定是酸溶液;
⑤植物油与水形成乳浊液,泥水是悬浊液;⑥饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液。
其中正确的个数有( )
A.2 B.3 C.4 D.5
A
二、溶质在溶解过程伴随的温度变化
吸收热量>放出热量,溶液温度降低 NH4NO3
吸收热量<放出热量,溶液温度升高 NaOH、CaO、浓硫酸
吸收热量=放出热量,溶液温度不变 NaCl等
1.溶质分子或离子的扩散过程(吸热)
2.溶质分子或离子的水合过程(放热)
溶解过程
【典型例题2】如图所示,向小试管中分别加入一定量的下列物质,右侧U形管中的液面右端明显下降,该物质可能是下列的( )
A.蔗糖 B.食盐
C.硝酸铵 D.氢氧化钠
C
考点二:溶质在溶解过程伴随的温度变化
【迁移训练2】将下列物质加入到水中,温度显著降低的是( )
A.NaCl B.CaO
C.NaOH D.NH4NO3
D
三、乳化
乳化与溶解的区别:
汽油:溶解衣物上的油污—溶解(物理变化)
洗涤剂:洗涤剂起乳化作用,能将衣物上大的油污分散成小液滴,小液滴随水流走—乳化(化学变化)
乳化剂:能使乳浊液稳定存在的物质(如洗涤剂等)。
乳化作用:乳化剂所起的作用叫做乳化作用。
【典型例题3】下列操作方法中,利用乳化作用的是( )
A.用食盐配制一定浓度的盐水
B.用汽油清洗油污
C.用煮沸软化硬水
D.用洗涤剂清洗油污
D
考点三:乳化
【迁移训练3】下列洗涤或除污过程应用乳化原理的是( )
A.用钢丝球刷除抄菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
D
四、饱和溶液与不饱和溶液
1.概念:在_________下,____________里,不能再溶解某溶质的溶液,叫作这种溶质的____溶液;还能继续溶解某溶质的溶液,叫作这种溶质的_______溶液。
不饱和
一定温度
一定量的溶剂
饱和
2.饱和溶液与不饱和溶液的判断方法
判断一定条件下某一溶液是不是某溶质的饱和溶液,是看该条件下溶液中_____________________。
是否能继续溶解该溶质
3.饱和溶液与不饱和溶液的相互转化
(1)对于大多数固体物质来说:
饱和溶液 不饱和溶液
①加溶剂;②升温
①加溶质;②降温;③蒸发溶剂
(2)特殊情况:
Ca(OH)2
饱和溶液
Ca(OH)2
不饱和溶液
①加水;②降温
①蒸发水;②升温;③加Ca(OH)2
4.饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
(1)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。
(2)在相同温度下,同种溶质的饱和溶液一定比不饱和溶液浓,也就是说,饱和溶液一定是该物质在该温度下最浓的溶液。
【典型例题4】在一定温度下,向盛有饱和KNO3溶液的烧杯中加入少量NaCl固体后,下列说法正确的是( )
A.所加的NaCl固体不溶解
B.KNO3的溶解度不变
C.KNO3溶液的溶质质量分数不变
D.降温结晶后剩余溶液为KNO3的不饱和溶液
B
考点四:饱和溶液与不饱和溶液
【迁移训练4】要将室温下一瓶接近饱和的石灰水(溶质为氢氧化钙)变成饱和溶液,小乐选择了如下方法:
①加入水;②加入氢氧化钙固体;③降低温度;④升高温度。
其中可行的是( )
A.②③ B.②④ C.①②③ D.①②④
B
(1)固体物质的溶解度是指在一定温度下,某固体物质在100g溶剂(通常为水)里达到饱和状态时所溶解的质量。
1.固体溶解度
(2)溶解度四要素
条件:
标准:
溶液状态:
单位:
一定温度
100克溶剂(一般指水)
饱和状态
质量(克)
五、溶解度
(3)溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 (20℃) >____ g 1~10 g 0.01~1 g <0.01 g
10
(4)溶解度曲线
用纵坐标表示溶解度,横坐标表示温度,根据某物质在不同温度时的溶解度,可以画出该物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
溶解度曲线 应 用
1.可知该物质在任一温度下的溶解度数值;
2.可比较同一温度下,不同溶质的溶解度大小;
3.交点M的意义:在t1℃时,A、B两种溶液的溶解度相等,均为 s1 g;
4.可比较不同的溶解度受温度影响的大小,曲线越陡,表示该溶质受温度影响越大;
5.处于曲线上任一点,表示该溶液处于饱和状态;处于曲线下方任一点,表示该溶液处于不饱和状态。处于曲线上方任一点,表示该溶液处于饱和状态且有剩余固体;
S (g)
t(℃)
S1
M
A
B
t1
2.气体溶解度
(1)定义:在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)气体溶解度的五要素:
①压强为101kPa ②一定温度 ③1体积水 ④达到饱和 ⑤气体的体积
(3)气体溶解度的影响因素:
①压强。压强大,溶解气体多。
②温度。温度高,溶解少
【典型例题5】在20℃时,100g水中最多可溶解A物质50g;在60℃时,100g水中最多可溶解B物质100g,则A、B 两种物质的溶解度大小比较为( )
A.无法比较 B.A=B
C.A<B D.A>B
A
考点五:溶解度
【迁移训练5-1】下列措施能使氯化钾在水中的溶解度增大的是( )
A.增加水的质量
B.增加氯化钾的质量
C.升高溶液的温度
D.把氯化钾粉碎,在溶解过程中不断搅拌
C
【迁移训练5-2】甲乙丙三种物质均不含结晶水,溶解度曲线如图所示,下列分析错误的是( )
A.将甲中A点变成B点可采用恒温蒸发溶剂的方法
B.将A点降温到t1℃甲、乙、丙均变为不饱和溶液
C.t2℃时,甲、乙、丙饱和溶液中,丙质量分数最大
D.甲中含有杂质乙,可采用加水溶解、蒸发浓缩、冷却结晶、过滤的方法提纯甲
B
【迁移训练5-3】打开汽水瓶盖后,有大量气泡冒出,下列说法正确的是( )
A.溶解度增大了
B.瓶内压强变小了
C.等气泡不再冒出时,二氧化碳已全部逸出
D.饱和溶液变成不饱和溶液
B
溶质质量
溶液质量
×100%
溶质的质量分数=
或=
溶质质量
溶质质量+溶剂质量
×100%
六、溶质的质量分数
1.定义:溶质的质量与溶液的质量之比。(通常以百分数表示)
2.计算公式
3.有关溶质质量分数的简单计算
(1)配制一定量的某一组成的溶液,求所需溶质和溶剂的量
(2)有关溶液稀释的计算
计算依据:稀释前后________的质量不变。
溶质
注意:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。
(3)有关化学方程式的计算
【典型例题6】现有100mL 20%的硫酸,其密度为1.14g/cm3,下列说法正确的是( )
A.该溶液含溶质20 g
B.该溶液中,溶质质量:溶液质量=1:6
C.该溶液中,溶质质量:溶剂质量=1:5
D.该溶液中,溶液质量:溶剂质量=5:4
D
考点六:溶质的质量分数
【迁移训练6-1】下列条件下的氢氧化钙溶液,溶质质量分数最大的是( )
A.80℃的饱和溶液 B.20℃的饱和溶液
C.80℃不饱和溶液 D.20℃的不饱和溶液
B
【迁移训练6-2】食盐在20℃时溶解度为36克,下列操作可以实现目的是( )
A.将100克15%的食盐溶液蒸发掉50克水,使溶液中食盐的质量分数达到30%
B.向50克5%的食盐溶液中加入5克食盐,使溶液中食盐的质量分数达到10%
C.向100克15%的食盐溶液中加入10克食盐,使溶液中食盐的质量分数达到25%
D.将50克5%的食盐溶液蒸发掉25克水,使溶液中食盐的质量分数达到10%
D
【迁移训练6-3】汽车、电动车一般使用铅酸蓄电池,某铅酸蓄电池用的是28%的稀硫酸,现要用1.0kg98%的浓硫酸配制该稀硫酸,则需加水( )
A.0.5kg B.1.5kg C.2.5kg D.3.5kg
C
七、配制一定溶质质量分数溶液
仪器:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
步骤:
计算
称量
溶解
装入试剂瓶
1.直接配制
2.用较浓的溶液的稀释配制:
仪器:量筒、胶头滴管、烧杯、玻璃棒
步骤:
计算
量取
稀释
装入试剂瓶
3.误差分析:
(1)所配溶液溶质质量分数偏小
凡是能导致溶质质量偏小或溶剂质量偏大的均可以导致所配溶液溶质质量分数偏小;
如:烧杯不干燥或烧杯有水;量筒中的液体溶质未全部倒出;药品和砝码放颠倒了(使用了游码);向烧杯转移固体溶质时,有一部分溶质撒落烧杯外;或药品不纯等。
(2)所配溶液溶质质量分数偏大
凡是能导致溶质质量偏大或溶剂质量偏小的均可以导致所配溶液溶质质量分数偏小;如①称量时,所用砝码已生锈或沾有油污;②量取溶剂时,俯视读量筒刻度。
【典型例题7】小明在实验操作技能考试中抽中的题目是“用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液”。他的有关做做法正确的是( )
A.用20mL量筒量取所需水的体积
B.用内壁附有水球的烧杯配制溶液
C.氯化钠直接放在天平左盘上称量3.0g
D.选择的玻璃仪器有烧杯、玻璃棒、胶头滴管、试剂瓶
D
考点七:配制一定溶质质量分数溶液
【迁移训练7-1】下列是“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
C
【迁移训练7-2】配制130g溶质质量分数为6%的氯化钠溶液时,下列操作会导致结果偏大的是( )
①称量的氯化钠固体中含有不溶性杂质;
②用量简量取水时俯视读数:
③将氯化钠固体放在托盘天平的右盘称量;
④往烧杯中加水时有水洒出;
⑤转移配好的溶液时有少量溅出。
A.②③ B.①④ C.②④ D.③⑤
C
八、结晶现象
1.晶体与结晶
(1)晶体:晶体一般有_______________,有________的熔、沸点。
(2)结晶:形成晶体的过程。晶体可由________溶液形成,析出晶体后的溶液是________溶液。
规则的几何形状
固定
饱和
饱和
(3)从溶液中析出晶体常用的两种方法
冷却结晶法(即冷却热饱和溶液)——一般适用于溶解度随降温改变________的溶质。
蒸发溶剂结晶法(即恒温蒸发溶剂)——一般适用于溶解度随温度变化改变________的溶质。
明显
不明显
2.结晶法的应用——粗盐的提纯
(1)目的:除去粗盐中________的杂质。
(2)步骤
难溶性
①溶解
a.仪器:__________、__________。
b.玻璃棒搅拌的作用:_________________________。
②过滤
a.过滤器组成:漏斗和滤纸。
b.过滤操作所用的仪器:______、烧杯、________、漏斗。
烧杯
玻璃棒
加速粗盐的溶解
铁架台
玻璃棒
c.过滤操作中玻璃棒的作用:____________。
d.操作要领:“一贴、二低、三靠”。即:“一贴”指________紧贴在漏斗内壁上;“二低”指____________低于漏斗边缘,________低于滤纸边缘;“三靠”指盛液烧杯口紧靠在倾斜的玻璃棒中部,________斜靠在三层滤纸一边,__________紧靠接液烧杯内壁。
e.适用范围:可用于把______态和______态的混合物分离。
引流液体
滤纸
滤纸边缘
液面
玻璃棒
漏斗下端
固
液
③蒸发
a.仪器:________、__________、__________、__________。
b.玻璃棒搅拌的作用:________________________________。
c.操作要领:当蒸发皿中出现________________时停止加热。
d.固体食盐洗涤
铁架台
酒精灯
蒸发皿
玻璃棒
防止由于局部温度过高造成液滴飞溅
较多量固体
(3)
【典型例题8】在20℃时,某固体物质(不含结晶水)的水溶液,经历如图变化
下列说法你认为正确的( )
A.溶液甲可能是饱和溶液
B.溶液丙若蒸发10g水,析出的晶体的质量是6g
C.该物质的溶解度是40g
D.溶液溶质质量分数:甲<乙=丙
D
考点八:结晶现象
【迁移训练8-1】下列关于溶液的说法正确的是( )
A.饱和溶液析出晶体后,其溶质的质量分数可能不变
B.在冰雪路面上撒食盐,可以加速冰雪的融化,其融雪的原理是NaCl降低了水的凝固点
C.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
D.用汽油除去衣服上的油污的原理是乳化作用
A
【迁移训练8-2】小吴在“粗盐提纯”实验考核时,完成了系列操作,如下几步操作中老师只给了一步正确的分,这一步是( )
A.过滤时玻璃棒靠在单层滤纸的一边
B.过滤时用玻璃棒对漏斗中液体搅拌
C.蒸发时对蒸发皿中的液体搅拌
D.蒸发时等到全部水蒸发完后再停止加热
C
【迁移训练8-3】粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
C
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
粤教版九年级下册
第七章 溶液
单元复习
1
知识框图
溶液
溶解与乳化
溶解
溶解时的吸热放热变化
什么是溶液
溶液的组成
溶液的特点
快慢的影响因素
溶解吸热
溶解放热
溶解温度不变
物质溶解的量
溶液浓稀的表示
溶液浓度
配制一定溶质质量分数的溶液
溶质质量分数
简单计算
计算
称量
溶解
装瓶
结晶现象
结晶与晶体
结晶法的应用
乳化
饱和溶液与不饱和溶液
固体溶解度
气体溶解度
2
知识回顾
一、溶解
像硫酸铜和食盐可以在水中溶解,称为“能溶物质”
泥沙、植物油在水中难溶解,称为“不溶物质”
溶液
悬浊液
乳浊液
均一稳定
不均一不稳定
形成
形成
特征
特征
1.溶液
(1)概念:一种或几种物质分散到另一种物质里,形成的均一、稳定的混合物。
(2)特点:
均一、稳定的混合物
颜色呢?
试举例?
含Cu2+的盐溶液:蓝色
含Fe2+的盐溶液:浅绿色
含Fe3+的盐溶液:黄色
体系 溶质 溶剂
气+液
固+液
液+液 无水
有水
气体
液体
固体
液体
量少
量多
非水物
水
溶液中溶质和溶剂的判断方法:
(3)组成:
溶质+溶剂
在通常情况下,水是最常用的溶剂。
(5)影响溶质溶解快慢的因素
_____________、 _____________________、 ____________能加快溶质在溶剂里的溶解。
温度升高
减小溶质颗粒
搅拌
(4)溶液命名:
XX 的 XX溶液
(溶质)
(溶剂)
如:蔗糖的水溶液或蔗糖溶液
像泥沙一样的不溶性固体小颗粒分散到水里形成的混浊液,称为悬浊液。
将油滴等不溶性小液滴分散到水里形成的混浊液,称为乳浊液。如牛奶、豆浆等。
悬浊液和乳浊液的共同特征:不均一、不稳定。
2.悬浊液和乳浊液
【典型例题1】下列溶液中,不是以水作溶剂的是( )
A.10g硝酸铵跟8g水组成的溶液
B.10g水跟8g硝酸铵组成的溶液
C.1g水跟9g酒精组成的溶液
D.100g酒精跟5g碘组成的溶液
考点一:溶解
D
【迁移训练1】下列关于溶液、悬浊液、乳浊液的说法:
①溶液一定是无色、均一、稳定、透明的液体;
②溶液中溶质可以有多种,但溶剂只有一种;
③溶液是纯净物,而浊液是混合物;
④酸溶液呈酸性,呈酸性的一定是酸溶液;
⑤植物油与水形成乳浊液,泥水是悬浊液;⑥饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液。
其中正确的个数有( )
A.2 B.3 C.4 D.5
A
二、溶质在溶解过程伴随的温度变化
吸收热量>放出热量,溶液温度降低 NH4NO3
吸收热量<放出热量,溶液温度升高 NaOH、CaO、浓硫酸
吸收热量=放出热量,溶液温度不变 NaCl等
1.溶质分子或离子的扩散过程(吸热)
2.溶质分子或离子的水合过程(放热)
溶解过程
【典型例题2】如图所示,向小试管中分别加入一定量的下列物质,右侧U形管中的液面右端明显下降,该物质可能是下列的( )
A.蔗糖 B.食盐
C.硝酸铵 D.氢氧化钠
C
考点二:溶质在溶解过程伴随的温度变化
【迁移训练2】将下列物质加入到水中,温度显著降低的是( )
A.NaCl B.CaO
C.NaOH D.NH4NO3
D
三、乳化
乳化与溶解的区别:
汽油:溶解衣物上的油污—溶解(物理变化)
洗涤剂:洗涤剂起乳化作用,能将衣物上大的油污分散成小液滴,小液滴随水流走—乳化(化学变化)
乳化剂:能使乳浊液稳定存在的物质(如洗涤剂等)。
乳化作用:乳化剂所起的作用叫做乳化作用。
【典型例题3】下列操作方法中,利用乳化作用的是( )
A.用食盐配制一定浓度的盐水
B.用汽油清洗油污
C.用煮沸软化硬水
D.用洗涤剂清洗油污
D
考点三:乳化
【迁移训练3】下列洗涤或除污过程应用乳化原理的是( )
A.用钢丝球刷除抄菜锅上的污垢
B.用酒精除去衣服上的碘
C.用汽油除去衣服上的油污
D.用洗洁精洗去餐具上的油脂
D
四、饱和溶液与不饱和溶液
1.概念:在_________下,____________里,不能再溶解某溶质的溶液,叫作这种溶质的____溶液;还能继续溶解某溶质的溶液,叫作这种溶质的_______溶液。
不饱和
一定温度
一定量的溶剂
饱和
2.饱和溶液与不饱和溶液的判断方法
判断一定条件下某一溶液是不是某溶质的饱和溶液,是看该条件下溶液中_____________________。
是否能继续溶解该溶质
3.饱和溶液与不饱和溶液的相互转化
(1)对于大多数固体物质来说:
饱和溶液 不饱和溶液
①加溶剂;②升温
①加溶质;②降温;③蒸发溶剂
(2)特殊情况:
Ca(OH)2
饱和溶液
Ca(OH)2
不饱和溶液
①加水;②降温
①蒸发水;②升温;③加Ca(OH)2
4.饱和溶液、不饱和溶液与浓溶液、稀溶液的关系
(1)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液。
(2)在相同温度下,同种溶质的饱和溶液一定比不饱和溶液浓,也就是说,饱和溶液一定是该物质在该温度下最浓的溶液。
【典型例题4】在一定温度下,向盛有饱和KNO3溶液的烧杯中加入少量NaCl固体后,下列说法正确的是( )
A.所加的NaCl固体不溶解
B.KNO3的溶解度不变
C.KNO3溶液的溶质质量分数不变
D.降温结晶后剩余溶液为KNO3的不饱和溶液
B
考点四:饱和溶液与不饱和溶液
【迁移训练4】要将室温下一瓶接近饱和的石灰水(溶质为氢氧化钙)变成饱和溶液,小乐选择了如下方法:
①加入水;②加入氢氧化钙固体;③降低温度;④升高温度。
其中可行的是( )
A.②③ B.②④ C.①②③ D.①②④
B
(1)固体物质的溶解度是指在一定温度下,某固体物质在100g溶剂(通常为水)里达到饱和状态时所溶解的质量。
1.固体溶解度
(2)溶解度四要素
条件:
标准:
溶液状态:
单位:
一定温度
100克溶剂(一般指水)
饱和状态
质量(克)
五、溶解度
(3)溶解度与溶解性的关系
溶解性 易溶 可溶 微溶 难溶
溶解度 (20℃) >____ g 1~10 g 0.01~1 g <0.01 g
10
(4)溶解度曲线
用纵坐标表示溶解度,横坐标表示温度,根据某物质在不同温度时的溶解度,可以画出该物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
溶解度曲线 应 用
1.可知该物质在任一温度下的溶解度数值;
2.可比较同一温度下,不同溶质的溶解度大小;
3.交点M的意义:在t1℃时,A、B两种溶液的溶解度相等,均为 s1 g;
4.可比较不同的溶解度受温度影响的大小,曲线越陡,表示该溶质受温度影响越大;
5.处于曲线上任一点,表示该溶液处于饱和状态;处于曲线下方任一点,表示该溶液处于不饱和状态。处于曲线上方任一点,表示该溶液处于饱和状态且有剩余固体;
S (g)
t(℃)
S1
M
A
B
t1
2.气体溶解度
(1)定义:在压强为101KPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)气体溶解度的五要素:
①压强为101kPa ②一定温度 ③1体积水 ④达到饱和 ⑤气体的体积
(3)气体溶解度的影响因素:
①压强。压强大,溶解气体多。
②温度。温度高,溶解少
【典型例题5】在20℃时,100g水中最多可溶解A物质50g;在60℃时,100g水中最多可溶解B物质100g,则A、B 两种物质的溶解度大小比较为( )
A.无法比较 B.A=B
C.A<B D.A>B
A
考点五:溶解度
【迁移训练5-1】下列措施能使氯化钾在水中的溶解度增大的是( )
A.增加水的质量
B.增加氯化钾的质量
C.升高溶液的温度
D.把氯化钾粉碎,在溶解过程中不断搅拌
C
【迁移训练5-2】甲乙丙三种物质均不含结晶水,溶解度曲线如图所示,下列分析错误的是( )
A.将甲中A点变成B点可采用恒温蒸发溶剂的方法
B.将A点降温到t1℃甲、乙、丙均变为不饱和溶液
C.t2℃时,甲、乙、丙饱和溶液中,丙质量分数最大
D.甲中含有杂质乙,可采用加水溶解、蒸发浓缩、冷却结晶、过滤的方法提纯甲
B
【迁移训练5-3】打开汽水瓶盖后,有大量气泡冒出,下列说法正确的是( )
A.溶解度增大了
B.瓶内压强变小了
C.等气泡不再冒出时,二氧化碳已全部逸出
D.饱和溶液变成不饱和溶液
B
溶质质量
溶液质量
×100%
溶质的质量分数=
或=
溶质质量
溶质质量+溶剂质量
×100%
六、溶质的质量分数
1.定义:溶质的质量与溶液的质量之比。(通常以百分数表示)
2.计算公式
3.有关溶质质量分数的简单计算
(1)配制一定量的某一组成的溶液,求所需溶质和溶剂的量
(2)有关溶液稀释的计算
计算依据:稀释前后________的质量不变。
溶质
注意:溶液是混合物,溶液的质量不能直接代入化学方程式中计算,必须换算成溶质的质量。
(3)有关化学方程式的计算
【典型例题6】现有100mL 20%的硫酸,其密度为1.14g/cm3,下列说法正确的是( )
A.该溶液含溶质20 g
B.该溶液中,溶质质量:溶液质量=1:6
C.该溶液中,溶质质量:溶剂质量=1:5
D.该溶液中,溶液质量:溶剂质量=5:4
D
考点六:溶质的质量分数
【迁移训练6-1】下列条件下的氢氧化钙溶液,溶质质量分数最大的是( )
A.80℃的饱和溶液 B.20℃的饱和溶液
C.80℃不饱和溶液 D.20℃的不饱和溶液
B
【迁移训练6-2】食盐在20℃时溶解度为36克,下列操作可以实现目的是( )
A.将100克15%的食盐溶液蒸发掉50克水,使溶液中食盐的质量分数达到30%
B.向50克5%的食盐溶液中加入5克食盐,使溶液中食盐的质量分数达到10%
C.向100克15%的食盐溶液中加入10克食盐,使溶液中食盐的质量分数达到25%
D.将50克5%的食盐溶液蒸发掉25克水,使溶液中食盐的质量分数达到10%
D
【迁移训练6-3】汽车、电动车一般使用铅酸蓄电池,某铅酸蓄电池用的是28%的稀硫酸,现要用1.0kg98%的浓硫酸配制该稀硫酸,则需加水( )
A.0.5kg B.1.5kg C.2.5kg D.3.5kg
C
七、配制一定溶质质量分数溶液
仪器:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒
步骤:
计算
称量
溶解
装入试剂瓶
1.直接配制
2.用较浓的溶液的稀释配制:
仪器:量筒、胶头滴管、烧杯、玻璃棒
步骤:
计算
量取
稀释
装入试剂瓶
3.误差分析:
(1)所配溶液溶质质量分数偏小
凡是能导致溶质质量偏小或溶剂质量偏大的均可以导致所配溶液溶质质量分数偏小;
如:烧杯不干燥或烧杯有水;量筒中的液体溶质未全部倒出;药品和砝码放颠倒了(使用了游码);向烧杯转移固体溶质时,有一部分溶质撒落烧杯外;或药品不纯等。
(2)所配溶液溶质质量分数偏大
凡是能导致溶质质量偏大或溶剂质量偏小的均可以导致所配溶液溶质质量分数偏小;如①称量时,所用砝码已生锈或沾有油污;②量取溶剂时,俯视读量筒刻度。
【典型例题7】小明在实验操作技能考试中抽中的题目是“用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液”。他的有关做做法正确的是( )
A.用20mL量筒量取所需水的体积
B.用内壁附有水球的烧杯配制溶液
C.氯化钠直接放在天平左盘上称量3.0g
D.选择的玻璃仪器有烧杯、玻璃棒、胶头滴管、试剂瓶
D
考点七:配制一定溶质质量分数溶液
【迁移训练7-1】下列是“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
C
【迁移训练7-2】配制130g溶质质量分数为6%的氯化钠溶液时,下列操作会导致结果偏大的是( )
①称量的氯化钠固体中含有不溶性杂质;
②用量简量取水时俯视读数:
③将氯化钠固体放在托盘天平的右盘称量;
④往烧杯中加水时有水洒出;
⑤转移配好的溶液时有少量溅出。
A.②③ B.①④ C.②④ D.③⑤
C
八、结晶现象
1.晶体与结晶
(1)晶体:晶体一般有_______________,有________的熔、沸点。
(2)结晶:形成晶体的过程。晶体可由________溶液形成,析出晶体后的溶液是________溶液。
规则的几何形状
固定
饱和
饱和
(3)从溶液中析出晶体常用的两种方法
冷却结晶法(即冷却热饱和溶液)——一般适用于溶解度随降温改变________的溶质。
蒸发溶剂结晶法(即恒温蒸发溶剂)——一般适用于溶解度随温度变化改变________的溶质。
明显
不明显
2.结晶法的应用——粗盐的提纯
(1)目的:除去粗盐中________的杂质。
(2)步骤
难溶性
①溶解
a.仪器:__________、__________。
b.玻璃棒搅拌的作用:_________________________。
②过滤
a.过滤器组成:漏斗和滤纸。
b.过滤操作所用的仪器:______、烧杯、________、漏斗。
烧杯
玻璃棒
加速粗盐的溶解
铁架台
玻璃棒
c.过滤操作中玻璃棒的作用:____________。
d.操作要领:“一贴、二低、三靠”。即:“一贴”指________紧贴在漏斗内壁上;“二低”指____________低于漏斗边缘,________低于滤纸边缘;“三靠”指盛液烧杯口紧靠在倾斜的玻璃棒中部,________斜靠在三层滤纸一边,__________紧靠接液烧杯内壁。
e.适用范围:可用于把______态和______态的混合物分离。
引流液体
滤纸
滤纸边缘
液面
玻璃棒
漏斗下端
固
液
③蒸发
a.仪器:________、__________、__________、__________。
b.玻璃棒搅拌的作用:________________________________。
c.操作要领:当蒸发皿中出现________________时停止加热。
d.固体食盐洗涤
铁架台
酒精灯
蒸发皿
玻璃棒
防止由于局部温度过高造成液滴飞溅
较多量固体
(3)
【典型例题8】在20℃时,某固体物质(不含结晶水)的水溶液,经历如图变化
下列说法你认为正确的( )
A.溶液甲可能是饱和溶液
B.溶液丙若蒸发10g水,析出的晶体的质量是6g
C.该物质的溶解度是40g
D.溶液溶质质量分数:甲<乙=丙
D
考点八:结晶现象
【迁移训练8-1】下列关于溶液的说法正确的是( )
A.饱和溶液析出晶体后,其溶质的质量分数可能不变
B.在冰雪路面上撒食盐,可以加速冰雪的融化,其融雪的原理是NaCl降低了水的凝固点
C.同种溶质的饱和溶液,一定比它的不饱和溶液的溶质质量分数大
D.用汽油除去衣服上的油污的原理是乳化作用
A
【迁移训练8-2】小吴在“粗盐提纯”实验考核时,完成了系列操作,如下几步操作中老师只给了一步正确的分,这一步是( )
A.过滤时玻璃棒靠在单层滤纸的一边
B.过滤时用玻璃棒对漏斗中液体搅拌
C.蒸发时对蒸发皿中的液体搅拌
D.蒸发时等到全部水蒸发完后再停止加热
C
【迁移训练8-3】粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
C
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
