化学人教版(2019)必修第一册2.2.2氯气实验室制法及氯离子的检验(共59张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册2.2.2氯气实验室制法及氯离子的检验(共59张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-29 00:00:00 | ||
图片预览










文档简介
(共59张PPT)
第2课时 氯气实验室制法及氯离子的检验
【课程标准】
1.了解实验室制取Cl2的原理和实验装置。
2.掌握Cl-的检验方法。
【素养目标】
1.知道可以通过分析、推理等方法研究Cl-的检验,建立认知模型,并能运用模型解释Cl-检验的本质和规律。(证据推理与模型认知)
2.能根据物质的特征反应和干扰因素选取适当的检验试剂来进行Cl-的检验;能根据反应原理选取实验装置制取氯气。(科学探究与创新意识)
课前自主学习
学习任务一 氯气的实验室制法
任务驱动:
氯气用于自来水消毒已100多年,目前仍然有很多地方大量采用,工业制
取氯气用电解饱和食盐水的方法,那么在实验室中怎么制取氯气呢
1.反应原理
实验室用MnO2和浓盐酸加热反应制取Cl2,反应的化学方程式为_____________________________________。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
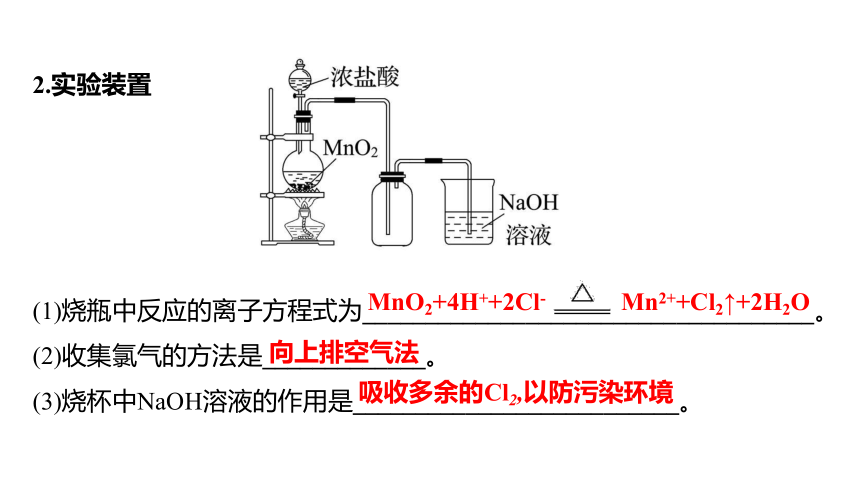
2.实验装置
(1)烧瓶中反应的离子方程式为____________________________________。
(2)收集氯气的方法是_____________。
(3)烧杯中NaOH溶液的作用是__________________________。
MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
向上排空气法
吸收多余的Cl2,以防污染环境
【情境·思考】
某化学兴趣小组在实验室制取氯气时,用含有 HCl 291 g的浓盐酸与足量的MnO2反应,能生成71 g Cl2吗
提示:不能。因为随着反应的进行,盐酸的浓度变小,MnO2与稀盐酸不再反应,故生成的Cl2小于71 g。
学习任务二 Cl-的检验
任务驱动:
用氯气消毒过的自来水含有氯离子,怎么检验其中含有的氯离子呢
氯离子(Cl-)的检验:
【想一想】
检验Cl-时,能否用稀盐酸进行酸化
提示:不能。因为盐酸中含有Cl-,影响Cl-的检验。
课堂合作探究
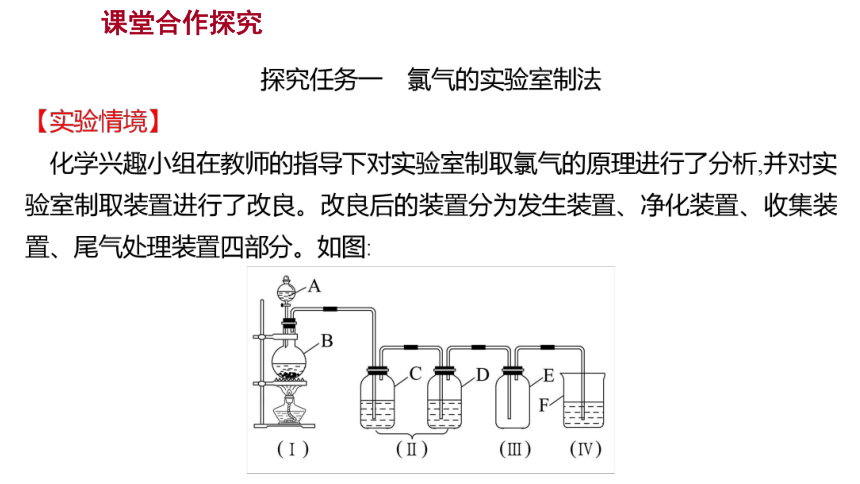
②仪器:铁架台、酒精灯、陶土网、A:_________(填写仪器名称,下同);
B:_________等。
③试剂:A中盛放_______(填写试剂名称,下同),B中盛放_________。
分液漏斗
圆底烧瓶
浓盐酸
二氧化锰
(2)净化装置(Ⅱ)。
组成 盛放试剂 试剂的作用
C _______________ ___________________
D _______ _________
(3)收集装置(Ⅲ)。
收集方法:___________法(装置E,Cl2的密度大于空气的密度)。
饱和氯化钠溶液
除去氯气中的氯化氢
浓硫酸
干燥氯气
向上排空气
2~3 mL试样 现象 解释或离子方程式
AgNO3溶液 稀硝酸
稀盐酸 _________ _______ _________________
NaCl溶液 _________ _______ _________________
Na2CO3溶液 _________ ___________ _________ _______________________
_______________________________
自来水 浑浊 浑浊 自来水中含有少量Cl-
白色沉淀
不溶解
Ag++Cl-===AgCl↓
白色沉淀
不溶解
Ag++Cl-===AgCl↓
白色沉淀
沉淀溶解并
产生气泡
2Ag++C===Ag2CO3↓,
Ag2CO3+2H+===2Ag++H2O+CO2↑
课堂学业达标
第2课时 氯气实验室制法及氯离子的检验
【课程标准】
1.了解实验室制取Cl2的原理和实验装置。
2.掌握Cl-的检验方法。
【素养目标】
1.知道可以通过分析、推理等方法研究Cl-的检验,建立认知模型,并能运用模型解释Cl-检验的本质和规律。(证据推理与模型认知)
2.能根据物质的特征反应和干扰因素选取适当的检验试剂来进行Cl-的检验;能根据反应原理选取实验装置制取氯气。(科学探究与创新意识)
课前自主学习
学习任务一 氯气的实验室制法
任务驱动:
氯气用于自来水消毒已100多年,目前仍然有很多地方大量采用,工业制
取氯气用电解饱和食盐水的方法,那么在实验室中怎么制取氯气呢
1.反应原理
实验室用MnO2和浓盐酸加热反应制取Cl2,反应的化学方程式为_____________________________________。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
2.实验装置
(1)烧瓶中反应的离子方程式为____________________________________。
(2)收集氯气的方法是_____________。
(3)烧杯中NaOH溶液的作用是__________________________。
MnO2+4H++2Cl- Mn2++Cl2↑+2H2O
向上排空气法
吸收多余的Cl2,以防污染环境
【情境·思考】
某化学兴趣小组在实验室制取氯气时,用含有 HCl 291 g的浓盐酸与足量的MnO2反应,能生成71 g Cl2吗
提示:不能。因为随着反应的进行,盐酸的浓度变小,MnO2与稀盐酸不再反应,故生成的Cl2小于71 g。
学习任务二 Cl-的检验
任务驱动:
用氯气消毒过的自来水含有氯离子,怎么检验其中含有的氯离子呢
氯离子(Cl-)的检验:
【想一想】
检验Cl-时,能否用稀盐酸进行酸化
提示:不能。因为盐酸中含有Cl-,影响Cl-的检验。
课堂合作探究
②仪器:铁架台、酒精灯、陶土网、A:_________(填写仪器名称,下同);
B:_________等。
③试剂:A中盛放_______(填写试剂名称,下同),B中盛放_________。
分液漏斗
圆底烧瓶
浓盐酸
二氧化锰
(2)净化装置(Ⅱ)。
组成 盛放试剂 试剂的作用
C _______________ ___________________
D _______ _________
(3)收集装置(Ⅲ)。
收集方法:___________法(装置E,Cl2的密度大于空气的密度)。
饱和氯化钠溶液
除去氯气中的氯化氢
浓硫酸
干燥氯气
向上排空气
2~3 mL试样 现象 解释或离子方程式
AgNO3溶液 稀硝酸
稀盐酸 _________ _______ _________________
NaCl溶液 _________ _______ _________________
Na2CO3溶液 _________ ___________ _________ _______________________
_______________________________
自来水 浑浊 浑浊 自来水中含有少量Cl-
白色沉淀
不溶解
Ag++Cl-===AgCl↓
白色沉淀
不溶解
Ag++Cl-===AgCl↓
白色沉淀
沉淀溶解并
产生气泡
2Ag++C===Ag2CO3↓,
Ag2CO3+2H+===2Ag++H2O+CO2↑
课堂学业达标
