2022-2023学年九年级化学人教版下册 第1--8单元综合复习测试题(word 含答案)
文档属性
| 名称 | 2022-2023学年九年级化学人教版下册 第1--8单元综合复习测试题(word 含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 528.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-29 00:00:00 | ||
图片预览




文档简介
第1--8单元综合复习测试题
一、单选题
1.食物加工过程中发生化学变化的是( )
A.碾米 B.淘米
C.洗菜 D.酿酒
2.下列有关合金的叙述中正确的是( )
①合金具有金属特性;②合金中的元素以单质形式存在;③合金中不一定含有金属;④钢是含杂质较少的铁合金;⑤合金属于金属材料;⑥生铁可完全溶解于稀盐酸
①②③④⑤⑥ B.①③④⑤⑥
C.①②④⑤ D.①④⑥
3.实验室常用的下列仪器中,由金属材料制成的是( )
A.试管架 B.坩埚钳
C.塑料药匙 D.蒸发皿
4.下列反应属于置换反应的是( )
A.H2O+CO═CO2+H2
B.2KI+Cl2═2KCl+I2
C.2SO2+O2=2SO3
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O
5.下列对实验现象的观察或记录中正确的是( )
A.将黄铜与纯铜互相刻划,黄铜表面出现的划痕更深
B.打磨过的铝丝插入硫酸铜溶液中,铝丝表面出现红色物质,溶液逐渐变成无色
C.一氧化碳与氧化铜加热充分反应后,固体由红色变成黑色
D.镁条在空气中燃烧,发出白光,生成氧化镁固体
6.金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
7.今年5月12日是我国第六个“防灾减灾日”。以下有关处理火灾现场方法错误的是( )
A.身上着火不可乱跑,要就地打滚使火熄灭
B.用水浇湿毛巾或衣物,捂住口鼻,低姿行走到安全通道
C.逃生路线被火封住,应退回室内,关闭门窗,向门窗浇水,发出求救信号
D.人员被火势围困在高层建筑时使用楼内电梯撤退
8.区分下列物质的方法中不可行的是( )
A.用观察颜色区分硫酸铜和硫酸亚铁溶液
B.用水区分碳酸钙和氯化钠
C.用闻气味区别氧气和氮气
D.用稀硫酸区分黄铜(Cu、Zn)和黄金
9.“11.27 夺命快递”致 1 人死亡 8 人中毒,原因是
快递物上沾有剧毒化工品——氟乙酸甲酯 (化学式:
C3H5FO2),关于氟乙酸甲酯的说法正确的是( )
A.氟乙酸甲酯中碳、氢、氟、氧四种元素的质量比为 3:5:1:2
B.氟乙酸甲酯的相对分子质量为 92g
C.贮存和运输氟乙酸甲酯时要密封,防止泄漏
D.氟乙酸甲酯分子由碳原子、氢原子、氟原子和氧分子构成
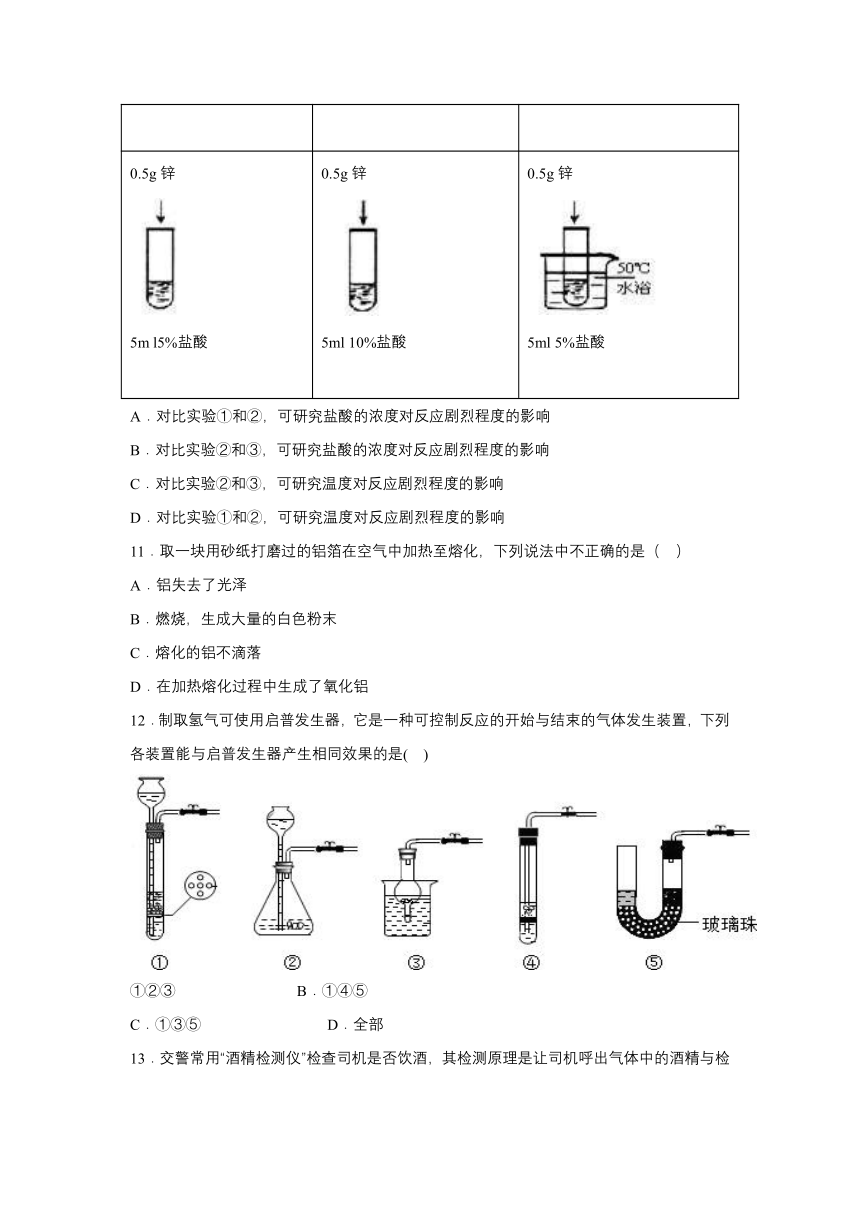
10.为探究影响锌与盐酸反应剧烈程度的因素,某小组设计了下列实验,下列说法正确的是( )
实验①
实验②
实验③
0.5g锌
5m l5%盐酸
0.5g锌
5ml 10%盐酸
0.5g锌
5ml 5%盐酸
A.对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响
B.对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响
C.对比实验②和③,可研究温度对反应剧烈程度的影响
D.对比实验①和②,可研究温度对反应剧烈程度的影响
11.取一块用砂纸打磨过的铝箔在空气中加热至熔化,下列说法中不正确的是( )
A.铝失去了光泽
B.燃烧,生成大量的白色粉末
C.熔化的铝不滴落
D.在加热熔化过程中生成了氧化铝
12.制取氢气可使用启普发生器,它是一种可控制反应的开始与结束的气体发生装置,下列各装置能与启普发生器产生相同效果的是( )
①②③ B.①④⑤
C.①③⑤ D.全部
13.交警常用“酒精检测仪”检查司机是否饮酒,其检测原理是让司机呼出气体中的酒精与检测仪中的物质发生反应: ,其中 X 的化学式和 Cr2(SO4)3中的 S 元素的化合价分别是( )
A.CO +3 价 B.O2 +6 价
C.CO2 +3 价 D.CO2 +6 价
14.下列涉及学科观点的有关说法正确的是( )
A.根据微粒观:水是由氢原子和氧原子构成的
B.根据守恒观:10mL酒精与10mL水混合后得到20mL液体
C.根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化
D.根据结构观:氦原子和镁原子最外层电子数相同,化学性质相同
15.对下列词语的有关化学原理解释不合理的是( )
A.风助火威——为燃烧提供足够多的氧气
B.火上浇油——隔绝空气
C.釜底抽薪——移去可燃物使火熄灭
D.钻木取火——使温度达到可燃物的着火点
16.下列各组物质中,前者是化合物,后者是混合物的是( )
A.水、铁水 B.氧气、铝土矿
C.氧化铝、石灰石 D.焦炭、炼铁高炉尾气
17.将质量相等的铝粉和铁粉分别与质量、浓度均相同的稀硫酸充分反应,下列所述的反应情况与图示可能相符的是( )
①铝粉、铁粉和硫酸均有剩余 ②硫酸、铝粉、铁粉均反应完
③硫酸、铁粉均反应完,铝粉有剩余
④硫酸、铝粉均反应完,铁粉有剩余
⑤铝粉、铁粉均反应完,硫酸有剩余
⑥硫酸反应完,铝粉、铁粉有剩余
①③⑤ B.③⑥
C.④⑥ D.②③⑤⑥
18.已知暖宝宝贴(主要成分为铁粉,木炭,食盐)的热量来源是铁粉的缓慢氧化,小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为 250mL)中的水的体积为 45mL(铁粉生锈消耗的水忽略不计),下列说法错误的是( )
A.该实验原理是利用铁粉生锈消耗氧气
B.通过本次实验数据测的空气中氧气的体积分数为 18%
C.若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足
D.必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积
19.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图,下列说法中正确的是( )
A.该反应为化合反应
B.丙一定为该反应的催化剂
C.此反应中乙物质和丁物质的质量比为3:2
D.丁的相对分子质量是甲的2倍
20.下列判断错误的是( )
A.若铜丝的质量为 mg,其在火焰上灼烧后的质量为 ng,则 mB.若高锰酸钾的质量为 mg,加热一段时间后剩余固体的质量为 ng,则 m>n
C.若木炭和坩埚的总质量为 mg,其燃烧后的灰烬和坩埚的总质量为 ng,则 m>n
D.若铁、硫酸铜溶液和烧杯的总质量为 mg,其反应后的混合物和烧杯的总质量为 ng,则 m二、填空题
21.下列是与人类的生活与未来密切的物质:
A 氢气 B 干冰 C 酒精 D 甲烷 E 铁粉 F 钛合金,选择相应的编号填空
① ___________是实验室常用的燃料,
② ___________可以提供清洁、高效的能源,
③ ___________是天然气的主要成分,
④ ___________可用于人工降雨,
⑤ ___________可用来同时吸收氧气和水分,以防止食品腐败.
⑥ ___________与人体具有很好的“相容性”,因此可以用来制造人造骨.
22.(1)化学基础知识是学好化学的关键,请按下列要求填空.
① 图 1 是某微粒的结构示意图.该微粒在化学反应中失去电子后形成粒子的符号 _____________。
② 写出一条从图 2 中获得的信息 _______________。
③ 如图 3 是汽车尾气治理过程中某反应的微观示意图.则该反应中 A 和 C 的化学计量数之比为________。
(2)水是生命的源泉,也是不可缺少的资源。
①自然界的水常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指 _____________;(填字母)
A 元素 B 原子
C 离子 D 分子
②净水器常用活性炭,主要是利用活性炭的______性。生活中,既能降低水的硬度,又能杀菌消毒的方法是___。
③电解水的装置如图所示,管 A、管 B 中的气体的质量比是_________, 在电解水的过程中,保持不变的粒子是________。
(3)人们常说的“五金”是指“金、银、铜、铁、锡”,在“五金”顺序中把金属___________的位置移到最后,正好符合由弱到强的金属活动性顺序。五种金属中,能和酸发生置换反应生成氢气的是___________(用符号表示)。
三、科普阅读题
23.阅读下面科普短文。
酱油是中国传统发酵调味品。酱油的鲜味和营养价值取决于氨基酸态氮含量的高低。氨基酸态氮是指以氨基酸形式存在的氮元素,其含量是衡量酱油营养价值的一项重要指标。氨基酸态氮含量越高,酱油品质越好,等级越高,标准见表1。
表1 酿造酱油等级标准
项目 指标
氨基酸态氮 g/100mL 特级 一级 二级 三级
≥0.80 0.70~0.79 0.55~0.69 0.40~0.54
酿造酱油是以大豆或脱脂大豆,小麦或麸皮为原料,经微生物发酵而成。食盐也是酱油酿造的重要原料之一。选用的食盐以氯化钠含量高、卤汁(氯化钾、氯化镁、硫酸钙等的混合物)少的品质为宜。酱油在酿造过程中会产生一系列带有特殊风味的物质。风味是传统发酵食品重要的质量指标,经实验测定发现。杀菌工艺对酱油风味物质的形成有一定影响。研究人员做了如下实验:将2份等量的生酱油分别加热到不同灭菌温度(90oC、98 oC)并保温20min,灭菌后快速降温到45oC,保持24小时后检测酱油鲜、咸、甜等9项风味,实验结果见图1,酱油营养丰富,但由于含盐量高,亦不可过量食用。
依据文章内容,回答下列问题。
(1)衡量酱油营养价值的重要指标是 _____ 。
(2)某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为 _____ 。
(3)卤汁是KCl、 _____ (用化学式表示)、CaSO4等组成的混合物。
(4)由图1可知,98℃灭菌条件下的酱油的 _____ 强于90℃灭菌条件下的酱油。
(5)下列说法正确的是 _____ (填序号)。
A 酱油酿造过程发生了化学变化
B 购买酱油时应关注标签上氨基酸态氮的含量
C 酱油的风味指的是酱油的香气、后味、协调感、浓厚感等
四、实验题
24.化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。
(1)图中标有序号①的仪器名称是________。
(2)实验室用A装置制取氧气,发生反应的化学方程式是________,在试管口放棉花团的作用是________。
(3)用双氧水制取氧气,探究石蜡燃烧的产物,应选择装置B与________、________(填字母)组合。收集过程中,检验氧气集满的方法是_________。
25.白磷、红磷都是可燃物,都可以在一定条件下燃烧.以下是利用它们的可燃性进行的三个实验,请分别回答问题。
(1)通过实验1可以探究燃烧的条件.说明燃烧需要的条件是可燃物与氧气接触和_____,铜片的主要作用是_____.
(2)通过实验2,待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到_____的现象时,可达到该实验目的.
(3)通过实验3可以验证质量守恒定律.实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡.整个实验过程中气球会出现的现象是_____.
(4)综合分析上述三个实验,以下说法正确的是_____.(填①~⑥序号)
①实验1中的热水只起加热的作用
②实验1要有通风设备
③实验2中红磷可以换成铁丝
④实验2若未达到实验目的,可能是由于装置气密性不好
⑤实验3中的气球起到了平衡瓶内外气体压强的作用
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂.
26.某化学兴趣小组用一氧化碳与氧化铁样品(含少量杂质)的反应来探究炼铁的原理,装置如图所示.请回答有关问题:
(1)实验开始时,应先通 CO 再加热,目的是_________。
(2)实验进行一段时间后,玻璃管 A 中固体由_________ 色逐渐变成________ 色。 A、B 装置内发生反应的方程式依次为 ______________; ________________。
(3)若方框中连接的是装置 C 和 D,导管口的连接顺序为 a→d→b→e,则 CO最终进入装置______中。
(4)除 CO 外,还有哪些物质可以还原 Fe2O3,________ (请写一种物质的化学式)。
(5)若反应过程中装置 A 固体质量的变化情况如图所示,则所取氧化铁样品主要成分 Fe2O3的质量为______g。
五、流程题
27.某化学第二课堂小组利用已学过的知识,准备利用含 FeSO4和 CuSO4的废水(无其他难溶杂质),从中获得硫酸亚铁晶体,其流程如下图所示:
(1)整个流程中,操作1进行了两次,操作1是_____(填操作名称)。
(2)金属 X 是_____(填化学符号),其加入废水后反应的化学方程式:___________;固体 A 中含有________(填化学符号)。写出固体 A 与稀硫酸反应的化学方程式为:______________。
六、计算题
28.为了测定某石灰石样品中碳酸钙的含量,取20g此样品,将80mL(密度为1.1g/cm3)的稀盐酸分四次加入样品使之充分反应(石灰石中的杂质不溶于水,也不与盐酸及生成物反应),每次用盐酸的体积与反应后剩余固体的质量见下表.
次数 一 二 三 四
加入盐酸的体积/mL 20 20 20 20
剩余固体的质量/g 14 8 m 3
计算:
(1)m的数值是_______。
(2)样品中碳酸钙的质量分数________。
(3)20g此样品与足量盐酸反应最多生成二氧化碳的质量为______?(写出计算过程,保留两位小数)
(4)实验过程中二氧化碳的质量与所加稀盐酸的体积的关系如图所示,图中b的数值为_______。(保留一位小数)
一、单选题
1.食物加工过程中发生化学变化的是( )
A.碾米 B.淘米
C.洗菜 D.酿酒
2.下列有关合金的叙述中正确的是( )
①合金具有金属特性;②合金中的元素以单质形式存在;③合金中不一定含有金属;④钢是含杂质较少的铁合金;⑤合金属于金属材料;⑥生铁可完全溶解于稀盐酸
①②③④⑤⑥ B.①③④⑤⑥
C.①②④⑤ D.①④⑥
3.实验室常用的下列仪器中,由金属材料制成的是( )
A.试管架 B.坩埚钳
C.塑料药匙 D.蒸发皿
4.下列反应属于置换反应的是( )
A.H2O+CO═CO2+H2
B.2KI+Cl2═2KCl+I2
C.2SO2+O2=2SO3
D.8HNO3+3Cu═3Cu(NO3)2+2NO↑+4H2O
5.下列对实验现象的观察或记录中正确的是( )
A.将黄铜与纯铜互相刻划,黄铜表面出现的划痕更深
B.打磨过的铝丝插入硫酸铜溶液中,铝丝表面出现红色物质,溶液逐渐变成无色
C.一氧化碳与氧化铜加热充分反应后,固体由红色变成黑色
D.镁条在空气中燃烧,发出白光,生成氧化镁固体
6.金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
7.今年5月12日是我国第六个“防灾减灾日”。以下有关处理火灾现场方法错误的是( )
A.身上着火不可乱跑,要就地打滚使火熄灭
B.用水浇湿毛巾或衣物,捂住口鼻,低姿行走到安全通道
C.逃生路线被火封住,应退回室内,关闭门窗,向门窗浇水,发出求救信号
D.人员被火势围困在高层建筑时使用楼内电梯撤退
8.区分下列物质的方法中不可行的是( )
A.用观察颜色区分硫酸铜和硫酸亚铁溶液
B.用水区分碳酸钙和氯化钠
C.用闻气味区别氧气和氮气
D.用稀硫酸区分黄铜(Cu、Zn)和黄金
9.“11.27 夺命快递”致 1 人死亡 8 人中毒,原因是
快递物上沾有剧毒化工品——氟乙酸甲酯 (化学式:
C3H5FO2),关于氟乙酸甲酯的说法正确的是( )
A.氟乙酸甲酯中碳、氢、氟、氧四种元素的质量比为 3:5:1:2
B.氟乙酸甲酯的相对分子质量为 92g
C.贮存和运输氟乙酸甲酯时要密封,防止泄漏
D.氟乙酸甲酯分子由碳原子、氢原子、氟原子和氧分子构成
10.为探究影响锌与盐酸反应剧烈程度的因素,某小组设计了下列实验,下列说法正确的是( )
实验①
实验②
实验③
0.5g锌
5m l5%盐酸
0.5g锌
5ml 10%盐酸
0.5g锌
5ml 5%盐酸
A.对比实验①和②,可研究盐酸的浓度对反应剧烈程度的影响
B.对比实验②和③,可研究盐酸的浓度对反应剧烈程度的影响
C.对比实验②和③,可研究温度对反应剧烈程度的影响
D.对比实验①和②,可研究温度对反应剧烈程度的影响
11.取一块用砂纸打磨过的铝箔在空气中加热至熔化,下列说法中不正确的是( )
A.铝失去了光泽
B.燃烧,生成大量的白色粉末
C.熔化的铝不滴落
D.在加热熔化过程中生成了氧化铝
12.制取氢气可使用启普发生器,它是一种可控制反应的开始与结束的气体发生装置,下列各装置能与启普发生器产生相同效果的是( )
①②③ B.①④⑤
C.①③⑤ D.全部
13.交警常用“酒精检测仪”检查司机是否饮酒,其检测原理是让司机呼出气体中的酒精与检测仪中的物质发生反应: ,其中 X 的化学式和 Cr2(SO4)3中的 S 元素的化合价分别是( )
A.CO +3 价 B.O2 +6 价
C.CO2 +3 价 D.CO2 +6 价
14.下列涉及学科观点的有关说法正确的是( )
A.根据微粒观:水是由氢原子和氧原子构成的
B.根据守恒观:10mL酒精与10mL水混合后得到20mL液体
C.根据转化观:一氧化碳和二氧化碳在一定条件下可相互转化
D.根据结构观:氦原子和镁原子最外层电子数相同,化学性质相同
15.对下列词语的有关化学原理解释不合理的是( )
A.风助火威——为燃烧提供足够多的氧气
B.火上浇油——隔绝空气
C.釜底抽薪——移去可燃物使火熄灭
D.钻木取火——使温度达到可燃物的着火点
16.下列各组物质中,前者是化合物,后者是混合物的是( )
A.水、铁水 B.氧气、铝土矿
C.氧化铝、石灰石 D.焦炭、炼铁高炉尾气
17.将质量相等的铝粉和铁粉分别与质量、浓度均相同的稀硫酸充分反应,下列所述的反应情况与图示可能相符的是( )
①铝粉、铁粉和硫酸均有剩余 ②硫酸、铝粉、铁粉均反应完
③硫酸、铁粉均反应完,铝粉有剩余
④硫酸、铝粉均反应完,铁粉有剩余
⑤铝粉、铁粉均反应完,硫酸有剩余
⑥硫酸反应完,铝粉、铁粉有剩余
①③⑤ B.③⑥
C.④⑥ D.②③⑤⑥
18.已知暖宝宝贴(主要成分为铁粉,木炭,食盐)的热量来源是铁粉的缓慢氧化,小涛同学设计使用暖宝宝贴来测定空气中氧气的含量,实验开始前的装置如图所示,实验后从量筒中流入玻璃瓶(容积为 250mL)中的水的体积为 45mL(铁粉生锈消耗的水忽略不计),下列说法错误的是( )
A.该实验原理是利用铁粉生锈消耗氧气
B.通过本次实验数据测的空气中氧气的体积分数为 18%
C.若实验测得空气中氧气体积分数偏低,可能是暖宝宝贴的使用数量不足
D.必须等温度计的读数恢复至实验前的温度后才能记录量筒内剩余水的体积
19.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图,下列说法中正确的是( )
A.该反应为化合反应
B.丙一定为该反应的催化剂
C.此反应中乙物质和丁物质的质量比为3:2
D.丁的相对分子质量是甲的2倍
20.下列判断错误的是( )
A.若铜丝的质量为 mg,其在火焰上灼烧后的质量为 ng,则 m
C.若木炭和坩埚的总质量为 mg,其燃烧后的灰烬和坩埚的总质量为 ng,则 m>n
D.若铁、硫酸铜溶液和烧杯的总质量为 mg,其反应后的混合物和烧杯的总质量为 ng,则 m
21.下列是与人类的生活与未来密切的物质:
A 氢气 B 干冰 C 酒精 D 甲烷 E 铁粉 F 钛合金,选择相应的编号填空
① ___________是实验室常用的燃料,
② ___________可以提供清洁、高效的能源,
③ ___________是天然气的主要成分,
④ ___________可用于人工降雨,
⑤ ___________可用来同时吸收氧气和水分,以防止食品腐败.
⑥ ___________与人体具有很好的“相容性”,因此可以用来制造人造骨.
22.(1)化学基础知识是学好化学的关键,请按下列要求填空.
① 图 1 是某微粒的结构示意图.该微粒在化学反应中失去电子后形成粒子的符号 _____________。
② 写出一条从图 2 中获得的信息 _______________。
③ 如图 3 是汽车尾气治理过程中某反应的微观示意图.则该反应中 A 和 C 的化学计量数之比为________。
(2)水是生命的源泉,也是不可缺少的资源。
①自然界的水常遭到污染,污染物中氮和磷含量过高会造成水中藻类过度繁殖,使水质恶化,这里的“氮和磷”是指 _____________;(填字母)
A 元素 B 原子
C 离子 D 分子
②净水器常用活性炭,主要是利用活性炭的______性。生活中,既能降低水的硬度,又能杀菌消毒的方法是___。
③电解水的装置如图所示,管 A、管 B 中的气体的质量比是_________, 在电解水的过程中,保持不变的粒子是________。
(3)人们常说的“五金”是指“金、银、铜、铁、锡”,在“五金”顺序中把金属___________的位置移到最后,正好符合由弱到强的金属活动性顺序。五种金属中,能和酸发生置换反应生成氢气的是___________(用符号表示)。
三、科普阅读题
23.阅读下面科普短文。
酱油是中国传统发酵调味品。酱油的鲜味和营养价值取决于氨基酸态氮含量的高低。氨基酸态氮是指以氨基酸形式存在的氮元素,其含量是衡量酱油营养价值的一项重要指标。氨基酸态氮含量越高,酱油品质越好,等级越高,标准见表1。
表1 酿造酱油等级标准
项目 指标
氨基酸态氮 g/100mL 特级 一级 二级 三级
≥0.80 0.70~0.79 0.55~0.69 0.40~0.54
酿造酱油是以大豆或脱脂大豆,小麦或麸皮为原料,经微生物发酵而成。食盐也是酱油酿造的重要原料之一。选用的食盐以氯化钠含量高、卤汁(氯化钾、氯化镁、硫酸钙等的混合物)少的品质为宜。酱油在酿造过程中会产生一系列带有特殊风味的物质。风味是传统发酵食品重要的质量指标,经实验测定发现。杀菌工艺对酱油风味物质的形成有一定影响。研究人员做了如下实验:将2份等量的生酱油分别加热到不同灭菌温度(90oC、98 oC)并保温20min,灭菌后快速降温到45oC,保持24小时后检测酱油鲜、咸、甜等9项风味,实验结果见图1,酱油营养丰富,但由于含盐量高,亦不可过量食用。
依据文章内容,回答下列问题。
(1)衡量酱油营养价值的重要指标是 _____ 。
(2)某酿造的酱油氨基酸态氮含量为0.90g/100mL,则该酱油的等级为 _____ 。
(3)卤汁是KCl、 _____ (用化学式表示)、CaSO4等组成的混合物。
(4)由图1可知,98℃灭菌条件下的酱油的 _____ 强于90℃灭菌条件下的酱油。
(5)下列说法正确的是 _____ (填序号)。
A 酱油酿造过程发生了化学变化
B 购买酱油时应关注标签上氨基酸态氮的含量
C 酱油的风味指的是酱油的香气、后味、协调感、浓厚感等
四、实验题
24.化学是一门以实验为基础的科学。根据如图所示的装置,回答下列问题。
(1)图中标有序号①的仪器名称是________。
(2)实验室用A装置制取氧气,发生反应的化学方程式是________,在试管口放棉花团的作用是________。
(3)用双氧水制取氧气,探究石蜡燃烧的产物,应选择装置B与________、________(填字母)组合。收集过程中,检验氧气集满的方法是_________。
25.白磷、红磷都是可燃物,都可以在一定条件下燃烧.以下是利用它们的可燃性进行的三个实验,请分别回答问题。
(1)通过实验1可以探究燃烧的条件.说明燃烧需要的条件是可燃物与氧气接触和_____,铜片的主要作用是_____.
(2)通过实验2,待集气瓶中的红磷熄灭,冷却后打开弹簧夹,当观察到_____的现象时,可达到该实验目的.
(3)通过实验3可以验证质量守恒定律.实验前将白磷放入锥形瓶中,称量装置的总质量,引燃白磷,待反应后再称量装置总质量,发现托盘天平保持平衡.整个实验过程中气球会出现的现象是_____.
(4)综合分析上述三个实验,以下说法正确的是_____.(填①~⑥序号)
①实验1中的热水只起加热的作用
②实验1要有通风设备
③实验2中红磷可以换成铁丝
④实验2若未达到实验目的,可能是由于装置气密性不好
⑤实验3中的气球起到了平衡瓶内外气体压强的作用
⑥实验3锥形瓶内事先放少量细沙的作用是防止瓶底炸裂.
26.某化学兴趣小组用一氧化碳与氧化铁样品(含少量杂质)的反应来探究炼铁的原理,装置如图所示.请回答有关问题:
(1)实验开始时,应先通 CO 再加热,目的是_________。
(2)实验进行一段时间后,玻璃管 A 中固体由_________ 色逐渐变成________ 色。 A、B 装置内发生反应的方程式依次为 ______________; ________________。
(3)若方框中连接的是装置 C 和 D,导管口的连接顺序为 a→d→b→e,则 CO最终进入装置______中。
(4)除 CO 外,还有哪些物质可以还原 Fe2O3,________ (请写一种物质的化学式)。
(5)若反应过程中装置 A 固体质量的变化情况如图所示,则所取氧化铁样品主要成分 Fe2O3的质量为______g。
五、流程题
27.某化学第二课堂小组利用已学过的知识,准备利用含 FeSO4和 CuSO4的废水(无其他难溶杂质),从中获得硫酸亚铁晶体,其流程如下图所示:
(1)整个流程中,操作1进行了两次,操作1是_____(填操作名称)。
(2)金属 X 是_____(填化学符号),其加入废水后反应的化学方程式:___________;固体 A 中含有________(填化学符号)。写出固体 A 与稀硫酸反应的化学方程式为:______________。
六、计算题
28.为了测定某石灰石样品中碳酸钙的含量,取20g此样品,将80mL(密度为1.1g/cm3)的稀盐酸分四次加入样品使之充分反应(石灰石中的杂质不溶于水,也不与盐酸及生成物反应),每次用盐酸的体积与反应后剩余固体的质量见下表.
次数 一 二 三 四
加入盐酸的体积/mL 20 20 20 20
剩余固体的质量/g 14 8 m 3
计算:
(1)m的数值是_______。
(2)样品中碳酸钙的质量分数________。
(3)20g此样品与足量盐酸反应最多生成二氧化碳的质量为______?(写出计算过程,保留两位小数)
(4)实验过程中二氧化碳的质量与所加稀盐酸的体积的关系如图所示,图中b的数值为_______。(保留一位小数)
同课章节目录
