2023春高中化学选择性必修2 (人教版2019)第三章第一节 物质的聚集状态与晶体的常识 课时练(含答案)
文档属性
| 名称 | 2023春高中化学选择性必修2 (人教版2019)第三章第一节 物质的聚集状态与晶体的常识 课时练(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 702.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-29 00:00:00 | ||
图片预览


文档简介
第一节 物质的聚集状态与晶体的常识
题组一 物质的聚集状态
1.下列关于等离子体的叙述错误的是( )
A.是物质的一种聚集状态
B.是一种混合物存在状态
C.具有导电性
D.基本构成微粒只有阴、阳离子
2.下列有关液晶的叙述不正确的是( )
A.具有液体的流动性、晶体的各向异性
B.用来制造液晶显示器
C.不是物质的一种聚集状态
D.液晶分子聚集在一起时,其分子间的相互作用很容易受温度、压力和电场的影响
3.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.X射线通过玻璃态水时,能产生谱线
题组二 晶体和非晶体
4.在水晶柱面上滴一滴熔化的石蜡,用一根红热的铁针刺中凝固的石蜡,会发现不同方向石蜡熔化的快慢不同,这是晶体的( )
A.自范性 B.均一性
C.晶胞“无隙并置”性 D.各向异性
5.如图是a、b两种不同物质的熔化曲线,下列说法正确的是( )
A.a没有固定的熔点 B.a是非晶体
C.b是晶体 D.b是非晶体
6.要得到较大颗粒的明矾晶体,在结晶时可采取的操作是( )
A.配制比室温高10~20 ℃的明矾饱和溶液,然后浸入悬挂的明矾小晶核,室温下静置
B.在沸水中配制明矾饱和溶液,然后急速冷却结晶
C.室温下,在明矾饱和溶液中投入明矾小晶核,静置
D.快速蒸发明矾饱和溶液至大量晶体析出
7.下列关于晶体性质的叙述不正确的是( )
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
题组三 晶胞的理解及应用
8.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是( )
A.相邻晶胞之间没有任何间隙
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.“并置”是指所有晶胞都是平行排列的
9.最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性,因这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )
A.Mg2CNi3 B.MgCNi3
C.MgCNi2 D.MgC2Ni
10.(2022·上海浦东新区高二检测)不能够支持石墨是晶体这一事实的选项是( )
A.石墨和金刚石互为同素异形体
B.石墨中的碳原子呈周期性有序排列
C.石墨的熔点为3 625 ℃
D.在石墨的X射线衍射图谱上有明锐的衍射峰
11.如图为一块密度、厚度均匀的矩形样品,长为宽的两倍,若用多用电表沿两对称轴测其电阻均为R,则这块样品一定是( )
A.金属 B.半导体 C.非晶体 D.晶体
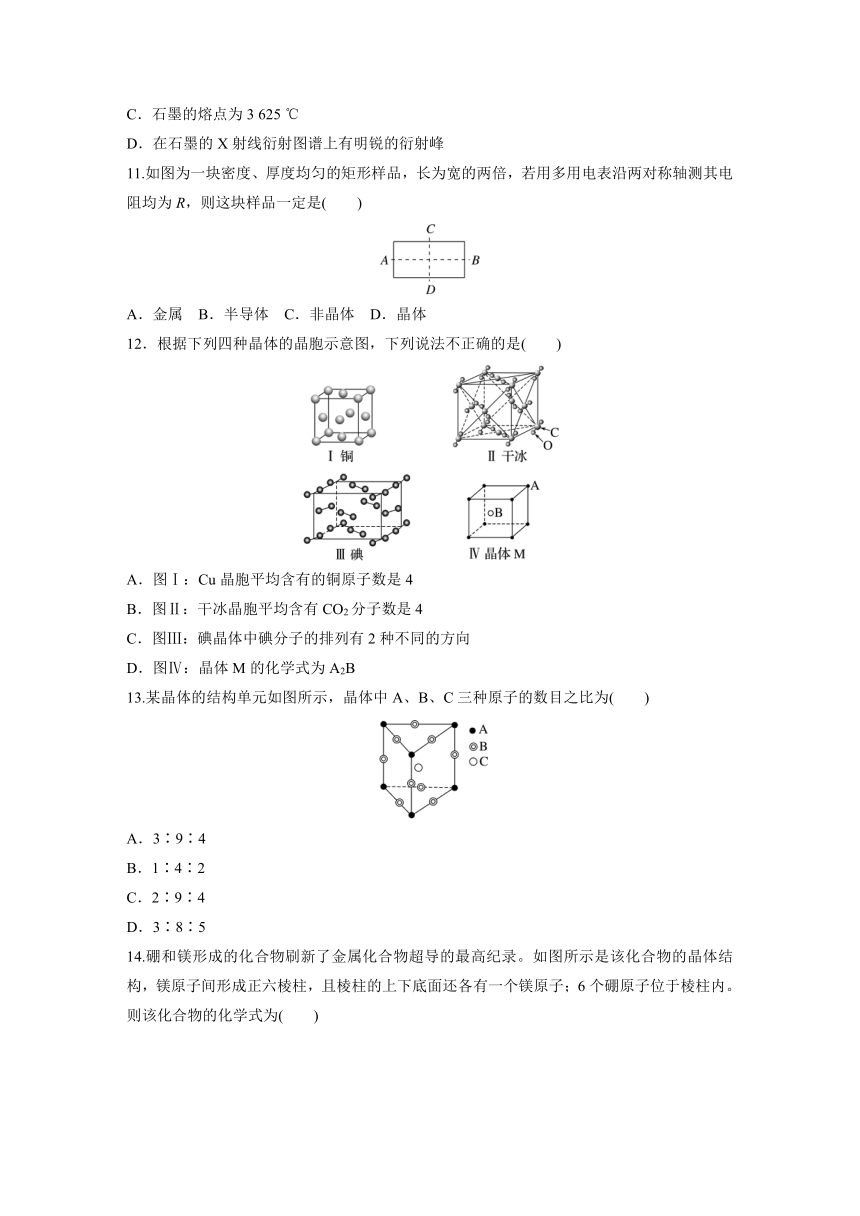
12.根据下列四种晶体的晶胞示意图,下列说法不正确的是( )
A.图Ⅰ:Cu晶胞平均含有的铜原子数是4
B.图Ⅱ:干冰晶胞平均含有CO2分子数是4
C.图Ⅲ:碘晶体中碘分子的排列有2种不同的方向
D.图Ⅳ:晶体M的化学式为A2B
13.某晶体的结构单元如图所示,晶体中A、B、C三种原子的数目之比为( )
A.3∶9∶4
B.1∶4∶2
C.2∶9∶4
D.3∶8∶5
14.硼和镁形成的化合物刷新了金属化合物超导的最高纪录。如图所示是该化合物的晶体结构,镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子;6个硼原子位于棱柱内。则该化合物的化学式为( )
A.MgB B.MgB2
C.Mg2B D.Mg3B2
15.固体二氧化硅有晶体和非晶体两种。根据下图回答:
(1)对比图Ⅰ和Ⅱ可知,晶体SiO2具有自范性,而非晶体SiO2没有自范性,本质原因是_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________。
(2)观察三个图,区分晶体SiO2和非晶体SiO2最可靠的科学方法是_____________________。
16.元素X的某价态离子Xn+中所有电子正好充满K、L、M三个能层,它与N3-形成晶体的晶胞结构如图所示。
(1)该晶体的阳离子与阴离子个数之比为______。
(2)该晶体中Xn+的n=________。
(3)X元素的原子序数是________。
(4)晶体中每个N3-被________个等距离的Xn+包围。
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
1.D 2.C 3.C 4.D
5.D [晶体有固定的熔点,由a的熔化曲线分析可知,中间有一段温度不变但一直在吸收能量,该段所对应的温度就是晶体a的熔点;由b的熔化曲线可知,温度一直升高,所以物质b没有固定的熔点,为非晶体。]
6.A [配制比室温高的明矾饱和溶液,当温度降低时,溶质的溶解度也降低,析出的明矾会附着在小晶核上,得到较大颗粒的明矾晶体;在沸水中配制明矾的饱和溶液,然后快速冷却或快速蒸发明矾饱和溶液至大量晶体析出,得到的都是小颗粒明矾晶体;室温下,在明矾饱和溶液中投入明矾小晶核,静置,不会得到较大颗粒的明矾晶体。]
7.B [晶体在不同方向上物质微粒的排列情况不同,即为各向异性,晶体的对称性是微观粒子按一定规律呈周期性重复排列,两者没有矛盾,故B错误;构成晶体的粒子在微观空间里呈现周期性的有序排列,则晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果,故C正确;由于晶体在不同方向上物质微粒的排列情况不同,即为各向异性,具有特定的方向性,故D正确。]
8.B [晶体并不是晶胞简单、随意堆积而成,而是晶胞平行排列而成的,且相邻晶胞之间没有任何间隙。]
9.B [根据晶胞结构可知,碳原子位于该晶胞的体心,所以该晶胞中含有一个碳原子,镁原子位于顶角处,因此镁原子个数为8×=1,所以该晶胞含有1个镁原子,镍原子位于面心处,因此镍原子个数为6×=3,所以该晶胞中含有3个镍原子,故该晶体的化学式为MgCNi3。]
10.A 11.D
12.D [A项,铜晶胞平均含有的铜原子数为×8+×6=4;B项,干冰晶胞平均含有的CO2分子数为×8+×6=4;C项,根据碘晶胞中碘分子的排列方向可知,碘晶体中碘分子的排列有2种不同的方向;D项,晶体M的晶胞中,N(A)∶N(B)=(×8)∶1=1∶1,故M的化学式可能为AB(或BA)。]
13.B [该结构中含A原子个数为6×=,B原子个数为6×+3×=2,C原子个数为1,则A、B、C原子的个数比为∶2∶1=1∶4∶2。]
14.B [棱柱内硼原子数为6,均属于这个晶胞;镁原子位于上、下面心(2个)及12个顶角,共有镁原子数为2×+12×=3,则镁、硼原子个数之比为1∶2。]
15.(1)构成晶体的粒子在微观空间里呈现周期性有序排列,而构成非晶体的粒子在微观空间里排列相对无序 (2)对固体二氧化硅进行X射线衍射实验
16.(1)3∶1 (2)1 (3)29 (4)6
解析 (1)Xn+位于晶胞的棱上,其数目为12×=3;N3-位于晶胞的顶角,其数目为8×=1,故二者个数之比为3∶1。(2)由晶体的化学式X3N知,X所带电荷数为1。(3)因为K、L、M三个能层充满,故Xn+有2、8、18结构,所以X的原子序数是29。(4)N3-位于晶胞顶角,故其被6个Xn+从上、下、左、右、前、后包围。
题组一 物质的聚集状态
1.下列关于等离子体的叙述错误的是( )
A.是物质的一种聚集状态
B.是一种混合物存在状态
C.具有导电性
D.基本构成微粒只有阴、阳离子
2.下列有关液晶的叙述不正确的是( )
A.具有液体的流动性、晶体的各向异性
B.用来制造液晶显示器
C.不是物质的一种聚集状态
D.液晶分子聚集在一起时,其分子间的相互作用很容易受温度、压力和电场的影响
3.水的状态除了气、液和固态外,还有玻璃态。它是由液态水急速冷却到165 K时形成的。玻璃态的水无固定形状,不存在晶体结构,且密度与普通液态水的密度相同,有关玻璃态水的叙述正确的是( )
A.水由液态变为玻璃态,体积缩小
B.水由液态变为玻璃态,体积膨胀
C.玻璃态是水的一种特殊状态
D.X射线通过玻璃态水时,能产生谱线
题组二 晶体和非晶体
4.在水晶柱面上滴一滴熔化的石蜡,用一根红热的铁针刺中凝固的石蜡,会发现不同方向石蜡熔化的快慢不同,这是晶体的( )
A.自范性 B.均一性
C.晶胞“无隙并置”性 D.各向异性
5.如图是a、b两种不同物质的熔化曲线,下列说法正确的是( )
A.a没有固定的熔点 B.a是非晶体
C.b是晶体 D.b是非晶体
6.要得到较大颗粒的明矾晶体,在结晶时可采取的操作是( )
A.配制比室温高10~20 ℃的明矾饱和溶液,然后浸入悬挂的明矾小晶核,室温下静置
B.在沸水中配制明矾饱和溶液,然后急速冷却结晶
C.室温下,在明矾饱和溶液中投入明矾小晶核,静置
D.快速蒸发明矾饱和溶液至大量晶体析出
7.下列关于晶体性质的叙述不正确的是( )
A.晶体的自范性指的是在适宜条件下晶体能够自发地呈现规则的多面体几何外形
B.晶体的各向异性和对称性是矛盾的
C.晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果
D.晶体的各向异性直接取决于微观粒子的排列具有特定的方向性
题组三 晶胞的理解及应用
8.整块晶体可以看作是数量巨大的晶胞“无隙并置”而成。对这句话的理解错误的是( )
A.相邻晶胞之间没有任何间隙
B.晶体是晶胞简单、随意堆积而成
C.晶胞排列时,取向相同
D.“并置”是指所有晶胞都是平行排列的
9.最近发现,只含镁、镍和碳三种元素的晶体竟然也具有超导性,因这三种元素都是常见元素,从而引起广泛关注。该新型超导晶体的一个晶胞如图所示,则该晶体的化学式为( )
A.Mg2CNi3 B.MgCNi3
C.MgCNi2 D.MgC2Ni
10.(2022·上海浦东新区高二检测)不能够支持石墨是晶体这一事实的选项是( )
A.石墨和金刚石互为同素异形体
B.石墨中的碳原子呈周期性有序排列
C.石墨的熔点为3 625 ℃
D.在石墨的X射线衍射图谱上有明锐的衍射峰
11.如图为一块密度、厚度均匀的矩形样品,长为宽的两倍,若用多用电表沿两对称轴测其电阻均为R,则这块样品一定是( )
A.金属 B.半导体 C.非晶体 D.晶体
12.根据下列四种晶体的晶胞示意图,下列说法不正确的是( )
A.图Ⅰ:Cu晶胞平均含有的铜原子数是4
B.图Ⅱ:干冰晶胞平均含有CO2分子数是4
C.图Ⅲ:碘晶体中碘分子的排列有2种不同的方向
D.图Ⅳ:晶体M的化学式为A2B
13.某晶体的结构单元如图所示,晶体中A、B、C三种原子的数目之比为( )
A.3∶9∶4
B.1∶4∶2
C.2∶9∶4
D.3∶8∶5
14.硼和镁形成的化合物刷新了金属化合物超导的最高纪录。如图所示是该化合物的晶体结构,镁原子间形成正六棱柱,且棱柱的上下底面还各有一个镁原子;6个硼原子位于棱柱内。则该化合物的化学式为( )
A.MgB B.MgB2
C.Mg2B D.Mg3B2
15.固体二氧化硅有晶体和非晶体两种。根据下图回答:
(1)对比图Ⅰ和Ⅱ可知,晶体SiO2具有自范性,而非晶体SiO2没有自范性,本质原因是_______________________________________________________________________________
_______________________________________________________________________________
_______________________________________________________________________________。
(2)观察三个图,区分晶体SiO2和非晶体SiO2最可靠的科学方法是_____________________。
16.元素X的某价态离子Xn+中所有电子正好充满K、L、M三个能层,它与N3-形成晶体的晶胞结构如图所示。
(1)该晶体的阳离子与阴离子个数之比为______。
(2)该晶体中Xn+的n=________。
(3)X元素的原子序数是________。
(4)晶体中每个N3-被________个等距离的Xn+包围。
第三章 晶体结构与性质
第一节 物质的聚集状态与晶体的常识
1.D 2.C 3.C 4.D
5.D [晶体有固定的熔点,由a的熔化曲线分析可知,中间有一段温度不变但一直在吸收能量,该段所对应的温度就是晶体a的熔点;由b的熔化曲线可知,温度一直升高,所以物质b没有固定的熔点,为非晶体。]
6.A [配制比室温高的明矾饱和溶液,当温度降低时,溶质的溶解度也降低,析出的明矾会附着在小晶核上,得到较大颗粒的明矾晶体;在沸水中配制明矾的饱和溶液,然后快速冷却或快速蒸发明矾饱和溶液至大量晶体析出,得到的都是小颗粒明矾晶体;室温下,在明矾饱和溶液中投入明矾小晶核,静置,不会得到较大颗粒的明矾晶体。]
7.B [晶体在不同方向上物质微粒的排列情况不同,即为各向异性,晶体的对称性是微观粒子按一定规律呈周期性重复排列,两者没有矛盾,故B错误;构成晶体的粒子在微观空间里呈现周期性的有序排列,则晶体的对称性是微观粒子按一定规律做周期性重复排列的必然结果,故C正确;由于晶体在不同方向上物质微粒的排列情况不同,即为各向异性,具有特定的方向性,故D正确。]
8.B [晶体并不是晶胞简单、随意堆积而成,而是晶胞平行排列而成的,且相邻晶胞之间没有任何间隙。]
9.B [根据晶胞结构可知,碳原子位于该晶胞的体心,所以该晶胞中含有一个碳原子,镁原子位于顶角处,因此镁原子个数为8×=1,所以该晶胞含有1个镁原子,镍原子位于面心处,因此镍原子个数为6×=3,所以该晶胞中含有3个镍原子,故该晶体的化学式为MgCNi3。]
10.A 11.D
12.D [A项,铜晶胞平均含有的铜原子数为×8+×6=4;B项,干冰晶胞平均含有的CO2分子数为×8+×6=4;C项,根据碘晶胞中碘分子的排列方向可知,碘晶体中碘分子的排列有2种不同的方向;D项,晶体M的晶胞中,N(A)∶N(B)=(×8)∶1=1∶1,故M的化学式可能为AB(或BA)。]
13.B [该结构中含A原子个数为6×=,B原子个数为6×+3×=2,C原子个数为1,则A、B、C原子的个数比为∶2∶1=1∶4∶2。]
14.B [棱柱内硼原子数为6,均属于这个晶胞;镁原子位于上、下面心(2个)及12个顶角,共有镁原子数为2×+12×=3,则镁、硼原子个数之比为1∶2。]
15.(1)构成晶体的粒子在微观空间里呈现周期性有序排列,而构成非晶体的粒子在微观空间里排列相对无序 (2)对固体二氧化硅进行X射线衍射实验
16.(1)3∶1 (2)1 (3)29 (4)6
解析 (1)Xn+位于晶胞的棱上,其数目为12×=3;N3-位于晶胞的顶角,其数目为8×=1,故二者个数之比为3∶1。(2)由晶体的化学式X3N知,X所带电荷数为1。(3)因为K、L、M三个能层充满,故Xn+有2、8、18结构,所以X的原子序数是29。(4)N3-位于晶胞顶角,故其被6个Xn+从上、下、左、右、前、后包围。
