沪教版(全国)化学专题复习物质构成的奥秘(含答案)
文档属性
| 名称 | 沪教版(全国)化学专题复习物质构成的奥秘(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 113.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-30 00:00:00 | ||
图片预览



文档简介
沪教版(全国) 化学专题复习 物质构成的奥秘
一、单选题
1.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
2.2020年6月23日我国的北斗导航“收官之星”在西昌发射成功,北斗导航卫星系统采用铷原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的原子结构示意图如图所示。下列说法不正确的是
A.铷单质具有导电性
B.m的值是37,n的值是1
C.铷的相对原子质量为85.47
D.氯化铷的化学式为RbCl2
3.物质由微观粒子构成。下列都由离子构成的一组物质是
A.氯化钠、硫酸铜 B.水、干冰 C.金刚石、氧化汞 D.氦气、氨气
4.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
5.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是
A.含有O2 B.由四种非金属元素组成
C.属于氧化物 D.其中氢元素的质量分数最大
6.在新冠疫情防控过程中,人们使用的一种免洗洗手消毒液里含有三氯羟基二苯醚(简称三氯生,化学式为C12H7O2Cl3)。下列表述正确的是
A.三氯生由碳、氢、氧、氯元素组成
B.一个三氯生分子中含有一个氧分子
C.三氯生的相对分子质量为289.5g
D.三氯生中氢、氧元素质量比为7:2
7.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是
A.NaCl B.KClO C.Cl2 D.ClO2
8.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
9.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
10.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
11.下列有关粒子的说法中正确的是
A.原子的原子核都是由质子和中子构成的 B.分子可分,而原子不可再分
C.原子可转化成离子,离子不能转化为原子 D.钠原子和钠离子核电荷数相同
12.已知碘原子的相对原子质量为127,其原子核内有74个中子,则碘原子核外的电子数为
A.74 B.53 C.54 D.72
13.原子核中一定含有的粒子是( )
A.中子 B.质子 C.电子 D.质子和电子
14.防疫期间常用酒精消毒,在消毒过程中我们能闻到酒精散发出的特殊气味,主要是因为
A.分子的体积很小 B.分子间有间隔
C.分子在不断运动 D.分子可以再分
15.人体中有50多种元素,含量如图。下列说法正确的是
A.人体中氢元素含量约为10%
B.含量最高的金属元素是钠
C.人体中微量元素共有10种
D.缺铁会引起骨质疏松
二、填空题
16.回答下列问题
(1)用元素符号或化学式填空:
①钙元素______;
②可用于制照明弹的金属________;
③二氧化硫______;
④碱式碳酸铜由_________元素组成
(2)下列实验操作中需要用到哪些仪器(填仪器名称)
①固体药品盛放在________中;
②取出固体药品所用的仪器是_________;
③夹持燃烧的镁条的仪器是_______;
④量取9.0mL的水需要用到__________。
(3)碳酸氢铵受热易分解符号表达式为:________,所以保存碳酸氢铵应注意________。
17.请用恰当的化学符号表示:
(1)三个碳原子_____。
(2)+1价的氢元素_____。
(3)三个钠离子_____。
(4)地壳中最多的元素_____。
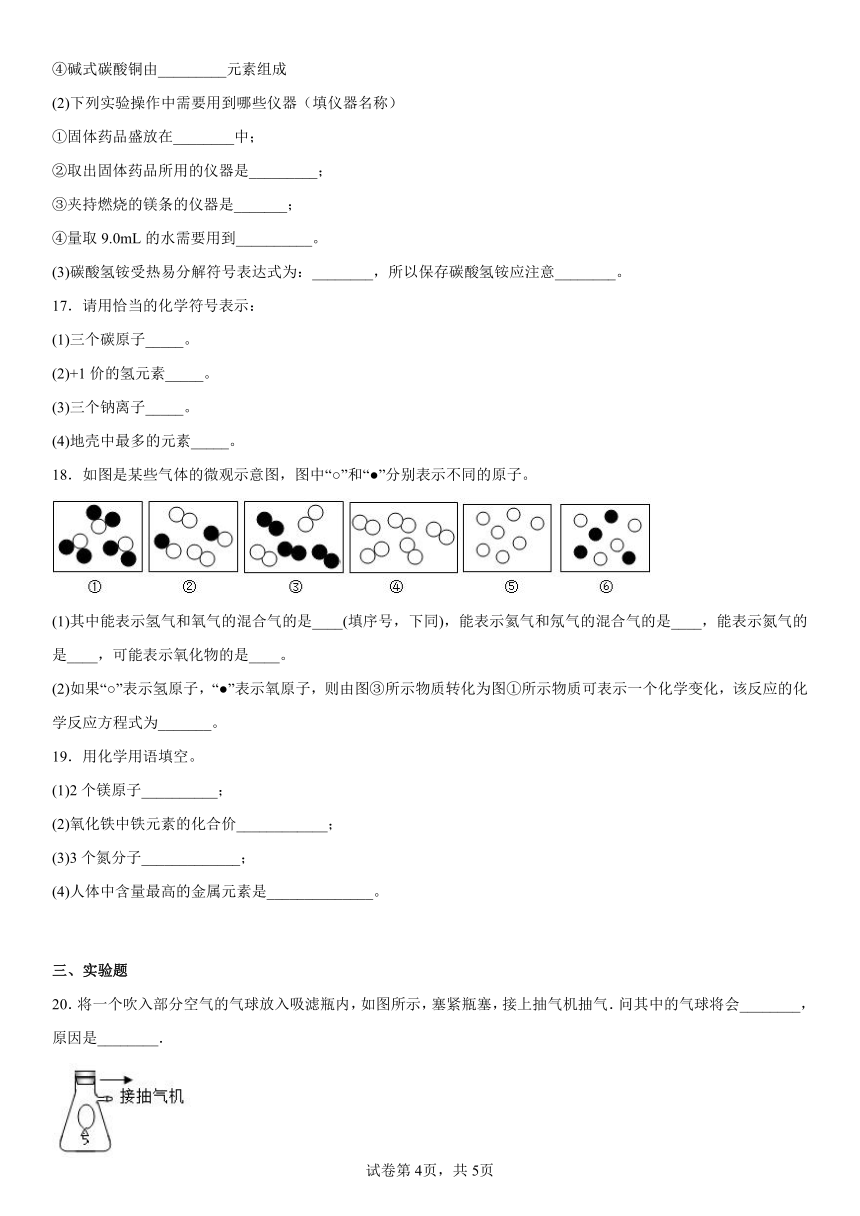
18.如图是某些气体的微观示意图,图中“○”和“●”分别表示不同的原子。
(1)其中能表示氢气和氧气的混合气的是____(填序号,下同),能表示氦气和氖气的混合气的是____,能表示氮气的是____,可能表示氧化物的是____。
(2)如果“○”表示氢原子,“●”表示氧原子,则由图③所示物质转化为图①所示物质可表示一个化学变化,该反应的化学反应方程式为_______。
19.用化学用语填空。
(1)2个镁原子__________;
(2)氧化铁中铁元素的化合价____________;
(3)3个氮分子_____________;
(4)人体中含量最高的金属元素是______________。
三、实验题
20.将一个吹入部分空气的气球放入吸滤瓶内,如图所示,塞紧瓶塞,接上抽气机抽气.问其中的气球将会________,原因是________.
21.图Ⅰ是晓娟按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小佳对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C.、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是_______;
(2)进行操作b时观察到的现象是_______;
(3)由此可以得到的实验结论是①_______,②_______;
(4)对比改进前的实验,改进后实验的优点是_______。
四、计算题
22.某品牌免洗手消毒凝胶,是以乙醇和正丙醇为主要有效成分的消毒凝胶,其中正丙醇的化学式为C3H7OH。请计算:
(1)一个正丙醇分子中含有_________个原子。
(2)正丙醇中碳、氢元素的质量比为_________(填最简整数比)。
23.葡萄糖(C6H12O6)是人类生命活动所需能量的重要来源,剧烈运动后肌肉酸痛是由于部分葡萄糖转化成了乳酸(C3H6O3)。
(1)C6H12O6的相对分子质量为___________。
(2)葡萄糖中碳元素的质量分数___________乳酸中碳元素的质量分数(填“>”、“<”或“=”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.A
4.B
5.B
6.A
7.C
8.A
9.D
10.D
11.D
12.B
13.B
14.C
15.A
16.(1) Ca Mg SO2 Cu、H、O、C
(2) 广口瓶 药匙 坩埚钳 量筒和滴管
(3) 密封阴凉处
17.(1)3C
(2)
(3)3Na+
(4)O
18. ③ ⑥ ④ ①
19.(1)2Mg
(2)
(3)3N2
(4)Ca
20. 变大 吸滤瓶内的空气分子减少,压强变小,球内的空气中分子间的空隙会变大,气体体积膨胀,气球会膨胀
21.(1)进行对比
(2)B试管中的酚酞溶液慢慢变红色,C试管中的酚酞溶液很快变红色
(3) 分子是真实存在的,并总在不断运动的 温度越高,分子运动速度越快
(4)能尽量防止氨气逸出(或能够说明分子运动的快慢等。)
22.(1)12
(2)9:2
23.(1)葡萄糖的相对分子质量为:12×6+12+16×6=180
(2)葡萄糖中碳元素的质量分数为:,乳酸中碳元素的质量分数为: ,故葡萄糖中碳元素的质量分数=乳酸中碳元素的质量分数
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
2.2020年6月23日我国的北斗导航“收官之星”在西昌发射成功,北斗导航卫星系统采用铷原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的原子结构示意图如图所示。下列说法不正确的是
A.铷单质具有导电性
B.m的值是37,n的值是1
C.铷的相对原子质量为85.47
D.氯化铷的化学式为RbCl2
3.物质由微观粒子构成。下列都由离子构成的一组物质是
A.氯化钠、硫酸铜 B.水、干冰 C.金刚石、氧化汞 D.氦气、氨气
4.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
5.荷叶中含有的荷叶碱(化学式为C19H21NO2)具有降脂、抑菌等作用。下列有关荷叶碱的说法,正确的是
A.含有O2 B.由四种非金属元素组成
C.属于氧化物 D.其中氢元素的质量分数最大
6.在新冠疫情防控过程中,人们使用的一种免洗洗手消毒液里含有三氯羟基二苯醚(简称三氯生,化学式为C12H7O2Cl3)。下列表述正确的是
A.三氯生由碳、氢、氧、氯元素组成
B.一个三氯生分子中含有一个氧分子
C.三氯生的相对分子质量为289.5g
D.三氯生中氢、氧元素质量比为7:2
7.按氯元素化合价由低至高的排列顺序,在HCl、X、HClO、KClO3中,X代表的是
A.NaCl B.KClO C.Cl2 D.ClO2
8.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
9.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
10.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
11.下列有关粒子的说法中正确的是
A.原子的原子核都是由质子和中子构成的 B.分子可分,而原子不可再分
C.原子可转化成离子,离子不能转化为原子 D.钠原子和钠离子核电荷数相同
12.已知碘原子的相对原子质量为127,其原子核内有74个中子,则碘原子核外的电子数为
A.74 B.53 C.54 D.72
13.原子核中一定含有的粒子是( )
A.中子 B.质子 C.电子 D.质子和电子
14.防疫期间常用酒精消毒,在消毒过程中我们能闻到酒精散发出的特殊气味,主要是因为
A.分子的体积很小 B.分子间有间隔
C.分子在不断运动 D.分子可以再分
15.人体中有50多种元素,含量如图。下列说法正确的是
A.人体中氢元素含量约为10%
B.含量最高的金属元素是钠
C.人体中微量元素共有10种
D.缺铁会引起骨质疏松
二、填空题
16.回答下列问题
(1)用元素符号或化学式填空:
①钙元素______;
②可用于制照明弹的金属________;
③二氧化硫______;
④碱式碳酸铜由_________元素组成
(2)下列实验操作中需要用到哪些仪器(填仪器名称)
①固体药品盛放在________中;
②取出固体药品所用的仪器是_________;
③夹持燃烧的镁条的仪器是_______;
④量取9.0mL的水需要用到__________。
(3)碳酸氢铵受热易分解符号表达式为:________,所以保存碳酸氢铵应注意________。
17.请用恰当的化学符号表示:
(1)三个碳原子_____。
(2)+1价的氢元素_____。
(3)三个钠离子_____。
(4)地壳中最多的元素_____。
18.如图是某些气体的微观示意图,图中“○”和“●”分别表示不同的原子。
(1)其中能表示氢气和氧气的混合气的是____(填序号,下同),能表示氦气和氖气的混合气的是____,能表示氮气的是____,可能表示氧化物的是____。
(2)如果“○”表示氢原子,“●”表示氧原子,则由图③所示物质转化为图①所示物质可表示一个化学变化,该反应的化学反应方程式为_______。
19.用化学用语填空。
(1)2个镁原子__________;
(2)氧化铁中铁元素的化合价____________;
(3)3个氮分子_____________;
(4)人体中含量最高的金属元素是______________。
三、实验题
20.将一个吹入部分空气的气球放入吸滤瓶内,如图所示,塞紧瓶塞,接上抽气机抽气.问其中的气球将会________,原因是________.
21.图Ⅰ是晓娟按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。于是小佳对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】
a.向B、C.、E三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。
b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:
(1)E试管放有酚酞溶液的目的是_______;
(2)进行操作b时观察到的现象是_______;
(3)由此可以得到的实验结论是①_______,②_______;
(4)对比改进前的实验,改进后实验的优点是_______。
四、计算题
22.某品牌免洗手消毒凝胶,是以乙醇和正丙醇为主要有效成分的消毒凝胶,其中正丙醇的化学式为C3H7OH。请计算:
(1)一个正丙醇分子中含有_________个原子。
(2)正丙醇中碳、氢元素的质量比为_________(填最简整数比)。
23.葡萄糖(C6H12O6)是人类生命活动所需能量的重要来源,剧烈运动后肌肉酸痛是由于部分葡萄糖转化成了乳酸(C3H6O3)。
(1)C6H12O6的相对分子质量为___________。
(2)葡萄糖中碳元素的质量分数___________乳酸中碳元素的质量分数(填“>”、“<”或“=”)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.A
4.B
5.B
6.A
7.C
8.A
9.D
10.D
11.D
12.B
13.B
14.C
15.A
16.(1) Ca Mg SO2 Cu、H、O、C
(2) 广口瓶 药匙 坩埚钳 量筒和滴管
(3) 密封阴凉处
17.(1)3C
(2)
(3)3Na+
(4)O
18. ③ ⑥ ④ ①
19.(1)2Mg
(2)
(3)3N2
(4)Ca
20. 变大 吸滤瓶内的空气分子减少,压强变小,球内的空气中分子间的空隙会变大,气体体积膨胀,气球会膨胀
21.(1)进行对比
(2)B试管中的酚酞溶液慢慢变红色,C试管中的酚酞溶液很快变红色
(3) 分子是真实存在的,并总在不断运动的 温度越高,分子运动速度越快
(4)能尽量防止氨气逸出(或能够说明分子运动的快慢等。)
22.(1)12
(2)9:2
23.(1)葡萄糖的相对分子质量为:12×6+12+16×6=180
(2)葡萄糖中碳元素的质量分数为:,乳酸中碳元素的质量分数为: ,故葡萄糖中碳元素的质量分数=乳酸中碳元素的质量分数
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
