科粤版(2012)化学专题复习生命之源-水(含答案)
文档属性
| 名称 | 科粤版(2012)化学专题复习生命之源-水(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 102.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-11-30 00:00:00 | ||
图片预览



文档简介
科粤版(2012) 化学专题复习 生命之源-水
一、单选题
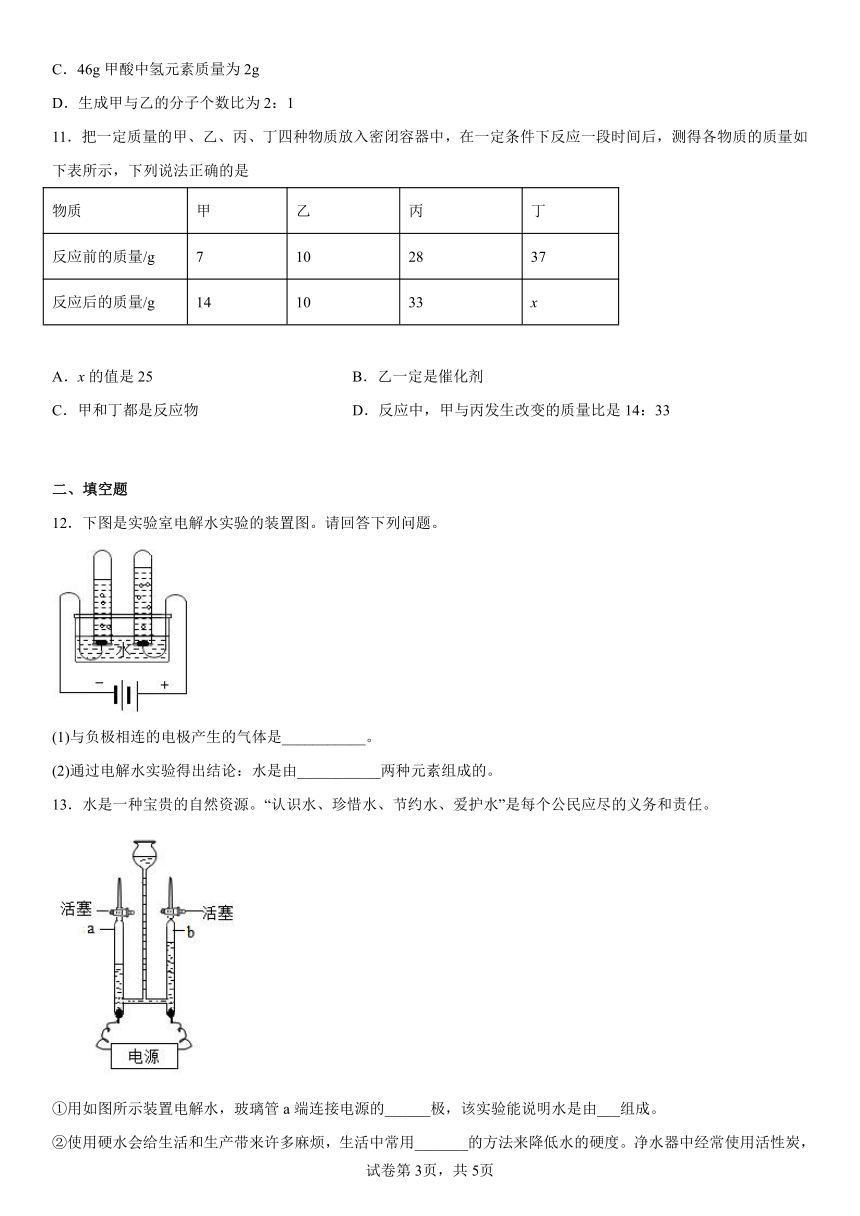
1.由太湖水生产自来水的部分处理过程如下。有关说法不正确的是
A.用细沙“过滤”可滤除水中的细小颗粒
B.用活性炭“吸附”可除去水中的色素和异味
C.上述处理过程应包含“蒸馏”
D.经过处理获得的自来水仍是混合物
2.我国科研人员将二氧化碳高效合成为可供微生物直接利用的物质X,合成过程中主要物质向转化的微现示意图如下、下列说法错误的是
A.催化剂提高了合成效率 B.X的化学式为CH2O
C.CO2合成的过程中伴随能量变化 D.一定有含氢元素的物质参与合成反应
3.清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下(图中的微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O2 B.参加反应的甲与乙的质量比为 3∶1
C.甲是单质,乙、丙、丁均为氧化物 D.该反应遵守质量守恒定律
4.载人航天器中处理CO2的另一种方法是将CO2与氢气反应,反应前后分子种类变化的微观示意图如下:
下列说法正确的是
A.乙和丙的元素组成相同 B.丙的相对分子质量为16
C.反应前后氧原子个数不相等 D.参加反应的甲和乙的分子个数比为4:1
5.广州北部水厂采用了先进的超滤膜净水技术,超滤膜能有效去除水中的悬浮物、藻类、细菌等不溶性杂质。关于水的净化,下列说法不正确的是
A.加入明矾能促进水中悬浮杂质沉降
B.活性炭可除去水中异味
C.超滤膜可降低水的硬度
D.自来水属于混合物
6.水对于生命活动、工农业生产具有重要意义、下列有关水的说法错误的是
A.农业上采用喷灌和滴灌可以节约用水
B.工业废水可以不经处理直接排入河道
C.生活中可以用煮沸的方法降低水的硬度
D.工业上可采用蒸馏法从海水中获取淡水
7.根据化学方程式,推断出B与A的相对分子质量相差( )
A.37.0 B.95.0 C.18.5 D.58.5
8.某物质1.6克在空气中充分燃烧共生成4.4克二氧化碳和3.6克水。则下列说法正确的是
①该物质中一定含有氧元素; ②该物质中一定不含氧元素; ③该物质中一定含有碳、氢元素; ④该物质的一个分子中碳、氢原子的个数比为1:4; ⑤该物质中氢元素的质量分数最大
A.①②③④⑤
B.②③④
C.③④⑤
D.②③④⑤
9.下列做法违背节水理念的是( )
A.防止水龙头滴漏
B.采用大水漫灌农作物
C.使用节水器具
D.循环利用工业用水
10.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
11.把一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表所示,下列说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 7 10 28 37
反应后的质量/g 14 10 33 x
A.x的值是25 B.乙一定是催化剂
C.甲和丁都是反应物 D.反应中,甲与丙发生改变的质量比是14:33
二、填空题
12.下图是实验室电解水实验的装置图。请回答下列问题。
(1)与负极相连的电极产生的气体是___________。
(2)通过电解水实验得出结论:水是由___________两种元素组成的。
13.水是一种宝贵的自然资源。“认识水、珍惜水、节约水、爱护水”是每个公民应尽的义务和责任。
①用如图所示装置电解水,玻璃管a端连接电源的______极,该实验能说明水是由___组成。
②使用硬水会给生活和生产带来许多麻烦,生活中常用_______的方法来降低水的硬度。净水器中经常使用活性炭,主要是利用活性炭的_______性。
③我国淡水资源并不丰富,节约用水是爱护水资源的一种途径,请写出节约用水的一种具体做法_____。
14.某工厂将矿物燃料燃烧产生的废气中的SO2收集起来,既可以生产稀硫酸,又能制备氢气。其反应过程如下图所示:
(1)写出反应器中发生化学反应的方程式_______。
(2)反应器中S元素的化合价变化为+4→_______。
(3)膜反应器中发生的是分解反应,则X的化学式是_______。
15.宏观、微观和符号之间建立联系是学习化学的重要思维方法。下图是某汽车尾气处理过程中发生的一个反应,请回答下列问题。
(1)图示中的物质,属于单质的是________(填化学式);
(2)该反应中,参加反应的X与生成的Y的分子个数最简整数比是____________;
(3)该反应前后,化合价发生了变化的元素是__________(填元素符号),该元素在图示相关物质中的最低化合价是_______。
三、实验题
16.请仔细观察下图,是测定化学反应前后质量变化的情况的实验,用以验证质量守恒定律。试回答:
(1)实验A中锥形瓶底部预先铺一层薄薄的细沙的目的_______。
(2)实验A中观察到锥形瓶内红磷燃烧,产生大量的_______,气球的现象是_______,装置放回天平后天平_______(填“平衡”“向左偏”“向右偏”),可用于验证质量守恒定律。
(3)上述三个反应前后容器中物质的总质量不相等的是____,符合质量守恒定律的是____(均填实验装置序号)
(4)实验B中,最终天平不平衡的原因是碳酸钠和盐酸反应生成的_______气体逸散空气中,最终没有称量到所有生成物的总质量。
(5)从微观角度分析化学变化遵守质量守恒定律的原因是:_______。
(6)该同学实验后反思:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在_______装置中进行。
17.下列是两个关于水的实验。
(1)实验1,反应的化学方程式为________。
(2)下列说法正确的是______(填序号)。
A 实验1,试管a中得到的气体能燃烧
B 实验1,反应前后原子的种类、个数均改变
C 实验2,水变化前后分子的种类不变
四、计算题
18.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是 。
(2)工业上用含氧化铁480t的赤铁矿为原料炼铁,可得到含杂质4%的生铁质量为多少?(根据化学方程式计算并写出解题过程)
19.化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.D
4.D
5.C
6.B
7.C
8.B
9.B
10.C
11.A
12.(1)H2
(2)氢和氧
13. 负 氢元素和氧元素 煮沸 吸附 淘米水浇花(合理即可)
14. +6 H2
15. N2 2:3 N -3
16.(1)防止红磷燃烧时放热炸裂瓶底
(2) 白烟 先膨胀后缩小 平衡
(3) B ABC
(4)CO2
(5)化学反应前后,原子的种类、数目、质量不变
(6)密闭
17. AC
18.(1)焦炭(2)350t
19.(1)4g。
(2)设反应后所得溶液中溶质的质量为x
解得:x=8g
反应后所得溶液中溶质的质量分数为:=16%
答:反应后所得溶液中溶质的质量分数为16%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.由太湖水生产自来水的部分处理过程如下。有关说法不正确的是
A.用细沙“过滤”可滤除水中的细小颗粒
B.用活性炭“吸附”可除去水中的色素和异味
C.上述处理过程应包含“蒸馏”
D.经过处理获得的自来水仍是混合物
2.我国科研人员将二氧化碳高效合成为可供微生物直接利用的物质X,合成过程中主要物质向转化的微现示意图如下、下列说法错误的是
A.催化剂提高了合成效率 B.X的化学式为CH2O
C.CO2合成的过程中伴随能量变化 D.一定有含氢元素的物质参与合成反应
3.清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下(图中的微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O2 B.参加反应的甲与乙的质量比为 3∶1
C.甲是单质,乙、丙、丁均为氧化物 D.该反应遵守质量守恒定律
4.载人航天器中处理CO2的另一种方法是将CO2与氢气反应,反应前后分子种类变化的微观示意图如下:
下列说法正确的是
A.乙和丙的元素组成相同 B.丙的相对分子质量为16
C.反应前后氧原子个数不相等 D.参加反应的甲和乙的分子个数比为4:1
5.广州北部水厂采用了先进的超滤膜净水技术,超滤膜能有效去除水中的悬浮物、藻类、细菌等不溶性杂质。关于水的净化,下列说法不正确的是
A.加入明矾能促进水中悬浮杂质沉降
B.活性炭可除去水中异味
C.超滤膜可降低水的硬度
D.自来水属于混合物
6.水对于生命活动、工农业生产具有重要意义、下列有关水的说法错误的是
A.农业上采用喷灌和滴灌可以节约用水
B.工业废水可以不经处理直接排入河道
C.生活中可以用煮沸的方法降低水的硬度
D.工业上可采用蒸馏法从海水中获取淡水
7.根据化学方程式,推断出B与A的相对分子质量相差( )
A.37.0 B.95.0 C.18.5 D.58.5
8.某物质1.6克在空气中充分燃烧共生成4.4克二氧化碳和3.6克水。则下列说法正确的是
①该物质中一定含有氧元素; ②该物质中一定不含氧元素; ③该物质中一定含有碳、氢元素; ④该物质的一个分子中碳、氢原子的个数比为1:4; ⑤该物质中氢元素的质量分数最大
A.①②③④⑤
B.②③④
C.③④⑤
D.②③④⑤
9.下列做法违背节水理念的是( )
A.防止水龙头滴漏
B.采用大水漫灌农作物
C.使用节水器具
D.循环利用工业用水
10.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
11.把一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表所示,下列说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 7 10 28 37
反应后的质量/g 14 10 33 x
A.x的值是25 B.乙一定是催化剂
C.甲和丁都是反应物 D.反应中,甲与丙发生改变的质量比是14:33
二、填空题
12.下图是实验室电解水实验的装置图。请回答下列问题。
(1)与负极相连的电极产生的气体是___________。
(2)通过电解水实验得出结论:水是由___________两种元素组成的。
13.水是一种宝贵的自然资源。“认识水、珍惜水、节约水、爱护水”是每个公民应尽的义务和责任。
①用如图所示装置电解水,玻璃管a端连接电源的______极,该实验能说明水是由___组成。
②使用硬水会给生活和生产带来许多麻烦,生活中常用_______的方法来降低水的硬度。净水器中经常使用活性炭,主要是利用活性炭的_______性。
③我国淡水资源并不丰富,节约用水是爱护水资源的一种途径,请写出节约用水的一种具体做法_____。
14.某工厂将矿物燃料燃烧产生的废气中的SO2收集起来,既可以生产稀硫酸,又能制备氢气。其反应过程如下图所示:
(1)写出反应器中发生化学反应的方程式_______。
(2)反应器中S元素的化合价变化为+4→_______。
(3)膜反应器中发生的是分解反应,则X的化学式是_______。
15.宏观、微观和符号之间建立联系是学习化学的重要思维方法。下图是某汽车尾气处理过程中发生的一个反应,请回答下列问题。
(1)图示中的物质,属于单质的是________(填化学式);
(2)该反应中,参加反应的X与生成的Y的分子个数最简整数比是____________;
(3)该反应前后,化合价发生了变化的元素是__________(填元素符号),该元素在图示相关物质中的最低化合价是_______。
三、实验题
16.请仔细观察下图,是测定化学反应前后质量变化的情况的实验,用以验证质量守恒定律。试回答:
(1)实验A中锥形瓶底部预先铺一层薄薄的细沙的目的_______。
(2)实验A中观察到锥形瓶内红磷燃烧,产生大量的_______,气球的现象是_______,装置放回天平后天平_______(填“平衡”“向左偏”“向右偏”),可用于验证质量守恒定律。
(3)上述三个反应前后容器中物质的总质量不相等的是____,符合质量守恒定律的是____(均填实验装置序号)
(4)实验B中,最终天平不平衡的原因是碳酸钠和盐酸反应生成的_______气体逸散空气中,最终没有称量到所有生成物的总质量。
(5)从微观角度分析化学变化遵守质量守恒定律的原因是:_______。
(6)该同学实验后反思:在探究化学反应前后物质的总质量是否发生改变时,对于有气体参加或有气体生成的反应一定要在_______装置中进行。
17.下列是两个关于水的实验。
(1)实验1,反应的化学方程式为________。
(2)下列说法正确的是______(填序号)。
A 实验1,试管a中得到的气体能燃烧
B 实验1,反应前后原子的种类、个数均改变
C 实验2,水变化前后分子的种类不变
四、计算题
18.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是 。
(2)工业上用含氧化铁480t的赤铁矿为原料炼铁,可得到含杂质4%的生铁质量为多少?(根据化学方程式计算并写出解题过程)
19.化学兴趣小组的同学用46g稀硫酸与一定质量的氧化铜恰好完全反应,反应后得到的溶液质量为50g。求:
(1)氧化铜的质量为:___________g。
(2)反应后所得溶液中溶质的质量分数。
【提示:CuO+H2SO4═CuSO4+H2O】
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.D
4.D
5.C
6.B
7.C
8.B
9.B
10.C
11.A
12.(1)H2
(2)氢和氧
13. 负 氢元素和氧元素 煮沸 吸附 淘米水浇花(合理即可)
14. +6 H2
15. N2 2:3 N -3
16.(1)防止红磷燃烧时放热炸裂瓶底
(2) 白烟 先膨胀后缩小 平衡
(3) B ABC
(4)CO2
(5)化学反应前后,原子的种类、数目、质量不变
(6)密闭
17. AC
18.(1)焦炭(2)350t
19.(1)4g。
(2)设反应后所得溶液中溶质的质量为x
解得:x=8g
反应后所得溶液中溶质的质量分数为:=16%
答:反应后所得溶液中溶质的质量分数为16%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
