福建省泉州市名校2022-2023学年高三上学期期中考联考化学试题(Word版含答案)
文档属性
| 名称 | 福建省泉州市名校2022-2023学年高三上学期期中考联考化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 533.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-02 00:00:00 | ||
图片预览




文档简介
泉州市名校2022-2023学年高三上学期期中考联考
化学试卷
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cu 64
一、选择题:本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一项符合题目要求。
1.我国是一个拥有五千年文化传承的文明古国,文物是传承文化的重要载体。下列对文物的说法正确的是( )
选项 A B C D
文物图片
文物 《千里江山图》 兵马俑 马王堆汉墓出土的丝绸 西汉皇后之玺
对文物的说法 可选用FeO作为红色颜料 制作兵马俑的黏土的主要成分为硅酸盐 丝绸可用NaOH溶液进行浸泡、洗涤 制作西汉皇后之玺的玉石为天然有机高分子材料
2.科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究,下列分类方法或概念表达科学合理的是( )
A.在水溶液中和熔融状态下都能导电的化合物才属于电解质
B.CaO、、、、CuO等金属氧化物都属于碱性氧化物
C.依据丁达尔效应可以将分散系分为胶体或非胶体(包括溶液和独液)两大类
D.金刚石、石墨和,、和,和分别属于碳、氢、氧的同位素
3.我国“奋斗者”号载人潜水器在马里亚纳海沟成功坐底,坐底深度为10909米。“奋斗者”号载人舱球壳的材料是一种由Ti、Al、Sn和Si等组成的合金,其中Si和Sn两种元素在元素周期表中位于同一纵列,下列有关说法错误的是( )
A.基态Sn原子的价电子排布式为
B.基态Si原子和基态Ti原子的价电子数不相等
C.基态Ti原子核外有7种能量不同的电子
D.基态Al原子核外有13种运动状态不同的电子
4.下列说法正确的是( )
A.用丁达尔效应区分溶液与胶体
B.用浓硫酸干燥碘化氢气体
C.用乙醇萃取碘水中的碘
D.用分液漏斗可分离溴苯和溴的混合物
5.下列离子方程式正确的是( )
A.过量铁粉与稀硝酸反应:
B.铜与浓硫酸在加热条件下反应:
C.将二氧化硫通入溴水中,溴水褪色:
D.向中投入固体:
6.下列变化中涉及氧化还原反应的是( )
A.向溴化钠溶液中滴加溶液,有浅黄色沉淀产生
B.向蛋白质溶液中滴入饱和NaCl溶液,有沉淀产生
C.向碱化的蔗糖水解液中滴加银氨溶液,水浴加热后有光亮的银镜出现
D.向含的溶液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生
7.下表所列各组物质中,物质之间通过一步反应不能实现“X→Y→Z”转化的是( )
选项 X Y Z
A
B
C
D
8.我国科研人员发现中药成分黄芩素(结构如图)能明显抑制新冠病毒的活性。下列有关黄芩素的说法正确的是( )
A分子中碳原子的杂化方式有3种
B.分子中所有原子一定共平面
C.在NaOH条件下能发生水解反应
D.1mol黄芩素最多能与8mol发生加成反应
9.X、Y、Z、W为原子序数依次增大的四种短周期主族元素。基态X原子的2p轨道半充满,Y是地壳中含量最高的元素,且其原子最外层电子数是W原子最外层电子数的2倍,Z为其同周期元素中原子半径最大的。下列说法正确的是( )
A.第一电离能:W>Z
B.最简单离子平径:YC.X的最高价氧化物对应的水化物为弱酸
D.由Z与Y形成的化合物只有一种
10.下列实验操作可以达到实验目的的是( )
实验目的 实验操作
A 制备胶体 将稀溶液滴入NaOH溶液中
B 比较Al和Fe的金属性强弱 将Al、Fe、NaOH溶液组成原电池
C 除去中混有的HCl气体 通入盛有饱和溶液的洗气瓶
D 除去Cu粉中混有的CuO 加入稀硝酸,过滤、洗涤、干燥
二、非选择题:本题共5小题,共60分。
11.(12分)前20号元素组成的某种化合物是实验室常用的一种化学试剂,W、X、Y、Z的原子序数依次增大,仅W、X位于同周期且W、X、Y的最外层电子数之和为15。回答下列问题:
(1)的结构示意图为____________,X在元素周期表中的位置为____________。
(2)常温下,将Z的单质投入水中,发生反应的离子方程式为__________________。
(3)将ZYWX的水溶液滴入溶液中,发生反应的离子方程式为__________________。
(4)ZYWX中的两种非金属元素的氢化物均可发生如下转化:
①若该氢化物的水溶液呈碱性,则该氢化物的电子式为______。图中该氢化物转化为甲的化学方程式为__________________。
②若该氢化物的水溶液呈酸性,则该氢化物与丙的浓溶液反应时,出现淡黄色浑浊且有刺激性气味的气体放出,每生成22.4L(标准状况下)气体,生成沉淀的质量为______。
12.(10分)镍铜合金是由60%镍、339%铜、7%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能和高温强度,耐蚀性强,耐磨性好,容易加工,可作为航空发动机的结构材料。根据所学知识,回答下列问题:
(1)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则绿色对应的辐射波长为______(填标号)。
A.577~492nm B.597~577nm C.622~597nm
(2)基态的价电子排布式为______。
(3)乙酰丙酮中键与键数目之比为______。
(4)Cu与Fe的第二电离能分别为,,大于的主要原因是________________________。
(5)已知的立方晶胞结构如图所示。
①已知a、b的坐标参数依次为(0,0,0)、,则d的坐标参数为______。
②晶胞边长为c pm,该晶体的密度为______,(列计算式,设为阿伏加德罗常数的数值)
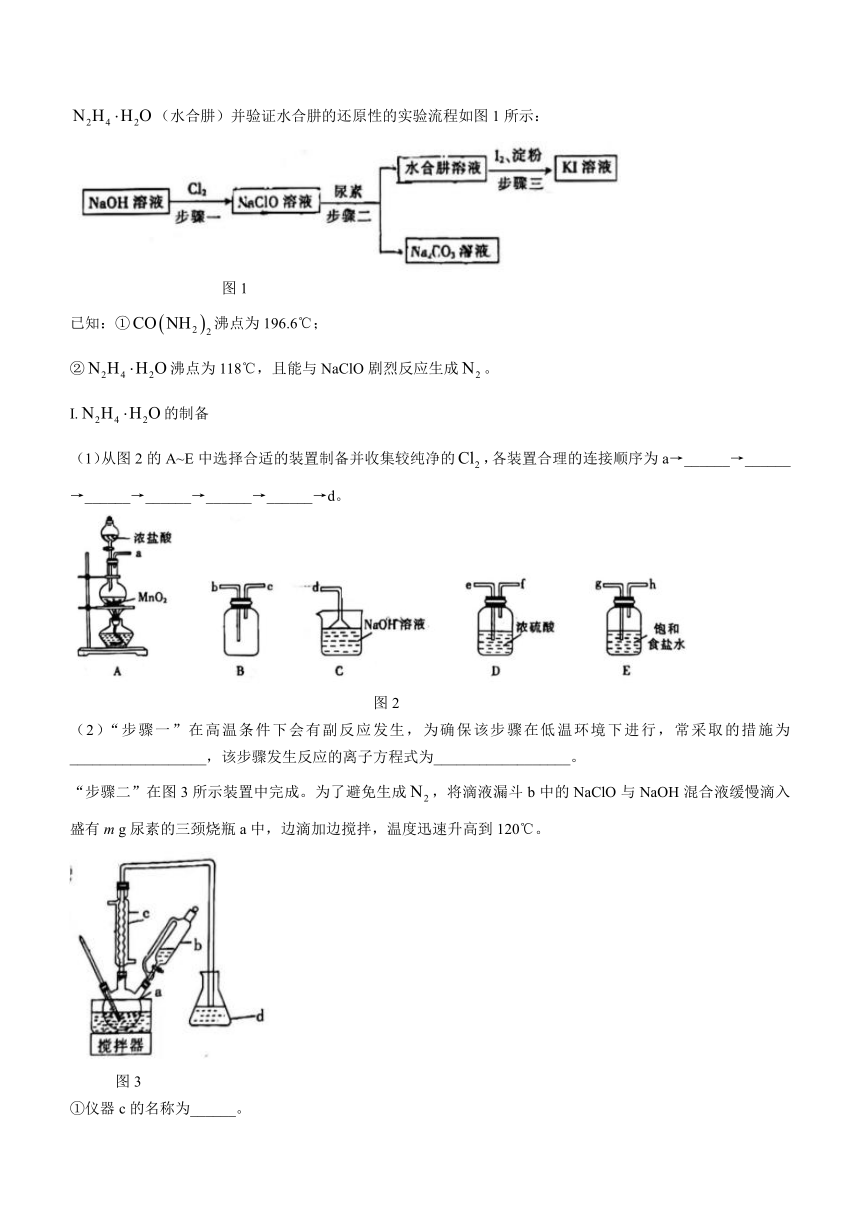
13.(14分)尿素是目前使用量较大的一种化学氮肥。某化学实验小组以尿素为原料制备(水合肼)并验证水合肼的还原性的实验流程如图1所示:
图1
已知:①沸点为196.6℃;
②沸点为118℃,且能与NaClO剧烈反应生成。
I.的制备
(1)从图2的A~E中选择合适的装置制备并收集较纯净的,各装置合理的连接顺序为a→______→______→______→______→______→______→d。
图2
(2)“步骤一”在高温条件下会有副反应发生,为确保该步骤在低温环境下进行,常采取的措施为__________________,该步骤发生反应的离子方程式为__________________。
“步骤二”在图3所示装置中完成。为了避免生成,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有m g尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
图3
①仪器c的名称为______。
②生成水合肼的化学方程式为__________________。
II.验证的还原性
(4)将“步骤二”制得的水合肼配成1000mL溶液,移出25mL溶液于锥形瓶中,滴加2滴淀粉溶液,用的溶液滴定,当滴定完全时,消耗溶液V mL。
①滴定过程中水合肼被氧化为,反应的化学方程式为__________________。
②配成的水合肼的浓度______(用含V的代数式表示)。
③的产率为______(用含m、V的代数式表示)。
14.(14分)硫化氢广泛存在于燃气及废水中、热分解或氧化硫化氢有利于环境保护并回收硫资源。回答下列问题:
(1)写出的电子式:______。
(2)与溶液反应可生成两种酸式盐,该反应的离子方程式为__________________。
(3)氯气可用于除去废水中,写出反应的化学方程式:__________________。
(4)将含尾气的空气按一定流速通入酸性溶液中,可实现含尾气的空气脱硫,在溶液吸收的过程中也发生了反应,溶液中的及被吸收的随时间t的变化如图1所示。时刻前,溶液中减小速率较快,时刻后,溶液中基本不变,其原因是________________________。
图1
(5)科学家设计出质子膜燃料电池,实现了利用废气资源回收能量并得到单质硫。质子膜燃料电池的结构如图2所示。
图2
①电极b极为______(填“正极”或“负极”),写出该电极的电极反应式:__________________。
②电池工作时,经质子膜进入______(填“a极”或“b极”)区。
15.(10分)化合物M具有行气活血功效,其一种合成路线如下:
请回答下列问题:
(1)A的结构简式为______,D中官能团的名称是______。
(2)C→D的反应类型是______。
(3)已知:E的分子式为,写出D→E的化学方程式:__________________。
(4)有机物G为F在催化剂、加热条件下与足量反应后得到的产物,则1molG含______mol手性碳原子。
(5)芳香化合物H是B的同分异构体,同时满足下列条件的H的结构有______种。其中核磁共振氢谱上有5组峰且峰面积之比为6∶4∶2∶1∶1的结构简式为____________。
①除苯环外不含其他的环,且分子中只含1种官能团
②苯环上有2种取代基,且取代基的数目为5
高三化学试卷参考答案
1.B 2.C 3.B 4.A 5.D 6.C 7.B 8.D 9.A 10.C
11.(1)(1分);第二周期第VA族(2分)
(2)(2分)
(3)(2分)
(4)①(1分); (2分)
②32g(2分)
12.(1)A(1分)
(2)(1分)
(3)7∶1(2分)
(4)基态铜原子失去1个电子后,形成了全充满的稳定结构,较难再失去1个电子(2分)
(5)①(2分) ②(2分)
13.(1)g;h;e;f;b;c(2分)
(2)冰水浴(或冷水浴,1分); (2分)
(3)①(球形)冷凝管(1分)
②(不打“↑”不扣分,2分)
(4)①(2分)
②(2分)
③(2分)
14.(1)(2分)
(2)(2分)
(3)(未写“↓”不扣分,2分)
(4)时刻前,溶液中的浓度较大,与反应速率较快;时刻后,溶液中的被空气氧化为,生成的与发生氧化还原反应,这两个反应的速率近似相等。因此溶液中的的物质的量基本不变(3分)
(5)①正极(2分); (2分)
②b极(1分)
15.(1)(1分);醚键、酮羰基(2分)
(2)氧化反应(1分)
(3)(2分)
(4)5(1分)
(5)6(2分);(或,1分)
化学试卷
本试卷满分100分,考试用时75分钟。
注意事项:
1.答题前,考生务必将自己的姓名、考生号、考场号、座位号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
4.可能用到的相对原子质量:H 1 C 12 N 14 O 16 S 32 Cu 64
一、选择题:本题共10小题,每小题4分,共40分。在每小题给出的四个选项中,只有一项符合题目要求。
1.我国是一个拥有五千年文化传承的文明古国,文物是传承文化的重要载体。下列对文物的说法正确的是( )
选项 A B C D
文物图片
文物 《千里江山图》 兵马俑 马王堆汉墓出土的丝绸 西汉皇后之玺
对文物的说法 可选用FeO作为红色颜料 制作兵马俑的黏土的主要成分为硅酸盐 丝绸可用NaOH溶液进行浸泡、洗涤 制作西汉皇后之玺的玉石为天然有机高分子材料
2.科学的分类能够反映事物的本质特征,有利于人们分门别类地进行深入研究,下列分类方法或概念表达科学合理的是( )
A.在水溶液中和熔融状态下都能导电的化合物才属于电解质
B.CaO、、、、CuO等金属氧化物都属于碱性氧化物
C.依据丁达尔效应可以将分散系分为胶体或非胶体(包括溶液和独液)两大类
D.金刚石、石墨和,、和,和分别属于碳、氢、氧的同位素
3.我国“奋斗者”号载人潜水器在马里亚纳海沟成功坐底,坐底深度为10909米。“奋斗者”号载人舱球壳的材料是一种由Ti、Al、Sn和Si等组成的合金,其中Si和Sn两种元素在元素周期表中位于同一纵列,下列有关说法错误的是( )
A.基态Sn原子的价电子排布式为
B.基态Si原子和基态Ti原子的价电子数不相等
C.基态Ti原子核外有7种能量不同的电子
D.基态Al原子核外有13种运动状态不同的电子
4.下列说法正确的是( )
A.用丁达尔效应区分溶液与胶体
B.用浓硫酸干燥碘化氢气体
C.用乙醇萃取碘水中的碘
D.用分液漏斗可分离溴苯和溴的混合物
5.下列离子方程式正确的是( )
A.过量铁粉与稀硝酸反应:
B.铜与浓硫酸在加热条件下反应:
C.将二氧化硫通入溴水中,溴水褪色:
D.向中投入固体:
6.下列变化中涉及氧化还原反应的是( )
A.向溴化钠溶液中滴加溶液,有浅黄色沉淀产生
B.向蛋白质溶液中滴入饱和NaCl溶液,有沉淀产生
C.向碱化的蔗糖水解液中滴加银氨溶液,水浴加热后有光亮的银镜出现
D.向含的溶液中滴入硝酸酸化的BaCl2溶液,有白色沉淀产生
7.下表所列各组物质中,物质之间通过一步反应不能实现“X→Y→Z”转化的是( )
选项 X Y Z
A
B
C
D
8.我国科研人员发现中药成分黄芩素(结构如图)能明显抑制新冠病毒的活性。下列有关黄芩素的说法正确的是( )
A分子中碳原子的杂化方式有3种
B.分子中所有原子一定共平面
C.在NaOH条件下能发生水解反应
D.1mol黄芩素最多能与8mol发生加成反应
9.X、Y、Z、W为原子序数依次增大的四种短周期主族元素。基态X原子的2p轨道半充满,Y是地壳中含量最高的元素,且其原子最外层电子数是W原子最外层电子数的2倍,Z为其同周期元素中原子半径最大的。下列说法正确的是( )
A.第一电离能:W>Z
B.最简单离子平径:Y
D.由Z与Y形成的化合物只有一种
10.下列实验操作可以达到实验目的的是( )
实验目的 实验操作
A 制备胶体 将稀溶液滴入NaOH溶液中
B 比较Al和Fe的金属性强弱 将Al、Fe、NaOH溶液组成原电池
C 除去中混有的HCl气体 通入盛有饱和溶液的洗气瓶
D 除去Cu粉中混有的CuO 加入稀硝酸,过滤、洗涤、干燥
二、非选择题:本题共5小题,共60分。
11.(12分)前20号元素组成的某种化合物是实验室常用的一种化学试剂,W、X、Y、Z的原子序数依次增大,仅W、X位于同周期且W、X、Y的最外层电子数之和为15。回答下列问题:
(1)的结构示意图为____________,X在元素周期表中的位置为____________。
(2)常温下,将Z的单质投入水中,发生反应的离子方程式为__________________。
(3)将ZYWX的水溶液滴入溶液中,发生反应的离子方程式为__________________。
(4)ZYWX中的两种非金属元素的氢化物均可发生如下转化:
①若该氢化物的水溶液呈碱性,则该氢化物的电子式为______。图中该氢化物转化为甲的化学方程式为__________________。
②若该氢化物的水溶液呈酸性,则该氢化物与丙的浓溶液反应时,出现淡黄色浑浊且有刺激性气味的气体放出,每生成22.4L(标准状况下)气体,生成沉淀的质量为______。
12.(10分)镍铜合金是由60%镍、339%铜、7%铁三种金属组成的合金材料。镍铜合金有较好的室温力学性能和高温强度,耐蚀性强,耐磨性好,容易加工,可作为航空发动机的结构材料。根据所学知识,回答下列问题:
(1)铜元素的焰色试验呈绿色,下列三种波长为橙、黄、绿色对应的波长,则绿色对应的辐射波长为______(填标号)。
A.577~492nm B.597~577nm C.622~597nm
(2)基态的价电子排布式为______。
(3)乙酰丙酮中键与键数目之比为______。
(4)Cu与Fe的第二电离能分别为,,大于的主要原因是________________________。
(5)已知的立方晶胞结构如图所示。
①已知a、b的坐标参数依次为(0,0,0)、,则d的坐标参数为______。
②晶胞边长为c pm,该晶体的密度为______,(列计算式,设为阿伏加德罗常数的数值)
13.(14分)尿素是目前使用量较大的一种化学氮肥。某化学实验小组以尿素为原料制备(水合肼)并验证水合肼的还原性的实验流程如图1所示:
图1
已知:①沸点为196.6℃;
②沸点为118℃,且能与NaClO剧烈反应生成。
I.的制备
(1)从图2的A~E中选择合适的装置制备并收集较纯净的,各装置合理的连接顺序为a→______→______→______→______→______→______→d。
图2
(2)“步骤一”在高温条件下会有副反应发生,为确保该步骤在低温环境下进行,常采取的措施为__________________,该步骤发生反应的离子方程式为__________________。
“步骤二”在图3所示装置中完成。为了避免生成,将滴液漏斗b中的NaClO与NaOH混合液缓慢滴入盛有m g尿素的三颈烧瓶a中,边滴加边搅拌,温度迅速升高到120℃。
图3
①仪器c的名称为______。
②生成水合肼的化学方程式为__________________。
II.验证的还原性
(4)将“步骤二”制得的水合肼配成1000mL溶液,移出25mL溶液于锥形瓶中,滴加2滴淀粉溶液,用的溶液滴定,当滴定完全时,消耗溶液V mL。
①滴定过程中水合肼被氧化为,反应的化学方程式为__________________。
②配成的水合肼的浓度______(用含V的代数式表示)。
③的产率为______(用含m、V的代数式表示)。
14.(14分)硫化氢广泛存在于燃气及废水中、热分解或氧化硫化氢有利于环境保护并回收硫资源。回答下列问题:
(1)写出的电子式:______。
(2)与溶液反应可生成两种酸式盐,该反应的离子方程式为__________________。
(3)氯气可用于除去废水中,写出反应的化学方程式:__________________。
(4)将含尾气的空气按一定流速通入酸性溶液中,可实现含尾气的空气脱硫,在溶液吸收的过程中也发生了反应,溶液中的及被吸收的随时间t的变化如图1所示。时刻前,溶液中减小速率较快,时刻后,溶液中基本不变,其原因是________________________。
图1
(5)科学家设计出质子膜燃料电池,实现了利用废气资源回收能量并得到单质硫。质子膜燃料电池的结构如图2所示。
图2
①电极b极为______(填“正极”或“负极”),写出该电极的电极反应式:__________________。
②电池工作时,经质子膜进入______(填“a极”或“b极”)区。
15.(10分)化合物M具有行气活血功效,其一种合成路线如下:
请回答下列问题:
(1)A的结构简式为______,D中官能团的名称是______。
(2)C→D的反应类型是______。
(3)已知:E的分子式为,写出D→E的化学方程式:__________________。
(4)有机物G为F在催化剂、加热条件下与足量反应后得到的产物,则1molG含______mol手性碳原子。
(5)芳香化合物H是B的同分异构体,同时满足下列条件的H的结构有______种。其中核磁共振氢谱上有5组峰且峰面积之比为6∶4∶2∶1∶1的结构简式为____________。
①除苯环外不含其他的环,且分子中只含1种官能团
②苯环上有2种取代基,且取代基的数目为5
高三化学试卷参考答案
1.B 2.C 3.B 4.A 5.D 6.C 7.B 8.D 9.A 10.C
11.(1)(1分);第二周期第VA族(2分)
(2)(2分)
(3)(2分)
(4)①(1分); (2分)
②32g(2分)
12.(1)A(1分)
(2)(1分)
(3)7∶1(2分)
(4)基态铜原子失去1个电子后,形成了全充满的稳定结构,较难再失去1个电子(2分)
(5)①(2分) ②(2分)
13.(1)g;h;e;f;b;c(2分)
(2)冰水浴(或冷水浴,1分); (2分)
(3)①(球形)冷凝管(1分)
②(不打“↑”不扣分,2分)
(4)①(2分)
②(2分)
③(2分)
14.(1)(2分)
(2)(2分)
(3)(未写“↓”不扣分,2分)
(4)时刻前,溶液中的浓度较大,与反应速率较快;时刻后,溶液中的被空气氧化为,生成的与发生氧化还原反应,这两个反应的速率近似相等。因此溶液中的的物质的量基本不变(3分)
(5)①正极(2分); (2分)
②b极(1分)
15.(1)(1分);醚键、酮羰基(2分)
(2)氧化反应(1分)
(3)(2分)
(4)5(1分)
(5)6(2分);(或,1分)
同课章节目录
