第四节 化学式(全)
图片预览



文档简介
课件25张PPT。第四节 化学式化学式:用元素符号表示单质或者化合 物组成的式子叫化学式。氧气(O2)
氮气(N2)
红磷(P)
二氧化碳(CO2)
二氧化硫(SO2)四氧化三铁(Fe3O4)
水(H2O)
氢气(H2)
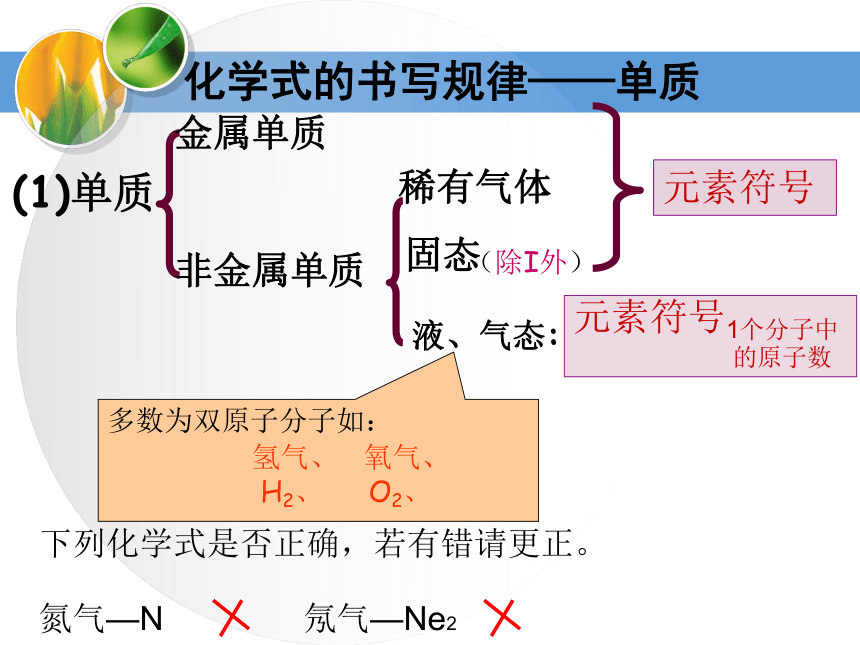
化学式表示的意义宏观意义:1、表示物质2、表示物质的组成微观意义:3、表示一个分子或原子 4、表示分子的构成 (1)单质金属单质
非金属单质
稀有气体固态液、气态:(除I外)多数为双原子分子如:
氢气、 氧气、
H2、 O2、 元素符号元素符号1个分子中
的原子数化学式的书写规律——单质下列化学式是否正确,若有错请更正。
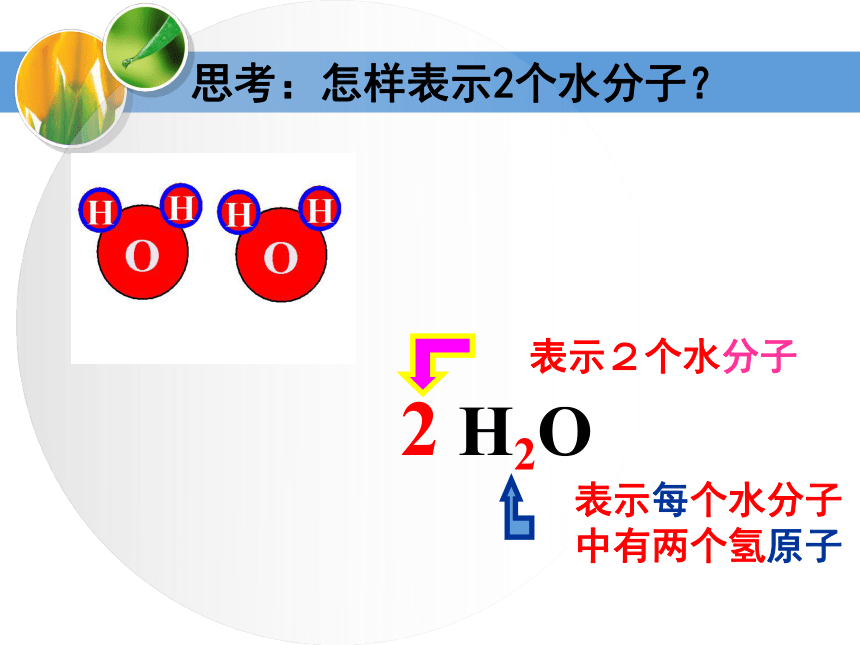
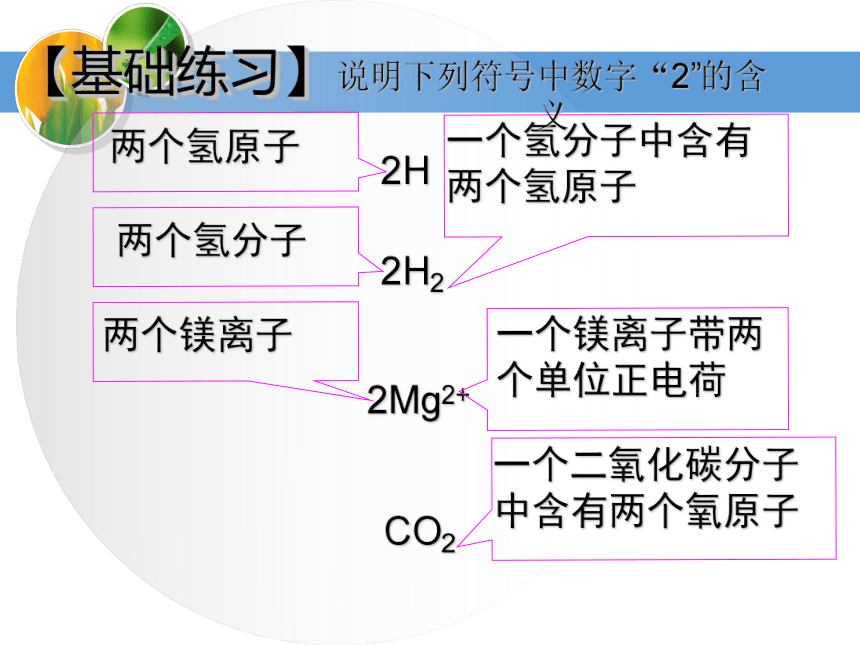
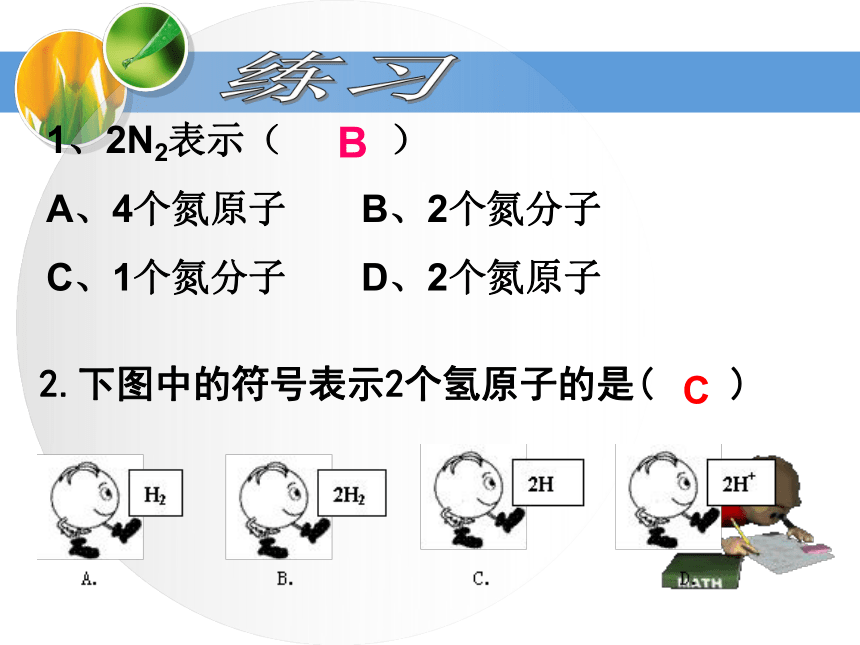
氮气—N 氖气—Ne2 思考:怎样表示2个水分子?H2O2【基础练习】2H22Mg2+CO22H说明下列符号中数字“2”的含义1、2N2表示( )
A、4个氮原子 B、2个氮分子
C、1个氮分子 D、2个氮原子B练习2.下图中的符号表示2个氢原子的是( )C3.下列符号:2N、N2 、H2O 、2CO、SO2 中,数字“2”的意义能用来表示分子个数的有( )
A.2个 B.1个 C. 4个 D.5个 B练习4.下列同学对“SO2”的认识中,不正确的是( ) A. B. C. D. B1、化合价概念:化学上用“化合价”来表示不同原子之间相互化合的数目。
单质元素化合价为零
化合价有正价和负价二、化合价化合物都有固定的组成,元素的原子之间有固定的个数比,如:2、化合价的表示方法:
1. 写在元素符号的正上方。
2. “+”、“ - ” 符号在前,数值在后。
3. “1”不能省略。例如:NaCl H2O+1-1+1-22分钟速记化合价口诀钾钠银氢+1价,
氟氯溴碘-1价,
钙镁钡锌+2价;
铝三硅四磷五价;
二四六硫,二四碳;
莫忘单质为零价。1.化合价有正价和负价。2.化合物中,通常氢为+1价,氧为-2 价,金属元素显正价 。3.许多元素的原子在不同的条件下可显示不
同的化合价。4.化合物里正负化合价的代数和为0。补:化合价的最高价不会超过+7价根据化学式求化合价KMnO4、K2MnO4、KClO3、H2SO4+7+6+5+6方法:化合物中元素的化合价代数和为零,利用不可变价求出可变价.1. 亚硝酸钠(NaNO2)是工业用盐,其外表似食盐,误食会使人中毒,亚硝酸钠中氮元素的化合价是( )
(A)十1 (B)十2 (C)十3 (D)十4C2. 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂,其中铁的化合价是( )
A、+2 B 、+3 C、+4 D、+6D3. 在Ca(ClO) 2中,氯元素的化合价为 氢氧化钙: Ca(OH)2 碳酸钙:CaCO3 氢氧化钠: NaOH 碳酸钡:BaCO3 氢氧化铁: Fe(OH)3 碳酸钠:Na2CO3观察下列物质的化学式原子团:做为一个整体参加反应的原子集团,也叫根原子团:作为一个整体参加反应的原子集团(就好象一个原子一样),原子团也叫做根。负一硝酸氢氧根
负二硫酸碳酸根
正一价的是铵根解密阿拉伯数字222个硫酸根离子2个硫酸根离子
硫酸根离子由硫元素和氧元素组成一个硫酸根离子有4个氧原子一个硫酸根离子所带电荷及化合价都为-2+6-2氧的化合价
为-2硫的化合价
为+6一、单质
金属单质:铁 铝
固态非金属单质:硫 磷
稀有气体:氖气 氦气氧气 氢气用元素符号表示(直接由原子构成)气体单质:O2H2一、单质如何写化合物的化学式呢?化学式的书写1. 写出组成物质的元素符号(正价在左,负价在右)
2. 根据正负代数和为零,确定原子个数比(交叉法)
3. 原子数写右下角,得化学式
4. 检查例:氧化铝、氯化镁练一练写出下面化合物的化学式。氧化铜 溴化镁 氯化锂,
氯化钙 氧化钠硫酸铝的化学式怎么写?根据元素和原子团的化合价写出下列物质的化学式KOHK2 SO4 Ca(OH)2CaSO4 Al(OH)3Al2(SO4)3Fe(OH)3Fe2(SO4)3+3巩固复习1.已知下列各元素的化合价,写出它们与氧结合成氧化物的化学式并命名:
Fe(+3) N(+5) Na(+1) C(+4)
Fe2O3 N2O5 Na2O CO22、写出下列各物质的化学式:
①氯化钠 ②氧化镁 ③氯化氢 ④氯化铁 NaClMgOHClFeCl3三、相对原子质量和式量相对分子质量(式量) 化学式中各原子的相对原子质量的总和。相对原子质量 原子实际质量与碳原子实际质量的一个比值,无单位根据化学式的计算
1、计算物质的相对分子质量1、计算KMnO4的相对分子质量。
2、计算(NH4)2CO3的相对分子质量。例1.计算二氧化碳(CO2)的相对分子质量。二氧化碳(CO2)的相对分子质量=12+16× 2=44例2.计算Cu2(OH)2CO3的相对分子质量。Cu2(OH)2CO3的相对分子质量=
64 × 2+(16+1) × 2+12+16 × 3=222已知R2O3的相对分子质量为102,氧的相对原子质量是16 ,则R 的相对原子质量是( )
A.56 B.27 C.112 D.7下列化学式(HnRO2n-2)的相对分子质量为M,则R的相对原子质量是 ( )
A.M-33n B.M-33n-32
C.M+33n+32 D.M-33n+32 B D
氮气(N2)
红磷(P)
二氧化碳(CO2)
二氧化硫(SO2)四氧化三铁(Fe3O4)
水(H2O)
氢气(H2)
化学式表示的意义宏观意义:1、表示物质2、表示物质的组成微观意义:3、表示一个分子或原子 4、表示分子的构成 (1)单质金属单质
非金属单质
稀有气体固态液、气态:(除I外)多数为双原子分子如:
氢气、 氧气、
H2、 O2、 元素符号元素符号1个分子中
的原子数化学式的书写规律——单质下列化学式是否正确,若有错请更正。
氮气—N 氖气—Ne2 思考:怎样表示2个水分子?H2O2【基础练习】2H22Mg2+CO22H说明下列符号中数字“2”的含义1、2N2表示( )
A、4个氮原子 B、2个氮分子
C、1个氮分子 D、2个氮原子B练习2.下图中的符号表示2个氢原子的是( )C3.下列符号:2N、N2 、H2O 、2CO、SO2 中,数字“2”的意义能用来表示分子个数的有( )
A.2个 B.1个 C. 4个 D.5个 B练习4.下列同学对“SO2”的认识中,不正确的是( ) A. B. C. D. B1、化合价概念:化学上用“化合价”来表示不同原子之间相互化合的数目。
单质元素化合价为零
化合价有正价和负价二、化合价化合物都有固定的组成,元素的原子之间有固定的个数比,如:2、化合价的表示方法:
1. 写在元素符号的正上方。
2. “+”、“ - ” 符号在前,数值在后。
3. “1”不能省略。例如:NaCl H2O+1-1+1-22分钟速记化合价口诀钾钠银氢+1价,
氟氯溴碘-1价,
钙镁钡锌+2价;
铝三硅四磷五价;
二四六硫,二四碳;
莫忘单质为零价。1.化合价有正价和负价。2.化合物中,通常氢为+1价,氧为-2 价,金属元素显正价 。3.许多元素的原子在不同的条件下可显示不
同的化合价。4.化合物里正负化合价的代数和为0。补:化合价的最高价不会超过+7价根据化学式求化合价KMnO4、K2MnO4、KClO3、H2SO4+7+6+5+6方法:化合物中元素的化合价代数和为零,利用不可变价求出可变价.1. 亚硝酸钠(NaNO2)是工业用盐,其外表似食盐,误食会使人中毒,亚硝酸钠中氮元素的化合价是( )
(A)十1 (B)十2 (C)十3 (D)十4C2. 高铁酸钠(Na2FeO4)是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂,其中铁的化合价是( )
A、+2 B 、+3 C、+4 D、+6D3. 在Ca(ClO) 2中,氯元素的化合价为 氢氧化钙: Ca(OH)2 碳酸钙:CaCO3 氢氧化钠: NaOH 碳酸钡:BaCO3 氢氧化铁: Fe(OH)3 碳酸钠:Na2CO3观察下列物质的化学式原子团:做为一个整体参加反应的原子集团,也叫根原子团:作为一个整体参加反应的原子集团(就好象一个原子一样),原子团也叫做根。负一硝酸氢氧根
负二硫酸碳酸根
正一价的是铵根解密阿拉伯数字222个硫酸根离子2个硫酸根离子
硫酸根离子由硫元素和氧元素组成一个硫酸根离子有4个氧原子一个硫酸根离子所带电荷及化合价都为-2+6-2氧的化合价
为-2硫的化合价
为+6一、单质
金属单质:铁 铝
固态非金属单质:硫 磷
稀有气体:氖气 氦气氧气 氢气用元素符号表示(直接由原子构成)气体单质:O2H2一、单质如何写化合物的化学式呢?化学式的书写1. 写出组成物质的元素符号(正价在左,负价在右)
2. 根据正负代数和为零,确定原子个数比(交叉法)
3. 原子数写右下角,得化学式
4. 检查例:氧化铝、氯化镁练一练写出下面化合物的化学式。氧化铜 溴化镁 氯化锂,
氯化钙 氧化钠硫酸铝的化学式怎么写?根据元素和原子团的化合价写出下列物质的化学式KOHK2 SO4 Ca(OH)2CaSO4 Al(OH)3Al2(SO4)3Fe(OH)3Fe2(SO4)3+3巩固复习1.已知下列各元素的化合价,写出它们与氧结合成氧化物的化学式并命名:
Fe(+3) N(+5) Na(+1) C(+4)
Fe2O3 N2O5 Na2O CO22、写出下列各物质的化学式:
①氯化钠 ②氧化镁 ③氯化氢 ④氯化铁 NaClMgOHClFeCl3三、相对原子质量和式量相对分子质量(式量) 化学式中各原子的相对原子质量的总和。相对原子质量 原子实际质量与碳原子实际质量的一个比值,无单位根据化学式的计算
1、计算物质的相对分子质量1、计算KMnO4的相对分子质量。
2、计算(NH4)2CO3的相对分子质量。例1.计算二氧化碳(CO2)的相对分子质量。二氧化碳(CO2)的相对分子质量=12+16× 2=44例2.计算Cu2(OH)2CO3的相对分子质量。Cu2(OH)2CO3的相对分子质量=
64 × 2+(16+1) × 2+12+16 × 3=222已知R2O3的相对分子质量为102,氧的相对原子质量是16 ,则R 的相对原子质量是( )
A.56 B.27 C.112 D.7下列化学式(HnRO2n-2)的相对分子质量为M,则R的相对原子质量是 ( )
A.M-33n B.M-33n-32
C.M+33n+32 D.M-33n+32 B D
同课章节目录
- 第1章 运动和力
- 1 机械运动
- 2 力
- 3 几种常见的力
- 4 运动和力
- 5 二力平衡的条件
- 第2章 压力 压强
- 1 压强
- 2 液体内部的压强
- 3 大气压强
- 4 流体的压强与流速的关系
- 第3章 浮力
- 1 密度
- 2 浮力
- 3 阿基米德原理
- 4 物体浮沉条件及其应用
- 第4章 植物的物质和能量的转化
- 1 绿色开花植物的营养器官
- 2 水在植物体中的代谢
- 3 无机盐在植物体内的代谢
- 4 植物的光合作用和呼吸作用
- 第5章 人体的物质和能量的转化
- 1 食物的消化和吸收
- 2 人体的呼吸
- 3 人体内的物质运输
- 4 人体的排泄
- 5 人体生命活动过程中物质和能量的转化
- 第6章 物质的构成
- 1 构成物质的微粒
- 2 元素
- 3 物质的分类
- 4 化学式
- 5 固态物质
