九年级化学人教版下册第八单元课题3《金属资源的利用与保护》(课件18页)
文档属性
| 名称 | 九年级化学人教版下册第八单元课题3《金属资源的利用与保护》(课件18页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 7.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-06 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
第八单元 金属与金属资源
课题3 金属资源的利用和保护
自然界中的几种矿石
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属如金银等有单质形式存在外,其余都以化合物的形式存在。
金
铂
银
以单质形式存在的金属
赤铁矿Fe2O3
磁铁矿Fe3O4
黄铁矿FeS2
黄铜矿CuFeS2
孔雀Cu2(OH)2CO3
铝土矿Al2O3
以化合物形式存在的金属
常见的铁矿石中理论上最适宜炼铁的两种矿石是什么?理由?
赤铁矿Fe2O3
磁铁矿Fe3O4
最适宜炼铁的两种矿石:
因为这两种矿石含铁量高(质量分数大),且含硫等“有害元素”少,冶炼时产生的污染小。
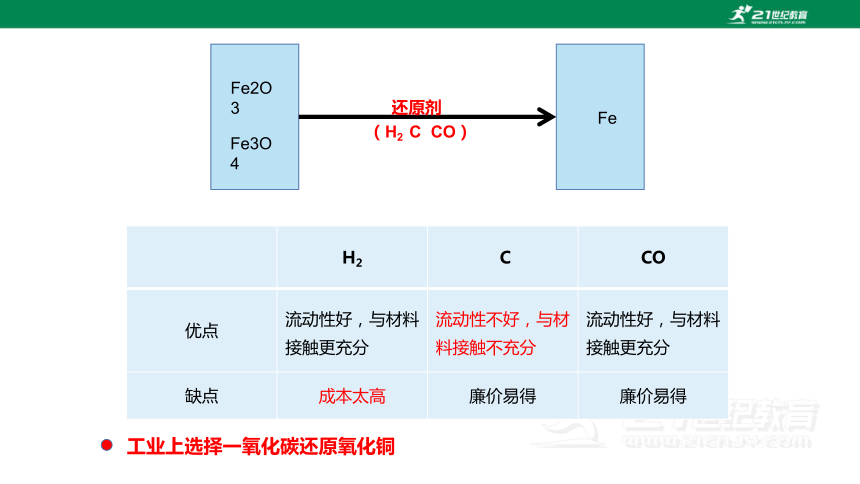
Fe2O3
Fe3O4
Fe
还原剂
(H2 C CO)
H2 C CO
优点 流动性好,与材料接触更充分 流动性不好,与材料接触不充分 流动性好,与材料接触更充分
缺点 成本太高 廉价易得 廉价易得
工业上选择一氧化碳还原氧化铜
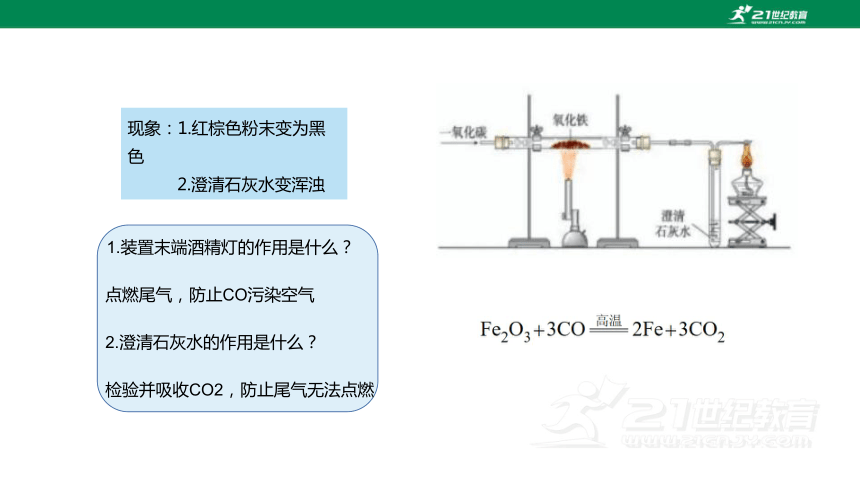
现象:1.红棕色粉末变为黑色
2.澄清石灰水变浑浊
1.装置末端酒精灯的作用是什么?
点燃尾气,防止CO污染空气
2.澄清石灰水的作用是什么?
检验并吸收CO2,防止尾气无法点燃
1.为什么要先通一段儿时间一氧化碳,再加热Fe2O3
排尽装置内的空气,防止加热发生爆炸。
2.为什么要先停止加热,待物质冷却后再停止通一氧化碳?
石灰水倒流使硬质玻璃管破裂;防止铁粉再次被氧化
炼铁高炉及炉内化学反应过程示意图
铁的冶炼
炼铁的原料
炼铁原理
将矿石中的二氧化硅转变为炉渣
涉及杂质问题的计算
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题
含杂质的计算一般做法如下:
第一步,将含杂质的物质质量转化成纯净物的质量;
纯净物的质量 = 不纯物质的总质量×纯度
纯度= ×100%
纯净物的质量
不纯物质的总质量
第二步,依据化学方程式,根据已知纯物质的质量计算未知纯物质的质量;
第三步,将纯物质转化成杂质物质的质量。
不纯物质的质量=纯净物的质量 ÷纯度
练习:某炼钢厂日产含杂质5%的生铁3000t,试计算:
(1)该3000t生铁中含纯铁多少吨?
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤铁矿石多少吨?(计算结果保留整数)
解得x ≈ 4790t
(2)设需含Fe2O3质量分数为85%的赤铁矿石的质量为x。
解:(1)生铁中含纯铁的质量=3000t×(1-5%)=2850t。
Fe2O3 + 3CO 2Fe + 3CO2
112
x×85% 2850t
160
x×85%
=
112
2850t
答:(1)该3000 t生铁中含纯铁2850t。
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤
铁矿石4790t。
高温
解得x ≈ 4790t
(2)设需含Fe2O3质量分数为85%的赤铁矿石的质量为x。
解:(1)生铁中含纯铁的质量=3000t×(1-5%)=2850t。
Fe2O3 + 3CO 2Fe + 3CO2
112
x×85% 2850t
160
x×85%
=
112
2850t
答:(1)该3000 t生铁中含纯铁2850t。
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤铁矿石4790t。
高温
铁制品锈蚀条件的探究
A B C
水 √ √
空气 √ √
现象 一段时间后生锈 一段时间后不生锈 一段时间后不生锈
问题一:证明铁生锈需要与氧气接触的实验是____________。
问题二:证明铁生锈需要与水接触的实验是_______________。
AB
AC
自行车的构件如支架、链条、钢圈等,分别采取了什么防锈措施?
镀铬
涂油
刷漆
防止金属锈蚀是保护金属资源的有力措施。
干
膜
改
镀
烤
保持铁制品表面洁净和干燥
在钢铁表面覆盖保护层
在钢铁表面镀一层其他金属
用化学方法使表面形成致密的氧化膜
加入其他金属,改变其组成
防锈
五字诀
防止铁生锈的方法
防止铁制品锈蚀的原理:
破坏铁制品锈蚀的条件,使铁制品隔绝空气或水。
只要破坏其中一个条件,
铁就不能生锈
金属资源的保护
金属资源丰富,为什么还要保护金属呢?
有效防止金属锈蚀
有计划、合理地开采矿物
回收和利用废旧金属
积极寻找金属的替代品
3
2
1
4
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
第八单元 金属与金属资源
课题3 金属资源的利用和保护
自然界中的几种矿石
地球上的金属资源广泛存在于地壳和海洋中,除少数很不活泼的金属如金银等有单质形式存在外,其余都以化合物的形式存在。
金
铂
银
以单质形式存在的金属
赤铁矿Fe2O3
磁铁矿Fe3O4
黄铁矿FeS2
黄铜矿CuFeS2
孔雀Cu2(OH)2CO3
铝土矿Al2O3
以化合物形式存在的金属
常见的铁矿石中理论上最适宜炼铁的两种矿石是什么?理由?
赤铁矿Fe2O3
磁铁矿Fe3O4
最适宜炼铁的两种矿石:
因为这两种矿石含铁量高(质量分数大),且含硫等“有害元素”少,冶炼时产生的污染小。
Fe2O3
Fe3O4
Fe
还原剂
(H2 C CO)
H2 C CO
优点 流动性好,与材料接触更充分 流动性不好,与材料接触不充分 流动性好,与材料接触更充分
缺点 成本太高 廉价易得 廉价易得
工业上选择一氧化碳还原氧化铜
现象:1.红棕色粉末变为黑色
2.澄清石灰水变浑浊
1.装置末端酒精灯的作用是什么?
点燃尾气,防止CO污染空气
2.澄清石灰水的作用是什么?
检验并吸收CO2,防止尾气无法点燃
1.为什么要先通一段儿时间一氧化碳,再加热Fe2O3
排尽装置内的空气,防止加热发生爆炸。
2.为什么要先停止加热,待物质冷却后再停止通一氧化碳?
石灰水倒流使硬质玻璃管破裂;防止铁粉再次被氧化
炼铁高炉及炉内化学反应过程示意图
铁的冶炼
炼铁的原料
炼铁原理
将矿石中的二氧化硅转变为炉渣
涉及杂质问题的计算
在实际生产时,所用的原料或产物一般都含有杂质,在计算用料和产量时,应考虑到杂质问题
含杂质的计算一般做法如下:
第一步,将含杂质的物质质量转化成纯净物的质量;
纯净物的质量 = 不纯物质的总质量×纯度
纯度= ×100%
纯净物的质量
不纯物质的总质量
第二步,依据化学方程式,根据已知纯物质的质量计算未知纯物质的质量;
第三步,将纯物质转化成杂质物质的质量。
不纯物质的质量=纯净物的质量 ÷纯度
练习:某炼钢厂日产含杂质5%的生铁3000t,试计算:
(1)该3000t生铁中含纯铁多少吨?
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤铁矿石多少吨?(计算结果保留整数)
解得x ≈ 4790t
(2)设需含Fe2O3质量分数为85%的赤铁矿石的质量为x。
解:(1)生铁中含纯铁的质量=3000t×(1-5%)=2850t。
Fe2O3 + 3CO 2Fe + 3CO2
112
x×85% 2850t
160
x×85%
=
112
2850t
答:(1)该3000 t生铁中含纯铁2850t。
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤
铁矿石4790t。
高温
解得x ≈ 4790t
(2)设需含Fe2O3质量分数为85%的赤铁矿石的质量为x。
解:(1)生铁中含纯铁的质量=3000t×(1-5%)=2850t。
Fe2O3 + 3CO 2Fe + 3CO2
112
x×85% 2850t
160
x×85%
=
112
2850t
答:(1)该3000 t生铁中含纯铁2850t。
(2)该炼钢厂每天需含Fe2O3质量分数为85%的赤铁矿石4790t。
高温
铁制品锈蚀条件的探究
A B C
水 √ √
空气 √ √
现象 一段时间后生锈 一段时间后不生锈 一段时间后不生锈
问题一:证明铁生锈需要与氧气接触的实验是____________。
问题二:证明铁生锈需要与水接触的实验是_______________。
AB
AC
自行车的构件如支架、链条、钢圈等,分别采取了什么防锈措施?
镀铬
涂油
刷漆
防止金属锈蚀是保护金属资源的有力措施。
干
膜
改
镀
烤
保持铁制品表面洁净和干燥
在钢铁表面覆盖保护层
在钢铁表面镀一层其他金属
用化学方法使表面形成致密的氧化膜
加入其他金属,改变其组成
防锈
五字诀
防止铁生锈的方法
防止铁制品锈蚀的原理:
破坏铁制品锈蚀的条件,使铁制品隔绝空气或水。
只要破坏其中一个条件,
铁就不能生锈
金属资源的保护
金属资源丰富,为什么还要保护金属呢?
有效防止金属锈蚀
有计划、合理地开采矿物
回收和利用废旧金属
积极寻找金属的替代品
3
2
1
4
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
同课章节目录
