2022-2023学年九年级化学人教版下册 11.1生活中常见的盐(第1课时)课件(共25张PPT)
文档属性
| 名称 | 2022-2023学年九年级化学人教版下册 11.1生活中常见的盐(第1课时)课件(共25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-06 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
11.1生活中常见的盐(第1课时)
人教版初中化学—九年级上册—第十一单元:盐 化肥
主要成分:氯化钠(NaCl)
主要成分:氯化钠(NaCl)+少量碘酸钾(KIO3)
盐:一类组成里含有金属离子(或NH4+)和酸根离子的化合物。
一、氯化钠的作用
2.氯化钠是人的正常生理活动所必不可少的。
钠离子对维持细胞内外正常的水分分布和促进
细胞内外物质交换起主要作用;
氯离子是胃液中的主要成分,具有促生盐酸、
帮助消化和增进食欲的作用。
人们每天都要摄入一些食盐来补充由于出汗、排尿等而排出的氯化钠,以满足人体的正常需要
1.氯化钠是重要的调味品,炒菜时如果不放食盐,菜将食之无味。
但长期食用过多食盐不利于人体健康。
(每人每天约需3~5g食盐)。
二、氯化钠的物理性质
白色晶体、有咸味、易溶于水。
NaCl
NaNO2
盐并不都能作为调味品。
如NaNO2、CuSO4、BaCl2等都有毒。
工业盐
三、氯化钠的用途
1.生活中用食盐腌渍蔬菜、鱼、肉、蛋等,腌制成的食品风味独特,而且还可延长保存时间;
公路上的积雪也可用氯化钠来消除。
2.医疗上的生理盐水是用氯化钠配制的,用于临床输液或外用于伤口清洁。
(原理:溶液的凝固点比纯水的凝固点低。)
(原理:0.9%氯化钠溶液的渗透压与人体血浆渗透压相等。)
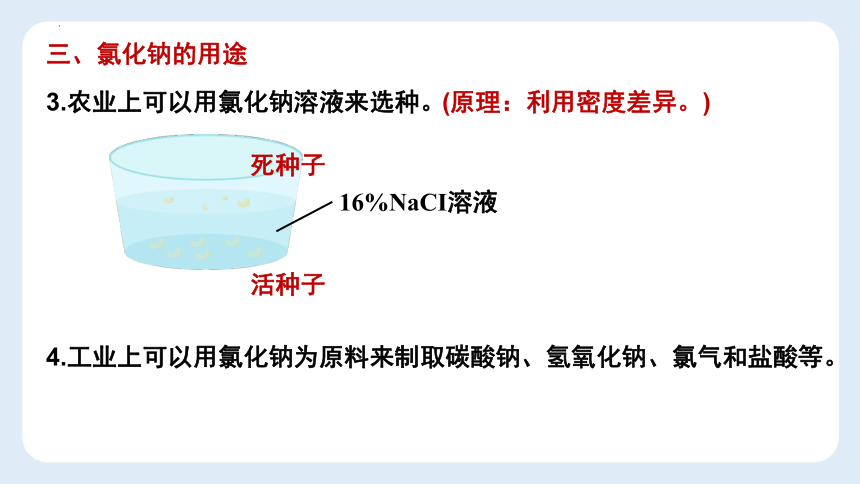
三、氯化钠的用途
3.农业上可以用氯化钠溶液来选种。
(原理:利用密度差异。)
16%NaCI溶液
4.工业上可以用氯化钠为原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
活种子
死种子
四、氯化钠的存在与制取
1.存在:
自然界中分布很广,海水、盐湖、盐井和盐矿中都蕴藏着氯化钠。
2.制取:
①通过晾晒海水或煮盐湖水、盐井水等,可以蒸发除去水分,得到粗盐;
②粗盐提纯。
(原理:氯化钠的溶解度受温度变化影响不大。)
练习:山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊——运城盐池。该湖每年可生产大量的NaCl,下列关于NaCl的说法正确的是( )
①碘盐的主要成分是NaCl,其中还含有少量的碘单质
②NaCl能融雪是因为其溶液的凝固点比水低
③NaCl与人体的生理活动有关,生理盐水中NaCl的质量分数为0.9%
④NaCl是白色晶体,易溶于水,其溶液可用于除铁锈
⑤NaCl的溶解度受温度影响较小,海水晒盐是用蒸发的方法使氯化钠结晶的
A.①②④ B.②③⑤ C.①②⑤ D.③④⑤
B
盐:一类组成里含有金属离子(或NH4+)和酸根离子的化合物。
氯化钠的物理性质
白色晶体、有咸味、易溶于水。
氯化钠的用途
1.生活中用食盐腌渍蔬菜、鱼、肉、蛋等,腌制成的食品风味独特,而且还可延长保存时间;
公路上的积雪也可用氯化钠来消除。
2.医疗上的生理盐水是用氯化钠配制的,用于临床输液或外用于伤口清洁。
(原理:溶液的凝固点比纯水的凝固点低。)
(原理:0.9%氯化钠溶液的渗透压与人体血浆渗透压相等。)
3.农业上可以用氯化钠溶液来选种。
(原理:利用密度差异。)
4.工业上可以用氯化钠为原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
氯化钠的存在与制取
1.存在:
自然界中分布很广,海水、盐湖、盐井和盐矿中都蕴藏着氯化钠。
2.制取:
①通过晾晒海水或煮盐湖水、盐井水等,可以蒸发除去水分,得到粗盐;
②粗盐提纯。
粗盐
含难溶性杂质 如:泥沙等
含可溶性杂质 如:MgCI2、CaCI2等
可溶性固体(难溶性固体)
过滤
粗盐
盐溶液
精盐
悬浊液
(含泥沙等)
实验目的:
1.体验固体混合物(5.0g的粗盐)初步提纯的实验过程。
2.学习蒸发操作技能,巩固溶解、过滤操作技能。
实验仪器:
托盘天平、药匙、烧杯、量筒(10mL)、玻璃棒、铁架台(带铁圈)、漏斗、滤纸、酒精灯、火柴、蒸发皿、坩埚钳等。
溶解
过滤
蒸发
药匙等
“左物右码”、
实验步骤:
1.称取
仪器:托盘天平、
操作要点:
瓶塞倒放
实验步骤:
1.称取
2.溶解
仪器:烧杯、
量筒(10mL)、
玻璃棒等
操作要点:用玻璃棒轻轻搅拌,加速溶解
实验步骤:
1.称取
2.溶解
仪器:烧杯、
量筒(10mL)、
玻璃棒等
操作要点:用玻璃棒轻轻搅拌,加速溶解
x
5.0-x
实验步骤:
1.称取
2.溶解
3.过滤
仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
操作要点:
“一贴”—— 滤纸紧贴在漏斗内壁上(蒸馏水润湿)
“二低”—— ①滤纸边缘低于漏斗口边缘
②液面低于滤纸边缘
“三靠”—— ①倾倒液体时,烧杯尖嘴紧靠玻璃棒
②玻璃棒末端紧靠漏斗内三层滤纸处
③漏斗下颈紧靠承接滤液的烧杯内壁
无色、澄清——
后续操作
浑浊——再过滤
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
仪器:蒸发皿、
酒精灯、
铁架台(带铁圈)
操作要点:
①蒸发皿中所盛液体的体积不应超过它容积的2/3
②加热过程中,
玻璃棒等
要用玻璃棒不断搅拌,
防止因局部温度过高造成液滴飞溅
③蒸发皿中出现较多固体时,停止加热,
利用余热使剩下的少量液体蒸干
④刚加热完毕的蒸发皿不能直接放在实验台上,
以免烫坏实验台;
如需取下可使用坩埚钳
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
精盐
粗盐
5.转移
仪器:玻璃棒
操作:用玻璃棒把固体转移到纸上
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
5.转移
6.计算产率
x
5.0-x
y
精盐产率 =
m(溶解粗盐)
×100%
y
5.0-x
×100%
m(精盐)
1.称取→ 2.溶解→ 3.过滤→4.蒸发 → 5.转移
思考:这样提纯得到的精盐是纯净物吗?
不是
其中还含有多种可溶性杂质
粗盐
精盐
1.称取 仪器:托盘天平、药匙等
2.溶解 仪器:烧杯、量筒(10mL)、玻璃棒等
3.过滤 仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
4.蒸发 仪器:蒸发皿、酒精灯、铁架台(带铁圈)、玻璃棒等
5.转移 仪器:玻璃棒等
6.计算产率
思考:在相关步骤中,玻璃棒的作用分别是什么?
搅拌,加速溶解
引流
搅拌,防止局部温度过高,
造成液滴飞溅
把精盐固体转移到纸上
练习:在粗盐提纯实验中,下列说法正确的是( )
A.溶解时,在量筒中,边加粗盐边搅拌
B.过滤时,漏斗中液体液面要低于滤纸的边缘
C.蒸发时,将蒸发皿内液体蒸干后停止加热
D.过滤和蒸发操作中,玻璃棒的作用相同
B
粗盐
盐溶液
精盐
悬浊液
(含泥沙等)
溶解
过滤
蒸发
1.称取 仪器:托盘天平、药匙等
2.溶解 仪器:烧杯、量筒(10mL)、玻璃棒等
3.过滤 仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
“左物右码”、
操作要点:
瓶塞倒放
操作要点:用玻璃棒轻轻搅拌,加速溶解
操作要点:
“一贴”—— 滤纸紧贴在漏斗内壁上(蒸馏水润湿)
“二低”—— ①滤纸边缘低于漏斗口边缘
②液面低于滤纸边缘
“三靠”—— ①倾倒液体时,烧杯尖嘴紧靠玻璃棒
②玻璃棒末端紧靠漏斗内三层滤纸处
③漏斗下颈紧靠承接滤液的烧杯内壁
4.蒸发 仪器:蒸发皿、酒精灯、铁架台(带铁圈)、玻璃棒等
5.转移 仪器:玻璃棒等
6.计算产率
操作要点:
①蒸发皿中所盛液体的体积不应超过它容积的2/3
②加热过程中,
要用玻璃棒不断搅拌,
防止因局部温度过高造成液滴飞溅
③蒸发皿中出现较多固体时,停止加热,
利用余热使剩下的少量液体蒸干
④刚加热完毕的蒸发皿不能直接放在实验台上,
以免烫坏实验台;
如需取下可使用坩埚钳
操作:用玻璃棒把固体转移到纸上
Thanks
11.1生活中常见的盐(第1课时)
人教版初中化学—九年级上册—第十一单元:盐 化肥
主要成分:氯化钠(NaCl)
主要成分:氯化钠(NaCl)+少量碘酸钾(KIO3)
盐:一类组成里含有金属离子(或NH4+)和酸根离子的化合物。
一、氯化钠的作用
2.氯化钠是人的正常生理活动所必不可少的。
钠离子对维持细胞内外正常的水分分布和促进
细胞内外物质交换起主要作用;
氯离子是胃液中的主要成分,具有促生盐酸、
帮助消化和增进食欲的作用。
人们每天都要摄入一些食盐来补充由于出汗、排尿等而排出的氯化钠,以满足人体的正常需要
1.氯化钠是重要的调味品,炒菜时如果不放食盐,菜将食之无味。
但长期食用过多食盐不利于人体健康。
(每人每天约需3~5g食盐)。
二、氯化钠的物理性质
白色晶体、有咸味、易溶于水。
NaCl
NaNO2
盐并不都能作为调味品。
如NaNO2、CuSO4、BaCl2等都有毒。
工业盐
三、氯化钠的用途
1.生活中用食盐腌渍蔬菜、鱼、肉、蛋等,腌制成的食品风味独特,而且还可延长保存时间;
公路上的积雪也可用氯化钠来消除。
2.医疗上的生理盐水是用氯化钠配制的,用于临床输液或外用于伤口清洁。
(原理:溶液的凝固点比纯水的凝固点低。)
(原理:0.9%氯化钠溶液的渗透压与人体血浆渗透压相等。)
三、氯化钠的用途
3.农业上可以用氯化钠溶液来选种。
(原理:利用密度差异。)
16%NaCI溶液
4.工业上可以用氯化钠为原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
活种子
死种子
四、氯化钠的存在与制取
1.存在:
自然界中分布很广,海水、盐湖、盐井和盐矿中都蕴藏着氯化钠。
2.制取:
①通过晾晒海水或煮盐湖水、盐井水等,可以蒸发除去水分,得到粗盐;
②粗盐提纯。
(原理:氯化钠的溶解度受温度变化影响不大。)
练习:山西河东地区是中华文明的发祥地之一,那里有一个被称为“中国死海”的湖泊——运城盐池。该湖每年可生产大量的NaCl,下列关于NaCl的说法正确的是( )
①碘盐的主要成分是NaCl,其中还含有少量的碘单质
②NaCl能融雪是因为其溶液的凝固点比水低
③NaCl与人体的生理活动有关,生理盐水中NaCl的质量分数为0.9%
④NaCl是白色晶体,易溶于水,其溶液可用于除铁锈
⑤NaCl的溶解度受温度影响较小,海水晒盐是用蒸发的方法使氯化钠结晶的
A.①②④ B.②③⑤ C.①②⑤ D.③④⑤
B
盐:一类组成里含有金属离子(或NH4+)和酸根离子的化合物。
氯化钠的物理性质
白色晶体、有咸味、易溶于水。
氯化钠的用途
1.生活中用食盐腌渍蔬菜、鱼、肉、蛋等,腌制成的食品风味独特,而且还可延长保存时间;
公路上的积雪也可用氯化钠来消除。
2.医疗上的生理盐水是用氯化钠配制的,用于临床输液或外用于伤口清洁。
(原理:溶液的凝固点比纯水的凝固点低。)
(原理:0.9%氯化钠溶液的渗透压与人体血浆渗透压相等。)
3.农业上可以用氯化钠溶液来选种。
(原理:利用密度差异。)
4.工业上可以用氯化钠为原料来制取碳酸钠、氢氧化钠、氯气和盐酸等。
氯化钠的存在与制取
1.存在:
自然界中分布很广,海水、盐湖、盐井和盐矿中都蕴藏着氯化钠。
2.制取:
①通过晾晒海水或煮盐湖水、盐井水等,可以蒸发除去水分,得到粗盐;
②粗盐提纯。
粗盐
含难溶性杂质 如:泥沙等
含可溶性杂质 如:MgCI2、CaCI2等
可溶性固体(难溶性固体)
过滤
粗盐
盐溶液
精盐
悬浊液
(含泥沙等)
实验目的:
1.体验固体混合物(5.0g的粗盐)初步提纯的实验过程。
2.学习蒸发操作技能,巩固溶解、过滤操作技能。
实验仪器:
托盘天平、药匙、烧杯、量筒(10mL)、玻璃棒、铁架台(带铁圈)、漏斗、滤纸、酒精灯、火柴、蒸发皿、坩埚钳等。
溶解
过滤
蒸发
药匙等
“左物右码”、
实验步骤:
1.称取
仪器:托盘天平、
操作要点:
瓶塞倒放
实验步骤:
1.称取
2.溶解
仪器:烧杯、
量筒(10mL)、
玻璃棒等
操作要点:用玻璃棒轻轻搅拌,加速溶解
实验步骤:
1.称取
2.溶解
仪器:烧杯、
量筒(10mL)、
玻璃棒等
操作要点:用玻璃棒轻轻搅拌,加速溶解
x
5.0-x
实验步骤:
1.称取
2.溶解
3.过滤
仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
操作要点:
“一贴”—— 滤纸紧贴在漏斗内壁上(蒸馏水润湿)
“二低”—— ①滤纸边缘低于漏斗口边缘
②液面低于滤纸边缘
“三靠”—— ①倾倒液体时,烧杯尖嘴紧靠玻璃棒
②玻璃棒末端紧靠漏斗内三层滤纸处
③漏斗下颈紧靠承接滤液的烧杯内壁
无色、澄清——
后续操作
浑浊——再过滤
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
仪器:蒸发皿、
酒精灯、
铁架台(带铁圈)
操作要点:
①蒸发皿中所盛液体的体积不应超过它容积的2/3
②加热过程中,
玻璃棒等
要用玻璃棒不断搅拌,
防止因局部温度过高造成液滴飞溅
③蒸发皿中出现较多固体时,停止加热,
利用余热使剩下的少量液体蒸干
④刚加热完毕的蒸发皿不能直接放在实验台上,
以免烫坏实验台;
如需取下可使用坩埚钳
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
精盐
粗盐
5.转移
仪器:玻璃棒
操作:用玻璃棒把固体转移到纸上
实验步骤:
1.称取
2.溶解
3.过滤
4.蒸发
5.转移
6.计算产率
x
5.0-x
y
精盐产率 =
m(溶解粗盐)
×100%
y
5.0-x
×100%
m(精盐)
1.称取→ 2.溶解→ 3.过滤→4.蒸发 → 5.转移
思考:这样提纯得到的精盐是纯净物吗?
不是
其中还含有多种可溶性杂质
粗盐
精盐
1.称取 仪器:托盘天平、药匙等
2.溶解 仪器:烧杯、量筒(10mL)、玻璃棒等
3.过滤 仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
4.蒸发 仪器:蒸发皿、酒精灯、铁架台(带铁圈)、玻璃棒等
5.转移 仪器:玻璃棒等
6.计算产率
思考:在相关步骤中,玻璃棒的作用分别是什么?
搅拌,加速溶解
引流
搅拌,防止局部温度过高,
造成液滴飞溅
把精盐固体转移到纸上
练习:在粗盐提纯实验中,下列说法正确的是( )
A.溶解时,在量筒中,边加粗盐边搅拌
B.过滤时,漏斗中液体液面要低于滤纸的边缘
C.蒸发时,将蒸发皿内液体蒸干后停止加热
D.过滤和蒸发操作中,玻璃棒的作用相同
B
粗盐
盐溶液
精盐
悬浊液
(含泥沙等)
溶解
过滤
蒸发
1.称取 仪器:托盘天平、药匙等
2.溶解 仪器:烧杯、量筒(10mL)、玻璃棒等
3.过滤 仪器:铁架台(带铁圈)、烧杯、漏斗、滤纸、玻璃棒等
“左物右码”、
操作要点:
瓶塞倒放
操作要点:用玻璃棒轻轻搅拌,加速溶解
操作要点:
“一贴”—— 滤纸紧贴在漏斗内壁上(蒸馏水润湿)
“二低”—— ①滤纸边缘低于漏斗口边缘
②液面低于滤纸边缘
“三靠”—— ①倾倒液体时,烧杯尖嘴紧靠玻璃棒
②玻璃棒末端紧靠漏斗内三层滤纸处
③漏斗下颈紧靠承接滤液的烧杯内壁
4.蒸发 仪器:蒸发皿、酒精灯、铁架台(带铁圈)、玻璃棒等
5.转移 仪器:玻璃棒等
6.计算产率
操作要点:
①蒸发皿中所盛液体的体积不应超过它容积的2/3
②加热过程中,
要用玻璃棒不断搅拌,
防止因局部温度过高造成液滴飞溅
③蒸发皿中出现较多固体时,停止加热,
利用余热使剩下的少量液体蒸干
④刚加热完毕的蒸发皿不能直接放在实验台上,
以免烫坏实验台;
如需取下可使用坩埚钳
操作:用玻璃棒把固体转移到纸上
Thanks
同课章节目录
