2022-2023学年化学京改版(2013) 第9章 溶液 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学京改版(2013) 第9章 溶液 单元练习(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 149.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-07 00:00:00 | ||
图片预览

文档简介
2022-2023学年化学京改版(2013)--溶液
一、单选题
1.下列说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶质均以离子形式分散到溶剂中
C.同一温度下,硝酸钾的饱和溶液比不饱和溶液浓
D.饱和溶液析出晶体后溶质质量分数一定变小
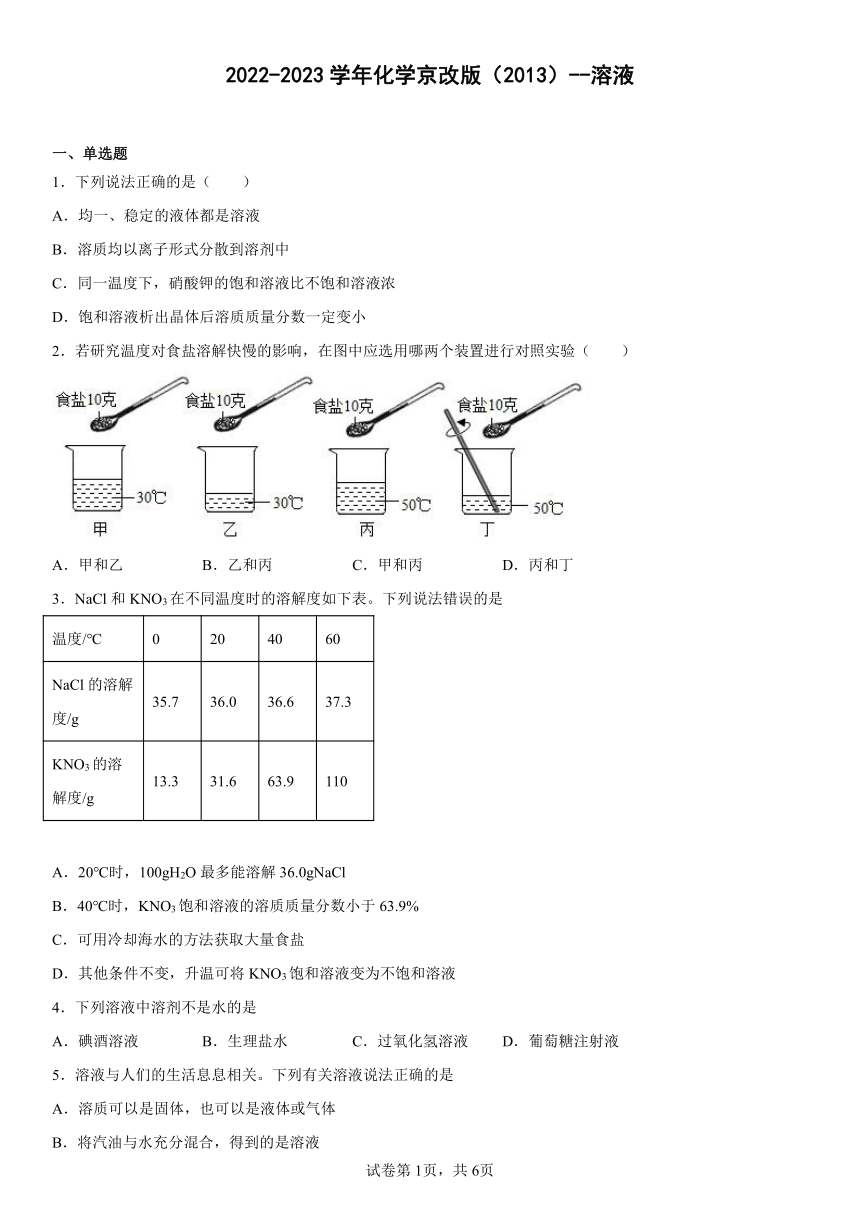
2.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
3.NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是
温度/℃ 0 20 40 60
NaCl的溶解度/g 35.7 36.0 36.6 37.3
KNO3的溶解度/g 13.3 31.6 63.9 110
A.20℃时,100gH2O最多能溶解36.0gNaCl
B.40℃时,KNO3饱和溶液的溶质质量分数小于63.9%
C.可用冷却海水的方法获取大量食盐
D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
4.下列溶液中溶剂不是水的是
A.碘酒溶液 B.生理盐水 C.过氧化氢溶液 D.葡萄糖注射液
5.溶液与人们的生活息息相关。下列有关溶液说法正确的是
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t°C时的不饱和溶液
6.现有一接近饱和的溶液,下列方法中一定能使之成为饱和溶液的是 ( )
①蒸发溶剂,②增加溶质,③降低温度,④加热升温
A.只有①② B.只有②③ C.①②③ D.①②④
7.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
8.下列饮料中,不属于溶液的是
A.汽水 B.白酒
C.酸奶 D.苏打水
9.下列物质用途主要由化学性质决定的是
A.稀有气体作电光源 B.生石灰用于食品加热
C.液氮制造低温环境 D.氯化钠配制生理盐水
10.20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
11.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是
A.白酒
B.蒸馏水
C.医用酒精
D.生理盐水
12.在“一定溶质质量分数的氯化钠溶液的配制”实验活动中,可能导致氯化钠溶液溶质质量分数偏大的是( )
A.量取水时量筒内事先有少量水
B.所用氯化钠固体不纯
C.称量时砝码和药品的位置放反
D.将量筒中的水倒入烧杯时有水溅出
13.“一定溶质质量分数的氯化钠溶液的配制”实验中,下列有关操作正确的是
A.取用 B.滴加
C.读数 D.溶解
14.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
15.取某固体物质5g加入20mL水中,测得溶液的温度随时间变化曲线如图所示。该固体物质可能是
A.NaCl B.NaOH C.NH4NO3 D.CaCO3
二、填空题
16.在实验室,用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液,回答下列问题
(1)需溶质质量分数为6%的氯化钠溶液______g。
(2)若用量筒量取水时仰视读数,而其它操作均正确,则所得溶液中溶质质量分数_____(选填“大于”“小于”或“等于”)3%。
(3)混匀时用到的玻璃仪器由烧杯、______。
17.写出下列溶液中溶质的化学式:
①石灰水_____;
②盐酸_____;
③食盐水_____;
④白磷的二硫化碳溶液_____;
⑤医用酒精_____;
⑥锌粒溶于硫酸中_____。
18.大连复州湾盐场是我国四大海盐场之一,利用传统的海水晒盐工艺,可得到氯化钠和氯化镁等物质,下图是氯化钠和氯化镁的溶解度曲线。
(1)两种物质中,______的溶解度受温度的影响较大。
(2)t℃时,氯化镁饱和溶液中溶质与溶剂的质量比为_______。
(3)将接近饱和的氯化钠溶液变为饱和溶液,可采用的一种方法是_______。
(4)海水晒盐是利用________的方法获得晶体。
19.甲、乙两种物质的溶解度曲线如图所示,请回答下列问题:
(1)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有_______(写一种)。
(2)将30℃时等质量的甲、乙的饱和溶液分别降温至t1℃,它们析出晶体(晶体中不含结晶水)的质量关系是_______(填“甲>乙”“甲<乙”或“甲=乙”)
三、实验题
20.配制一定溶质质量分数的氯化钠溶液的过程如下图所示:
(1)写出图中标号a仪器的名称:_____。
(2)配制50g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠_____g,水_____g。
(3)称量氯化钠时,氯化钠应放在托盘天平的_____盘。(填“左”或“右”)
(4)溶解过程中玻璃棒的作用是_____。
(5)对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有_____。(填序号)
A.称量时,药品与砝码放反了 B.量取水的体积时,仰视读数 C装瓶时,有少量溶液洒出
(6)把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是_____g。
21.科学兴趣小组的同学做粗盐(只含有难溶性杂质)提纯实验,并用所得的精盐配制50g6%的氯化钠溶液。回答下列问题:
实验一:粗盐提纯
(1)上图中操作有错误的是______(填数字序号)。
(2)操作⑥中,当观察到蒸发皿中_____时,停止加热。
(3)海水晒盐采用上图操作⑥的原理,不采用冷却氯化钠浓溶液的方法,原因是氯化钠的溶解度_____。
实验二:用提纯得到的精盐配制50g6%的氯化钠溶液
(1)计算。需要氯化钠_____g,蒸馏水______mL。
(2)称量、量取。量取水的体积时,若仰视读数,所配溶液的溶质质量分数会______6%(填“>”“<”或“=”)。
(3)溶解。用玻璃棒搅拌的目的是_______。
(4)装瓶、贴标签。
四、计算题
22.某品牌补钙剂主要成分含碳酸钙,为了测定该品牌补钙剂中CaCO3的质量分数,取该补钙剂制成的粉末20g,逐滴滴入稀盐酸(补钙剂中其他成分不与盐酸反应),得到数据如图所示,请根据有关信息回答问题
(1)该补钙剂刚好完全反应时产生气体的质量为 克。
(2)该品牌补钙剂中CaCO3的质量分数是多少?
(3)该盐酸中溶质的质量分数。
23.过氧化氢溶液常用于家庭、医疗等方面,它具有杀菌、漂白、防腐和除臭等作用。医疗上常用3%的过氧化氢溶液消毒。
(1)过氧化氢中氢、氧元素的质量比为_____。
(2)若配制500g溶质质量分数为3%的过氧化氢溶液,需溶质质量分数为30%的过氧化氢溶液的质量是_____。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.A
5.A
6.A
7.D
8.C
9.B
10.C
11.B
12.D
13.D
14.A
15.C
16. 25 小于 玻璃棒
17. Ca(OH)2 HCl NaCl P C2H5OH ZnSO4
18. 氯化镁 7:10 增加溶质(或其它合理答案) 蒸发结晶
19.(1)降低温度或加溶质或蒸发溶剂
(2)甲>乙
20. 量筒 7.5 42.5 左 搅拌,加快溶解的速率 AB 100
21. ⑤ 有较多的固体出现时 随温度变化不大 3g 47mL < 加速溶解
22.(1)4.4
(2)解:设补钙剂中碳酸钙的质量为, 参加反应的氯化氢的质量为.
该品牌补钙剂中CaCO3的质量分数为:
答:该品牌补钙剂中CaCO3的质量分数是50%。
(3)该盐酸中溶质的质量分数为:.
答:该盐酸中溶质的质量分数为7.3%。
23.(1)过氧化氢(H2O2)中氢、氧元素的质量比为(1×2):(16×2)=1:16;
(2)设需溶质质量分数为30%的过氧化氢溶液的质量为x,则:
500g×3%=x×30% 解得:x=50g
故答为:(1)1:16;(2)50g。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列说法正确的是( )
A.均一、稳定的液体都是溶液
B.溶质均以离子形式分散到溶剂中
C.同一温度下,硝酸钾的饱和溶液比不饱和溶液浓
D.饱和溶液析出晶体后溶质质量分数一定变小
2.若研究温度对食盐溶解快慢的影响,在图中应选用哪两个装置进行对照实验( )
A.甲和乙 B.乙和丙 C.甲和丙 D.丙和丁
3.NaCl和KNO3在不同温度时的溶解度如下表。下列说法错误的是
温度/℃ 0 20 40 60
NaCl的溶解度/g 35.7 36.0 36.6 37.3
KNO3的溶解度/g 13.3 31.6 63.9 110
A.20℃时,100gH2O最多能溶解36.0gNaCl
B.40℃时,KNO3饱和溶液的溶质质量分数小于63.9%
C.可用冷却海水的方法获取大量食盐
D.其他条件不变,升温可将KNO3饱和溶液变为不饱和溶液
4.下列溶液中溶剂不是水的是
A.碘酒溶液 B.生理盐水 C.过氧化氢溶液 D.葡萄糖注射液
5.溶液与人们的生活息息相关。下列有关溶液说法正确的是
A.溶质可以是固体,也可以是液体或气体
B.将汽油与水充分混合,得到的是溶液
C.将10%的某溶液倒出一半,剩余溶液中溶质的质量分数为20%
D.某饱和溶液降温到t℃析出晶体后,得到的溶液是t°C时的不饱和溶液
6.现有一接近饱和的溶液,下列方法中一定能使之成为饱和溶液的是 ( )
①蒸发溶剂,②增加溶质,③降低温度,④加热升温
A.只有①② B.只有②③ C.①②③ D.①②④
7.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
8.下列饮料中,不属于溶液的是
A.汽水 B.白酒
C.酸奶 D.苏打水
9.下列物质用途主要由化学性质决定的是
A.稀有气体作电光源 B.生石灰用于食品加热
C.液氮制造低温环境 D.氯化钠配制生理盐水
10.20℃时,NaCl的溶解度为36g。配制此温度下20g质量分数为5%的NaCl溶液,下列说法正确的是( )
A.配制该溶液需要5g NaCl
B.该溶液为饱和溶液
C.将该溶液长时间敞口放置,最终有晶体析出
D.配溶液时,量取所需体积的水倒入烧杯,有少量水洒出,则所配溶液浓度小于5%
11.溶液在我们生活中有着广泛的用途。下列物质不属于溶液的是
A.白酒
B.蒸馏水
C.医用酒精
D.生理盐水
12.在“一定溶质质量分数的氯化钠溶液的配制”实验活动中,可能导致氯化钠溶液溶质质量分数偏大的是( )
A.量取水时量筒内事先有少量水
B.所用氯化钠固体不纯
C.称量时砝码和药品的位置放反
D.将量筒中的水倒入烧杯时有水溅出
13.“一定溶质质量分数的氯化钠溶液的配制”实验中,下列有关操作正确的是
A.取用 B.滴加
C.读数 D.溶解
14.要想从食盐溶液中得到食盐晶体,宜采取的方法是( )
A.蒸发溶剂的方法 B.冷却热饱和溶液的方法
C.倒掉部分溶液的方法 D.升高温度的方法
15.取某固体物质5g加入20mL水中,测得溶液的温度随时间变化曲线如图所示。该固体物质可能是
A.NaCl B.NaOH C.NH4NO3 D.CaCO3
二、填空题
16.在实验室,用溶质质量分数为6%的氯化钠溶液配制50g溶质质量分数为3%的氯化钠溶液,回答下列问题
(1)需溶质质量分数为6%的氯化钠溶液______g。
(2)若用量筒量取水时仰视读数,而其它操作均正确,则所得溶液中溶质质量分数_____(选填“大于”“小于”或“等于”)3%。
(3)混匀时用到的玻璃仪器由烧杯、______。
17.写出下列溶液中溶质的化学式:
①石灰水_____;
②盐酸_____;
③食盐水_____;
④白磷的二硫化碳溶液_____;
⑤医用酒精_____;
⑥锌粒溶于硫酸中_____。
18.大连复州湾盐场是我国四大海盐场之一,利用传统的海水晒盐工艺,可得到氯化钠和氯化镁等物质,下图是氯化钠和氯化镁的溶解度曲线。
(1)两种物质中,______的溶解度受温度的影响较大。
(2)t℃时,氯化镁饱和溶液中溶质与溶剂的质量比为_______。
(3)将接近饱和的氯化钠溶液变为饱和溶液,可采用的一种方法是_______。
(4)海水晒盐是利用________的方法获得晶体。
19.甲、乙两种物质的溶解度曲线如图所示,请回答下列问题:
(1)要使接近饱和的甲溶液变成饱和溶液,可采用的方法有_______(写一种)。
(2)将30℃时等质量的甲、乙的饱和溶液分别降温至t1℃,它们析出晶体(晶体中不含结晶水)的质量关系是_______(填“甲>乙”“甲<乙”或“甲=乙”)
三、实验题
20.配制一定溶质质量分数的氯化钠溶液的过程如下图所示:
(1)写出图中标号a仪器的名称:_____。
(2)配制50g质量分数为15%的氯化钠溶液,所需氯化钠和水的质量分别为:氯化钠_____g,水_____g。
(3)称量氯化钠时,氯化钠应放在托盘天平的_____盘。(填“左”或“右”)
(4)溶解过程中玻璃棒的作用是_____。
(5)对配制的溶液进行检测发现溶质质量分数偏小,其原因可能有_____。(填序号)
A.称量时,药品与砝码放反了 B.量取水的体积时,仰视读数 C装瓶时,有少量溶液洒出
(6)把50g质量分数为15%的氯化钠溶液稀释成5%的氯化钠溶液,需要水的质量是_____g。
21.科学兴趣小组的同学做粗盐(只含有难溶性杂质)提纯实验,并用所得的精盐配制50g6%的氯化钠溶液。回答下列问题:
实验一:粗盐提纯
(1)上图中操作有错误的是______(填数字序号)。
(2)操作⑥中,当观察到蒸发皿中_____时,停止加热。
(3)海水晒盐采用上图操作⑥的原理,不采用冷却氯化钠浓溶液的方法,原因是氯化钠的溶解度_____。
实验二:用提纯得到的精盐配制50g6%的氯化钠溶液
(1)计算。需要氯化钠_____g,蒸馏水______mL。
(2)称量、量取。量取水的体积时,若仰视读数,所配溶液的溶质质量分数会______6%(填“>”“<”或“=”)。
(3)溶解。用玻璃棒搅拌的目的是_______。
(4)装瓶、贴标签。
四、计算题
22.某品牌补钙剂主要成分含碳酸钙,为了测定该品牌补钙剂中CaCO3的质量分数,取该补钙剂制成的粉末20g,逐滴滴入稀盐酸(补钙剂中其他成分不与盐酸反应),得到数据如图所示,请根据有关信息回答问题
(1)该补钙剂刚好完全反应时产生气体的质量为 克。
(2)该品牌补钙剂中CaCO3的质量分数是多少?
(3)该盐酸中溶质的质量分数。
23.过氧化氢溶液常用于家庭、医疗等方面,它具有杀菌、漂白、防腐和除臭等作用。医疗上常用3%的过氧化氢溶液消毒。
(1)过氧化氢中氢、氧元素的质量比为_____。
(2)若配制500g溶质质量分数为3%的过氧化氢溶液,需溶质质量分数为30%的过氧化氢溶液的质量是_____。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.A
5.A
6.A
7.D
8.C
9.B
10.C
11.B
12.D
13.D
14.A
15.C
16. 25 小于 玻璃棒
17. Ca(OH)2 HCl NaCl P C2H5OH ZnSO4
18. 氯化镁 7:10 增加溶质(或其它合理答案) 蒸发结晶
19.(1)降低温度或加溶质或蒸发溶剂
(2)甲>乙
20. 量筒 7.5 42.5 左 搅拌,加快溶解的速率 AB 100
21. ⑤ 有较多的固体出现时 随温度变化不大 3g 47mL < 加速溶解
22.(1)4.4
(2)解:设补钙剂中碳酸钙的质量为, 参加反应的氯化氢的质量为.
该品牌补钙剂中CaCO3的质量分数为:
答:该品牌补钙剂中CaCO3的质量分数是50%。
(3)该盐酸中溶质的质量分数为:.
答:该盐酸中溶质的质量分数为7.3%。
23.(1)过氧化氢(H2O2)中氢、氧元素的质量比为(1×2):(16×2)=1:16;
(2)设需溶质质量分数为30%的过氧化氢溶液的质量为x,则:
500g×3%=x×30% 解得:x=50g
故答为:(1)1:16;(2)50g。
答案第1页,共2页
答案第1页,共2页
