课题1 溶液的形成(课件43页)
图片预览










文档简介
(共43张PPT)
第九单元 溶液
课题1 溶液的形成
1.了解溶液、溶质和溶剂概念;
2.能根据溶液的基本特征正确区分溶液和乳浊液; 3.常识性了解溶液在工农业生产科学实验及日常生活中的应用;
4.了解溶解时的吸热和放热现象
学习目标
学习定位
蓝色星球
地球的表面大部分被海水覆盖着,但海水是又苦又咸的,这是为什么呢?
海水中溶解了氯化钠等物质,它是一种混合物。
生活中的液体
说一说你生活中接触到的液体物质有哪些?
【思考1】同学们都喝过糖水,糖水是甜的,但在糖水中为什么看不到糖呢?
【思考2】前面我们接触了一些化学反应,如氢氧化钠溶液与硫酸铜溶液的反应,为什么这两种物质要放在溶液中反应呢?
【思考3】衣服上的油污,为什么用水洗不掉,而用汽油或洗涤剂可以洗掉呢?它们洗掉油污的原理是不是一样的呢?
实验9-1、在20 mL水中加入一匙蔗糖,用玻璃棒搅拌,还能看到蔗糖吗
实验:蔗糖溶解
【微观解释】蔗糖分子在水分子的作用下运动扩散到水分子中去了。
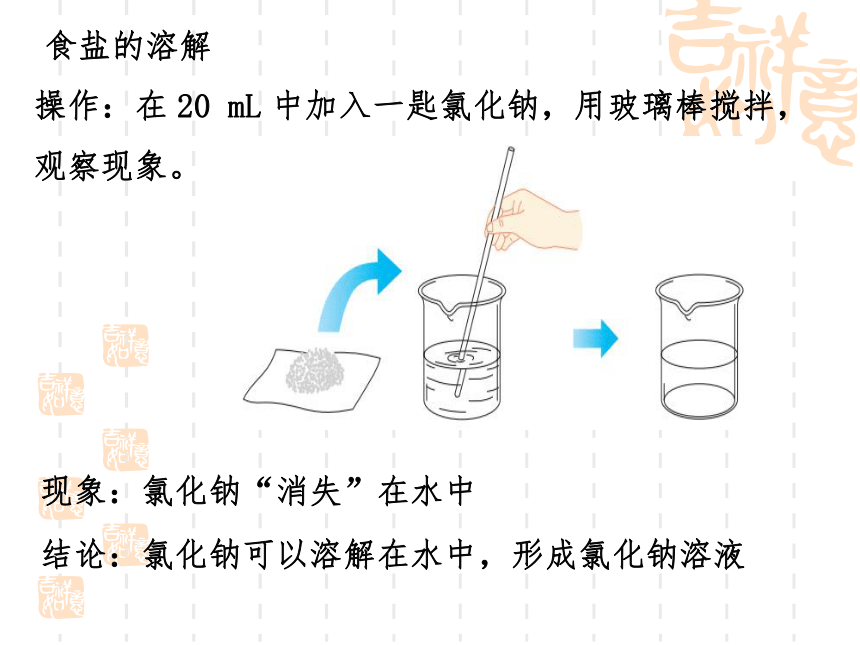
食盐的溶解
操作:在 20 mL 中加入一匙氯化钠,用玻璃棒搅拌,观察现象。
现象:氯化钠“消失”在水中
结论:氯化钠可以溶解在水中,形成氯化钠溶液
氯化钠溶于水:
溶
解
前
溶解中
溶解后
【微观解释】氯离子和钠离子在水分子的作用下运动扩散到水分子中去了。
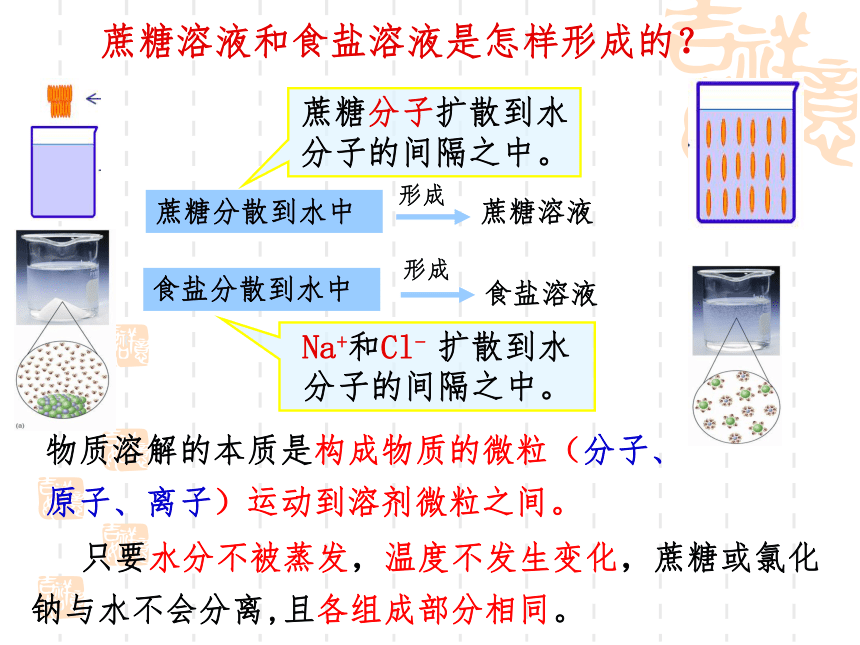
蔗糖溶液和食盐溶液是怎样形成的?
蔗糖分散到水中
食盐分散到水中
形成
蔗糖溶液
形成
食盐溶液
蔗糖分子扩散到水分子的间隔之中。
Na+和Cl- 扩散到水分子的间隔之中。
物质溶解的本质是构成物质的微粒(分子、原子、离子)运动到溶剂微粒之间。
只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,且各组成部分相同。
1、定义:
均一性:指溶液任一部分的组成和性质完全相同(颜色、密度、浓度等)
稳定性:在外界条件(温度、溶剂量等)不变时, 溶剂与溶质不会分离 (静置不会沉淀或分层)
混合物:凡是溶液都属于混合物
一、溶液
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物就是溶液。
2、特征:
均一性、稳定性
溶质
溶剂
溶液
+
3、溶液的组成
溶液
溶质:
溶剂:
被溶解的物质 如:蔗糖、食盐
能溶解其它物质的物质 如:水
(≥1种)
(1种)
2、V溶液 V质+ V剂
<
6、溶液的命名:
分子之间存在间隔
4、溶液、溶质与溶剂之间的量的关系
=
1、m溶液 m质+m剂
以微粒(分子、原子、离子)的形式存在
5、溶液中各物质的存在形式:
加入水中的 物质 溶质 溶剂 溶液名称
蔗 糖
食 盐
硫酸铜
蔗 糖
水
水
水
食 盐
硫酸铜
蔗糖的水溶液或蔗糖溶液
食盐的水溶液或食盐溶液
硫酸铜的水溶液或硫酸铜溶液
某溶质的某溶剂溶液 某溶质溶液(当溶剂为水时)
溶液 溶质(溶解前的状态) 溶剂(状态)
高锰酸钾溶液
碘 酒
硫酸溶液
稀盐酸
高锰酸钾(固体)
碘(固体)
硫酸(液体)
氯化氢 (气体)
水
酒精
水
水
(液态)
(液态)
(液态)
(液态)
溶质可以为:
固体、液体、气体
我会填
、某溶质某溶剂
水是最常用的溶剂,此外,汽油、酒精等也可作溶剂。
溶剂通常是液体,也可以是固体或气体。
溶液 名称 石灰水 酒精 溶液 碘酒 盐酸 稀硫酸 氢氧化钠溶液 硫酸铜溶液
溶质
溶剂
H2O
H2O
H2O
H2O
H2O
H2O
C2H5OH
H2SO4
HCl
C2H5OH
Ca(OH)2
I2
CuSO4
NaOH
①气体和液体形成的溶液:气体是溶质
②固体和液体形成的溶液: 固体是溶质
③液体和液体形成的溶液:量多的是溶剂,量少的溶质
④水和其他液体形成的溶液:无论质量大小,水为溶剂
7、溶液组成的判断:
反应 过量的锌加入H2SO4中 锌加入过量的H2SO4中 过量的石灰石加入H2SO4中 石灰石加入过量的HCl中 CO2通入水中 CO2恰好与石灰水反应
反应前的溶质
反应后的溶质
H2SO4
H2SO4
ZnSO4
ZnSO4
H2SO4
HCl
CaCl2
HCl
HCl
CaCl2
无
H2CO3
Ca(OH)2
无
Zn + H2SO4 = ZnSO4+ H2↑
CaCO3+ 2HCl = CaCl2+ H2O+CO2↑
CO2+ H2O = H2CO3
CO2+ Ca(OH)2 = CaCO3↓ +H2O
无土栽培
化学试剂
医药制剂
食品饮料
【思考】化学反应常在溶液中进行的
原因 。
加快反应速率
8、溶液的用途
一种番茄营养液的配方
肥料名称 用量(毫克/升)
硝酸钙 硝酸钾 硫酸镁 过磷酸钙 590
606
492
680
交流讨论
1.均一、稳定的液体一定是溶液吗?
不一定,如酒精、水等。溶液是均一、稳定的混合物。
2.将蔗糖溶液和氯化钠溶液混合,还是溶液吗?
是,氯化钠和蔗糖都是溶质。
溶液中的溶质可以有多种,如海水。
3.溶液一定是液体吗?
不一定。也可以是气体或固体。
含Cu2+的溶液呈蓝色
含Fe2+的溶液呈浅绿色
含Fe3+的溶液呈黄色
KMnO4的溶液呈紫红色
4.溶液一定是无色的吗?
不一定,大多数溶液无色,有些溶液是有颜色的。
课堂精练
1.判断下列有关溶液的说法是否正确
①凡是无色、透明、稳定的液体都是溶液
②溶液都是无色的
③溶质一定是以离子的形式分散在溶剂中
④溶液中可以有一种或多种溶质
⑤一定量的溶剂中,加入氯化钠越多,得到的溶液质量越大
⑥将氯化钠放入植物油中搅拌,能形成溶液
⑦溶液一定是混合物
⑧从一杯糖水中倒出一半,则剩余糖水的甜度变小
⑨实验室常将固体配成溶液,以提高反应速率
2、下列说法正确的是:
A、溶液一定是液体
B、生铁也是溶液
C、50mL酒精和50mL水混合得到100mL溶液
D、盐水和糖水都是溶液,两者混合在一起,则不是溶液了
3.下列各组物质充分混合后,能得到溶液的是:
A.沙土和水 B.冰和水
C.碘和酒精 D.花生油和水
4.铁和过量稀硫酸充分反应后,所得溶液中的溶质是:
A.只有铁 B.只有硫酸亚铁
C.只有硫酸铁 D.有硫酸亚铁和硫酸
C
D
B
实验探究二:溶质与溶剂的关系
[实验]9-2 不同的溶质在不同的溶剂中的溶解性
在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。
试管号 溶质 溶剂 溶解情况
1 碘 水
2 高锰酸钾 水
结论
●不同的溶质在同一种溶剂中的溶解情况不同
碘难溶于水
溶解,溶液呈紫色
溶解,溶液呈棕色
高锰酸钾难溶于汽油
① 碘 汽油
② 高锰酸钾 汽油
试管号 溶质 溶剂 溶解情况
结论
●同一种溶质在不同的溶剂中溶解情况不同
碘难溶于水
溶解,溶液呈紫色
溶解,溶液呈棕色
高锰酸钾难溶于汽油
② 高锰酸钾 汽油
2 碘 汽油
① 高锰酸钾 水
1 碘 水
9、溶质与溶剂的辨证关系:
相同溶质在不同种溶剂里的溶解能力不同。
不同溶质在同种溶剂里的溶解能力不同。
即:溶质或溶剂的种类(性质)决定了物质的溶解能力
碘+水
碘+汽油
高锰酸钾+水
高锰酸钾+汽油
探究实验9-3:水和乙醇能够互溶吗?
在盛有2 mL水的试管中滴入2~3 滴红墨水(用红墨水是为了显色,利于观察),向其中缓缓加入约2mL的酒精。
溶剂 溶质 振荡前现象 振荡后现象 静置后现象 结论
水 乙醇
液体出现了分层现象
液体溶为一体,颜色均匀,不分层
酒精能与水互溶
稳定,不分层
水中滴入红墨水,振荡
加入乙醇,不要振荡
振荡,静置
“摇摇冰” 是一种即用即冷的罐装饮料。在饮料罐的夹层中分别装有硝酸铵和水,喝的时候将底部的旋钮转一下,使硝酸铵和水混合,罐内饮料就会变成冷饮。
为什么硝酸铵与水混合后,罐内饮料会变成冷饮呢?
[活动与探究]:现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH 。试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。
二、溶解时的吸热或放热现象
具体步骤
(1)测量水的温度
(2)加入物质
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
溶质溶解后水的温度/℃
结 论
固体溶解
固体溶解
固体溶解
溶解时温度不变
溶解时温度降低
溶解时放出升高
(3)搅拌、加促溶解
(4)加物质后溶液的温度
物质在溶解过程中常伴随着热量的变化
1.有的物质溶解时放出热量,温度升高
浓硫酸(液体)、氢氧化钠
2.有的物质溶解时吸收热量,温度降低
硝酸铵
3.有的物质溶解时没有明显的热量变化
氯化钠、蔗糖等
注意:氧化钙(生石灰)遇水是反应放热,而不是溶解放热。
溶解是物理变化
加快物质溶解速度的方法:
(1)搅拌
(2)加热
(3)将固体研碎
扩散过程:溶质分子(或离子)扩散到溶剂分子中去—吸收热量
溶解:
水合过程:溶剂分子结合溶质分子(或离子)—放出热量
同时进行
当吸热=放热时,溶液温度不变
当吸热﹥放热时,溶液温度降低
当吸热﹤放热时,溶液温度升高
物质溶于水时温度变化的实质:
将氯化钠、硝酸铵、氢氧化钠
三种固体分别加入试管中
若U型管液面无明显变化,则固体是
水
固体
若U型管液面左高右低,则固体是
若U型管液面左低右高,则固体是
氯化钠
硝酸铵
氢氧化钠
溶解时的吸热或放热的应用
实验9-4:
(无洗涤剂)
乳浊液
(小液滴分散到液体里形成的混合物)
三、乳化现象
药品:植物油、洗涤剂、水
仪器:试管、胶头滴管
试管内加入的物质 现 象
振荡前 振荡后 静置后
水和植物油
分层
浑浊
分层
倒出液体后试管是否干净?
不干净
(有洗涤剂)
乳化作用
洗涤剂在清洗油污时起的作用是什么?
试管内加入的物质 现 象
振荡前 振荡后 静置后
倒出液体后试 管是否干净?
水和植物油
分层
浑浊
较干净
浑浊但不分层
中加2-3滴洗涤剂
洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,所形成的乳浊液稳定性增强。
洗涤剂的这种作用称为乳化作用
3、存在:
(没加乳化剂时不稳定,静置后会分层。
加了乳化剂时较稳定,静置后不分层)
1、乳浊液:
小液滴分散到液体里形成的混合物
4、乳化现象:
2、特征:
物质以小液滴(许多分子的聚合体)的形式存在
如:油水混合物、牛奶、豆浆、酸奶、乳胶漆......
洗涤剂、洗面奶、洗发水去油污的原理都是乳化
用洗涤剂去油污
洗涤剂有乳化功能,能使油分散成无数细小的液滴而不聚成大的油珠。这些小液滴能随水流走。达到洗净衣物的目的。
生活小常识
在生活中有时有这样的现象,当油渍滴到了你的衣服上时,你将怎么办?怎样洗盘子比较干净?
植物油大油滴
洗涤剂
分散成小油滴
(乳化)
水冲洗
(乳浊液)
随水流走
植物油大油滴
汽油
(溶解)
植物油的汽油溶液
水冲洗
随水流走
用洗发剂洗去头发上的油脂
你知道吗
洗涤剂和汽油去除油污的原理的区别
汽修工人手上沾上油污时,常用汽油洗去
固体小颗粒分散到液体里形成的混合物
2、特征:
以固体小颗粒(许多分子的聚合体)的形式存在
通常,不溶于水的固体小颗粒在水里可形成悬浊液
如:碳酸钙 + 水 (泥+水)
乳浊液、悬浊液都不稳定,久置会分层或沉淀。
四、悬浊液
1、定义:
不均一、不稳定,静置后会沉淀
3、存在:
溶质
被溶解
的物质
一种或几种
物质
分散到
另一种 物 质
溶剂
均一、稳定的混合物
溶液
乳浊液
乳化现象
乳化剂
能溶解其他
物质的物质
二:溶解时的吸热和放热现象
物质在溶解过程中有的吸收热量,有的放出热量。
一、溶液
1、如右图所示,向小试管中分别加入下列一定量的物质,右侧U形管中液面未发生明显变化,该物质是 ( )
A.氢氧化钠固体
B.浓硫酸
C.硝酸铵晶体
D.氯化钠晶体
D
2、练习与巩固:右图所示,向小试管中加入一定量的下列物质,U形管液面右侧未发生改变,该物质是( )
U形管液面右侧升高,该物质是( )
U形管液面右侧降低,该物质是( )
A、浓硫酸 B、烧碱 C、生石灰
D、蔗糖 E、硝酸铵 F、氯化钠
DF
ABC
E
3、下列关于溶液的说法正确的是( )
A、均一、稳定的液体都是溶液
B、溶液是均一、稳定的纯净物
C、溶液是无色透明的液体
D、溶液是均一、稳定的混合物
4、将少量下列物质分别放入水中,充分搅拌,不能形成溶液的是( )
A.蔗糖 B.牛奶
C.酒精 D.白醋
5、可以作为溶质的( )
A、只有固体 B、只有液体
C、只有气体 D、气、液、固体都可以
第九单元 溶液
课题1 溶液的形成
1.了解溶液、溶质和溶剂概念;
2.能根据溶液的基本特征正确区分溶液和乳浊液; 3.常识性了解溶液在工农业生产科学实验及日常生活中的应用;
4.了解溶解时的吸热和放热现象
学习目标
学习定位
蓝色星球
地球的表面大部分被海水覆盖着,但海水是又苦又咸的,这是为什么呢?
海水中溶解了氯化钠等物质,它是一种混合物。
生活中的液体
说一说你生活中接触到的液体物质有哪些?
【思考1】同学们都喝过糖水,糖水是甜的,但在糖水中为什么看不到糖呢?
【思考2】前面我们接触了一些化学反应,如氢氧化钠溶液与硫酸铜溶液的反应,为什么这两种物质要放在溶液中反应呢?
【思考3】衣服上的油污,为什么用水洗不掉,而用汽油或洗涤剂可以洗掉呢?它们洗掉油污的原理是不是一样的呢?
实验9-1、在20 mL水中加入一匙蔗糖,用玻璃棒搅拌,还能看到蔗糖吗
实验:蔗糖溶解
【微观解释】蔗糖分子在水分子的作用下运动扩散到水分子中去了。
食盐的溶解
操作:在 20 mL 中加入一匙氯化钠,用玻璃棒搅拌,观察现象。
现象:氯化钠“消失”在水中
结论:氯化钠可以溶解在水中,形成氯化钠溶液
氯化钠溶于水:
溶
解
前
溶解中
溶解后
【微观解释】氯离子和钠离子在水分子的作用下运动扩散到水分子中去了。
蔗糖溶液和食盐溶液是怎样形成的?
蔗糖分散到水中
食盐分散到水中
形成
蔗糖溶液
形成
食盐溶液
蔗糖分子扩散到水分子的间隔之中。
Na+和Cl- 扩散到水分子的间隔之中。
物质溶解的本质是构成物质的微粒(分子、原子、离子)运动到溶剂微粒之间。
只要水分不被蒸发,温度不发生变化,蔗糖或氯化钠与水不会分离,且各组成部分相同。
1、定义:
均一性:指溶液任一部分的组成和性质完全相同(颜色、密度、浓度等)
稳定性:在外界条件(温度、溶剂量等)不变时, 溶剂与溶质不会分离 (静置不会沉淀或分层)
混合物:凡是溶液都属于混合物
一、溶液
一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物就是溶液。
2、特征:
均一性、稳定性
溶质
溶剂
溶液
+
3、溶液的组成
溶液
溶质:
溶剂:
被溶解的物质 如:蔗糖、食盐
能溶解其它物质的物质 如:水
(≥1种)
(1种)
2、V溶液 V质+ V剂
<
6、溶液的命名:
分子之间存在间隔
4、溶液、溶质与溶剂之间的量的关系
=
1、m溶液 m质+m剂
以微粒(分子、原子、离子)的形式存在
5、溶液中各物质的存在形式:
加入水中的 物质 溶质 溶剂 溶液名称
蔗 糖
食 盐
硫酸铜
蔗 糖
水
水
水
食 盐
硫酸铜
蔗糖的水溶液或蔗糖溶液
食盐的水溶液或食盐溶液
硫酸铜的水溶液或硫酸铜溶液
某溶质的某溶剂溶液 某溶质溶液(当溶剂为水时)
溶液 溶质(溶解前的状态) 溶剂(状态)
高锰酸钾溶液
碘 酒
硫酸溶液
稀盐酸
高锰酸钾(固体)
碘(固体)
硫酸(液体)
氯化氢 (气体)
水
酒精
水
水
(液态)
(液态)
(液态)
(液态)
溶质可以为:
固体、液体、气体
我会填
、某溶质某溶剂
水是最常用的溶剂,此外,汽油、酒精等也可作溶剂。
溶剂通常是液体,也可以是固体或气体。
溶液 名称 石灰水 酒精 溶液 碘酒 盐酸 稀硫酸 氢氧化钠溶液 硫酸铜溶液
溶质
溶剂
H2O
H2O
H2O
H2O
H2O
H2O
C2H5OH
H2SO4
HCl
C2H5OH
Ca(OH)2
I2
CuSO4
NaOH
①气体和液体形成的溶液:气体是溶质
②固体和液体形成的溶液: 固体是溶质
③液体和液体形成的溶液:量多的是溶剂,量少的溶质
④水和其他液体形成的溶液:无论质量大小,水为溶剂
7、溶液组成的判断:
反应 过量的锌加入H2SO4中 锌加入过量的H2SO4中 过量的石灰石加入H2SO4中 石灰石加入过量的HCl中 CO2通入水中 CO2恰好与石灰水反应
反应前的溶质
反应后的溶质
H2SO4
H2SO4
ZnSO4
ZnSO4
H2SO4
HCl
CaCl2
HCl
HCl
CaCl2
无
H2CO3
Ca(OH)2
无
Zn + H2SO4 = ZnSO4+ H2↑
CaCO3+ 2HCl = CaCl2+ H2O+CO2↑
CO2+ H2O = H2CO3
CO2+ Ca(OH)2 = CaCO3↓ +H2O
无土栽培
化学试剂
医药制剂
食品饮料
【思考】化学反应常在溶液中进行的
原因 。
加快反应速率
8、溶液的用途
一种番茄营养液的配方
肥料名称 用量(毫克/升)
硝酸钙 硝酸钾 硫酸镁 过磷酸钙 590
606
492
680
交流讨论
1.均一、稳定的液体一定是溶液吗?
不一定,如酒精、水等。溶液是均一、稳定的混合物。
2.将蔗糖溶液和氯化钠溶液混合,还是溶液吗?
是,氯化钠和蔗糖都是溶质。
溶液中的溶质可以有多种,如海水。
3.溶液一定是液体吗?
不一定。也可以是气体或固体。
含Cu2+的溶液呈蓝色
含Fe2+的溶液呈浅绿色
含Fe3+的溶液呈黄色
KMnO4的溶液呈紫红色
4.溶液一定是无色的吗?
不一定,大多数溶液无色,有些溶液是有颜色的。
课堂精练
1.判断下列有关溶液的说法是否正确
①凡是无色、透明、稳定的液体都是溶液
②溶液都是无色的
③溶质一定是以离子的形式分散在溶剂中
④溶液中可以有一种或多种溶质
⑤一定量的溶剂中,加入氯化钠越多,得到的溶液质量越大
⑥将氯化钠放入植物油中搅拌,能形成溶液
⑦溶液一定是混合物
⑧从一杯糖水中倒出一半,则剩余糖水的甜度变小
⑨实验室常将固体配成溶液,以提高反应速率
2、下列说法正确的是:
A、溶液一定是液体
B、生铁也是溶液
C、50mL酒精和50mL水混合得到100mL溶液
D、盐水和糖水都是溶液,两者混合在一起,则不是溶液了
3.下列各组物质充分混合后,能得到溶液的是:
A.沙土和水 B.冰和水
C.碘和酒精 D.花生油和水
4.铁和过量稀硫酸充分反应后,所得溶液中的溶质是:
A.只有铁 B.只有硫酸亚铁
C.只有硫酸铁 D.有硫酸亚铁和硫酸
C
D
B
实验探究二:溶质与溶剂的关系
[实验]9-2 不同的溶质在不同的溶剂中的溶解性
在两支试管中各加入2mL~3mL水,分别加入1~2小粒碘或高锰酸钾;另取两支试管各加入2mL~3mL汽油,再分别加入1~2小粒碘或高锰酸钾。振荡,观察现象。
试管号 溶质 溶剂 溶解情况
1 碘 水
2 高锰酸钾 水
结论
●不同的溶质在同一种溶剂中的溶解情况不同
碘难溶于水
溶解,溶液呈紫色
溶解,溶液呈棕色
高锰酸钾难溶于汽油
① 碘 汽油
② 高锰酸钾 汽油
试管号 溶质 溶剂 溶解情况
结论
●同一种溶质在不同的溶剂中溶解情况不同
碘难溶于水
溶解,溶液呈紫色
溶解,溶液呈棕色
高锰酸钾难溶于汽油
② 高锰酸钾 汽油
2 碘 汽油
① 高锰酸钾 水
1 碘 水
9、溶质与溶剂的辨证关系:
相同溶质在不同种溶剂里的溶解能力不同。
不同溶质在同种溶剂里的溶解能力不同。
即:溶质或溶剂的种类(性质)决定了物质的溶解能力
碘+水
碘+汽油
高锰酸钾+水
高锰酸钾+汽油
探究实验9-3:水和乙醇能够互溶吗?
在盛有2 mL水的试管中滴入2~3 滴红墨水(用红墨水是为了显色,利于观察),向其中缓缓加入约2mL的酒精。
溶剂 溶质 振荡前现象 振荡后现象 静置后现象 结论
水 乙醇
液体出现了分层现象
液体溶为一体,颜色均匀,不分层
酒精能与水互溶
稳定,不分层
水中滴入红墨水,振荡
加入乙醇,不要振荡
振荡,静置
“摇摇冰” 是一种即用即冷的罐装饮料。在饮料罐的夹层中分别装有硝酸铵和水,喝的时候将底部的旋钮转一下,使硝酸铵和水混合,罐内饮料就会变成冷饮。
为什么硝酸铵与水混合后,罐内饮料会变成冷饮呢?
[活动与探究]:现有试管、烧杯、玻璃棒、温度计等仪器和固态NaCl、NH4NO3、NaOH 。试设计实验方案,探究它们溶解于水时是放出热量还是吸收热量。
二、溶解时的吸热或放热现象
具体步骤
(1)测量水的温度
(2)加入物质
水中加入的溶质 NaCl NH4NO3 NaOH
加入溶质前水的温度/℃
溶解现象
溶质溶解后水的温度/℃
结 论
固体溶解
固体溶解
固体溶解
溶解时温度不变
溶解时温度降低
溶解时放出升高
(3)搅拌、加促溶解
(4)加物质后溶液的温度
物质在溶解过程中常伴随着热量的变化
1.有的物质溶解时放出热量,温度升高
浓硫酸(液体)、氢氧化钠
2.有的物质溶解时吸收热量,温度降低
硝酸铵
3.有的物质溶解时没有明显的热量变化
氯化钠、蔗糖等
注意:氧化钙(生石灰)遇水是反应放热,而不是溶解放热。
溶解是物理变化
加快物质溶解速度的方法:
(1)搅拌
(2)加热
(3)将固体研碎
扩散过程:溶质分子(或离子)扩散到溶剂分子中去—吸收热量
溶解:
水合过程:溶剂分子结合溶质分子(或离子)—放出热量
同时进行
当吸热=放热时,溶液温度不变
当吸热﹥放热时,溶液温度降低
当吸热﹤放热时,溶液温度升高
物质溶于水时温度变化的实质:
将氯化钠、硝酸铵、氢氧化钠
三种固体分别加入试管中
若U型管液面无明显变化,则固体是
水
固体
若U型管液面左高右低,则固体是
若U型管液面左低右高,则固体是
氯化钠
硝酸铵
氢氧化钠
溶解时的吸热或放热的应用
实验9-4:
(无洗涤剂)
乳浊液
(小液滴分散到液体里形成的混合物)
三、乳化现象
药品:植物油、洗涤剂、水
仪器:试管、胶头滴管
试管内加入的物质 现 象
振荡前 振荡后 静置后
水和植物油
分层
浑浊
分层
倒出液体后试管是否干净?
不干净
(有洗涤剂)
乳化作用
洗涤剂在清洗油污时起的作用是什么?
试管内加入的物质 现 象
振荡前 振荡后 静置后
倒出液体后试 管是否干净?
水和植物油
分层
浑浊
较干净
浑浊但不分层
中加2-3滴洗涤剂
洗涤剂能使植物油在水中分散成无数细小的液滴,而不聚集成大的油珠,从而使油和水不再分层,所形成的乳浊液稳定性增强。
洗涤剂的这种作用称为乳化作用
3、存在:
(没加乳化剂时不稳定,静置后会分层。
加了乳化剂时较稳定,静置后不分层)
1、乳浊液:
小液滴分散到液体里形成的混合物
4、乳化现象:
2、特征:
物质以小液滴(许多分子的聚合体)的形式存在
如:油水混合物、牛奶、豆浆、酸奶、乳胶漆......
洗涤剂、洗面奶、洗发水去油污的原理都是乳化
用洗涤剂去油污
洗涤剂有乳化功能,能使油分散成无数细小的液滴而不聚成大的油珠。这些小液滴能随水流走。达到洗净衣物的目的。
生活小常识
在生活中有时有这样的现象,当油渍滴到了你的衣服上时,你将怎么办?怎样洗盘子比较干净?
植物油大油滴
洗涤剂
分散成小油滴
(乳化)
水冲洗
(乳浊液)
随水流走
植物油大油滴
汽油
(溶解)
植物油的汽油溶液
水冲洗
随水流走
用洗发剂洗去头发上的油脂
你知道吗
洗涤剂和汽油去除油污的原理的区别
汽修工人手上沾上油污时,常用汽油洗去
固体小颗粒分散到液体里形成的混合物
2、特征:
以固体小颗粒(许多分子的聚合体)的形式存在
通常,不溶于水的固体小颗粒在水里可形成悬浊液
如:碳酸钙 + 水 (泥+水)
乳浊液、悬浊液都不稳定,久置会分层或沉淀。
四、悬浊液
1、定义:
不均一、不稳定,静置后会沉淀
3、存在:
溶质
被溶解
的物质
一种或几种
物质
分散到
另一种 物 质
溶剂
均一、稳定的混合物
溶液
乳浊液
乳化现象
乳化剂
能溶解其他
物质的物质
二:溶解时的吸热和放热现象
物质在溶解过程中有的吸收热量,有的放出热量。
一、溶液
1、如右图所示,向小试管中分别加入下列一定量的物质,右侧U形管中液面未发生明显变化,该物质是 ( )
A.氢氧化钠固体
B.浓硫酸
C.硝酸铵晶体
D.氯化钠晶体
D
2、练习与巩固:右图所示,向小试管中加入一定量的下列物质,U形管液面右侧未发生改变,该物质是( )
U形管液面右侧升高,该物质是( )
U形管液面右侧降低,该物质是( )
A、浓硫酸 B、烧碱 C、生石灰
D、蔗糖 E、硝酸铵 F、氯化钠
DF
ABC
E
3、下列关于溶液的说法正确的是( )
A、均一、稳定的液体都是溶液
B、溶液是均一、稳定的纯净物
C、溶液是无色透明的液体
D、溶液是均一、稳定的混合物
4、将少量下列物质分别放入水中,充分搅拌,不能形成溶液的是( )
A.蔗糖 B.牛奶
C.酒精 D.白醋
5、可以作为溶质的( )
A、只有固体 B、只有液体
C、只有气体 D、气、液、固体都可以
同课章节目录
