2022-2023学年化学鲁教版(五四学制)第五单元 定量研究化学反应 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学鲁教版(五四学制)第五单元 定量研究化学反应 单元练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 179.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-08 00:00:00 | ||
图片预览


文档简介
2022-2023学年化学鲁教版(五四学制)--定量研究化学反应
一、单选题
1.清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下(图中的微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O2 B.参加反应的甲与乙的质量比为 3∶1
C.甲是单质,乙、丙、丁均为氧化物 D.该反应遵守质量守恒定律
2.利用催化剂将工厂废气中的二氧化碳转化为燃料x,是实现“碳中和”的路径之一,该反应的化学方程式为,X的化学式为
A.C B.CH4 C.CH3OH D.CH2O
3.元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是
A.CoO
B.CoO3
C.Co2O3
D.Co3O4
4.实验室里一般不能制得氧气的物质是
A.高锰酸钾 B.氯酸钾 C.氯化钠 D.过氧化氢
5.在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用化学方程式表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
6.在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,化学方程式为。则X是
A.NO2
B.CO
C.NO
D.N2O5
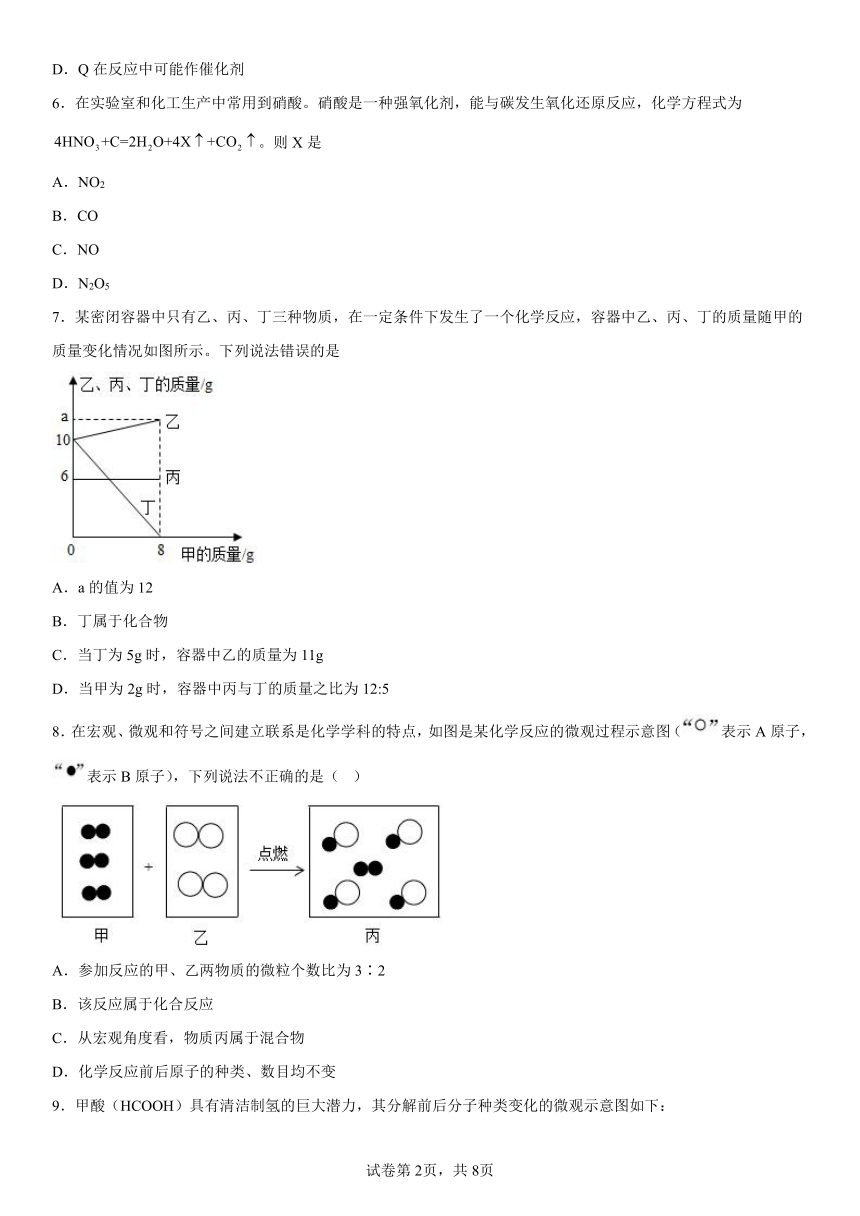
7.某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是
A.a的值为12
B.丁属于化合物
C.当丁为5g时,容器中乙的质量为11g
D.当甲为2g时,容器中丙与丁的质量之比为12:5
8.在宏观、微观和符号之间建立联系是化学学科的特点,如图是某化学反应的微观过程示意图(表示A原子,表示B原子),下列说法不正确的是( )
A.参加反应的甲、乙两物质的微粒个数比为3∶2
B.该反应属于化合反应
C.从宏观角度看,物质丙属于混合物
D.化学反应前后原子的种类、数目均不变
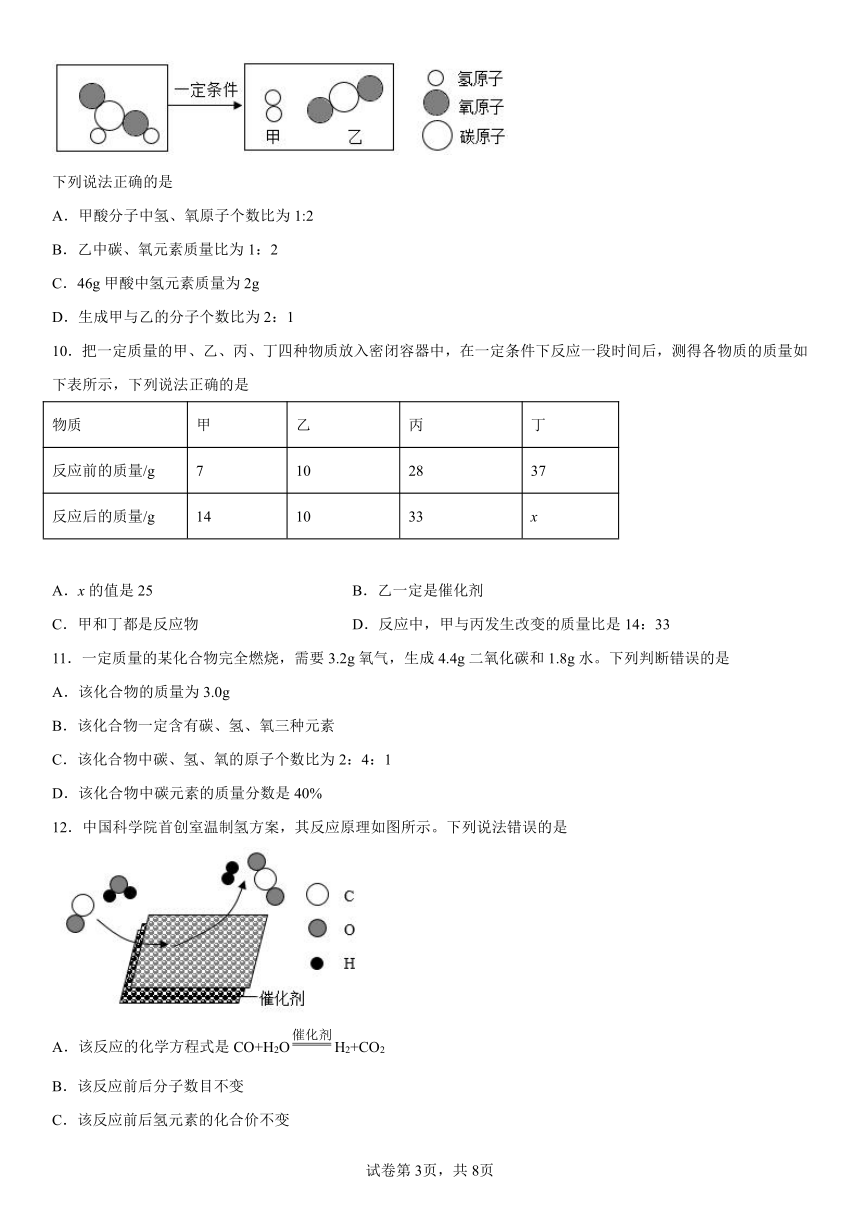
9.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
10.把一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表所示,下列说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 7 10 28 37
反应后的质量/g 14 10 33 x
A.x的值是25 B.乙一定是催化剂
C.甲和丁都是反应物 D.反应中,甲与丙发生改变的质量比是14:33
11.一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
12.中国科学院首创室温制氢方案,其反应原理如图所示。下列说法错误的是
A.该反应的化学方程式是CO+H2OH2+CO2
B.该反应前后分子数目不变
C.该反应前后氢元素的化合价不变
D.反应物CO和H2O都是氧化物
13.将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
下列有关说法正确的是
A.m=0
B.发生反应的甲、乙质量比为3:1
C.该反应是化合反应
D.丙一定作催化剂
14.将氯化氢转化为氯气的技术是当今化学研究的热点之一,下图是该反应的微观示意图
(其中:表示氢原子,表示氧原子,表示氯原子)
下列说法正确的是
A.该反应涉及两种氧化物 B.生成物均由两种元素组成
C.参加反应的两种物质的质量比为73:16 D.反应前后分子总数不变
二、填空题
15.某同学用镁条在空气中燃烧(只考虑氧气参加反应)验证质量守恒定律,请回答下列问题:
(1)实验前打磨镁条的目的是_________,镁条燃烧化学方程式是__________。
(2)反应时测得固体质量的变化如图所示,则参加反应的氧气的质量为________(用m1和m2表示),该反应_________(填“遵守”或“不遵守”)质量守恒定律
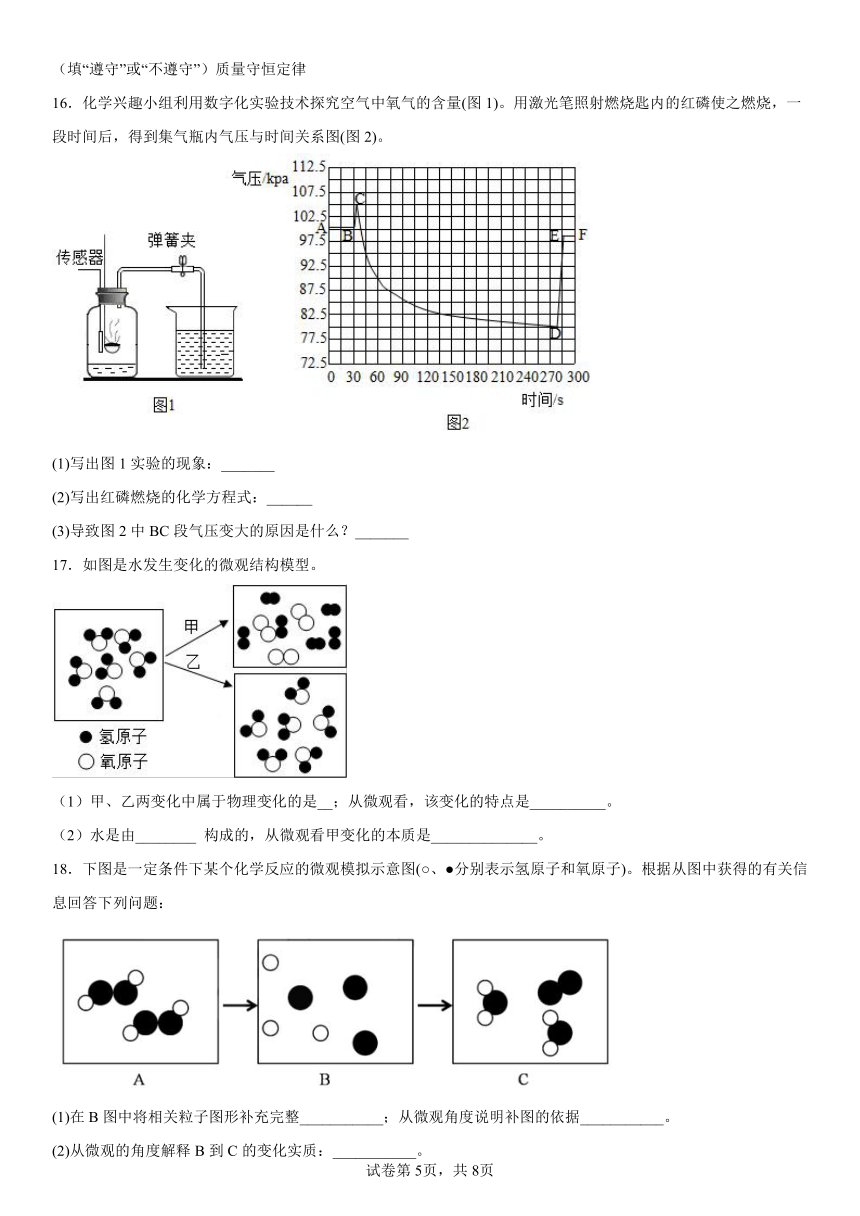
16.化学兴趣小组利用数字化实验技术探究空气中氧气的含量(图1)。用激光笔照射燃烧匙内的红磷使之燃烧,一段时间后,得到集气瓶内气压与时间关系图(图2)。
(1)写出图1实验的现象:_______
(2)写出红磷燃烧的化学方程式:______
(3)导致图2中BC段气压变大的原因是什么?_______
17.如图是水发生变化的微观结构模型。
(1)甲、乙两变化中属于物理变化的是__;从微观看,该变化的特点是__________。
(2)水是由________ 构成的,从微观看甲变化的本质是______________。
18.下图是一定条件下某个化学反应的微观模拟示意图(○、●分别表示氢原子和氧原子)。根据从图中获得的有关信息回答下列问题:
(1)在B图中将相关粒子图形补充完整___________;从微观角度说明补图的依据___________。
(2)从微观的角度解释B到C的变化实质:___________。
(3)化学反应前后质量守恒的微观解释:参加反应的各物质的原子重新组合而生成其他物质的过程在化学反应中反应前后,___________。
19.用化学用语(元素符号、离子符号、化学式、化学方程式)填空:
(1)三个亚铁离子_____;
(2)碳的+2 价氧化物_____;
(3)由空气中含量最多的元素、地壳中含量最多的非金属元素和地壳中含量最多的金属 元素共同组成的化合物的化学式_____;
(4)在尘埃的催化作用下,二氧化硫和氧气反应生成三氧化硫(SO3):_____。
三、实验题
20.下列装置常用于实验室制取气体。
(1)仪器①的名称是__________。
(2)用装置甲制取氧气,采用该收集方法的依据是__________。用收集的氧气做铁丝燃烧实验,应预先在集气瓶中加入少量的__________。
(3)用装置乙制取气体,实验结束时,为防止水槽里的水倒流,应采取的操作是__________。
(4)在加热条件下,用醋酸钠( CH3COONa)固体与碱石灰固体中的氢氧化钠反应制取甲烷,同时生成碳酸钠,应选用的装置是__________(填“甲”或“乙”),反应的化学方程式为__________。
21.对蜡烛及其燃烧的探究(描述现象时不可出现产物名称)
(1)火焰:_____、_____、_____(温度最高)
(2)比较各火焰层温度:用一火柴梗平放入火焰中。现象:两端先碳化;结论:外焰温度最高
(3)检验产物H2O:用干冷烧杯罩火焰上方,烧杯内有水雾<说明蜡烛燃烧生成了_____,其中含有_____元素;石灰水变浑浊,说明蜡烛燃烧生成了_____,说明蜡烛中含有_____元素>CO2:取下烧杯,倒入澄清石灰水,振荡,变浑浊<说明蜡烛燃烧生成了_____,说明蜡烛中含有_____元素>
(4)熄灭后:有白烟(为石蜡蒸气遇冷形成的石蜡固体小颗粒),点燃白烟,蜡烛复燃<说明蜡烛燃烧是蜡烛气化后的石蜡蒸气燃烧>
四、计算题
22.硅是支撑信息产业的重要材料,工业上,在电炉中用炭粉还原二氧化硅制得硅单质。若往电炉里加入125kg含96%二氧化硅的石英砂(杂质不参与反应)和足量的炭粉,使它们发生如下反应:,计算:
①参加反应的 SiO2的质量______;
②理论上可制得硅单质的质量_______.
23.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是 。
(2)工业上用含氧化铁480t的赤铁矿为原料炼铁,可得到含杂质4%的生铁质量为多少?(根据化学方程式计算并写出解题过程)
24.氧气是人类生产活动的重要资源。
(1)下列属于O2的化学性质的是_____(填标号)。
A O2能支持燃烧
B O2的密度比空气的密度略大
C O2在低温、高压时能变为液体或固体
(2)小圳同学进行实验室制备O2的相关探究。
【查阅】他得知在KClO3分解制O2的反应中,Fe2O3可作催化剂。
【实验】他用电子秤称取0.49gFe2O3和一定量的KClO3,充分混合后加热至KClO3完全分解,冷却至室温,称得剩余固体的质量为1.98g。
【计算】①剩余固体中KCl 的质量。
②该反应生成O2的质量(根据化学方程式写出完整的计算步骤)。
【思考】他发现制备O2较慢,猜测KClO3和Fe2O3的质量比可能会影响反应的快慢。
【探究】③他调节KClO3和Fe2O3的质量比制备O2,整理数据绘制出如图,从图中得出KClO3和Fe2O3最佳质量比是________。
【结论】④根据质量守恒定律,请你计算出小圳同学在【实验】中称取的KClO3的质量为______g,KClO3和Fe2O3的质量比是________(填最简比),不是最佳质量比。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.C
5.D
6.A
7.D
8.A
9.C
10.A
11.C
12.C
13.C
14.C
15.(1) 除去表面的氧化膜和污垢
(2) m2-m1 遵守
16.(1)红磷燃烧产生大量白烟,温度冷却至室温后,打开止水夹,烧杯中的水进入集气瓶中,进入水的体积约占空气总体积的
(2)4P+5O22P2O5
(3)红磷燃烧放热,集气瓶内温度升高,气体压强变大
17. 乙 水分子本身没有改变,分之间间隔变大 水分子 水分子破裂为氢原子和氧原子,每两个氢原子结合为一个氢分子,每两个氧原子结合为一个氧分子
18.(1) 补一个氢原子和一个氧原子 化学反应中原子的种类个数均不发生改变
(2)每2个氢原子和1个氧原子结合成1个水分子,每2个氧原子结合成1个氧分子
(3)原子的种类、个数、质量均不发生改变
19. 3Fe2+ CO Al(NO3)3 2SO2+O2 2SO3
20. 长颈漏斗 氧气的密度比空气大 水或铺一层细沙 先将导管移出水面,然后熄灭酒精灯 乙
21. 焰心 内焰 外焰 水 氢 二氧化碳 碳 二氧化碳和水 碳、氢
22.120kg; 56kg
23.(1)焦炭(2)350t
24.(1)A (2)①1.49g ②0.96g ③5:4 ④2.45;5:1
答案第1页,共2页
答案第1页,共2页
一、单选题
1.清华大学研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化成液体燃料甲醇,其微观示意图如下(图中的微粒恰好完全反应)。下列说法正确的是
A.丁的化学式为H2O2 B.参加反应的甲与乙的质量比为 3∶1
C.甲是单质,乙、丙、丁均为氧化物 D.该反应遵守质量守恒定律
2.利用催化剂将工厂废气中的二氧化碳转化为燃料x,是实现“碳中和”的路径之一,该反应的化学方程式为,X的化学式为
A.C B.CH4 C.CH3OH D.CH2O
3.元素钴(Co)有多种化合价,将9.3gCo(OH)2在空气中加热至290℃时完全脱水,得到8.3g钴的氧化物,该氧化物的化学式是
A.CoO
B.CoO3
C.Co2O3
D.Co3O4
4.实验室里一般不能制得氧气的物质是
A.高锰酸钾 B.氯酸钾 C.氯化钠 D.过氧化氢
5.在一个密闭容器中放入P、Q、R、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。则关于此反应的认识正确的是( )
物质 P Q R W
反应前的质量(g) 5 2 14 18
反应后的质量(g) 20 x 4 13
A.参加化学反应的P和W的质量比为3:2
B.该反应用化学方程式表示为:
C.反应后容器中R与Q的质量比为1:2
D.Q在反应中可能作催化剂
6.在实验室和化工生产中常用到硝酸。硝酸是一种强氧化剂,能与碳发生氧化还原反应,化学方程式为。则X是
A.NO2
B.CO
C.NO
D.N2O5
7.某密闭容器中只有乙、丙、丁三种物质,在一定条件下发生了一个化学反应,容器中乙、丙、丁的质量随甲的质量变化情况如图所示。下列说法错误的是
A.a的值为12
B.丁属于化合物
C.当丁为5g时,容器中乙的质量为11g
D.当甲为2g时,容器中丙与丁的质量之比为12:5
8.在宏观、微观和符号之间建立联系是化学学科的特点,如图是某化学反应的微观过程示意图(表示A原子,表示B原子),下列说法不正确的是( )
A.参加反应的甲、乙两物质的微粒个数比为3∶2
B.该反应属于化合反应
C.从宏观角度看,物质丙属于混合物
D.化学反应前后原子的种类、数目均不变
9.甲酸(HCOOH)具有清洁制氢的巨大潜力,其分解前后分子种类变化的微观示意图如下:
下列说法正确的是
A.甲酸分子中氢、氧原子个数比为1:2
B.乙中碳、氧元素质量比为1:2
C.46g甲酸中氢元素质量为2g
D.生成甲与乙的分子个数比为2:1
10.把一定质量的甲、乙、丙、丁四种物质放入密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如下表所示,下列说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 7 10 28 37
反应后的质量/g 14 10 33 x
A.x的值是25 B.乙一定是催化剂
C.甲和丁都是反应物 D.反应中,甲与丙发生改变的质量比是14:33
11.一定质量的某化合物完全燃烧,需要3.2g氧气,生成4.4g二氧化碳和1.8g水。下列判断错误的是
A.该化合物的质量为3.0g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
12.中国科学院首创室温制氢方案,其反应原理如图所示。下列说法错误的是
A.该反应的化学方程式是CO+H2OH2+CO2
B.该反应前后分子数目不变
C.该反应前后氢元素的化合价不变
D.反应物CO和H2O都是氧化物
13.将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如下:
物质 甲 乙 丙 丁
反应前的质量/g 30 10 5 5
反应后的质量/g 2 4 m 39
下列有关说法正确的是
A.m=0
B.发生反应的甲、乙质量比为3:1
C.该反应是化合反应
D.丙一定作催化剂
14.将氯化氢转化为氯气的技术是当今化学研究的热点之一,下图是该反应的微观示意图
(其中:表示氢原子,表示氧原子,表示氯原子)
下列说法正确的是
A.该反应涉及两种氧化物 B.生成物均由两种元素组成
C.参加反应的两种物质的质量比为73:16 D.反应前后分子总数不变
二、填空题
15.某同学用镁条在空气中燃烧(只考虑氧气参加反应)验证质量守恒定律,请回答下列问题:
(1)实验前打磨镁条的目的是_________,镁条燃烧化学方程式是__________。
(2)反应时测得固体质量的变化如图所示,则参加反应的氧气的质量为________(用m1和m2表示),该反应_________(填“遵守”或“不遵守”)质量守恒定律
16.化学兴趣小组利用数字化实验技术探究空气中氧气的含量(图1)。用激光笔照射燃烧匙内的红磷使之燃烧,一段时间后,得到集气瓶内气压与时间关系图(图2)。
(1)写出图1实验的现象:_______
(2)写出红磷燃烧的化学方程式:______
(3)导致图2中BC段气压变大的原因是什么?_______
17.如图是水发生变化的微观结构模型。
(1)甲、乙两变化中属于物理变化的是__;从微观看,该变化的特点是__________。
(2)水是由________ 构成的,从微观看甲变化的本质是______________。
18.下图是一定条件下某个化学反应的微观模拟示意图(○、●分别表示氢原子和氧原子)。根据从图中获得的有关信息回答下列问题:
(1)在B图中将相关粒子图形补充完整___________;从微观角度说明补图的依据___________。
(2)从微观的角度解释B到C的变化实质:___________。
(3)化学反应前后质量守恒的微观解释:参加反应的各物质的原子重新组合而生成其他物质的过程在化学反应中反应前后,___________。
19.用化学用语(元素符号、离子符号、化学式、化学方程式)填空:
(1)三个亚铁离子_____;
(2)碳的+2 价氧化物_____;
(3)由空气中含量最多的元素、地壳中含量最多的非金属元素和地壳中含量最多的金属 元素共同组成的化合物的化学式_____;
(4)在尘埃的催化作用下,二氧化硫和氧气反应生成三氧化硫(SO3):_____。
三、实验题
20.下列装置常用于实验室制取气体。
(1)仪器①的名称是__________。
(2)用装置甲制取氧气,采用该收集方法的依据是__________。用收集的氧气做铁丝燃烧实验,应预先在集气瓶中加入少量的__________。
(3)用装置乙制取气体,实验结束时,为防止水槽里的水倒流,应采取的操作是__________。
(4)在加热条件下,用醋酸钠( CH3COONa)固体与碱石灰固体中的氢氧化钠反应制取甲烷,同时生成碳酸钠,应选用的装置是__________(填“甲”或“乙”),反应的化学方程式为__________。
21.对蜡烛及其燃烧的探究(描述现象时不可出现产物名称)
(1)火焰:_____、_____、_____(温度最高)
(2)比较各火焰层温度:用一火柴梗平放入火焰中。现象:两端先碳化;结论:外焰温度最高
(3)检验产物H2O:用干冷烧杯罩火焰上方,烧杯内有水雾<说明蜡烛燃烧生成了_____,其中含有_____元素;石灰水变浑浊,说明蜡烛燃烧生成了_____,说明蜡烛中含有_____元素>CO2:取下烧杯,倒入澄清石灰水,振荡,变浑浊<说明蜡烛燃烧生成了_____,说明蜡烛中含有_____元素>
(4)熄灭后:有白烟(为石蜡蒸气遇冷形成的石蜡固体小颗粒),点燃白烟,蜡烛复燃<说明蜡烛燃烧是蜡烛气化后的石蜡蒸气燃烧>
四、计算题
22.硅是支撑信息产业的重要材料,工业上,在电炉中用炭粉还原二氧化硅制得硅单质。若往电炉里加入125kg含96%二氧化硅的石英砂(杂质不参与反应)和足量的炭粉,使它们发生如下反应:,计算:
①参加反应的 SiO2的质量______;
②理论上可制得硅单质的质量_______.
23.工业上,把铁矿石和石灰石等物质一起加入高炉,通入热空气,经过一系列反应最终可得到生铁。
(1)炼铁的原料除了铁矿石和石灰石外,还需要的一种物质是 。
(2)工业上用含氧化铁480t的赤铁矿为原料炼铁,可得到含杂质4%的生铁质量为多少?(根据化学方程式计算并写出解题过程)
24.氧气是人类生产活动的重要资源。
(1)下列属于O2的化学性质的是_____(填标号)。
A O2能支持燃烧
B O2的密度比空气的密度略大
C O2在低温、高压时能变为液体或固体
(2)小圳同学进行实验室制备O2的相关探究。
【查阅】他得知在KClO3分解制O2的反应中,Fe2O3可作催化剂。
【实验】他用电子秤称取0.49gFe2O3和一定量的KClO3,充分混合后加热至KClO3完全分解,冷却至室温,称得剩余固体的质量为1.98g。
【计算】①剩余固体中KCl 的质量。
②该反应生成O2的质量(根据化学方程式写出完整的计算步骤)。
【思考】他发现制备O2较慢,猜测KClO3和Fe2O3的质量比可能会影响反应的快慢。
【探究】③他调节KClO3和Fe2O3的质量比制备O2,整理数据绘制出如图,从图中得出KClO3和Fe2O3最佳质量比是________。
【结论】④根据质量守恒定律,请你计算出小圳同学在【实验】中称取的KClO3的质量为______g,KClO3和Fe2O3的质量比是________(填最简比),不是最佳质量比。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.C
5.D
6.A
7.D
8.A
9.C
10.A
11.C
12.C
13.C
14.C
15.(1) 除去表面的氧化膜和污垢
(2) m2-m1 遵守
16.(1)红磷燃烧产生大量白烟,温度冷却至室温后,打开止水夹,烧杯中的水进入集气瓶中,进入水的体积约占空气总体积的
(2)4P+5O22P2O5
(3)红磷燃烧放热,集气瓶内温度升高,气体压强变大
17. 乙 水分子本身没有改变,分之间间隔变大 水分子 水分子破裂为氢原子和氧原子,每两个氢原子结合为一个氢分子,每两个氧原子结合为一个氧分子
18.(1) 补一个氢原子和一个氧原子 化学反应中原子的种类个数均不发生改变
(2)每2个氢原子和1个氧原子结合成1个水分子,每2个氧原子结合成1个氧分子
(3)原子的种类、个数、质量均不发生改变
19. 3Fe2+ CO Al(NO3)3 2SO2+O2 2SO3
20. 长颈漏斗 氧气的密度比空气大 水或铺一层细沙 先将导管移出水面,然后熄灭酒精灯 乙
21. 焰心 内焰 外焰 水 氢 二氧化碳 碳 二氧化碳和水 碳、氢
22.120kg; 56kg
23.(1)焦炭(2)350t
24.(1)A (2)①1.49g ②0.96g ③5:4 ④2.45;5:1
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
