2022-2023学年化学人教版 第三单元 物质构成的奥秘 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学人教版 第三单元 物质构成的奥秘 单元练习(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 141.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-08 16:22:35 | ||
图片预览




文档简介
2022-2023学年化学人教版---物质构成的奥秘
一、单选题
1.人类的生存离不开氧气,下列关于氧气说法错误的是
A.硫在氧气中燃烧,产生淡蓝色火焰
B.保持氧气化学性质的最小粒子是氧分子
C.氧气有助燃性,可用于航天
D.氧气能供给呼吸,与体内的物质反应释放能量,维持生命活动
2.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
3.物质由微观粒子构成。下列都由离子构成的一组物质是
A.氯化钠、硫酸铜 B.水、干冰 C.金刚石、氧化汞 D.氦气、氨气
4.如图是几种微粒的结构示意图,根据图示判断以下说法不正确的是
A.B元素属于金属元素
B.A与C元素具有相似的化学性质
C.C原子在化学反应中容易失去两个电子形成阳离子
D.B、C、D元素位于同一周期
5.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
6.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为
A.硒
B.硅
C.铝
D.锡
7.原子核中一定含有的粒子是( )
A.中子 B.质子 C.电子 D.质子和电子
8.一定条件下在密闭容器里加热冰,温度和时间的关系如图所示,①②③表示水在不同时刻的存在状态。下列有关判断正确的是
A.水分子间的间隔:②>③
B.水分子的运动速率:①>③
C.水分子的质量:①=②=③
D.②→③的过程中水发生了分解
9.我们在商场常看到“补锌”、“补铁”等字样的食品,其中“锌”、“铁”是指
A.元素 B.原子 C.分子 D.单质
10.根据图中提供的信息判断,下列说法不正确的是
A.①③属于同种元素
B.②表示的元素常见化合价为+1价
C.硒元素的相对原子质量是34
D.③④为稳定结构
11.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
12.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
13.下列有关粒子的说法中正确的是
A.原子的原子核都是由质子和中子构成的 B.分子可分,而原子不可再分
C.原子可转化成离子,离子不能转化为原子 D.钠原子和钠离子核电荷数相同
14.2020年6月23日我国的北斗导航“收官之星”在西昌发射成功,北斗导航卫星系统采用铷原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的原子结构示意图如图所示。下列说法不正确的是
A.铷单质具有导电性
B.m的值是37,n的值是1
C.铷的相对原子质量为85.47
D.氯化铷的化学式为RbCl2
二、填空题
15.图甲是铝元素在元素周期表中的相关信息,图乙是几种微粒的结构示意图,仔细分析答题:
(1)图甲中,铝元素的信息有处错误,请加以改正_________;
(2)铝原子的相对原子质量_________ ;
(3)图乙中,属于稳定结构的原子是____ (填序号, 下同);
(4)图乙中,与铝不属于同一周期元素的是_________。
16.元素周期表是学习和研究化学的重要工具,元素周期表的一部分如下表,请根据下表回答有关问题。
(1)观察第2、3周期的元素,这两个周期开头的元素是______,结尾的元素是_______。(填“金属元素”“非金属元素"或“稀有气体元素”)
(2)磷原子的质子数是______,相对原子质量是_______。
(3)元素周期表中,同族元素的化学性质具有一定的相似性,同周期元素的化学性质具有一定的速变规律。
①同族元素的化学性质相似的原因是_______。
②同周期元素的原子的最外层电子数的变化规律是________。
17.化学用语是学习化学的重要工具。请用适当的化学符号填空。
(1)保持氦气化学性质的最小粒子______。
(2)地壳中含量最多的金属元素______。
(3)标出H2O中氢元素的化合价______。
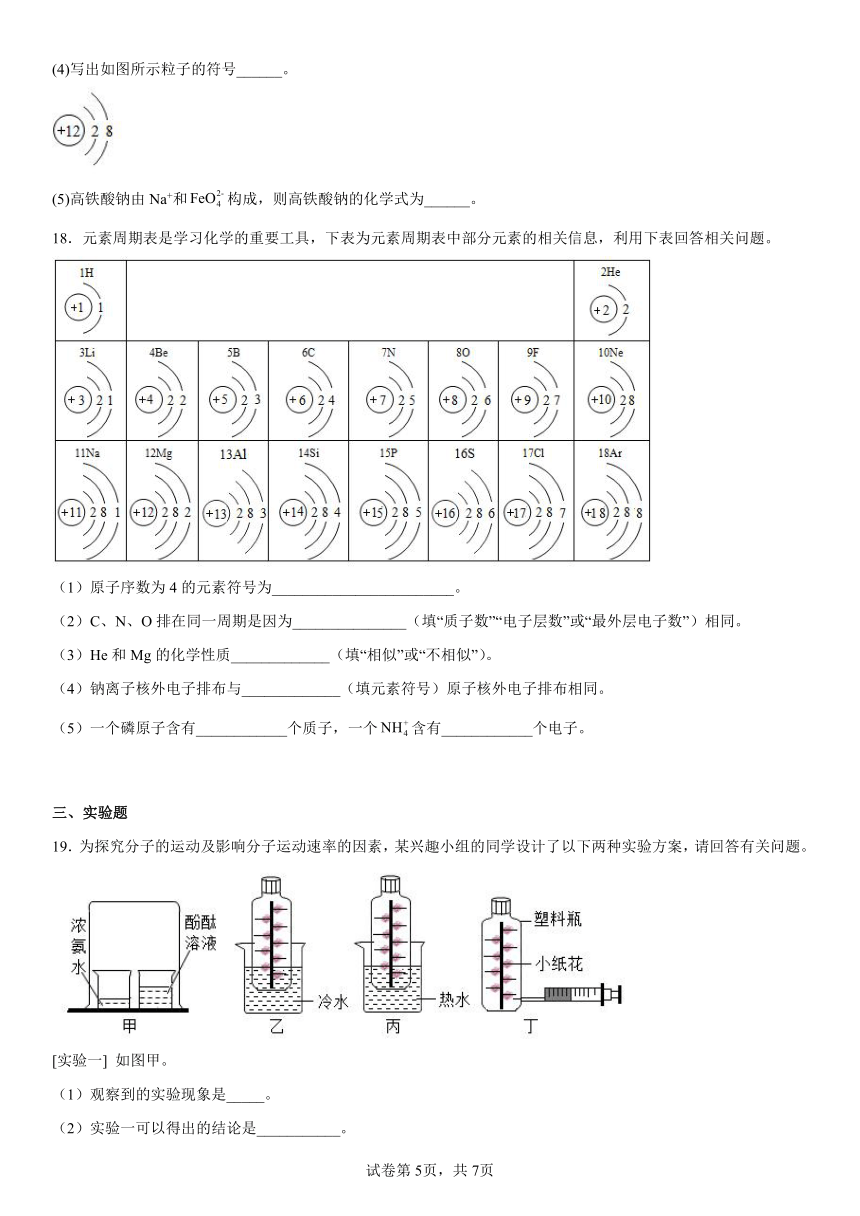
(4)写出如图所示粒子的符号______。
(5)高铁酸钠由Na+和构成,则高铁酸钠的化学式为______。
18.元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。
(1)原子序数为4的元素符号为________________________。
(2)C、N、O排在同一周期是因为_______________(填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质_____________(填“相似”或“不相似”)。
(4)钠离子核外电子排布与_____________(填元素符号)原子核外电子排布相同。
(5)一个磷原子含有____________个质子,一个含有____________个电子。
三、实验题
19.为探究分子的运动及影响分子运动速率的因素,某兴趣小组的同学设计了以下两种实验方案,请回答有关问题。
[实验一] 如图甲。
(1)观察到的实验现象是_____。
(2)实验一可以得出的结论是___________。
[实验二] 如图乙、图丙。图乙、图丙中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图丁的操作方式分别用注射器向图乙和图丙的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40 ℃的热水中。
(1)观察到的现象是__________________。
(2)实验中塑料瓶和纸花的大小、形状,浓氨水的滴数等实验条件需要保持相同,是因为对比实验中需要用到___法。
(3)实验二除可得出实验一的结论外,还可以得出的结论是_________。
20.如图的实验1、实验2两个实验是教材上册P63的探究微粒性质实验操作示意图。
①根据实验1中最后观察到的实验现象,说明__________。
②久置后的实验2中溶液变红的烧杯是_________,说明___________。
③根据上述实验现象判断下列说法中正确的是________。
A氨分子在不断运动
B浓氨水具有挥发性
C酚酞分子不运动
D酚酞分子运动慢
四、计算题
21.已知碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,铁原子的质量为9.288×10-26kg。请填空或进行计算:
(注:第2、3小问写出计算过程并对钠原子质量计算结果保留三位小数)
(1)钠原子核内有____________个中子。
(2)一个钠原子的质量为多少?
(3)铁原子的相对原子质量是多少?
22.若R原子的相对原子质量为23,核内质子数比中子数少一个,求
(1)R原子的中子数__________。
(2)该原子为_____________原子(填符号)
(3)画出该原子的离子结构示意图____________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.A
4.B
5.D
6.B
7.B
8.C
9.A
10.C
11.A
12.B
13.D
14.D
15. Al 26.98 AD A
16.(1) 金属元素 稀有气体元素
(2) 15 30.97
(3) 同族元素原子的最外层电子数相同 从左到右,最外层电子数依次递增
17.(1)He
(2)Al
(3)
(4)Mg2+
(5)Na2FeO4
18. Be 电子层数 不相似 Ne 15 10
19. 酚酞溶液变红 分子在不断运动 小纸花自下而上依次变红,且图丙中的纸花比图乙中的纸花更快变红 控制变量 温度越高,分子运动速率越快
20. 酚酞试液遇浓氨水变红 C 氨气分子运动 AB
21.(1)12
(2)解:设一个钠原子的质量为x。
由题可知:碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,有:
钠原子的相对原子质量为,
x=3.820×10-26kg
答:一个钠原子的质量为3.820×10-26kg。
(3)解:铁原子的相对原子质量为
答:铁原子的相对原子质量为56。
22.(1)12
(2)Na
(3)
答案第1页,共2页
答案第1页,共2页
一、单选题
1.人类的生存离不开氧气,下列关于氧气说法错误的是
A.硫在氧气中燃烧,产生淡蓝色火焰
B.保持氧气化学性质的最小粒子是氧分子
C.氧气有助燃性,可用于航天
D.氧气能供给呼吸,与体内的物质反应释放能量,维持生命活动
2.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
3.物质由微观粒子构成。下列都由离子构成的一组物质是
A.氯化钠、硫酸铜 B.水、干冰 C.金刚石、氧化汞 D.氦气、氨气
4.如图是几种微粒的结构示意图,根据图示判断以下说法不正确的是
A.B元素属于金属元素
B.A与C元素具有相似的化学性质
C.C原子在化学反应中容易失去两个电子形成阳离子
D.B、C、D元素位于同一周期
5.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
6.“化学”一词最早出于清朝的《化学鉴原》一书,该书把地壳中含量第二的元素翻译成“矽(xi)”,如今把这种“矽”元素命名为
A.硒
B.硅
C.铝
D.锡
7.原子核中一定含有的粒子是( )
A.中子 B.质子 C.电子 D.质子和电子
8.一定条件下在密闭容器里加热冰,温度和时间的关系如图所示,①②③表示水在不同时刻的存在状态。下列有关判断正确的是
A.水分子间的间隔:②>③
B.水分子的运动速率:①>③
C.水分子的质量:①=②=③
D.②→③的过程中水发生了分解
9.我们在商场常看到“补锌”、“补铁”等字样的食品,其中“锌”、“铁”是指
A.元素 B.原子 C.分子 D.单质
10.根据图中提供的信息判断,下列说法不正确的是
A.①③属于同种元素
B.②表示的元素常见化合价为+1价
C.硒元素的相对原子质量是34
D.③④为稳定结构
11.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
12.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
13.下列有关粒子的说法中正确的是
A.原子的原子核都是由质子和中子构成的 B.分子可分,而原子不可再分
C.原子可转化成离子,离子不能转化为原子 D.钠原子和钠离子核电荷数相同
14.2020年6月23日我国的北斗导航“收官之星”在西昌发射成功,北斗导航卫星系统采用铷原子钟提供精确时间,铷元素在元素周期表中的相关信息与铷原子的原子结构示意图如图所示。下列说法不正确的是
A.铷单质具有导电性
B.m的值是37,n的值是1
C.铷的相对原子质量为85.47
D.氯化铷的化学式为RbCl2
二、填空题
15.图甲是铝元素在元素周期表中的相关信息,图乙是几种微粒的结构示意图,仔细分析答题:
(1)图甲中,铝元素的信息有处错误,请加以改正_________;
(2)铝原子的相对原子质量_________ ;
(3)图乙中,属于稳定结构的原子是____ (填序号, 下同);
(4)图乙中,与铝不属于同一周期元素的是_________。
16.元素周期表是学习和研究化学的重要工具,元素周期表的一部分如下表,请根据下表回答有关问题。
(1)观察第2、3周期的元素,这两个周期开头的元素是______,结尾的元素是_______。(填“金属元素”“非金属元素"或“稀有气体元素”)
(2)磷原子的质子数是______,相对原子质量是_______。
(3)元素周期表中,同族元素的化学性质具有一定的相似性,同周期元素的化学性质具有一定的速变规律。
①同族元素的化学性质相似的原因是_______。
②同周期元素的原子的最外层电子数的变化规律是________。
17.化学用语是学习化学的重要工具。请用适当的化学符号填空。
(1)保持氦气化学性质的最小粒子______。
(2)地壳中含量最多的金属元素______。
(3)标出H2O中氢元素的化合价______。
(4)写出如图所示粒子的符号______。
(5)高铁酸钠由Na+和构成,则高铁酸钠的化学式为______。
18.元素周期表是学习化学的重要工具,下表为元素周期表中部分元素的相关信息,利用下表回答相关问题。
(1)原子序数为4的元素符号为________________________。
(2)C、N、O排在同一周期是因为_______________(填“质子数”“电子层数”或“最外层电子数”)相同。
(3)He和Mg的化学性质_____________(填“相似”或“不相似”)。
(4)钠离子核外电子排布与_____________(填元素符号)原子核外电子排布相同。
(5)一个磷原子含有____________个质子,一个含有____________个电子。
三、实验题
19.为探究分子的运动及影响分子运动速率的因素,某兴趣小组的同学设计了以下两种实验方案,请回答有关问题。
[实验一] 如图甲。
(1)观察到的实验现象是_____。
(2)实验一可以得出的结论是___________。
[实验二] 如图乙、图丙。图乙、图丙中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图丁的操作方式分别用注射器向图乙和图丙的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40 ℃的热水中。
(1)观察到的现象是__________________。
(2)实验中塑料瓶和纸花的大小、形状,浓氨水的滴数等实验条件需要保持相同,是因为对比实验中需要用到___法。
(3)实验二除可得出实验一的结论外,还可以得出的结论是_________。
20.如图的实验1、实验2两个实验是教材上册P63的探究微粒性质实验操作示意图。
①根据实验1中最后观察到的实验现象,说明__________。
②久置后的实验2中溶液变红的烧杯是_________,说明___________。
③根据上述实验现象判断下列说法中正确的是________。
A氨分子在不断运动
B浓氨水具有挥发性
C酚酞分子不运动
D酚酞分子运动慢
四、计算题
21.已知碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,铁原子的质量为9.288×10-26kg。请填空或进行计算:
(注:第2、3小问写出计算过程并对钠原子质量计算结果保留三位小数)
(1)钠原子核内有____________个中子。
(2)一个钠原子的质量为多少?
(3)铁原子的相对原子质量是多少?
22.若R原子的相对原子质量为23,核内质子数比中子数少一个,求
(1)R原子的中子数__________。
(2)该原子为_____________原子(填符号)
(3)画出该原子的离子结构示意图____________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.D
3.A
4.B
5.D
6.B
7.B
8.C
9.A
10.C
11.A
12.B
13.D
14.D
15. Al 26.98 AD A
16.(1) 金属元素 稀有气体元素
(2) 15 30.97
(3) 同族元素原子的最外层电子数相同 从左到右,最外层电子数依次递增
17.(1)He
(2)Al
(3)
(4)Mg2+
(5)Na2FeO4
18. Be 电子层数 不相似 Ne 15 10
19. 酚酞溶液变红 分子在不断运动 小纸花自下而上依次变红,且图丙中的纸花比图乙中的纸花更快变红 控制变量 温度越高,分子运动速率越快
20. 酚酞试液遇浓氨水变红 C 氨气分子运动 AB
21.(1)12
(2)解:设一个钠原子的质量为x。
由题可知:碳-12原子的质量是1.993×10-26kg,钠原子的相对原子质量为23,有:
钠原子的相对原子质量为,
x=3.820×10-26kg
答:一个钠原子的质量为3.820×10-26kg。
(3)解:铁原子的相对原子质量为
答:铁原子的相对原子质量为56。
22.(1)12
(2)Na
(3)
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
