2022-2023学年化学科粤版(2012) 第二章 空气、物质的构成 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学科粤版(2012) 第二章 空气、物质的构成 单元练习(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 141.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-08 00:00:00 | ||
图片预览




文档简介
2022-2023学年化学科粤版(2012)--空气、物质的构成
一、单选题
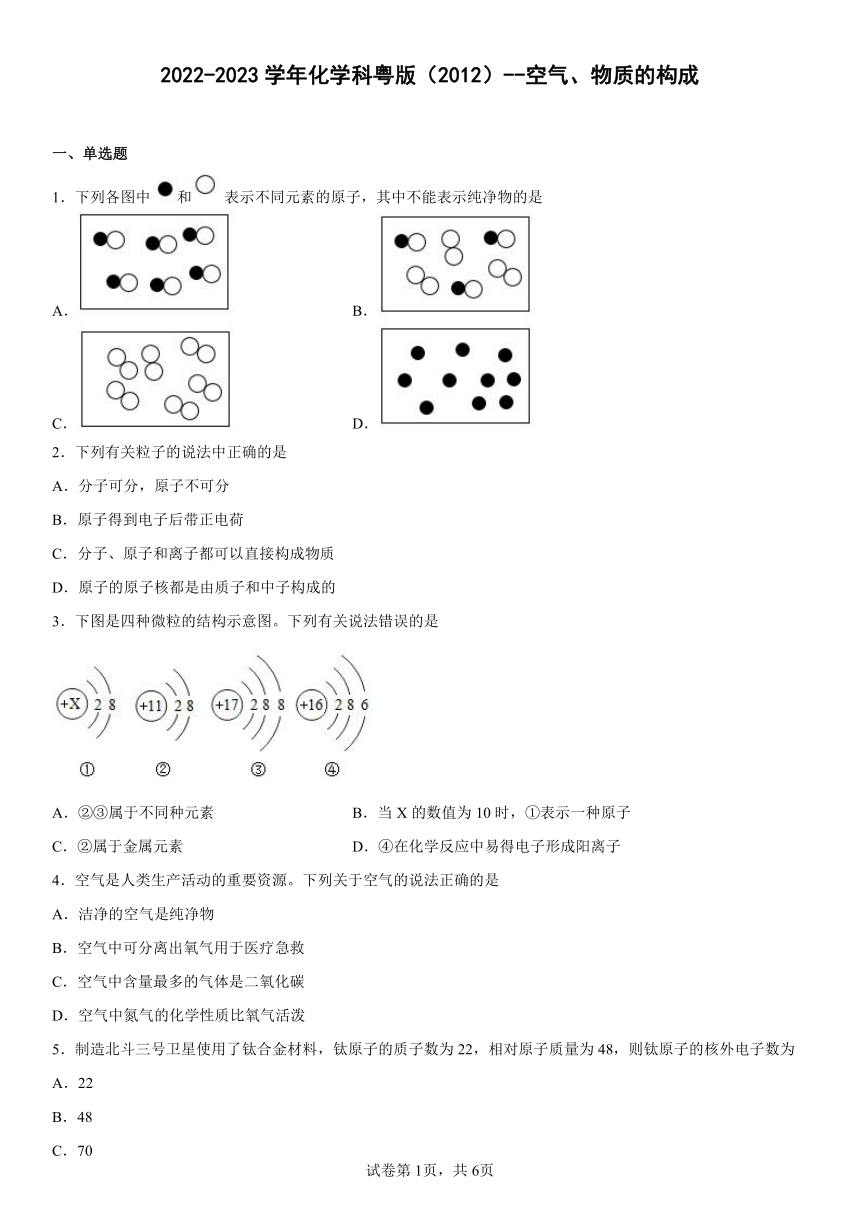
1.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
2.下列有关粒子的说法中正确的是
A.分子可分,原子不可分
B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质
D.原子的原子核都是由质子和中子构成的
3.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
4.空气是人类生产活动的重要资源。下列关于空气的说法正确的是
A.洁净的空气是纯净物
B.空气中可分离出氧气用于医疗急救
C.空气中含量最多的气体是二氧化碳
D.空气中氮气的化学性质比氧气活泼
5.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
6.已知碘原子的相对原子质量为127,其原子核内有74个中子,则碘原子核外的电子数为
A.74 B.53 C.54 D.72
7.下列关于空气的说法错误的是
A.空气是一种混合物
B.空气是一种宝贵的资源
C.稀有气体化学性质很不活泼,不与任何物质发生化学反应
D.空气中氧气的体积分数约为21%
8.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
9.下列事实的微观解释中,不正确的是
A.墙内开花墙外可闻到花香——分子在不断地运动
B.蔗糖放入水中溶解一一蔗糖分子分解了
C.氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
10.西岭雪山是著名旅游胜地,下列对其景色的微观解释错误的是
选项 景色 解释
A 春天花香四溢 分子在不断运动
B 夏天云消雾散 水分子间隔发生了变化
C 秋天层林尽染 分子种类不同性质不同
D 冬天白雪皑皑 水分子种类发生了变化
A.A B.B C.C D.D
11.氮化镓是生产5G芯片的关键材料之一、氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是
A.镓是金属元素
B.氮原子的核内质子数为7
C.镓元素的相对原子质量是69.72g
D.氮化镓中氮元素的化合价为-3价
12.用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是
A.集气瓶中产生大量白烟 B.红磷燃烧一段时间后熄灭
C.烧杯中的水倒吸进入集气瓶 D.集气瓶中水面最终上升至1处
13.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
14.空气是人类生产活动的重要资源。下列生活生产中用到的气体不是来自空气的是
A.炼钢过程用到的氧气
B.磁悬浮列车用到的氮气
C.用于生产氮肥的氨气
D.制作电光源的稀有气体
15.“加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是
A.单质 B.元素 C.金属 D.维生素
二、填空题
16.请写出下列物质的名称。
(1)应用于磁悬浮列车的气体是_______。
(2)拉瓦锡测定空气中氧气含量实验中红色固体_______。
(3)常用于制造霓虹灯的一类气体总称为________。
(4)写出一种污染大气的有害气体_________。
17.元素周期表是学习和研究化学的重要工具,元素周期表的一部分如下表,请根据下表回答有关问题。
(1)观察第2、3周期的元素,这两个周期开头的元素是______,结尾的元素是_______。(填“金属元素”“非金属元素"或“稀有气体元素”)
(2)磷原子的质子数是______,相对原子质量是_______。
(3)元素周期表中,同族元素的化学性质具有一定的相似性,同周期元素的化学性质具有一定的速变规律。
①同族元素的化学性质相似的原因是_______。
②同周期元素的原子的最外层电子数的变化规律是________。
18.多角度认识物质及其变化,能帮助我们更全面了解物质世界。
(1)图1为空气成分的示意图,物质B的化学式为 ___ 。
(2)利用红磷燃烧测定空气里物质B含量的实验装置如图2所示。红磷燃烧反应的化学方程式为 _____ ,该反应属于 _____ (填基本反应类型)。
19.元素周期表是学习化学的重要工具,下表是元素周期表的一部分,请回答下列问题:
(1)不同元素之间的最本质区别是____________不同;
(2)表中与氧元素化学性质相似的是___________元素;
(3)12号元素的原子在化学反应中比较容易__________(填“得到”或“失去”)电子;
(4)11-18号元素在表中处于同一周期的原因是它们原子结构中的__________ 相同。
20.根据下列粒子结构示意图,回答问题。
(1)A、B、C、D所示粒子共表示______________种元素(填数字)。
(2)D所示粒子在化学反应中容易_____________电子(填“得到”或“失去”) 。
(3)若E中x=10时,则该粒子属于____________(填“原子”或“离子”)。
三、实验题
21.为探究分子的运动及影响分子运动速率的因素,某兴趣小组的同学设计了以下两种实验方案,请回答下列问题:
实验1(如图1)。
(1)该实验能观察到的现象是______。
(2)该方案的不足之处是______(写出一点即可)。
实验2(如图2、图3、图4)。
图2、图3中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细铁丝固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)该实验观察到的现象是______。
(4)由此可得出的结论是______。
22.某化学兴趣活动小组为测定空气中氧气的含量,进行如下探究实验:
如图所示,在一个具有刻度和可以滑动的活塞的玻璃容器中放入一粒白磷(白磷燃烧所需的最低温度为40℃),将玻璃容器固定好,放在盛有85℃热水的烧杯上。请回答下列问题:
(1)实验中可以看到玻璃容器内白磷燃烧时的现象是(与红磷燃烧相似)___________,该反应的符号表达式____________。实验结束后,恢复至常温,活塞应停在刻度__________处,出现该现象的原因是:白磷燃烧消耗了空气中气态的__________而生成了固态的________,从而使玻璃容器内的气体体积__________(填“增大”、“减小”或“不变”)。
(2)玻璃容器内余下的气体主要是____________。
(3)此反应中白磷要过量,目的是___________。
四、计算题
23.已知碳12原子的质量为1.993×10-26kg,一种钛原子的质量为7.951×10-26kg,则钛原子的相对原子质量是_____(保留整数);钛原子的原子核外有22个电子,则其核内中子数为_____;镁原子的相对原子质量是24,则等质量的金属钛和金属镁含有原子的数目关系:钛_____镁(填“>”或“=”或“<”)。
24.已知一个X原子的质量为9.296×10-26 kg,一个碳12原子的质量为1.993×10-26 kg,又知X原子中的质子数比中子数少4。
求:(1)X原子的相对原子质量(结果保留整数)。
(2)X原子的电子数是多少。
25.(1)已知一个M原子的质量为a kg,一个碳12原子的质量为b kg,则M原子的相对原子质量为 (用a、b表示)。
(2)已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m g,计算该硫原子的质量。(写出计算过程)
(3)已知镁的相对原子质量为24,铝的相对原子质量为27,计算等质量的镁、铝中镁原子和铝原子的个数比。 试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.D
4.B
5.A
6.B
7.C
8.B
9.B
10.D
11.C
12.D
13.D
14.C
15.B
16.(1)氮气
(2)氧化汞
(3)稀有气体
(4)二氧化硫一氧化碳二氧化氮
17.(1) 金属元素 稀有气体元素
(2) 15 30.97
(3) 同族元素原子的最外层电子数相同 从左到右,最外层电子数依次递增
18. O2 化合反应
19. 质子数(或核电荷数) 硫(或S) 失去 电子层数
20. 3 得到 原子
21.(1)酚酞试液变红
(2)未做对比实验,证据不足(合理即可)
(3)小红花变红,且图3先变红
(4)分子做无规则运动,且温度越高分子运动速率越快
22.(1) 放热,产生大量白烟 4 氧气O2 五氧化二磷P2O5 减小
(2)氮气N2
(3)除尽装置中的氧气
23.(1)碳12原子中原子核内有6个质子,6个中子的质量为,一种钛原子的质量为,则该钛原子的相对原子质量为;
答:钛原子的相对原子质量是48。
(2)根据相对原子质量≈质子数+中子数,则钛原子中子数;
答:钛原子核内中子数为26。
(3)钛<镁。
24.(1)56 (2)26
25.(1) (2)2m g(3)9∶8
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列各图中和表示不同元素的原子,其中不能表示纯净物的是
A. B.
C. D.
2.下列有关粒子的说法中正确的是
A.分子可分,原子不可分
B.原子得到电子后带正电荷
C.分子、原子和离子都可以直接构成物质
D.原子的原子核都是由质子和中子构成的
3.下图是四种微粒的结构示意图。下列有关说法错误的是
A.②③属于不同种元素 B.当X的数值为10时,①表示一种原子
C.②属于金属元素 D.④在化学反应中易得电子形成阳离子
4.空气是人类生产活动的重要资源。下列关于空气的说法正确的是
A.洁净的空气是纯净物
B.空气中可分离出氧气用于医疗急救
C.空气中含量最多的气体是二氧化碳
D.空气中氮气的化学性质比氧气活泼
5.制造北斗三号卫星使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,则钛原子的核外电子数为
A.22
B.48
C.70
D.26
6.已知碘原子的相对原子质量为127,其原子核内有74个中子,则碘原子核外的电子数为
A.74 B.53 C.54 D.72
7.下列关于空气的说法错误的是
A.空气是一种混合物
B.空气是一种宝贵的资源
C.稀有气体化学性质很不活泼,不与任何物质发生化学反应
D.空气中氧气的体积分数约为21%
8.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
9.下列事实的微观解释中,不正确的是
A.墙内开花墙外可闻到花香——分子在不断地运动
B.蔗糖放入水中溶解一一蔗糖分子分解了
C.氧气和液氧都能支持燃烧——物质的分子相同,其化学性质相同
D.水壶中的水烧开沸腾后,壶盖被顶起——水分子间的间隔增大
10.西岭雪山是著名旅游胜地,下列对其景色的微观解释错误的是
选项 景色 解释
A 春天花香四溢 分子在不断运动
B 夏天云消雾散 水分子间隔发生了变化
C 秋天层林尽染 分子种类不同性质不同
D 冬天白雪皑皑 水分子种类发生了变化
A.A B.B C.C D.D
11.氮化镓是生产5G芯片的关键材料之一、氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是
A.镓是金属元素
B.氮原子的核内质子数为7
C.镓元素的相对原子质量是69.72g
D.氮化镓中氮元素的化合价为-3价
12.用下图装置可验证空气中O2的含量。下列现象能表明O2含量的是
A.集气瓶中产生大量白烟 B.红磷燃烧一段时间后熄灭
C.烧杯中的水倒吸进入集气瓶 D.集气瓶中水面最终上升至1处
13.科学家因锂离子电池发展的研究获诺贝尔化学奖。结合图示,有关锂的说法正确的是
A.属于非金属元素
B.相对原子质量是6.941g
C. 表示核内有3个电子
D.离子符号是Li+.
14.空气是人类生产活动的重要资源。下列生活生产中用到的气体不是来自空气的是
A.炼钢过程用到的氧气
B.磁悬浮列车用到的氮气
C.用于生产氮肥的氨气
D.制作电光源的稀有气体
15.“加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是
A.单质 B.元素 C.金属 D.维生素
二、填空题
16.请写出下列物质的名称。
(1)应用于磁悬浮列车的气体是_______。
(2)拉瓦锡测定空气中氧气含量实验中红色固体_______。
(3)常用于制造霓虹灯的一类气体总称为________。
(4)写出一种污染大气的有害气体_________。
17.元素周期表是学习和研究化学的重要工具,元素周期表的一部分如下表,请根据下表回答有关问题。
(1)观察第2、3周期的元素,这两个周期开头的元素是______,结尾的元素是_______。(填“金属元素”“非金属元素"或“稀有气体元素”)
(2)磷原子的质子数是______,相对原子质量是_______。
(3)元素周期表中,同族元素的化学性质具有一定的相似性,同周期元素的化学性质具有一定的速变规律。
①同族元素的化学性质相似的原因是_______。
②同周期元素的原子的最外层电子数的变化规律是________。
18.多角度认识物质及其变化,能帮助我们更全面了解物质世界。
(1)图1为空气成分的示意图,物质B的化学式为 ___ 。
(2)利用红磷燃烧测定空气里物质B含量的实验装置如图2所示。红磷燃烧反应的化学方程式为 _____ ,该反应属于 _____ (填基本反应类型)。
19.元素周期表是学习化学的重要工具,下表是元素周期表的一部分,请回答下列问题:
(1)不同元素之间的最本质区别是____________不同;
(2)表中与氧元素化学性质相似的是___________元素;
(3)12号元素的原子在化学反应中比较容易__________(填“得到”或“失去”)电子;
(4)11-18号元素在表中处于同一周期的原因是它们原子结构中的__________ 相同。
20.根据下列粒子结构示意图,回答问题。
(1)A、B、C、D所示粒子共表示______________种元素(填数字)。
(2)D所示粒子在化学反应中容易_____________电子(填“得到”或“失去”) 。
(3)若E中x=10时,则该粒子属于____________(填“原子”或“离子”)。
三、实验题
21.为探究分子的运动及影响分子运动速率的因素,某兴趣小组的同学设计了以下两种实验方案,请回答下列问题:
实验1(如图1)。
(1)该实验能观察到的现象是______。
(2)该方案的不足之处是______(写出一点即可)。
实验2(如图2、图3、图4)。
图2、图3中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细铁丝固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图4的操作方式分别用注射器向图2和图3的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
(3)该实验观察到的现象是______。
(4)由此可得出的结论是______。
22.某化学兴趣活动小组为测定空气中氧气的含量,进行如下探究实验:
如图所示,在一个具有刻度和可以滑动的活塞的玻璃容器中放入一粒白磷(白磷燃烧所需的最低温度为40℃),将玻璃容器固定好,放在盛有85℃热水的烧杯上。请回答下列问题:
(1)实验中可以看到玻璃容器内白磷燃烧时的现象是(与红磷燃烧相似)___________,该反应的符号表达式____________。实验结束后,恢复至常温,活塞应停在刻度__________处,出现该现象的原因是:白磷燃烧消耗了空气中气态的__________而生成了固态的________,从而使玻璃容器内的气体体积__________(填“增大”、“减小”或“不变”)。
(2)玻璃容器内余下的气体主要是____________。
(3)此反应中白磷要过量,目的是___________。
四、计算题
23.已知碳12原子的质量为1.993×10-26kg,一种钛原子的质量为7.951×10-26kg,则钛原子的相对原子质量是_____(保留整数);钛原子的原子核外有22个电子,则其核内中子数为_____;镁原子的相对原子质量是24,则等质量的金属钛和金属镁含有原子的数目关系:钛_____镁(填“>”或“=”或“<”)。
24.已知一个X原子的质量为9.296×10-26 kg,一个碳12原子的质量为1.993×10-26 kg,又知X原子中的质子数比中子数少4。
求:(1)X原子的相对原子质量(结果保留整数)。
(2)X原子的电子数是多少。
25.(1)已知一个M原子的质量为a kg,一个碳12原子的质量为b kg,则M原子的相对原子质量为 (用a、b表示)。
(2)已知某氧原子的相对原子质量为16,某硫原子的相对原子质量为32。如果该氧原子的质量为m g,计算该硫原子的质量。(写出计算过程)
(3)已知镁的相对原子质量为24,铝的相对原子质量为27,计算等质量的镁、铝中镁原子和铝原子的个数比。 试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.D
4.B
5.A
6.B
7.C
8.B
9.B
10.D
11.C
12.D
13.D
14.C
15.B
16.(1)氮气
(2)氧化汞
(3)稀有气体
(4)二氧化硫一氧化碳二氧化氮
17.(1) 金属元素 稀有气体元素
(2) 15 30.97
(3) 同族元素原子的最外层电子数相同 从左到右,最外层电子数依次递增
18. O2 化合反应
19. 质子数(或核电荷数) 硫(或S) 失去 电子层数
20. 3 得到 原子
21.(1)酚酞试液变红
(2)未做对比实验,证据不足(合理即可)
(3)小红花变红,且图3先变红
(4)分子做无规则运动,且温度越高分子运动速率越快
22.(1) 放热,产生大量白烟 4 氧气O2 五氧化二磷P2O5 减小
(2)氮气N2
(3)除尽装置中的氧气
23.(1)碳12原子中原子核内有6个质子,6个中子的质量为,一种钛原子的质量为,则该钛原子的相对原子质量为;
答:钛原子的相对原子质量是48。
(2)根据相对原子质量≈质子数+中子数,则钛原子中子数;
答:钛原子核内中子数为26。
(3)钛<镁。
24.(1)56 (2)26
25.(1) (2)2m g(3)9∶8
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
