2014届高一化学同步达标训练:《硫和氮的氧化物1》(新人教版必修1)
文档属性
| 名称 | 2014届高一化学同步达标训练:《硫和氮的氧化物1》(新人教版必修1) |  | |
| 格式 | zip | ||
| 文件大小 | 102.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-01-05 08:52:10 | ||
图片预览

文档简介
硫和氮的氧化物
一、选择题 (每小题有一个或两个选项)
1.下列元素在自然界中只能以化合态形式存在的是( )
A.N B.O C.Si D.S
2.原创题下列氧化物不是酸酐的是( ) A.N2O5 B.NO2 C.N2O3 D.SO2
3.下列关于NO的说法错误的是 ( )
A.NO是酸性氧化物 B.NO是汽车尾气的有害成分之一
C.NO可以在大气中稳定存在 D.NO能够与人体血红蛋白结合,造成人体缺氧中毒
4.一定物质的量的SO2与NaOH溶液反应,所得溶液中含Na2SO3和NaHSO3,若两者物质的量之比为3﹕5,则参加反应的SO2与NaOH的物质的量之比为( )
A.3﹕5 B.1﹕2 C.18﹕8 D.8﹕11
5.环保部门每天通过新闻媒体向社会发布以污染物浓度为标准确定的空气质量信息。在下列各种物质中,不属于空气质量指标的是( )[来源:学|科|网]
A.二氧化碳 B.氮氧化物 C.二氧化硫 D.悬浮颗粒
6.我国已经成功发射了“神舟”五号宇宙载人飞船。发射飞船的运载火箭,其推进剂引燃后发射剧烈反应,产生大量高温气体从火箭尾部喷出。引燃后的高温气体主要是CO2、H2O、N2、NO,这些气体均为无色,但在卫星发射现场看到火箭尾部喷出大量红色气体,产生红烟的原因是( )[来源:学科网ZXXK]
A.高温下,N2遇空气生成NO2 B.NO遇空气生成NO2
C.CO2与NO反应生成NO2 D.NO与H2O反应生成NO2
7.向倒扣在水槽中盛有NO的试管中缓慢通入35mLO2,反应完成后,若试管内的液面仍保持在原来的位置,则试管中原NO的体积是 ( )
A.20mL B.15mL C.10mL D.5mL
8.原创题实验室可用右图所示装置干燥、收集气体R,则R可能是 ( )
A.NO B.NO2 C.H2 D.Cl2
9.在常温常压下,下列各组气体不能共存的是( )[来源:学科网ZXXK]
A.SO2和O2 B.NO2和NO C.O2和N2 D.NO和O2
10.在NO2被水吸收的反应中,发生还原反应和氧化反应的物质的质量之比为( )
A.3?1 B.1?3 C.1?2 D.2?1
11.原创题下列有关NO2的说法正确的是( )[来源:学,科,网]
A.NO2溶于水生成硝酸,所以NO2是硝酸的酸酐 B.NO2既有氧化性又有还原性
C.NO2是N2与O2直接化合的产物 D.NO2可用向上排空气法收集
12.下列酸的酸酐中,不能由单质和氧气直接反应制得的是( )
A.HNO3 B.H2CO3 C.H2SO4 D.H2SO3
13.除去CO2中混有的少量SO2气体,最好选用的试剂是( )[来源:学科网]
A.澄清石灰水 B.品红溶液 C.溴水 D.饱和NaHCO3溶液
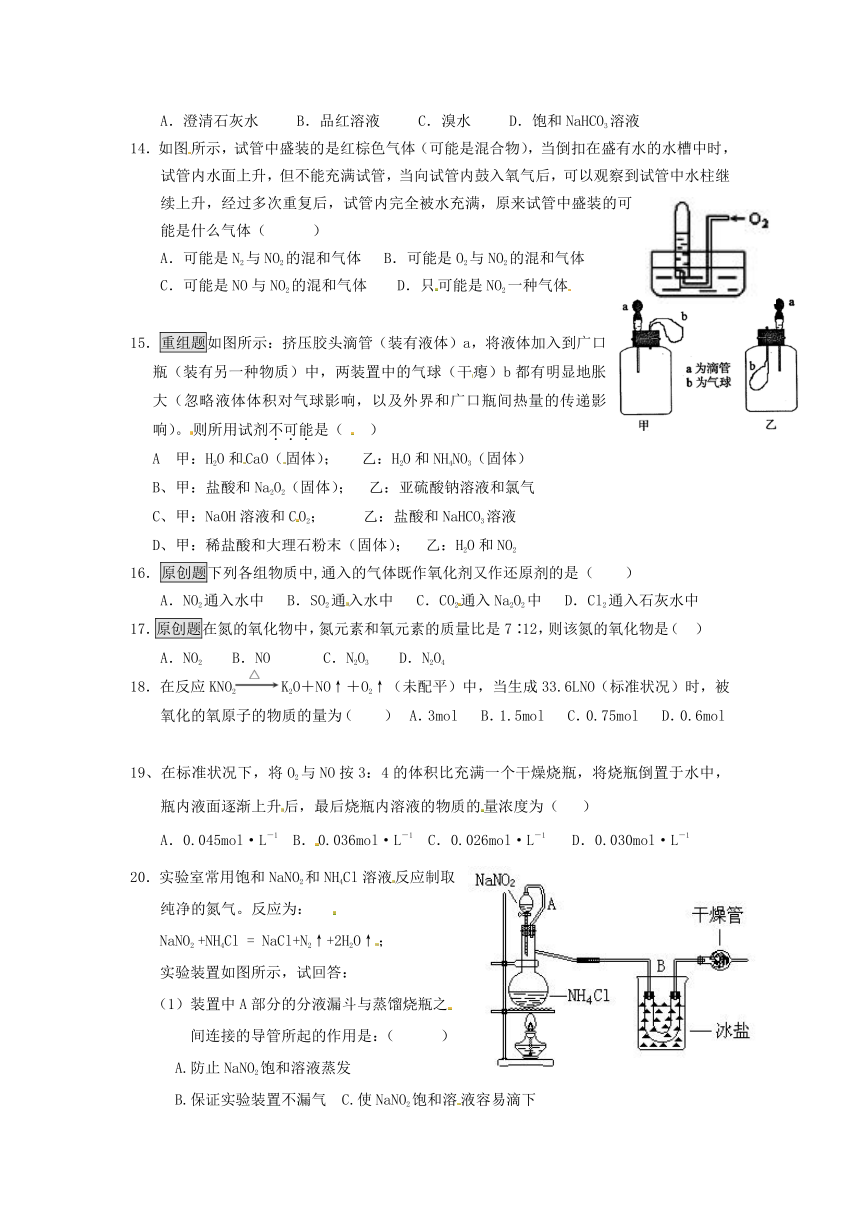
14.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
A.可能是N2与NO2的混和气体 B.可能是O2与NO2的混和气体
C.可能是NO与NO2的混和气体 D.只可能是NO2一种气体
[来源:学科网ZXXK]
15.重组题如图所示:挤压胶头滴管(装有液体)a,将液体加入到广口瓶(装有另一种物质)中,两装置中的气球(干瘪)b都有明显地胀大(忽略液体体积对气球影响,以及外界和广口瓶间热量的传递影响)。则所用试剂不可能是( )
A 甲:H2O和CaO(固体); 乙:H2O和NH4NO3(固体)
B、甲:盐酸和Na2O2(固体); 乙:亚硫酸钠溶液和氯气
C、甲:NaOH溶液和CO2; 乙:盐酸和NaHCO3溶液
D、甲:稀盐酸和大理石粉末(固体); 乙:H2O和NO2
16.原创题下列各组物质中,通入的气体既作氧化剂又作还原剂的是( )
A.NO2通入水中 B.SO2通入水中 C.CO2通入Na2O2中 D.Cl2通入石灰水中
17.原创题在氮的氧化物中,氮元素和氧元素的质量比是7∶12,则该氮的氧化物是( )
A.NO2 B.NO C.N2O3 D.N2O4
18.在反应KNO2K2O+NO↑+O2↑(未配平)中,当生成33.6LNO(标准状况)时,被氧化的氧原子的物质的量为( ) A.3mol B.1.5mol C.0.75mol D.0.6mol[来源:Z。xx。k.Com]
19、在标准状况下,将O2与NO按3:4的体积比充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升后,最后烧瓶内溶液的物质的量浓度为( )[来源:学,科,网Z,X,X,K]
A.0.045mol·L-1 B.0.036mol·L-1 C.0.026mol·L-1 D.0.030mol·L-1
20.实验室常用饱和NaNO2和NH4Cl溶液反应制取纯净的氮气。反应为:[来源:Z&xx&k.Com]
NaNO2 +NH4Cl = NaCl+N2↑+2H2O↑;
实验装置如图所示,试回答:
(1)装置中A部分的分液漏斗与蒸馏烧瓶之
间连接的导管所起的作用是:( )
A.防止NaNO2饱和溶液蒸发
B.保证实验装置不漏气 C.使NaNO2饱和溶液容易滴下
(2)B部分的作用是:( ) A.冷凝 B.冷却氮气 C.缓冲氮气流
(3) 加热前必须进行一个操作步骤是:____ _____;加热片刻后,即应移去酒精灯以防反应物冲出,其原因是:__________________________________________
(4)收集N2前必须进行的步骤是:____
收集N2最适宜的方法是( )
A.用排气法收集在集气瓶中 B.用排水法收集在集气瓶中 C.直接收集在球胆或塑料袋中
21.常温下A和B两种常见气体组成混和气体(A的分子量大于B),经分析,混和气体中,只含有氮氢两种元素,而且,不论A和B以何种比例混和,氮和氢的质量比总大于14:3,
(1)由此可确定A是 ,B是 ,[来源:Z_xx_k.Com]
(2)若上述混合气体中氮元素和氢元素的质量比为7:1,则在混合气体中A和B的物质的量之比为__ __;A在混合气体中的物质的量百分数为___ _。
22.X、Y、Z三种气体都是大气污染物,在工业上通常用碱液吸收。已知X是化石燃料燃烧的产物之一,是造成酸雨的主要物质;Y是一种单质,其水溶液具有漂白性;Z是硝酸工业和汽车尾气的有害物质之一,易溶于水。请写出下列有关反应的化学方程式。
(1)X在一定条件下与氧气反应;
(2)Y与消石灰反应
(3)Z溶于水 [来源:学&科&网]
23.NO分子因污染空气而臭名昭著。近年来发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO也被称为“明星分子”。回答以下问题:
(1)NO的危害在于( )
(A)破坏臭氧层(B)高温下使一些金属被氧化(C)造成酸雨(D)与人体血红蛋白结合
(2)在含有Cu+离子的酶的活性中心中,亚硝酸根离子(NO2-)可以转化为NO,写出两者在酸性环境下反应的离子方程式:
(3)在常温下把NO气体压缩到100个大气压,在一个体积固定的容器中加热到50℃,发现气体的压力迅速降低,压力降低到略小于原压力的2/3就不再发生变化,已知其中一种产物是N2O,写出上述反应的化学方程式: 。
(4)说明(3)中最后的气体的总压力小于原压力的2/3的原因是
24、已知室温下几种盐的溶解度由大到小的顺序是: NH4Cl > NaCl > NH4HCO3 > NaHCO3, 实验室利用它们在溶解度上的差异制取化工原料B, 其步骤如下:
已知:滤液中主要成分为NH4Cl 回答下列问题:
(1)晶体A的名称是 , 生成该晶体的化学方程式是 ;
(2)操作(Ⅰ)和(Ⅱ)的顺序不能颠倒的原因是 ; [来源:学.科.网]
(3)操作(Ⅲ)中使用玻璃棒的作用是 ;
(4)第Ⅳ步的化学反应方程式是 ;
(5)整个过程中没有涉及到的反应类型是( )[来源:Zxxk.Com]
A.化合反应 B.复分解反应 C.分解反应 D.置换反应[来源:学科网ZXXK]
答案:1C 2B 3AC 4D 5A 6B 7A 8C 9D 10C 11BD 12AC 13D 14BC 15C 16AD 17C 18C 19C [来源:学科网]
20、 (1) C (2) A (3)检查气密性 反应放热 (4)排尽空气 C
21、(1)N2,NH3 (2)1:4 ,20%
22(1)2SO2+O22SO3 (2)2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O
△
(3)3NO2+H2O2HNO3+NO
23.(1)ACD (2)Cu++NO2-+2H+=NO↑+ Cu2++H2O
(3)3NO=N2O+NO2 (4)有少量NO2转化为N2O4
24 (1)碳酸氢钠 NH3 + CO2 + NaCl + H 2O = NaHCO3( + NH4Cl
(2)CO2溶解度小, 溶解的量少, 产生的HCO3浓度小, 不利于NaHCO3结晶析出。
(3)引流。
(4)2NaHCO3Na 2CO3 + CO2( + H2O
(5)D
一、选择题 (每小题有一个或两个选项)
1.下列元素在自然界中只能以化合态形式存在的是( )
A.N B.O C.Si D.S
2.原创题下列氧化物不是酸酐的是( ) A.N2O5 B.NO2 C.N2O3 D.SO2
3.下列关于NO的说法错误的是 ( )
A.NO是酸性氧化物 B.NO是汽车尾气的有害成分之一
C.NO可以在大气中稳定存在 D.NO能够与人体血红蛋白结合,造成人体缺氧中毒
4.一定物质的量的SO2与NaOH溶液反应,所得溶液中含Na2SO3和NaHSO3,若两者物质的量之比为3﹕5,则参加反应的SO2与NaOH的物质的量之比为( )
A.3﹕5 B.1﹕2 C.18﹕8 D.8﹕11
5.环保部门每天通过新闻媒体向社会发布以污染物浓度为标准确定的空气质量信息。在下列各种物质中,不属于空气质量指标的是( )[来源:学|科|网]
A.二氧化碳 B.氮氧化物 C.二氧化硫 D.悬浮颗粒
6.我国已经成功发射了“神舟”五号宇宙载人飞船。发射飞船的运载火箭,其推进剂引燃后发射剧烈反应,产生大量高温气体从火箭尾部喷出。引燃后的高温气体主要是CO2、H2O、N2、NO,这些气体均为无色,但在卫星发射现场看到火箭尾部喷出大量红色气体,产生红烟的原因是( )[来源:学科网ZXXK]
A.高温下,N2遇空气生成NO2 B.NO遇空气生成NO2
C.CO2与NO反应生成NO2 D.NO与H2O反应生成NO2
7.向倒扣在水槽中盛有NO的试管中缓慢通入35mLO2,反应完成后,若试管内的液面仍保持在原来的位置,则试管中原NO的体积是 ( )
A.20mL B.15mL C.10mL D.5mL
8.原创题实验室可用右图所示装置干燥、收集气体R,则R可能是 ( )
A.NO B.NO2 C.H2 D.Cl2
9.在常温常压下,下列各组气体不能共存的是( )[来源:学科网ZXXK]
A.SO2和O2 B.NO2和NO C.O2和N2 D.NO和O2
10.在NO2被水吸收的反应中,发生还原反应和氧化反应的物质的质量之比为( )
A.3?1 B.1?3 C.1?2 D.2?1
11.原创题下列有关NO2的说法正确的是( )[来源:学,科,网]
A.NO2溶于水生成硝酸,所以NO2是硝酸的酸酐 B.NO2既有氧化性又有还原性
C.NO2是N2与O2直接化合的产物 D.NO2可用向上排空气法收集
12.下列酸的酸酐中,不能由单质和氧气直接反应制得的是( )
A.HNO3 B.H2CO3 C.H2SO4 D.H2SO3
13.除去CO2中混有的少量SO2气体,最好选用的试剂是( )[来源:学科网]
A.澄清石灰水 B.品红溶液 C.溴水 D.饱和NaHCO3溶液
14.如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中时,试管内水面上升,但不能充满试管,当向试管内鼓入氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的可能是什么气体( )
A.可能是N2与NO2的混和气体 B.可能是O2与NO2的混和气体
C.可能是NO与NO2的混和气体 D.只可能是NO2一种气体
[来源:学科网ZXXK]
15.重组题如图所示:挤压胶头滴管(装有液体)a,将液体加入到广口瓶(装有另一种物质)中,两装置中的气球(干瘪)b都有明显地胀大(忽略液体体积对气球影响,以及外界和广口瓶间热量的传递影响)。则所用试剂不可能是( )
A 甲:H2O和CaO(固体); 乙:H2O和NH4NO3(固体)
B、甲:盐酸和Na2O2(固体); 乙:亚硫酸钠溶液和氯气
C、甲:NaOH溶液和CO2; 乙:盐酸和NaHCO3溶液
D、甲:稀盐酸和大理石粉末(固体); 乙:H2O和NO2
16.原创题下列各组物质中,通入的气体既作氧化剂又作还原剂的是( )
A.NO2通入水中 B.SO2通入水中 C.CO2通入Na2O2中 D.Cl2通入石灰水中
17.原创题在氮的氧化物中,氮元素和氧元素的质量比是7∶12,则该氮的氧化物是( )
A.NO2 B.NO C.N2O3 D.N2O4
18.在反应KNO2K2O+NO↑+O2↑(未配平)中,当生成33.6LNO(标准状况)时,被氧化的氧原子的物质的量为( ) A.3mol B.1.5mol C.0.75mol D.0.6mol[来源:Z。xx。k.Com]
19、在标准状况下,将O2与NO按3:4的体积比充满一个干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升后,最后烧瓶内溶液的物质的量浓度为( )[来源:学,科,网Z,X,X,K]
A.0.045mol·L-1 B.0.036mol·L-1 C.0.026mol·L-1 D.0.030mol·L-1
20.实验室常用饱和NaNO2和NH4Cl溶液反应制取纯净的氮气。反应为:[来源:Z&xx&k.Com]
NaNO2 +NH4Cl = NaCl+N2↑+2H2O↑;
实验装置如图所示,试回答:
(1)装置中A部分的分液漏斗与蒸馏烧瓶之
间连接的导管所起的作用是:( )
A.防止NaNO2饱和溶液蒸发
B.保证实验装置不漏气 C.使NaNO2饱和溶液容易滴下
(2)B部分的作用是:( ) A.冷凝 B.冷却氮气 C.缓冲氮气流
(3) 加热前必须进行一个操作步骤是:____ _____;加热片刻后,即应移去酒精灯以防反应物冲出,其原因是:__________________________________________
(4)收集N2前必须进行的步骤是:____
收集N2最适宜的方法是( )
A.用排气法收集在集气瓶中 B.用排水法收集在集气瓶中 C.直接收集在球胆或塑料袋中
21.常温下A和B两种常见气体组成混和气体(A的分子量大于B),经分析,混和气体中,只含有氮氢两种元素,而且,不论A和B以何种比例混和,氮和氢的质量比总大于14:3,
(1)由此可确定A是 ,B是 ,[来源:Z_xx_k.Com]
(2)若上述混合气体中氮元素和氢元素的质量比为7:1,则在混合气体中A和B的物质的量之比为__ __;A在混合气体中的物质的量百分数为___ _。
22.X、Y、Z三种气体都是大气污染物,在工业上通常用碱液吸收。已知X是化石燃料燃烧的产物之一,是造成酸雨的主要物质;Y是一种单质,其水溶液具有漂白性;Z是硝酸工业和汽车尾气的有害物质之一,易溶于水。请写出下列有关反应的化学方程式。
(1)X在一定条件下与氧气反应;
(2)Y与消石灰反应
(3)Z溶于水 [来源:学&科&网]
23.NO分子因污染空气而臭名昭著。近年来发现少量的NO在生物体内许多组织中存在,它有扩张血管、免疫、增强记忆的功能,而成为当前生命科学的研究热点,NO也被称为“明星分子”。回答以下问题:
(1)NO的危害在于( )
(A)破坏臭氧层(B)高温下使一些金属被氧化(C)造成酸雨(D)与人体血红蛋白结合
(2)在含有Cu+离子的酶的活性中心中,亚硝酸根离子(NO2-)可以转化为NO,写出两者在酸性环境下反应的离子方程式:
(3)在常温下把NO气体压缩到100个大气压,在一个体积固定的容器中加热到50℃,发现气体的压力迅速降低,压力降低到略小于原压力的2/3就不再发生变化,已知其中一种产物是N2O,写出上述反应的化学方程式: 。
(4)说明(3)中最后的气体的总压力小于原压力的2/3的原因是
24、已知室温下几种盐的溶解度由大到小的顺序是: NH4Cl > NaCl > NH4HCO3 > NaHCO3, 实验室利用它们在溶解度上的差异制取化工原料B, 其步骤如下:
已知:滤液中主要成分为NH4Cl 回答下列问题:
(1)晶体A的名称是 , 生成该晶体的化学方程式是 ;
(2)操作(Ⅰ)和(Ⅱ)的顺序不能颠倒的原因是 ; [来源:学.科.网]
(3)操作(Ⅲ)中使用玻璃棒的作用是 ;
(4)第Ⅳ步的化学反应方程式是 ;
(5)整个过程中没有涉及到的反应类型是( )[来源:Zxxk.Com]
A.化合反应 B.复分解反应 C.分解反应 D.置换反应[来源:学科网ZXXK]
答案:1C 2B 3AC 4D 5A 6B 7A 8C 9D 10C 11BD 12AC 13D 14BC 15C 16AD 17C 18C 19C [来源:学科网]
20、 (1) C (2) A (3)检查气密性 反应放热 (4)排尽空气 C
21、(1)N2,NH3 (2)1:4 ,20%
22(1)2SO2+O22SO3 (2)2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O
△
(3)3NO2+H2O2HNO3+NO
23.(1)ACD (2)Cu++NO2-+2H+=NO↑+ Cu2++H2O
(3)3NO=N2O+NO2 (4)有少量NO2转化为N2O4
24 (1)碳酸氢钠 NH3 + CO2 + NaCl + H 2O = NaHCO3( + NH4Cl
(2)CO2溶解度小, 溶解的量少, 产生的HCO3浓度小, 不利于NaHCO3结晶析出。
(3)引流。
(4)2NaHCO3Na 2CO3 + CO2( + H2O
(5)D
