2022-2023学年化学京改版(2013) 第11章 酸与碱 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学京改版(2013) 第11章 酸与碱 单元练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 236.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-09 00:00:00 | ||
图片预览


文档简介
2022-2023学年化学京改版(2013)--酸与碱
一、单选题
1.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被蚁酸腐蚀的是
A.铜制塑像 B.镀锌水管 C.大理石栏杆 D.铝合金门窗
2.下列关于氢氧化钠的描述中不正确的是
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
3.下列现象从微观粒子的角度解释错误的是
选项 现象 解释
A 路过梨花园,闻到梨花香 分子在不停运动
B 100mL水与100mL酒精混合后体积小于200mL 分子之间有间隔
C 氢氧化钠溶液能导电 溶液中存在自由移动的钠离子、氢氧根离子
D 温度计水银球受热体积膨胀 温度升高汞原子体积变大
A.A B.B C.C D.D
4.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
5.下列常用来改良酸性土壤的物质是
A.熟石灰
B.硫酸
C.烧碱
D.食盐
6.下列关于Ca(OH)2的说法错误的是
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
7.向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,符合题意的是
A.X是水,Y是氧化钙
B.X是水,Y是氢氧化钠
C.X是水,Y是硝酸铵
D.X是水,Y是氯化钠
8.下列能使紫色石蕊试液和无色酚酞试液均变色的是
A.pH=1的盐酸
B.pH=3的硫酸
C.pH=7的氯化钠溶液
D.pH=14的氢氧化钾溶液
9.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
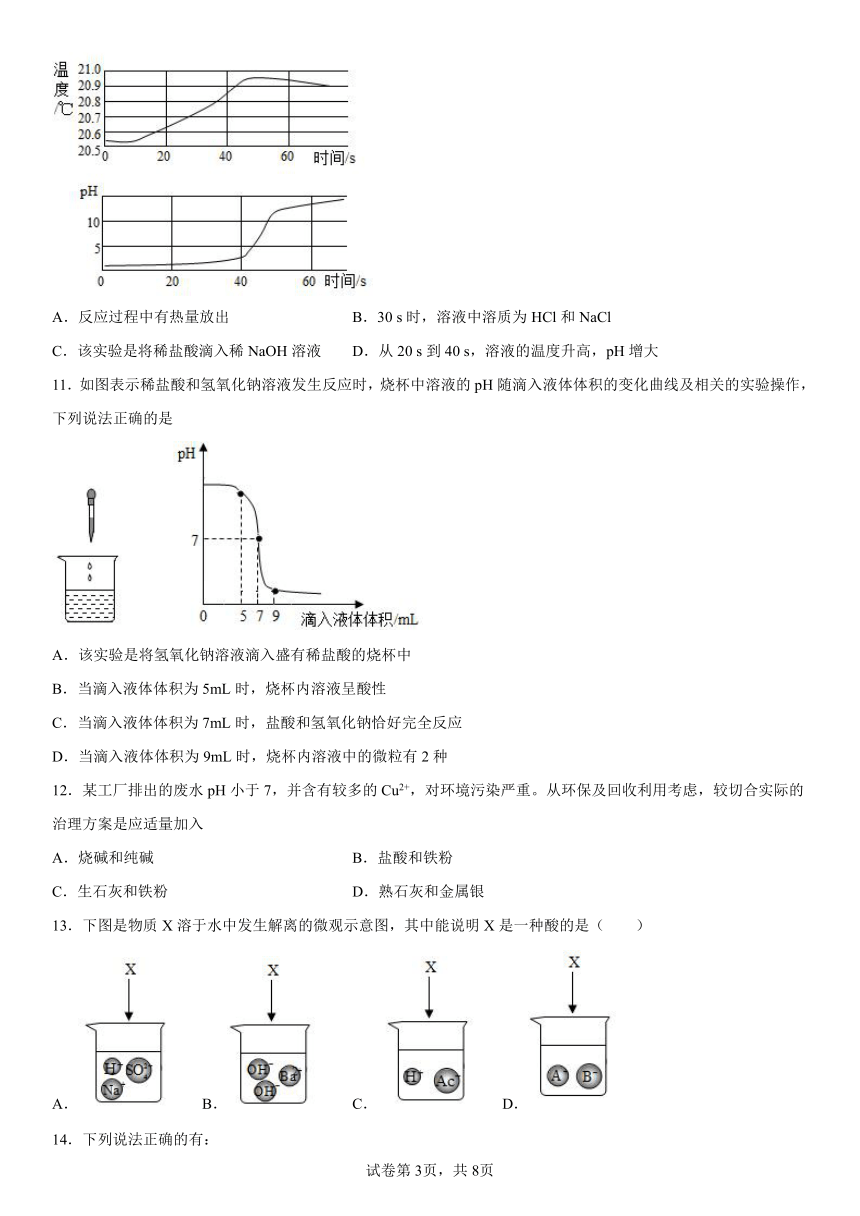
10.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是
A.反应过程中有热量放出 B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液 D.从20 s到40 s,溶液的温度升高,pH增大
11.如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是
A.该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中
B.当滴入液体体积为5mL时,烧杯内溶液呈酸性
C.当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应
D.当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种
12.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
13.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A. B. C. D.
14.下列说法正确的有:
①中和反应生成盐和水,则有盐和水生成的反应一定是中和反应
②化合物由两种及两种以上的元素组成,则由两种及两种元素以上组成的物质一定是化合物
③可燃性气体与空气混合点燃易爆炸,所以点燃可燃性气体前一定要验纯
④活泼金属与酸反应有气体产生,与酸反应产生气体的一定是活泼金属
⑤等质量的锌粉和铁粉分别与两份完全相同的稀硫酸反应,产生氢气的量相同时,铁粉一定有剩余
⑥稀有气体做电光源是因为它们的化学性质稳定
A.2 个 B.3 个 C.4 个 D.5 个
15.化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
二、填空题
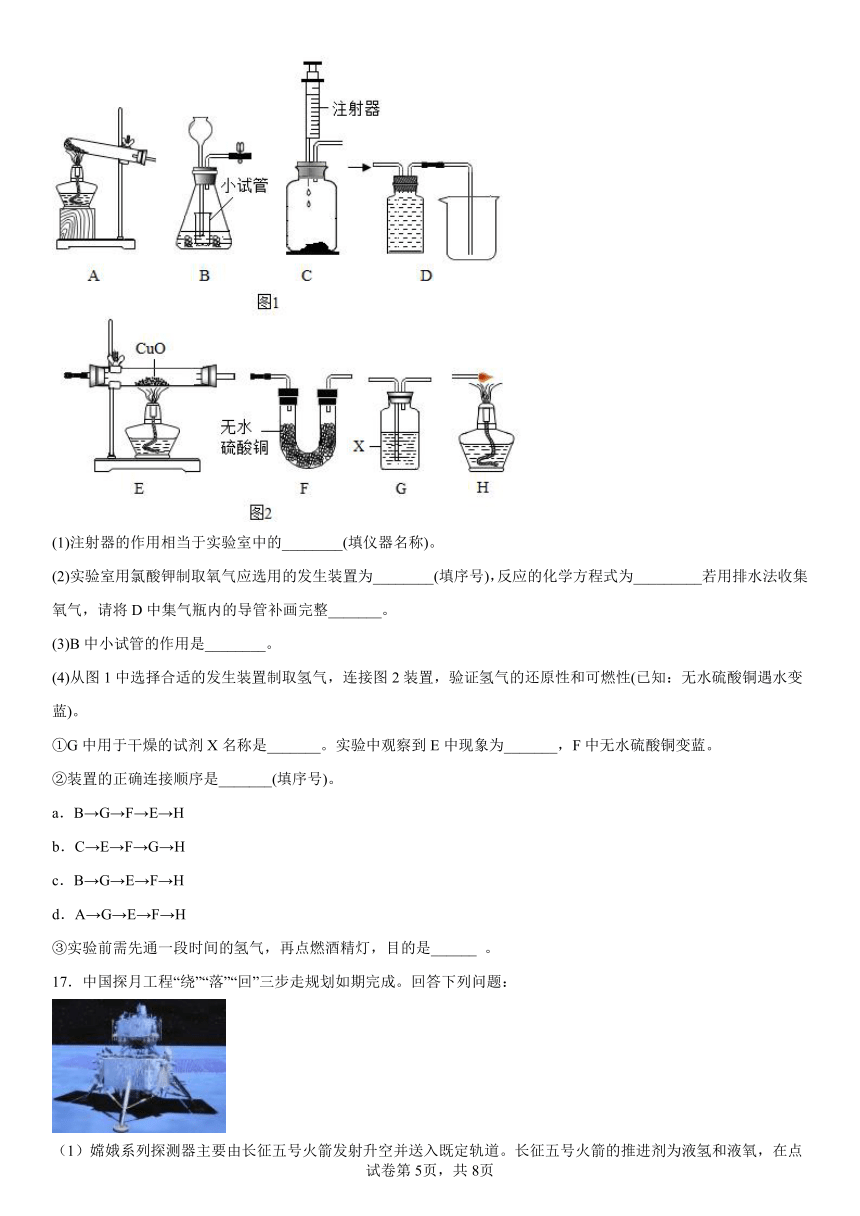
16.图1是某实验小组组装的实验室制取气体的装置,请回答下列问题。
(1)注射器的作用相当于实验室中的________(填仪器名称)。
(2)实验室用氯酸钾制取氧气应选用的发生装置为________(填序号),反应的化学方程式为_________若用排水法收集氧气,请将D中集气瓶内的导管补画完整_______。
(3)B中小试管的作用是________。
(4)从图1中选择合适的发生装置制取氢气,连接图2装置,验证氢气的还原性和可燃性(已知:无水硫酸铜遇水变蓝)。
①G中用于干燥的试剂X名称是_______。实验中观察到E中现象为_______,F中无水硫酸铜变蓝。
②装置的正确连接顺序是_______(填序号)。
a.B→G→F→E→H
b.C→E→F→G→H
c.B→G→E→F→H
d.A→G→E→F→H
③实验前需先通一段时间的氢气,再点燃酒精灯,目的是______ 。
17.中国探月工程“绕”“落”“回”三步走规划如期完成。回答下列问题:
(1)嫦娥系列探测器主要由长征五号火箭发射升空并送入既定轨道。长征五号火箭的推进剂为液氢和液氧,在点燃条件下两者发生反应的化学方程式______;嫦娥四号的月球车靠太阳能从月夜中唤醒,下列能源中,与太阳能一样属于新能源的是______。
A风能 B潮汐能 C化石燃料
(2)月球上有丰富的He-3,He-3的核能开发,被认为是解决未来世界能源、环境等问题的主要途径之一。已知He-3原子核内有2个质子1个中子,则He-3原子结构示意图为______。
A B
C D
(3)2020年12月17日,嫦娥五号携带月壤样品成功返回地球。月球岩石中橄榄石主要成分为:Mg2SiO4和Fe2SiO4,其中属于金属元素的有______(填元素名称),Fe2SiO4中带点元素化合价为______。
(4)嫦娥工程下一步是载人登月,宇航员在太空中都是在密闭容器内用生石灰与水反应给食物加热,该反应的化学方程式是______,写出生石灰的另一种用途______。
18.如图为某中和反应的示意图。图中的阴离子符号为_____________;写出一个符合如图反应的化学方程式____________;若将酸滴入加有酚酞的碱溶液中,至恰好中和时溶液由红色变为_____________;
19.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是_______________ 。
(2)在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是_____________________________。
②下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
____,____,____。
③下列金属中能与盐酸发生类似反应的是____(填选项)。
A.Cu B.Mg C.Al D.Ag
20.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
n(H+)与n(OH-)的相对大小 溶液的酸碱性
n(H+)>n(OH-) 酸性
n(H+)=n(OH-) 中性
n(H+)<n(OH-) 碱性
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)______n(OH-)(填“>”或“=”或“<”,下同)。
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是____________,原因是该溶液中n(H+)______n(OH-)。
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)______n(OH-)。
三、推断题
21.A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系。请回答:
(1)反应①的基本反应类型是______。
(2)写出反应②的化学方程式______。
(3)E的化学式是______,产生无色气体E的原因是______。
(4)金属C在______的条件下容易生锈;保护金属资源的有效途径是______(只写一条)。
四、流程题
22.铝在地壳中主要以铝土矿的形式存在,铝土矿的主要成分为A12O3(含有少量Fe2O3、SiO2等杂质)。工业上冶炼铝的工艺流程见图:
(1)铝土矿中的SiO2不溶于水,也不与盐酸反应,操作①的目的是______。
(2)操作③得到的 受热分解生成Al2O3,该反应的化学方程式为______,铝土矿经过操作①~④的目的是______。
(3)在冰晶石作助熔剂条件下,高温电解A12O3得到金属铝,该反应的化学方程式为______。
五、计算题
23.某造纸厂在造纸过程中会产生含氢氧化钠的废水,需经处理至中性后才能排放。现有5%的稀盐酸365kg。能处理废水中氢氧化钠的质量是______?
24.常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈_______色
(2)计算稀盐酸中溶质质量分数?试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.D
5.A
6.B
7.C
8.D
9.D
10.C
11.C
12.C
13.C
14.A
15.C
16.(1)分液漏斗
(2) A 2KClO32KCl+3O2↑
(3)形成液封,防止生成的气体从漏斗口逸出
(4) 浓硫酸 黑色粉末变红 c
排尽装置内的空气,防止爆炸
17. AB D 镁元素、铁元素 +2 作干燥剂
18. C1-、 OH- 无色
19. 分子之间的间隔 固体逐渐减少,溶液由无色变为浅绿色,有气泡产生 H+ Cl- Fe2+ B、C
20. = 溶液变红 < >
21. 化合反应 H2 铁与过量稀硫酸反应产生氢气(或反应②中稀硫酸过量) 潮湿的空气中(或与空气和水同时接触) 防止金属腐蚀(或回收利用废旧金属、合理有效地开采矿物、寻找金属的代用品等)
22. 除去SiO2 得到纯净的Al2O3
23.解:设废水中氢氧化钠的质量为x
x=20kg
答:能处理废水中氢氧化钠的质量是20kg。
24.(1)无
(2) 稀盐酸中溶质质量分数为3.65%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易被蚁酸腐蚀的是
A.铜制塑像 B.镀锌水管 C.大理石栏杆 D.铝合金门窗
2.下列关于氢氧化钠的描述中不正确的是
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
3.下列现象从微观粒子的角度解释错误的是
选项 现象 解释
A 路过梨花园,闻到梨花香 分子在不停运动
B 100mL水与100mL酒精混合后体积小于200mL 分子之间有间隔
C 氢氧化钠溶液能导电 溶液中存在自由移动的钠离子、氢氧根离子
D 温度计水银球受热体积膨胀 温度升高汞原子体积变大
A.A B.B C.C D.D
4.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
5.下列常用来改良酸性土壤的物质是
A.熟石灰
B.硫酸
C.烧碱
D.食盐
6.下列关于Ca(OH)2的说法错误的是
A.微溶于水,水溶液呈碱性
B.能与酸反应,可用于治疗胃酸过多
C.与CuSO4溶液按一定比例混合,可配制波尔多液
D.澄清溶液可用来检验CO2
7.向液体X中加入固体Y,观察到U形管内红墨水左侧液面上升。下列液体X和固体Y的组合,符合题意的是
A.X是水,Y是氧化钙
B.X是水,Y是氢氧化钠
C.X是水,Y是硝酸铵
D.X是水,Y是氯化钠
8.下列能使紫色石蕊试液和无色酚酞试液均变色的是
A.pH=1的盐酸
B.pH=3的硫酸
C.pH=7的氯化钠溶液
D.pH=14的氢氧化钾溶液
9.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
10.实验小组用传感器探究稀NaOH溶液与稀盐酸反应过程中温度和pH的变化。测定结果如图所示,下列说法不正确的是
A.反应过程中有热量放出 B.30 s时,溶液中溶质为HCl和NaCl
C.该实验是将稀盐酸滴入稀NaOH溶液 D.从20 s到40 s,溶液的温度升高,pH增大
11.如图表示稀盐酸和氢氧化钠溶液发生反应时,烧杯中溶液的pH随滴入液体体积的变化曲线及相关的实验操作,下列说法正确的是
A.该实验是将氢氧化钠溶液滴入盛有稀盐酸的烧杯中
B.当滴入液体体积为5mL时,烧杯内溶液呈酸性
C.当滴入液体体积为7mL时,盐酸和氢氧化钠恰好完全反应
D.当滴入液体体积为9mL时,烧杯内溶液中的微粒有2种
12.某工厂排出的废水pH小于7,并含有较多的Cu2+,对环境污染严重。从环保及回收利用考虑,较切合实际的治理方案是应适量加入
A.烧碱和纯碱 B.盐酸和铁粉
C.生石灰和铁粉 D.熟石灰和金属银
13.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A. B. C. D.
14.下列说法正确的有:
①中和反应生成盐和水,则有盐和水生成的反应一定是中和反应
②化合物由两种及两种以上的元素组成,则由两种及两种元素以上组成的物质一定是化合物
③可燃性气体与空气混合点燃易爆炸,所以点燃可燃性气体前一定要验纯
④活泼金属与酸反应有气体产生,与酸反应产生气体的一定是活泼金属
⑤等质量的锌粉和铁粉分别与两份完全相同的稀硫酸反应,产生氢气的量相同时,铁粉一定有剩余
⑥稀有气体做电光源是因为它们的化学性质稳定
A.2 个 B.3 个 C.4 个 D.5 个
15.化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
二、填空题
16.图1是某实验小组组装的实验室制取气体的装置,请回答下列问题。
(1)注射器的作用相当于实验室中的________(填仪器名称)。
(2)实验室用氯酸钾制取氧气应选用的发生装置为________(填序号),反应的化学方程式为_________若用排水法收集氧气,请将D中集气瓶内的导管补画完整_______。
(3)B中小试管的作用是________。
(4)从图1中选择合适的发生装置制取氢气,连接图2装置,验证氢气的还原性和可燃性(已知:无水硫酸铜遇水变蓝)。
①G中用于干燥的试剂X名称是_______。实验中观察到E中现象为_______,F中无水硫酸铜变蓝。
②装置的正确连接顺序是_______(填序号)。
a.B→G→F→E→H
b.C→E→F→G→H
c.B→G→E→F→H
d.A→G→E→F→H
③实验前需先通一段时间的氢气,再点燃酒精灯,目的是______ 。
17.中国探月工程“绕”“落”“回”三步走规划如期完成。回答下列问题:
(1)嫦娥系列探测器主要由长征五号火箭发射升空并送入既定轨道。长征五号火箭的推进剂为液氢和液氧,在点燃条件下两者发生反应的化学方程式______;嫦娥四号的月球车靠太阳能从月夜中唤醒,下列能源中,与太阳能一样属于新能源的是______。
A风能 B潮汐能 C化石燃料
(2)月球上有丰富的He-3,He-3的核能开发,被认为是解决未来世界能源、环境等问题的主要途径之一。已知He-3原子核内有2个质子1个中子,则He-3原子结构示意图为______。
A B
C D
(3)2020年12月17日,嫦娥五号携带月壤样品成功返回地球。月球岩石中橄榄石主要成分为:Mg2SiO4和Fe2SiO4,其中属于金属元素的有______(填元素名称),Fe2SiO4中带点元素化合价为______。
(4)嫦娥工程下一步是载人登月,宇航员在太空中都是在密闭容器内用生石灰与水反应给食物加热,该反应的化学方程式是______,写出生石灰的另一种用途______。
18.如图为某中和反应的示意图。图中的阴离子符号为_____________;写出一个符合如图反应的化学方程式____________;若将酸滴入加有酚酞的碱溶液中,至恰好中和时溶液由红色变为_____________;
19.盐酸是一种重要的化工产品,也是实验室中重要的化学试剂。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是_______________ 。
(2)在盐酸中加入过量的铁粉充分反应。
①可以看到的现象是_____________________________。
②下图表示该反应前后溶液中存在的主要离子,请写出每种图形代表的离子(填离子符号):
____,____,____。
③下列金属中能与盐酸发生类似反应的是____(填选项)。
A.Cu B.Mg C.Al D.Ag
20.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
n(H+)与n(OH-)的相对大小 溶液的酸碱性
n(H+)>n(OH-) 酸性
n(H+)=n(OH-) 中性
n(H+)<n(OH-) 碱性
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)______n(OH-)(填“>”或“=”或“<”,下同)。
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是____________,原因是该溶液中n(H+)______n(OH-)。
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)______n(OH-)。
三、推断题
21.A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系。请回答:
(1)反应①的基本反应类型是______。
(2)写出反应②的化学方程式______。
(3)E的化学式是______,产生无色气体E的原因是______。
(4)金属C在______的条件下容易生锈;保护金属资源的有效途径是______(只写一条)。
四、流程题
22.铝在地壳中主要以铝土矿的形式存在,铝土矿的主要成分为A12O3(含有少量Fe2O3、SiO2等杂质)。工业上冶炼铝的工艺流程见图:
(1)铝土矿中的SiO2不溶于水,也不与盐酸反应,操作①的目的是______。
(2)操作③得到的 受热分解生成Al2O3,该反应的化学方程式为______,铝土矿经过操作①~④的目的是______。
(3)在冰晶石作助熔剂条件下,高温电解A12O3得到金属铝,该反应的化学方程式为______。
五、计算题
23.某造纸厂在造纸过程中会产生含氢氧化钠的废水,需经处理至中性后才能排放。现有5%的稀盐酸365kg。能处理废水中氢氧化钠的质量是______?
24.常温下,一锥形瓶中盛有10g溶质质量分数为4%的氢氧化钠溶液,先向其中滴加2滴酚酞试液,再逐滴滴加一定溶质质量分数的稀盐酸,用pH传感器测得溶液pH与加入稀盐酸的关系曲线如图所示,请回答下列问题:
(1)图中B点溶液呈_______色
(2)计算稀盐酸中溶质质量分数?试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.C
3.D
4.D
5.A
6.B
7.C
8.D
9.D
10.C
11.C
12.C
13.C
14.A
15.C
16.(1)分液漏斗
(2) A 2KClO32KCl+3O2↑
(3)形成液封,防止生成的气体从漏斗口逸出
(4) 浓硫酸 黑色粉末变红 c
排尽装置内的空气,防止爆炸
17. AB D 镁元素、铁元素 +2 作干燥剂
18. C1-、 OH- 无色
19. 分子之间的间隔 固体逐渐减少,溶液由无色变为浅绿色,有气泡产生 H+ Cl- Fe2+ B、C
20. = 溶液变红 < >
21. 化合反应 H2 铁与过量稀硫酸反应产生氢气(或反应②中稀硫酸过量) 潮湿的空气中(或与空气和水同时接触) 防止金属腐蚀(或回收利用废旧金属、合理有效地开采矿物、寻找金属的代用品等)
22. 除去SiO2 得到纯净的Al2O3
23.解:设废水中氢氧化钠的质量为x
x=20kg
答:能处理废水中氢氧化钠的质量是20kg。
24.(1)无
(2) 稀盐酸中溶质质量分数为3.65%。
答案第1页,共2页
答案第1页,共2页
