2022-2023学年化学京改版(2013)第8章 碳的世界 单元练习(含答案)
文档属性
| 名称 | 2022-2023学年化学京改版(2013)第8章 碳的世界 单元练习(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 114.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-09 00:00:00 | ||
图片预览




文档简介
2022-2023学年化学京改版(2013)--碳的世界
一、单选题
1.下列关于碳及其化合物的说法正确的是
A.金刚石、石墨和C60的性质相似
B.木炭在氧气中燃烧,生成物一定是二氧化碳
C.CO2灭火既利用了CO2的物理性质,又利用了其化学性质
D.在煤炉上放一壶水能防止一氧化碳中毒
2.石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
3.关于二氧化碳的用途,下列说法错误的是
A.灭火 B.生产汽水 C.气体肥料 D.供给呼吸
4.“碳家族”的成员很多,用途很广。下列说法正确的是
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
5.成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
6.“碳达峰、碳中和”是近期频繁出现的热词。关于碳循环和氧循环,下列说法不正确的是
A.碳循环和氧循环过程中均发生了化学变化
B.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环分别是指二氧化碳和氧气的循环
7.下列有关碳及其氧化物的说法正确的是
A.CO2是引起温室效应的主要气体,因此大气中CO2的含量越少越好
B.碳的单质有多种,用途各不相同,是因为它们的物理性质各不相同
C.CO具有可燃性,在空气中燃烧产生黄色火焰
D.焦炭在工业上用于冶炼金属,在反应中表现出氧化性
8.下列与碳和碳的氧化物有关的说法中,正确的是
A.煤炉上放一盆水可防止CO中毒
B.CO2能使紫色石蕊溶液变红,说明CO2显酸性
C.CO和CO2化学性质不同的原因是分子构成不同
D.用墨绘制的古画经久不变色,说明碳不与任何物质反应
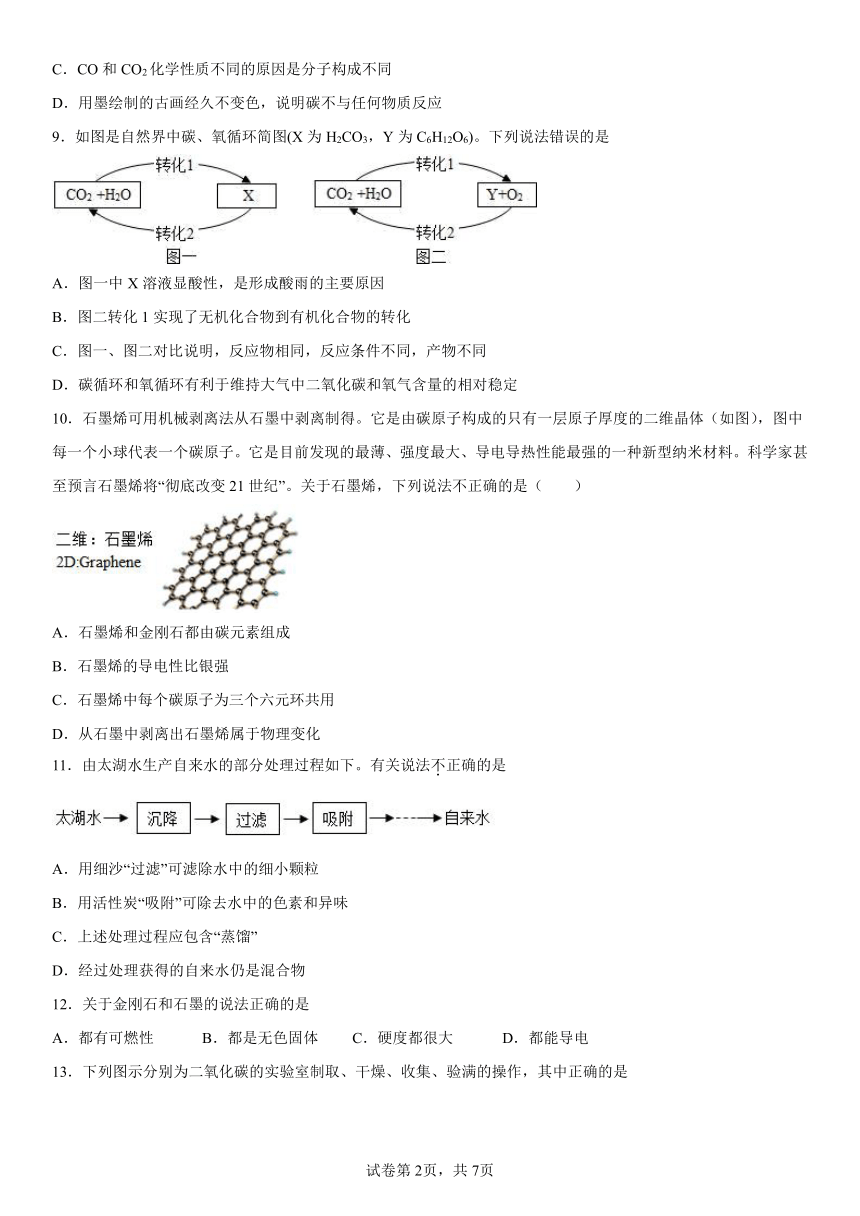
9.如图是自然界中碳、氧循环简图(X为H2CO3,Y为C6H12O6)。下列说法错误的是
A.图一中X溶液显酸性,是形成酸雨的主要原因
B.图二转化1实现了无机化合物到有机化合物的转化
C.图一、图二对比说明,反应物相同,反应条件不同,产物不同
D.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
10.石墨烯可用机械剥离法从石墨中剥离制得。它是由碳原子构成的只有一层原子厚度的二维晶体(如图),图中每一个小球代表一个碳原子。它是目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料。科学家甚至预言石墨烯将“彻底改变21世纪”。关于石墨烯,下列说法不正确的是( )
A.石墨烯和金刚石都由碳元素组成
B.石墨烯的导电性比银强
C.石墨烯中每个碳原子为三个六元环共用
D.从石墨中剥离出石墨烯属于物理变化
11.由太湖水生产自来水的部分处理过程如下。有关说法不正确的是
A.用细沙“过滤”可滤除水中的细小颗粒
B.用活性炭“吸附”可除去水中的色素和异味
C.上述处理过程应包含“蒸馏”
D.经过处理获得的自来水仍是混合物
12.关于金刚石和石墨的说法正确的是
A.都有可燃性 B.都是无色固体 C.硬度都很大 D.都能导电
13.下列图示分别为二氧化碳的实验室制取、干燥、收集、验满的操作,其中正确的是
A.制取 B.干燥
C.收集 D.验满
14.坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
二、填空题
15.碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ.碳的多样性
(1)金刚石和C60的化学性质相似,但物理性质却存在着很大差异。原因是__________。
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_________(填“单质”或“化合物”)。
Ⅱ.“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。
(3)CO2的过度排放会造成_________的加剧。结合生活实际,列举可为实现“碳中和”做出直接贡献的一种措施:___________。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。
①NaOH吸收。NaOH溶液吸收CO2生成 NaHCO3的化学方程式为_______________。
②CaO吸收。CaC2O4在高温下分解制得疏松多孔的CaO,同时产生CO、CO2。该反应所得CO、CO2的分子个数之比为________。
(5)CO2与H2在一定条件下转化为CH4(反应过程如图所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中,除CH4外另一种生成物为__________(填化学式),MgO的作用是_________。
②天然气(主要成分为CH4)已成为居民的生活用气,是因为CH4在空气中燃烧时______(填“吸收”或“放出”)热量。
16.请你结合所学的化学知识回答下列问题:
①请选择合适物质的编号填空:A一氧化碳;B活性炭;C氢气;D氦气;E二氧化硫。与酸雨形成有关的是_____;可用于防毒面具的是_____;可充入霓虹灯内且通电时会发出有色光的是_____;
② 固定和利用二氧化碳能有效减少空气中的温室气体。例如,工业上利用CO2和NH3生产尿素,反应的化学方程式为CO2+2NH3CO(NH2)2+X,则X的化学式为_____。
17.近五年来,我国在科技、文化、环境等方面创新发展。
I.大国重器——航天、航空取得重大突破
2018年4月2日,天宫一号目标飞行器圆满完成各项任务返回大气层。这标志着我国航天、航空事业进入了新时代。
(1)硅是天宮一号动力源太阳能电池的主要构成材料。单质硅是由石英(SiO2)固体与碳在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为__________。
(2)硅是计算机芯片的基体材料,但其导热性不好,而金刚石在导热性方面远超过硅,于是它成了芯片基体材料的最佳选择。
①从原子结构上分析,金刚石(C)和硅有相似化学性质的原因是_____________________。
②因天然金刚石资源稀少,难以满足要求。人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷(CH4)等为原料制造金刚石薄膜。
下列说法不正确的是_________(写字母序号)。
A一种元素可以组成多种性质不同的单质
B石墨合成金刚石发生的是物理变化
C石墨与金刚石物理性质不同是因为原子的结构不同
D物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
③不仅硅与碳具有相似化学性质,其氧化物二氧化硅和二氧化碳也有相似化学性质。试写出二氧化碳与氢氧化钙溶液反应的化学方程式____。
18.化学用语是学习化学的基本工具,请用正确的化学用语填空:
(1)氧化铁________。
(2)温室效应的主要气体________。
(3)氯化镁中的阳离子是_________。
(4)2个氮原子________。
19.物质世界离不开化学,把下列符合题意物质的序号写在横线上:
①二氧化碳②二氧化硫③氮气④氧气⑤四氧化三铁⑥稀有气体
(1)黑色固体物质有_____;
(2)能供给呼吸支持燃烧的物质是_____;
(3)有刺激性气味且对空气构成污染的气体是_____;
(4)通常用作保护气和通电时发出有色光的是_____;
(5)能使澄清石灰水变浑浊且参与植物光合作用的是_____。
三、推断题
20.已知A、B、C是初中化学常见的物质,B、C组成元素相同。其相互反应及转化关系如图所示。(图中“→”表示物质间存在转化关系;部分反应物、生成物和反应条件已略去)。请回答。
(1)A物质的化学式可能是_____。
(2)B的一种用途是_____。
(3)A到C的转化_____是化合反应(填“一定”或“不一定”)。
(4)写出C→B反应的化学方程式_____,此反应属于_____反应(填“吸热”或“放热”)。
四、流程题
21.铁矿和铜矿都有多个种类,矿业上常用俗称,例如主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)的铜矿俗称辉铜矿、一种用辉铜矿冶炼铜的主要工艺流程如下:
(1)上述流程中,将辉铜矿“磨细”的目的是___________。
(2)“高温脱硫”阶段,主要反应的化学方程式为:,则X的化学式为_______,若直接将大量X气体排放到空气中,则可能会形成_______,造成建筑雕像腐蚀、森林破坏等环境污染问题。
(3)“金属还原”阶段,焦炭的作用是__和生成还原剂CO,还原生成铜的化学方程式为:__。
(4)“吹炼”的目的是将粗铜中所含易被氧化的杂质___(填化学式)氧化,使其易结合成炉渣。
五、计算题
22.鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙的质量分数,小华同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中滴加足量的稀盐酸,加入稀盐酸的量与生成气体的量的关系如图所示。试求该鸡蛋壳中钙元素的质量分数____。(假设鸡蛋壳中其他物质不与稀盐酸反应)
23.某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 1 2 3 4
加入样品的质量/g 5 10 15 20
生成CO2的质量/g 1.54 3.08 4.4 m
(1)m=_____;
(2)试计算这种石灰石矿中碳酸钙的质量分数.
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.D
4.C
5.B
6.D
7.B
8.C
9.A
10.D
11.C
12.A
13.C
14.B
15.(1)碳原子的排列方式不同
(2)单质
(3) 温室效应 尽量采用公共出行(其他合理答案也可)
(4) 1:1
(5) H2O 催化剂 放出
16. E B D H2O
17. SiO2+ 2CSi+2CO↑ 最外层电子数相同 BC Ca(OH)2+CO2=CaCO3↓+H2O
18.(1)Fe2O3
(2)CO2
(3)Mg2+
(4)2N
19.(1)⑤
(2)④
(3)②
(4)⑥
(5)①
20.(1)C或O2
(2)做燃料(合理即可)
(3)不一定
(4) C+CO22CO 吸热
21.(1)增大反应物接触面积,加快反应
(2) SO2 酸雨
(3) 提供热量
(4)Fe
22.20%
23.(1)4.4
(2)设实验1中加入5g石灰石矿中碳酸钙的质量为x,
解得,
则石灰石矿中碳酸钙的质量分数为
答:这种石灰石矿中碳酸钙的质量分数为70%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列关于碳及其化合物的说法正确的是
A.金刚石、石墨和C60的性质相似
B.木炭在氧气中燃烧,生成物一定是二氧化碳
C.CO2灭火既利用了CO2的物理性质,又利用了其化学性质
D.在煤炉上放一壶水能防止一氧化碳中毒
2.石墨烯是一种非常优良的纳米材料,由碳元素组成,化学性质和石墨相似,还具有超强导电、导热的性能。关于石墨烯的认识错误的是
A.可作散热材料 B.是一种新型化合物
C.常温下化学性质稳定 D.可作新型电池的电极
3.关于二氧化碳的用途,下列说法错误的是
A.灭火 B.生产汽水 C.气体肥料 D.供给呼吸
4.“碳家族”的成员很多,用途很广。下列说法正确的是
A.石墨不具有导电性 B.C60单质是由碳原子直接构成的
C.活性炭具有吸附性 D.金刚石和石墨里碳原子的排列方式相同
5.成都以“碳达峰、碳中和”为目标,引领城市绿色低碳发展。下列做法利于实现此目标的是
A.石油炼制 B.太阳能发电 C.燃煤脱硫 D.酒精作燃料
6.“碳达峰、碳中和”是近期频繁出现的热词。关于碳循环和氧循环,下列说法不正确的是
A.碳循环和氧循环过程中均发生了化学变化
B.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
C.绿色植物的生长过程,既涉及碳循环,又涉及氧循环
D.碳循环和氧循环分别是指二氧化碳和氧气的循环
7.下列有关碳及其氧化物的说法正确的是
A.CO2是引起温室效应的主要气体,因此大气中CO2的含量越少越好
B.碳的单质有多种,用途各不相同,是因为它们的物理性质各不相同
C.CO具有可燃性,在空气中燃烧产生黄色火焰
D.焦炭在工业上用于冶炼金属,在反应中表现出氧化性
8.下列与碳和碳的氧化物有关的说法中,正确的是
A.煤炉上放一盆水可防止CO中毒
B.CO2能使紫色石蕊溶液变红,说明CO2显酸性
C.CO和CO2化学性质不同的原因是分子构成不同
D.用墨绘制的古画经久不变色,说明碳不与任何物质反应
9.如图是自然界中碳、氧循环简图(X为H2CO3,Y为C6H12O6)。下列说法错误的是
A.图一中X溶液显酸性,是形成酸雨的主要原因
B.图二转化1实现了无机化合物到有机化合物的转化
C.图一、图二对比说明,反应物相同,反应条件不同,产物不同
D.碳循环和氧循环有利于维持大气中二氧化碳和氧气含量的相对稳定
10.石墨烯可用机械剥离法从石墨中剥离制得。它是由碳原子构成的只有一层原子厚度的二维晶体(如图),图中每一个小球代表一个碳原子。它是目前发现的最薄、强度最大、导电导热性能最强的一种新型纳米材料。科学家甚至预言石墨烯将“彻底改变21世纪”。关于石墨烯,下列说法不正确的是( )
A.石墨烯和金刚石都由碳元素组成
B.石墨烯的导电性比银强
C.石墨烯中每个碳原子为三个六元环共用
D.从石墨中剥离出石墨烯属于物理变化
11.由太湖水生产自来水的部分处理过程如下。有关说法不正确的是
A.用细沙“过滤”可滤除水中的细小颗粒
B.用活性炭“吸附”可除去水中的色素和异味
C.上述处理过程应包含“蒸馏”
D.经过处理获得的自来水仍是混合物
12.关于金刚石和石墨的说法正确的是
A.都有可燃性 B.都是无色固体 C.硬度都很大 D.都能导电
13.下列图示分别为二氧化碳的实验室制取、干燥、收集、验满的操作,其中正确的是
A.制取 B.干燥
C.收集 D.验满
14.坚持低碳生活、绿色发展,促进人与自然和谐共生,下列做法与这一理念不相符的是
A.限制燃放烟花 B.发展燃煤发电 C.分类处理垃圾 D.倡导公交出行
二、填空题
15.碳及其化合物的综合利用使世界变得更加绚丽多彩。
Ⅰ.碳的多样性
(1)金刚石和C60的化学性质相似,但物理性质却存在着很大差异。原因是__________。
(2)从石墨中分离出的单层石墨片(石墨烯)是目前人工制得的最薄材料,单层石墨片属于_________(填“单质”或“化合物”)。
Ⅱ.“碳中和”的实现
“碳中和”是指一定时间内CO2的排放量与吸收量基本相当。CO2的捕集、利用是实现“碳中和”的重要途径。我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。
(3)CO2的过度排放会造成_________的加剧。结合生活实际,列举可为实现“碳中和”做出直接贡献的一种措施:___________。
(4)工业生产中产生的CO2经吸收剂处理可实现CO2的捕集。
①NaOH吸收。NaOH溶液吸收CO2生成 NaHCO3的化学方程式为_______________。
②CaO吸收。CaC2O4在高温下分解制得疏松多孔的CaO,同时产生CO、CO2。该反应所得CO、CO2的分子个数之比为________。
(5)CO2与H2在一定条件下转化为CH4(反应过程如图所示,虚线处部分中间产物略去),可实现CO2的再利用。
①该反应中,除CH4外另一种生成物为__________(填化学式),MgO的作用是_________。
②天然气(主要成分为CH4)已成为居民的生活用气,是因为CH4在空气中燃烧时______(填“吸收”或“放出”)热量。
16.请你结合所学的化学知识回答下列问题:
①请选择合适物质的编号填空:A一氧化碳;B活性炭;C氢气;D氦气;E二氧化硫。与酸雨形成有关的是_____;可用于防毒面具的是_____;可充入霓虹灯内且通电时会发出有色光的是_____;
② 固定和利用二氧化碳能有效减少空气中的温室气体。例如,工业上利用CO2和NH3生产尿素,反应的化学方程式为CO2+2NH3CO(NH2)2+X,则X的化学式为_____。
17.近五年来,我国在科技、文化、环境等方面创新发展。
I.大国重器——航天、航空取得重大突破
2018年4月2日,天宫一号目标飞行器圆满完成各项任务返回大气层。这标志着我国航天、航空事业进入了新时代。
(1)硅是天宮一号动力源太阳能电池的主要构成材料。单质硅是由石英(SiO2)固体与碳在高温条件下反应制得的,同时生成一种可燃性气体,该反应的化学方程式为__________。
(2)硅是计算机芯片的基体材料,但其导热性不好,而金刚石在导热性方面远超过硅,于是它成了芯片基体材料的最佳选择。
①从原子结构上分析,金刚石(C)和硅有相似化学性质的原因是_____________________。
②因天然金刚石资源稀少,难以满足要求。人们就根据金刚石的组成和结构设法制造金刚石。现有两种制造金刚石的方法,一是以石墨为原料在高温高压和催化剂的条件下合成;二是在较低温度和压力下用甲烷(CH4)等为原料制造金刚石薄膜。
下列说法不正确的是_________(写字母序号)。
A一种元素可以组成多种性质不同的单质
B石墨合成金刚石发生的是物理变化
C石墨与金刚石物理性质不同是因为原子的结构不同
D物质的性质在很大程度上决定了物质的用途,但不是唯一的决定因素
③不仅硅与碳具有相似化学性质,其氧化物二氧化硅和二氧化碳也有相似化学性质。试写出二氧化碳与氢氧化钙溶液反应的化学方程式____。
18.化学用语是学习化学的基本工具,请用正确的化学用语填空:
(1)氧化铁________。
(2)温室效应的主要气体________。
(3)氯化镁中的阳离子是_________。
(4)2个氮原子________。
19.物质世界离不开化学,把下列符合题意物质的序号写在横线上:
①二氧化碳②二氧化硫③氮气④氧气⑤四氧化三铁⑥稀有气体
(1)黑色固体物质有_____;
(2)能供给呼吸支持燃烧的物质是_____;
(3)有刺激性气味且对空气构成污染的气体是_____;
(4)通常用作保护气和通电时发出有色光的是_____;
(5)能使澄清石灰水变浑浊且参与植物光合作用的是_____。
三、推断题
20.已知A、B、C是初中化学常见的物质,B、C组成元素相同。其相互反应及转化关系如图所示。(图中“→”表示物质间存在转化关系;部分反应物、生成物和反应条件已略去)。请回答。
(1)A物质的化学式可能是_____。
(2)B的一种用途是_____。
(3)A到C的转化_____是化合反应(填“一定”或“不一定”)。
(4)写出C→B反应的化学方程式_____,此反应属于_____反应(填“吸热”或“放热”)。
四、流程题
21.铁矿和铜矿都有多个种类,矿业上常用俗称,例如主要成分为Cu2S(含少量Fe2O3、SiO2等杂质)的铜矿俗称辉铜矿、一种用辉铜矿冶炼铜的主要工艺流程如下:
(1)上述流程中,将辉铜矿“磨细”的目的是___________。
(2)“高温脱硫”阶段,主要反应的化学方程式为:,则X的化学式为_______,若直接将大量X气体排放到空气中,则可能会形成_______,造成建筑雕像腐蚀、森林破坏等环境污染问题。
(3)“金属还原”阶段,焦炭的作用是__和生成还原剂CO,还原生成铜的化学方程式为:__。
(4)“吹炼”的目的是将粗铜中所含易被氧化的杂质___(填化学式)氧化,使其易结合成炉渣。
五、计算题
22.鸡蛋壳的主要成分是碳酸钙。为了测定鸡蛋壳中钙的质量分数,小华同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中滴加足量的稀盐酸,加入稀盐酸的量与生成气体的量的关系如图所示。试求该鸡蛋壳中钙元素的质量分数____。(假设鸡蛋壳中其他物质不与稀盐酸反应)
23.某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 1 2 3 4
加入样品的质量/g 5 10 15 20
生成CO2的质量/g 1.54 3.08 4.4 m
(1)m=_____;
(2)试计算这种石灰石矿中碳酸钙的质量分数.
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.B
3.D
4.C
5.B
6.D
7.B
8.C
9.A
10.D
11.C
12.A
13.C
14.B
15.(1)碳原子的排列方式不同
(2)单质
(3) 温室效应 尽量采用公共出行(其他合理答案也可)
(4) 1:1
(5) H2O 催化剂 放出
16. E B D H2O
17. SiO2+ 2CSi+2CO↑ 最外层电子数相同 BC Ca(OH)2+CO2=CaCO3↓+H2O
18.(1)Fe2O3
(2)CO2
(3)Mg2+
(4)2N
19.(1)⑤
(2)④
(3)②
(4)⑥
(5)①
20.(1)C或O2
(2)做燃料(合理即可)
(3)不一定
(4) C+CO22CO 吸热
21.(1)增大反应物接触面积,加快反应
(2) SO2 酸雨
(3) 提供热量
(4)Fe
22.20%
23.(1)4.4
(2)设实验1中加入5g石灰石矿中碳酸钙的质量为x,
解得,
则石灰石矿中碳酸钙的质量分数为
答:这种石灰石矿中碳酸钙的质量分数为70%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
