2022-2023学年化学人教版第八单元金属和金属材料 单元练习 (有答案)
文档属性
| 名称 | 2022-2023学年化学人教版第八单元金属和金属材料 单元练习 (有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 599.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-10 00:00:00 | ||
图片预览




文档简介
2022-2023学年化学人教版--金属和金属材料
一、单选题
1.“构建生命共同体”体现人与自然和谐共生。下列说法与该理念不相符的是
A.全民义务植树活动 B.大肆开采矿物资源
C.生活废水处理排放 D.长江流域十年禁渔
2.金属M与AgNO3溶液发生反应:,下列说法中正确的是
A.在金属活动性顺序里,M一定排在氢的前面
B.M的金属活动性比Ag弱
C.M可能是铝
D.反应前后M元素的化合价发生了改变
3.物质的性质决定用途。下列物质的用途中利用其化学性质的是
A.氧气用于气焊 B.干冰用于人工降雨
C.铜用于制导线 D.活性炭用于除冰箱异味
4.为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是
A.MgCl2溶液、Cu、Sn
B.Mg、Cu、SnCl2溶液
C.Mg、Sn、Cu、盐酸
D.MgCl2溶液、Sn、CuCl2溶液
5.下列反应属于置换反应的是( )
A.
B.
C.
D.
6.下列对实验现象的描述正确的是
A.铁丝在空气中燃烧,有黑色固体生成 B.光亮的铜丝放入稀硫酸中,产生大量气泡
C.红磷在氧气中燃烧,产生大量白烟 D.硫粉在氧气中燃烧,产生淡蓝色火焰
7.化学知识可以指导生活实践。下列说法不正确的是
A.加热煮沸不能降低水的硬度 B.用肥皂水区分硬水和软水
C.不锈钢抗锈蚀性能比铁好 D.炒菜时油锅着火可用锅盖盖灭
8.《天工开物》对钢铁冶炼过程有如下记载。有关说法正确的是
A.“垦土拾锭”:铁元素是地壳中含量最高的金属元素
B.“淘洗铁砂”:铁矿石(主要成分为Fe2O3)能溶于水
C.“生熟炼铁”:冶炼铁过程中发生了化学变化
D.“锤锻成钢”:生铁高温锻打成钢,碳元素含量升高
9.北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材科的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
10.硬铝常用于制造火箭、飞机的外壳,铝元素的相关信息如图所示,下列说法正确的是
A.铝元素的相对原子质量为13 B.Al2O3中Al为+2价
C.硬铝的强度和硬度比铝的大 D.铝是地壳中含量最多的元素
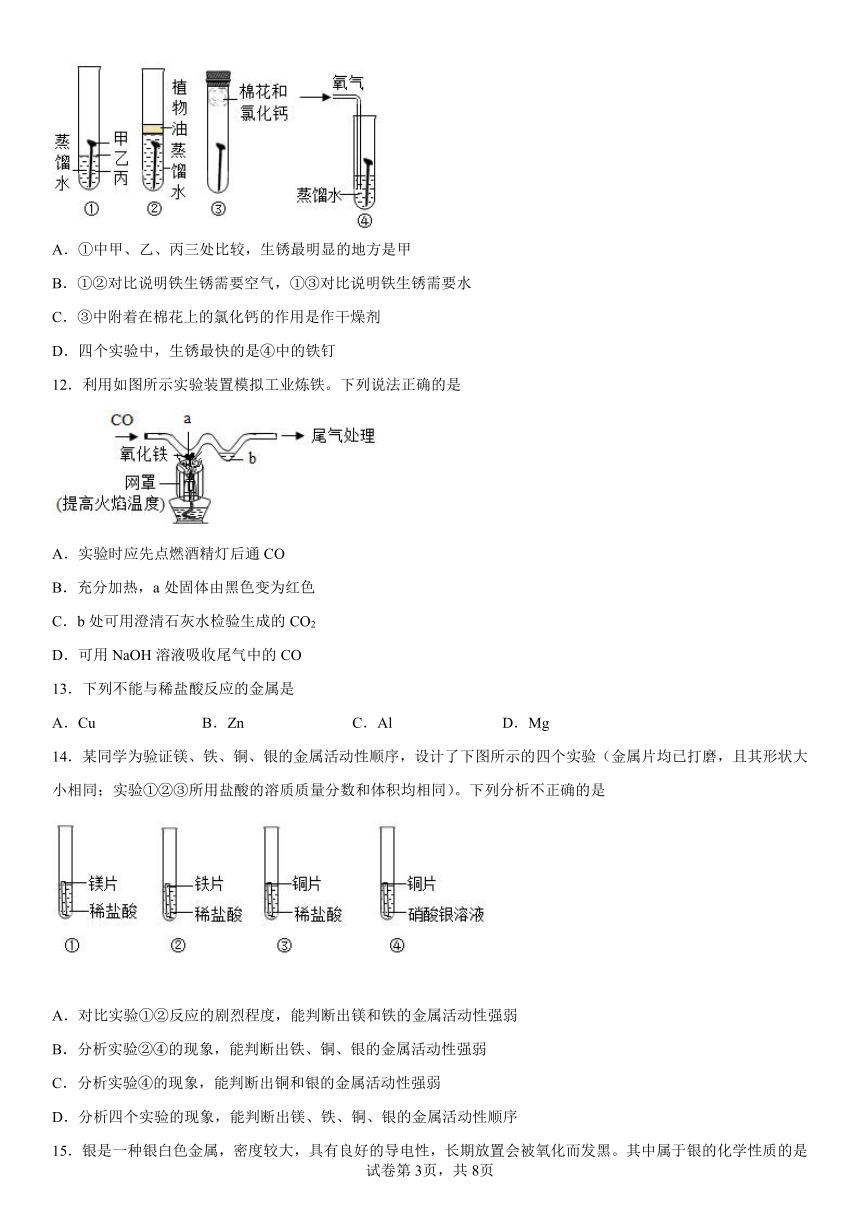
11.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
12.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
13.下列不能与稀盐酸反应的金属是
A.Cu B.Zn C.Al D.Mg
14.某同学为验证镁、铁、铜、银的金属活动性顺序,设计了下图所示的四个实验(金属片均已打磨,且其形状大小相同;实验①②③所用盐酸的溶质质量分数和体积均相同)。下列分析不正确的是
A.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱
B.分析实验②④的现象,能判断出铁、铜、银的金属活动性强弱
C.分析实验④的现象,能判断出铜和银的金属活动性强弱
D.分析四个实验的现象,能判断出镁、铁、铜、银的金属活动性顺序
15.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是
A.银白色 B.密度较大 C.导电性良好 D.能被氧化
二、填空题
16.纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。
(1)纽扣电池的外壳可以加工得很薄,说明金属具有_____性。
(2)氧化银加热分解可以得到两种单质,其化学反应方程式为_______。
(3)该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是_____,为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是________(填序号)。
A 银表面没有气泡生成
B 铁表面最终生成气体的总量比锌多
C 铁表面产生气泡的速率比锌慢
17.人类的生产生活离不开金属。
(1)日常生活用品大多用到了金属材料,现在年产量最高的金属是________。
(2)铝制品具有较好的抗腐蚀性能是因为________ (用化学方程式表示)。
(3)现有镁、铁、银的混合物若干放入硫酸铜溶液中,充分反应后过滤,向滤渣中加入稀盐酸,观察到有气泡冒出,则滤渣中一定含有________。
(4)现有一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。
①若所加硫酸铜溶液不足,则滤液中一定含有的溶质为________(填化学式)。
②若所加硫酸铜溶液过量,则该镀锌铁片中铁与锌的质量最简比为________。
18.金属在生产、生活和社会发展中的应用较为广泛。
(1)铜丝,铝丝常用作导线,是因为它们具有良好的______性。
(2)早在明代宋应星所著的《天工开物》里就对铁器的生产和使用有所记载,到了现代,炼铁技术得到进一步发展。炼铁的原理是利用一氧化碳与氧化铁的反应,请写出该反应的化学方程式_______,该反应_______(填“属于”或“不属于”)置换反应。
(3)钢窗表面喷漆不仅美观,而且可有效防止铁与空气中的_____触而生锈。
(4)某同学对含X、Y、铜、银四种金属的混合物进行如下探究,根据实验流程回答下列问题:
①四种金属的活动性由强到弱的顺序是 _______。
②滤液C中所含溶质的成分可能有______种情况。
19.我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的合金制造技术取得重大突破。根据所学知识回答问题。
(1)生铁和钢都是铁的合金,其中含碳量较高的是____________。
(2)探究Al与酸的反应前,用砂纸打磨铝条,是为了除去_______(填化学式)。
(3)某合金中含有金属钪(Sc)。 相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性Sc_____Zn(填“>”或“<”)。根据上述结论,下列说法不正确的是_________(填序号)。
A.将Sc投入CuSO4溶液中有红色物质析出
B.仅用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag能验证钪和铁的活动性强弱
C.仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(4)已知Sc与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式________________。
20.《天工开物》中记载了采矿和冶炼金属锡的场景。
(1)采矿(图1) “水锡……其质黑色……愈经淘取”。水中淘取锡砂(指锡矿石)时,所用容器的孔径需_____(选填“大于”或“小于”)锡砂颗粒大小。锡砂主要成分为SnO2,_____(选填“易”或“难)溶于水。
(2)治炼(图2) “凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”
①鼓入足量空气能使木炭_______从而提高炉温。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是________。
(3)使用
①锡往往与其它金属制成合金使用,目的是_______(选填 “增大”或“减小”)硬度。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是___________。
三、推断题
21.A~G均为初中化学常见物质,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去)。已知:B为黑色固体,C、E均为无色气体,其中C是空气的主要成分之一;F、G均为金属单质,其中F为红色。请回答下列问题:
(1)物质C为_______。
(2)物质B在反应①中的作用是_______。
(3)反应④的化学方程式为_______。
(4)实验室用反应③制取气体E时,可选用如图所示装置中的_______(填序号)。
四、流程题
22.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如下:
请回答:
(1)A的化学式 __________ 。
(2)反应②的化学方程式为 _____________________ 。
(3)反应③的化学方程式为 _____________________ 。
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有 __________ (填化学式),滤液中一定含有的溶质是 __________ (填化学式)。
五、计算题
23.某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案,取100g上述废液,向其中加入2.8g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,求:
⑴回收得到铜的质量为多少_______?(写出计算过程)
⑵回收得到硫酸亚铁的质量是_____g(计算结果保留两位小数)。
24.为测定黄铜(铜锌合金)样品中铜的质量分数,小明取一定质量的样品放入烧杯中,分2次加入质量分数相同的稀硫酸,实验过程和数据如图所示。
请计算:
(1)生成氢气的总质量是______g。
(2)黄铜样品中铜的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.A
4.A
5.C
6.C
7.A
8.C
9.D
10.C
11.A
12.C
13.A
14.B
15.D
16. 延展性 锌、铁、银 B
17. 铁(Fe) Fe、Cu和Ag FeSO4和ZnSO4 112:13
18. 导电 不属于 氧气和水 Y>X>铜>银 3
19. 生铁 Al2O3 > B 2Sc+6HCl===2ScCl3+3H2↑
20.(1) 小于 难
(2) 完全燃烧 形成合金熔点降低
(3) 增大 锡器会与酸性物质反应
21. 氧气(O2) 催化作用(催化剂) ①③或①⑤
22. CO2 CO2+C 2CO 3CO+Fe2O3 2Fe+3CO2 Ag Fe(NO3)2
23.(1)3.2g,(2)14.94g
24.(1)0.4
(2)充分反应后,产生氢气的质量为0.4g。
解:设黄铜样品中锌的质量为x。
黄铜样品中铜的质量为
黄铜样品中铜的质量分数为
答:黄铜样品中铜的质量分数为67.5%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.“构建生命共同体”体现人与自然和谐共生。下列说法与该理念不相符的是
A.全民义务植树活动 B.大肆开采矿物资源
C.生活废水处理排放 D.长江流域十年禁渔
2.金属M与AgNO3溶液发生反应:,下列说法中正确的是
A.在金属活动性顺序里,M一定排在氢的前面
B.M的金属活动性比Ag弱
C.M可能是铝
D.反应前后M元素的化合价发生了改变
3.物质的性质决定用途。下列物质的用途中利用其化学性质的是
A.氧气用于气焊 B.干冰用于人工降雨
C.铜用于制导线 D.活性炭用于除冰箱异味
4.为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是
A.MgCl2溶液、Cu、Sn
B.Mg、Cu、SnCl2溶液
C.Mg、Sn、Cu、盐酸
D.MgCl2溶液、Sn、CuCl2溶液
5.下列反应属于置换反应的是( )
A.
B.
C.
D.
6.下列对实验现象的描述正确的是
A.铁丝在空气中燃烧,有黑色固体生成 B.光亮的铜丝放入稀硫酸中,产生大量气泡
C.红磷在氧气中燃烧,产生大量白烟 D.硫粉在氧气中燃烧,产生淡蓝色火焰
7.化学知识可以指导生活实践。下列说法不正确的是
A.加热煮沸不能降低水的硬度 B.用肥皂水区分硬水和软水
C.不锈钢抗锈蚀性能比铁好 D.炒菜时油锅着火可用锅盖盖灭
8.《天工开物》对钢铁冶炼过程有如下记载。有关说法正确的是
A.“垦土拾锭”:铁元素是地壳中含量最高的金属元素
B.“淘洗铁砂”:铁矿石(主要成分为Fe2O3)能溶于水
C.“生熟炼铁”:冶炼铁过程中发生了化学变化
D.“锤锻成钢”:生铁高温锻打成钢,碳元素含量升高
9.北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材科的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
10.硬铝常用于制造火箭、飞机的外壳,铝元素的相关信息如图所示,下列说法正确的是
A.铝元素的相对原子质量为13 B.Al2O3中Al为+2价
C.硬铝的强度和硬度比铝的大 D.铝是地壳中含量最多的元素
11.下图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
12.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
13.下列不能与稀盐酸反应的金属是
A.Cu B.Zn C.Al D.Mg
14.某同学为验证镁、铁、铜、银的金属活动性顺序,设计了下图所示的四个实验(金属片均已打磨,且其形状大小相同;实验①②③所用盐酸的溶质质量分数和体积均相同)。下列分析不正确的是
A.对比实验①②反应的剧烈程度,能判断出镁和铁的金属活动性强弱
B.分析实验②④的现象,能判断出铁、铜、银的金属活动性强弱
C.分析实验④的现象,能判断出铜和银的金属活动性强弱
D.分析四个实验的现象,能判断出镁、铁、铜、银的金属活动性顺序
15.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是
A.银白色 B.密度较大 C.导电性良好 D.能被氧化
二、填空题
16.纽扣电池是生活中常用的电源,下图是银锌纽扣电池的构造示意图,回答下列问题。
(1)纽扣电池的外壳可以加工得很薄,说明金属具有_____性。
(2)氧化银加热分解可以得到两种单质,其化学反应方程式为_______。
(3)该电池中涉及的铁、锌、银三种金属,它们的金属活动性由强到弱的顺序是_____,为了验证该结论,某同学向质量、外形相同的铁片、锌片、银片中分别加入足量15%的稀盐酸,以下现象中不能成为该结论证据的是________(填序号)。
A 银表面没有气泡生成
B 铁表面最终生成气体的总量比锌多
C 铁表面产生气泡的速率比锌慢
17.人类的生产生活离不开金属。
(1)日常生活用品大多用到了金属材料,现在年产量最高的金属是________。
(2)铝制品具有较好的抗腐蚀性能是因为________ (用化学方程式表示)。
(3)现有镁、铁、银的混合物若干放入硫酸铜溶液中,充分反应后过滤,向滤渣中加入稀盐酸,观察到有气泡冒出,则滤渣中一定含有________。
(4)现有一块镀锌铁片,其质量为6.25g,把它放入一定量的硫酸铜溶液中充分反应后过滤,得到一定量的滤液和7.04g滤渣。
①若所加硫酸铜溶液不足,则滤液中一定含有的溶质为________(填化学式)。
②若所加硫酸铜溶液过量,则该镀锌铁片中铁与锌的质量最简比为________。
18.金属在生产、生活和社会发展中的应用较为广泛。
(1)铜丝,铝丝常用作导线,是因为它们具有良好的______性。
(2)早在明代宋应星所著的《天工开物》里就对铁器的生产和使用有所记载,到了现代,炼铁技术得到进一步发展。炼铁的原理是利用一氧化碳与氧化铁的反应,请写出该反应的化学方程式_______,该反应_______(填“属于”或“不属于”)置换反应。
(3)钢窗表面喷漆不仅美观,而且可有效防止铁与空气中的_____触而生锈。
(4)某同学对含X、Y、铜、银四种金属的混合物进行如下探究,根据实验流程回答下列问题:
①四种金属的活动性由强到弱的顺序是 _______。
②滤液C中所含溶质的成分可能有______种情况。
19.我国自主设计的大型客机成功试飞,首艘国产航母正式下水,标志着我国的合金制造技术取得重大突破。根据所学知识回答问题。
(1)生铁和钢都是铁的合金,其中含碳量较高的是____________。
(2)探究Al与酸的反应前,用砂纸打磨铝条,是为了除去_______(填化学式)。
(3)某合金中含有金属钪(Sc)。 相同条件下,取相同状态的金属钪和锌分别与相同浓度的盐酸反应,钪产生气泡速率明显更快,则金属活动性Sc_____Zn(填“>”或“<”)。根据上述结论,下列说法不正确的是_________(填序号)。
A.将Sc投入CuSO4溶液中有红色物质析出
B.仅用Fe(NO3)2溶液、Sc(NO3)3溶液、Ag能验证钪和铁的活动性强弱
C.仅用Fe、Sc、稀H2SO4溶液能验证钪和铁的活动性强弱
(4)已知Sc与稀盐酸发生置换反应,生成+3价化合物。写出该反应的化学方程式________________。
20.《天工开物》中记载了采矿和冶炼金属锡的场景。
(1)采矿(图1) “水锡……其质黑色……愈经淘取”。水中淘取锡砂(指锡矿石)时,所用容器的孔径需_____(选填“大于”或“小于”)锡砂颗粒大小。锡砂主要成分为SnO2,_____(选填“易”或“难)溶于水。
(2)治炼(图2) “凡煎炼亦用洪炉,入砂数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化。”
①鼓入足量空气能使木炭_______从而提高炉温。
②炼锡时,有关键的一步“点铅勾锡”,即加铅能使锡较易熔化流出,其原因是________。
(3)使用
①锡往往与其它金属制成合金使用,目的是_______(选填 “增大”或“减小”)硬度。
②古代锡器常用来饮酒喝茶,很少装酸性物质,原因是___________。
三、推断题
21.A~G均为初中化学常见物质,它们之间的相互转化关系如图所示(部分反应物、生成物及反应条件已略去)。已知:B为黑色固体,C、E均为无色气体,其中C是空气的主要成分之一;F、G均为金属单质,其中F为红色。请回答下列问题:
(1)物质C为_______。
(2)物质B在反应①中的作用是_______。
(3)反应④的化学方程式为_______。
(4)实验室用反应③制取气体E时,可选用如图所示装置中的_______(填序号)。
四、流程题
22.某钢铁厂高炉炼铁的主要原料是焦炭、赤铁矿石(主要含Fe2O3)、空气等,主要反应过程如下:
请回答:
(1)A的化学式 __________ 。
(2)反应②的化学方程式为 _____________________ 。
(3)反应③的化学方程式为 _____________________ 。
(4)向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有 __________ (填化学式),滤液中一定含有的溶质是 __________ (填化学式)。
五、计算题
23.某化工厂产生的废液中含有硫酸亚铁和硫酸铜(不考虑其它物质),为回收铜和硫酸亚铁,研究人员设计出“用铁处理”的方案,取100g上述废液,向其中加入2.8g铁粉,恰好完全反应,测得反应后溶液中溶质的质量分数为15%,求:
⑴回收得到铜的质量为多少_______?(写出计算过程)
⑵回收得到硫酸亚铁的质量是_____g(计算结果保留两位小数)。
24.为测定黄铜(铜锌合金)样品中铜的质量分数,小明取一定质量的样品放入烧杯中,分2次加入质量分数相同的稀硫酸,实验过程和数据如图所示。
请计算:
(1)生成氢气的总质量是______g。
(2)黄铜样品中铜的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.D
3.A
4.A
5.C
6.C
7.A
8.C
9.D
10.C
11.A
12.C
13.A
14.B
15.D
16. 延展性 锌、铁、银 B
17. 铁(Fe) Fe、Cu和Ag FeSO4和ZnSO4 112:13
18. 导电 不属于 氧气和水 Y>X>铜>银 3
19. 生铁 Al2O3 > B 2Sc+6HCl===2ScCl3+3H2↑
20.(1) 小于 难
(2) 完全燃烧 形成合金熔点降低
(3) 增大 锡器会与酸性物质反应
21. 氧气(O2) 催化作用(催化剂) ①③或①⑤
22. CO2 CO2+C 2CO 3CO+Fe2O3 2Fe+3CO2 Ag Fe(NO3)2
23.(1)3.2g,(2)14.94g
24.(1)0.4
(2)充分反应后,产生氢气的质量为0.4g。
解:设黄铜样品中锌的质量为x。
黄铜样品中铜的质量为
黄铜样品中铜的质量分数为
答:黄铜样品中铜的质量分数为67.5%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
