课题2第1课时 金属的化学性质(1)-2022-2023学年九年级化学下册同步教学精品课件(28页)(人教版)
文档属性
| 名称 | 课题2第1课时 金属的化学性质(1)-2022-2023学年九年级化学下册同步教学精品课件(28页)(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-12 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第八单元
课题2 金属的化学性质课时1
1.知道镁、铝、铁、铜等常见金属与氧气的反应,并能解释生活中的现象
2.探究常见金属与盐酸、硫酸的反应,了解金属的活动性
3.知道置换反应的概念与特征
这是博物馆里的金属文物,观察它们的外观,试着给这些金属按化学性质的活泼程度由活泼到不活泼排序
一、金属与氧气反应
根据信息,写出反应的方程式。
金属 信息 方程式
镁
铝
铁
铜
2Mg+O2 = 2MgO
4Al+3O2 = 2Al2O3
3Fe+2O2 Fe3O4
2Cu+O2 = 2CuO
加热
想一想
比较表中金属的活动性。
Al
弱
强
Mg
Fe
Cu
Au
综合上述信息可知:
1.大多数金属都能与 反应,反应剧烈程度 (是否相同)。
氧气
不同
想一想
俗话说“真金不怕火炼”,请利用金属的化学性质来解释。
金的化学性质不活泼,在高温下也不与氧气反应
铝的抗腐蚀性
铝在常温下就能与氧气反应。铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
2、铝制品为什么不能用钢刷刷洗呢?
想一想
1、银色防锈漆里面的金属是?为什么它能防锈?
钢刷除去铝锅表面致密的的氧化铝薄膜,就不能保护里层的铝不再与氧气反应,使铝锅容易被腐蚀。
铝,铝在常温下与氧气反应,生成一层致密的氧化铝薄膜阻止金属再被锈蚀。
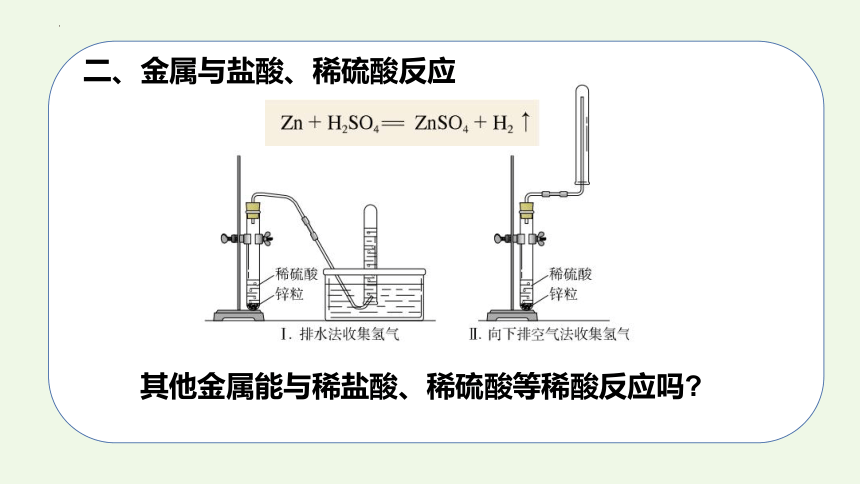
二、金属与盐酸、稀硫酸反应
其他金属能与稀盐酸、稀硫酸等稀酸反应吗
在试管里放入少量镁,加入5 mL稀盐酸,用燃着的小木条放在试管口,观察现象,并判断反应后生成了什么气体。
实验
Mg+ 2HCl=H2↑+MgCl2
产生气泡很快
实验
参照上述实验步骤,分别在放有少量锌、铁或铜的试管中加入稀盐酸,观察现象,比较反应的剧烈程度。如果有气体生成,判断生成的是什么气体。
现象 反应的化学方程式
锌
铁
铜
产生气泡较快
产生气泡较慢
无气泡
Zn+2HCl=H2↑+ZnCl2
Fe+2HCl=H2↑+FeCl2
不反应
探究
请设计实验探究金属能否与稀硫酸反应,若能反应请设计实验比较哪种金属比较活泼。
控制变量
金属
稀硫酸
比较方法:
实验仪器和药品:
试管若干支、镊子、镁片、锌片、铁片、铜片(金属已打磨)、稀硫酸
相同质量
相同形状
相同体积
相同浓度
产生气体的快慢
①比较相同时间内产生气体的体积
②比较产生相同体积的气体所用的时间
金属 现象 反应的化学方程式
镁
锌
铁
铜
产生气泡很快
产生气泡较快
产生气泡较慢
无气泡
Mg+H2SO4=H2↑+MgSO4
Zn+H2SO4=H2↑+ZnSO4
Fe+H2SO4=H2↑+FeSO4
不反应
1.哪些金属能与盐酸、稀硫酸发生反应 反应的剧烈程度如何 反应后生成了什么气体 哪些金属不能与盐酸、稀硫酸发生反应 根据反应时是否有氢气产生,将金属分为两类。
强
弱
Mg
Zn
Fe
(H)
Cu
讨论
根据上述实验现象以及反应的化学方程式讨论。
在实验室制取氢气,选择锌的理由是什么?
2.对于能发生的反应,从反应物和生成物的物质类别如单质、化合物的角度分析,这些反应有什么特点 将这一类反应与化合反应、分解反应进行比较。
这种由一种 与一种 反应,生成另一种
和另一种 的反应叫做 。
单质
单质
化合物
化合物
置换反应
小结
金属
化学性质
一、金属与氧气反应
二、金属与盐酸、稀硫酸反应
置换反应
特点:单质+化合物→单质+化合物
可根据金属与氧气反应的难易和反应现象的剧烈程度不同判断金属活动性强弱
可根据金属是否与盐酸或稀硫酸反应,或反应的剧烈程度判断金属的活动性强弱
国际互联网上报道:目前世界上约有近50亿人患有不同程度的缺铁性贫血。联合国卫生组织经过严密的科学分析认为:我国的铁锅是最理想的炊具,可有效减少缺铁性贫血的发生,如果在炒菜时经常加入适量的食醋,效果会更好。
思考:为什么我国的铁锅是最理想的炊具,其依据的化学原理是什么?
少量的单质铁会随着饭菜进入胃中(胃酸中含有盐酸),少量单质铁会与醋酸反应,生成易被人体吸收的铁。
链接生活
熬制中药一般用砂锅或陶罐而不用铁锅,你能猜测一下其中的原因吗?
铁的金属活动性比较强,而中草药中含有一种叫鞣酸的物质,它们之间能发生置换反应,生成不溶于水的鞣酸铁,使药液中有效含量降低,并生成对人体有害的毒性物质。
1.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.各种金属都能与盐酸发生置换反应
D.根据金属与氧气反应的难易程度可以初步比较
金属的活动性
练一练
D
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A 铝不易发生化学反应
B 铝的氧化物容易发生还原反应
C 铝不易被氧化
D 铝易氧化,但氧化铝具有保护内部铝的作用
D
3.我市倡导自行车“低碳出行”.采用碳纤维材料的自行车轻便、机械强度大,这应用了碳纤维的 (填“物理”或“化学”)性质;自行车采用铝合金材料,金属铝具有较强抗腐蚀性的原因: 。
物理
铝与氧气能生成致密的氧化铝薄膜
4、下列反应最适合用于实验室制取氢气是( )
A.铜和稀硫酸 B.镁和稀盐酸
C.锌和稀硫酸 D.铁和稀硝酸
5、某金属放在稀硫酸中,不产生气泡,该金属可能是( )
A、Cu B、Zn C、Al D、Mg
6.下列物质中,不能用金属和稀硫酸直接反应制得的是( )
A.硫酸镁 B.硫酸铜 C.硫酸铁 D.硫酸锌
C
A
C
7、下列物质不能由金属酸反应直接生成的是( )
A. ZnCl2 B.CuSO4 C.FeCl2 D.MgSO4
8.下列物质可以由相应的金属和酸发生而制得的是( )
A.Fe2(SO4)3 B.AgCl C. CuCl2 D.Al2(SO4)3
9. 列物质①FeCl3 ②ZnCl2 ③CuCl2 ④AlCl3中,能用金属和盐酸直接反应制得的物质是( )
A.①② B.②④ C.③④ D.①③
B
D
B
10.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易北蚁酸腐蚀的是( )
A.镀锌水管 B.铜制塑像
C.大理石栏杆 D.铝合金门窗
B
因为酸性食品会与铝、铁反应而将其腐蚀
11.你家庭厨房中盛放醋的容器是什么材料的呢?能用铁或铝制容器吗?
12. 实验室的废酸液不能直接倒入下水道,是因为 ;
会腐蚀金属管道
13.钛合金是21世纪重要的材料,工业上制取钛的一个反应是:TiCl4+2Mg == Ti+2MgCl2,该反应类型属于( )
A 化合反应 B 分解反应 C 置换反应 D 都不属于
C
14.芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:
SiO2 + 2C Si +2CO↑
该反应的基本类型是( )
A.化合反应 B.分解反应 C.置换反应 D.都不属于
高温
C
15、下列反应属于置换反应的是( )
①H2+CuO===Cu+H2O
②2CO+O2===2CO2
③Zn+2HCl===ZnCl2+H2↑
④Fe2O3+3CO===2Fe+3CO2
A、①④ B、②③ C、①③ D、②④
C
加热
点燃
高温
16、下列反应属于置换反应的是( )
A.氧化钙与水反应 B. 铁与盐酸反应
C.实验室制取二氧化碳 D.加热高锰酸钾制取氧气
B
17、有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为 ( )
A、X>Y>Z B、Z>Y>X C、Y>X>Z D、Z>X>Y
B
18.有X、Y、Z三种金属单质,X在常温下就能与氧气发生反应,Y、Z常温下几乎不与氧气反应;如果把Y、Z分别放入稀硫酸中,Y溶解并产生氢气,Z不反应。根据以上事实判断X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X Z Y B.X Y Z C.Y Z X D.Z Y X
B
19.从铁矿石中冶炼出的是生铁,往生铁中加入足量的稀盐酸充分反应后,剩余的黑色残渣主要是 。
20.已知锰(Mn)的金属活动性强于锌,不锈钢材料中锰若析出进入人体胃中,会与胃液(主要成分是盐酸)中的盐酸发生置换反应,反应产物中锰元素化合价+2价,请写出该反应的化学方程式 ;
碳
Mn+2HCl=MnCl2+H2↑
21.请设计实验除去括号中的杂质
① Cu(Zn) ② Cu(Fe)
第八单元
课题2 金属的化学性质课时1
1.知道镁、铝、铁、铜等常见金属与氧气的反应,并能解释生活中的现象
2.探究常见金属与盐酸、硫酸的反应,了解金属的活动性
3.知道置换反应的概念与特征
这是博物馆里的金属文物,观察它们的外观,试着给这些金属按化学性质的活泼程度由活泼到不活泼排序
一、金属与氧气反应
根据信息,写出反应的方程式。
金属 信息 方程式
镁
铝
铁
铜
2Mg+O2 = 2MgO
4Al+3O2 = 2Al2O3
3Fe+2O2 Fe3O4
2Cu+O2 = 2CuO
加热
想一想
比较表中金属的活动性。
Al
弱
强
Mg
Fe
Cu
Au
综合上述信息可知:
1.大多数金属都能与 反应,反应剧烈程度 (是否相同)。
氧气
不同
想一想
俗话说“真金不怕火炼”,请利用金属的化学性质来解释。
金的化学性质不活泼,在高温下也不与氧气反应
铝的抗腐蚀性
铝在常温下就能与氧气反应。铝在空气中与氧气反应,其表面生成一层致密的氧化铝(Al2O3)薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
2、铝制品为什么不能用钢刷刷洗呢?
想一想
1、银色防锈漆里面的金属是?为什么它能防锈?
钢刷除去铝锅表面致密的的氧化铝薄膜,就不能保护里层的铝不再与氧气反应,使铝锅容易被腐蚀。
铝,铝在常温下与氧气反应,生成一层致密的氧化铝薄膜阻止金属再被锈蚀。
二、金属与盐酸、稀硫酸反应
其他金属能与稀盐酸、稀硫酸等稀酸反应吗
在试管里放入少量镁,加入5 mL稀盐酸,用燃着的小木条放在试管口,观察现象,并判断反应后生成了什么气体。
实验
Mg+ 2HCl=H2↑+MgCl2
产生气泡很快
实验
参照上述实验步骤,分别在放有少量锌、铁或铜的试管中加入稀盐酸,观察现象,比较反应的剧烈程度。如果有气体生成,判断生成的是什么气体。
现象 反应的化学方程式
锌
铁
铜
产生气泡较快
产生气泡较慢
无气泡
Zn+2HCl=H2↑+ZnCl2
Fe+2HCl=H2↑+FeCl2
不反应
探究
请设计实验探究金属能否与稀硫酸反应,若能反应请设计实验比较哪种金属比较活泼。
控制变量
金属
稀硫酸
比较方法:
实验仪器和药品:
试管若干支、镊子、镁片、锌片、铁片、铜片(金属已打磨)、稀硫酸
相同质量
相同形状
相同体积
相同浓度
产生气体的快慢
①比较相同时间内产生气体的体积
②比较产生相同体积的气体所用的时间
金属 现象 反应的化学方程式
镁
锌
铁
铜
产生气泡很快
产生气泡较快
产生气泡较慢
无气泡
Mg+H2SO4=H2↑+MgSO4
Zn+H2SO4=H2↑+ZnSO4
Fe+H2SO4=H2↑+FeSO4
不反应
1.哪些金属能与盐酸、稀硫酸发生反应 反应的剧烈程度如何 反应后生成了什么气体 哪些金属不能与盐酸、稀硫酸发生反应 根据反应时是否有氢气产生,将金属分为两类。
强
弱
Mg
Zn
Fe
(H)
Cu
讨论
根据上述实验现象以及反应的化学方程式讨论。
在实验室制取氢气,选择锌的理由是什么?
2.对于能发生的反应,从反应物和生成物的物质类别如单质、化合物的角度分析,这些反应有什么特点 将这一类反应与化合反应、分解反应进行比较。
这种由一种 与一种 反应,生成另一种
和另一种 的反应叫做 。
单质
单质
化合物
化合物
置换反应
小结
金属
化学性质
一、金属与氧气反应
二、金属与盐酸、稀硫酸反应
置换反应
特点:单质+化合物→单质+化合物
可根据金属与氧气反应的难易和反应现象的剧烈程度不同判断金属活动性强弱
可根据金属是否与盐酸或稀硫酸反应,或反应的剧烈程度判断金属的活动性强弱
国际互联网上报道:目前世界上约有近50亿人患有不同程度的缺铁性贫血。联合国卫生组织经过严密的科学分析认为:我国的铁锅是最理想的炊具,可有效减少缺铁性贫血的发生,如果在炒菜时经常加入适量的食醋,效果会更好。
思考:为什么我国的铁锅是最理想的炊具,其依据的化学原理是什么?
少量的单质铁会随着饭菜进入胃中(胃酸中含有盐酸),少量单质铁会与醋酸反应,生成易被人体吸收的铁。
链接生活
熬制中药一般用砂锅或陶罐而不用铁锅,你能猜测一下其中的原因吗?
铁的金属活动性比较强,而中草药中含有一种叫鞣酸的物质,它们之间能发生置换反应,生成不溶于水的鞣酸铁,使药液中有效含量降低,并生成对人体有害的毒性物质。
1.下列关于金属的说法正确的是( )
A.各种金属在常温下都不能与氧气反应
B.各种金属在高温下都能与氧气反应
C.各种金属都能与盐酸发生置换反应
D.根据金属与氧气反应的难易程度可以初步比较
金属的活动性
练一练
D
2.小兰家中收藏一件清末的铝制佛像,该佛像至今保存十分完好。其主要原因是( )
A 铝不易发生化学反应
B 铝的氧化物容易发生还原反应
C 铝不易被氧化
D 铝易氧化,但氧化铝具有保护内部铝的作用
D
3.我市倡导自行车“低碳出行”.采用碳纤维材料的自行车轻便、机械强度大,这应用了碳纤维的 (填“物理”或“化学”)性质;自行车采用铝合金材料,金属铝具有较强抗腐蚀性的原因: 。
物理
铝与氧气能生成致密的氧化铝薄膜
4、下列反应最适合用于实验室制取氢气是( )
A.铜和稀硫酸 B.镁和稀盐酸
C.锌和稀硫酸 D.铁和稀硝酸
5、某金属放在稀硫酸中,不产生气泡,该金属可能是( )
A、Cu B、Zn C、Al D、Mg
6.下列物质中,不能用金属和稀硫酸直接反应制得的是( )
A.硫酸镁 B.硫酸铜 C.硫酸铁 D.硫酸锌
C
A
C
7、下列物质不能由金属酸反应直接生成的是( )
A. ZnCl2 B.CuSO4 C.FeCl2 D.MgSO4
8.下列物质可以由相应的金属和酸发生而制得的是( )
A.Fe2(SO4)3 B.AgCl C. CuCl2 D.Al2(SO4)3
9. 列物质①FeCl3 ②ZnCl2 ③CuCl2 ④AlCl3中,能用金属和盐酸直接反应制得的物质是( )
A.①② B.②④ C.③④ D.①③
B
D
B
10.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,能腐蚀很多物质。下列最不容易北蚁酸腐蚀的是( )
A.镀锌水管 B.铜制塑像
C.大理石栏杆 D.铝合金门窗
B
因为酸性食品会与铝、铁反应而将其腐蚀
11.你家庭厨房中盛放醋的容器是什么材料的呢?能用铁或铝制容器吗?
12. 实验室的废酸液不能直接倒入下水道,是因为 ;
会腐蚀金属管道
13.钛合金是21世纪重要的材料,工业上制取钛的一个反应是:TiCl4+2Mg == Ti+2MgCl2,该反应类型属于( )
A 化合反应 B 分解反应 C 置换反应 D 都不属于
C
14.芯片是电脑、“智能”加点的核心部件,它是用高纯度硅制成的。下面是生产单质硅过程中的一个重要反应:
SiO2 + 2C Si +2CO↑
该反应的基本类型是( )
A.化合反应 B.分解反应 C.置换反应 D.都不属于
高温
C
15、下列反应属于置换反应的是( )
①H2+CuO===Cu+H2O
②2CO+O2===2CO2
③Zn+2HCl===ZnCl2+H2↑
④Fe2O3+3CO===2Fe+3CO2
A、①④ B、②③ C、①③ D、②④
C
加热
点燃
高温
16、下列反应属于置换反应的是( )
A.氧化钙与水反应 B. 铁与盐酸反应
C.实验室制取二氧化碳 D.加热高锰酸钾制取氧气
B
17、有X、Y、Z三种金属,如果把这三种金属均投入到稀硫酸中,X、Y表面均无明显现象,Z表面有大量气泡产生。若将X、Y这两种金属放在氧气中加热,X表面无明显现象,Y表面发黑。则这三种金属活动性顺序为 ( )
A、X>Y>Z B、Z>Y>X C、Y>X>Z D、Z>X>Y
B
18.有X、Y、Z三种金属单质,X在常温下就能与氧气发生反应,Y、Z常温下几乎不与氧气反应;如果把Y、Z分别放入稀硫酸中,Y溶解并产生氢气,Z不反应。根据以上事实判断X、Y、Z三种金属的活动性由强到弱的顺序是( )
A.X Z Y B.X Y Z C.Y Z X D.Z Y X
B
19.从铁矿石中冶炼出的是生铁,往生铁中加入足量的稀盐酸充分反应后,剩余的黑色残渣主要是 。
20.已知锰(Mn)的金属活动性强于锌,不锈钢材料中锰若析出进入人体胃中,会与胃液(主要成分是盐酸)中的盐酸发生置换反应,反应产物中锰元素化合价+2价,请写出该反应的化学方程式 ;
碳
Mn+2HCl=MnCl2+H2↑
21.请设计实验除去括号中的杂质
① Cu(Zn) ② Cu(Fe)
同课章节目录
