4.4.3 有关化学式的计算 课件 2022-2023学年九年级上册人教版化学(共15张PPT)
文档属性
| 名称 | 4.4.3 有关化学式的计算 课件 2022-2023学年九年级上册人教版化学(共15张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 325.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-12 00:00:00 | ||
图片预览




文档简介
(共15张PPT)
第四单元 自然界的水
课题4 化学式与化合价
人教版
第三课时
1.会计算相对分子质量;
2.会计算化合物中各元素的质量比及某元素的质量分数;
3.能看懂某些商品标签或说明说明书上标示的物质含量。
教学目标
H
H
O
H
H
O
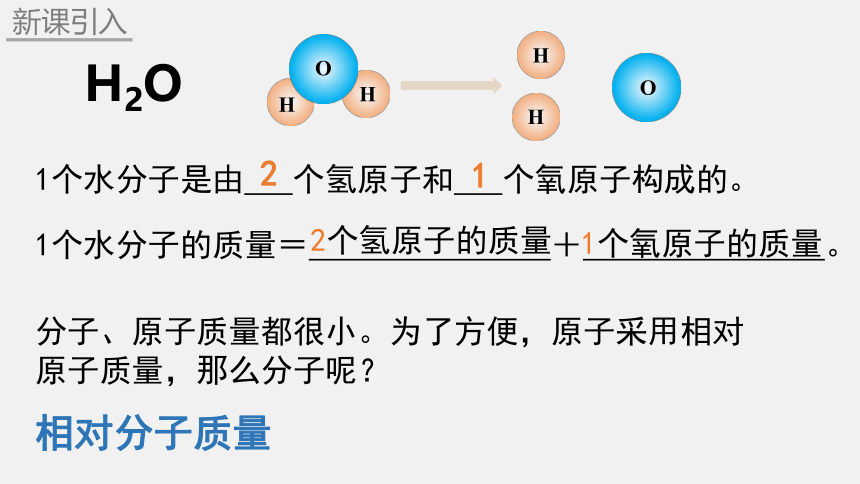
H2O
1个水分子是由 个氢原子和 个氧原子构成的。
1个水分子的质量= + 。
2
1
2个氢原子的质量
1个氧原子的质量
分子、原子质量都很小。为了方便,原子采用相对原子质量,那么分子呢?
相对分子质量
新课引入
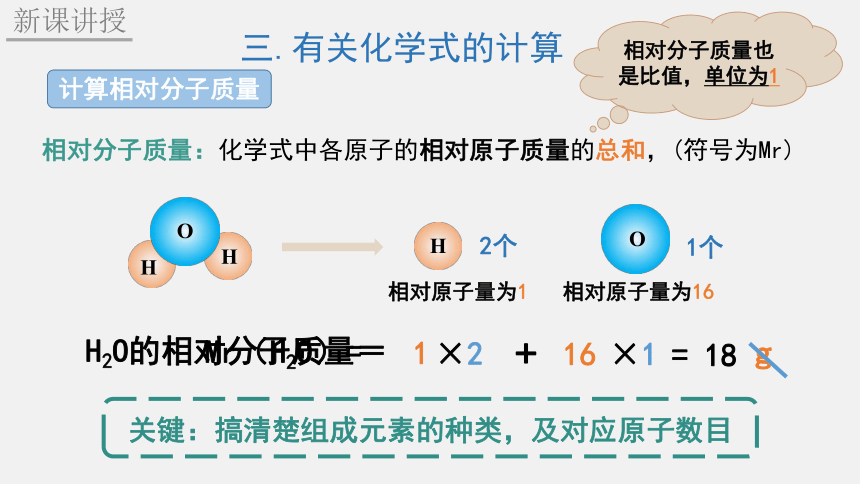
相对分子质量:化学式中各原子的相对原子质量的总和,(符号为Mr)
H
H
O
H
O
相对原子量为1
相对原子量为16
Mr(H2O)=
= 18
1
×2
+
16
×1
2个
1个
g
关键:搞清楚组成元素的种类,及对应原子数目
H2O的相对分子质量=
相对分子质量也是比值,单位为1
三.有关化学式的计算
新课讲授
计算相对分子质量
相对原子质量: H-1 N-14 O-16 Al-27 S-32 K-39 Ca-40
1.计算 NH4NO3的相对分子质量
2.计算Al2(SO4)3的相对分子质量
Mr[Al2(SO4)3] = 27×2 + (32×1+16×4)×3
= 342
Mr[NH4NO3] = 14×2 + 1×4 + 16×3
= 80
3.计算KAl(SO4)2·12H2O的相对分子质量
Mr[KAl(SO4)2·12H2O] = 39 + 27 + (32+16×4)×2 + 12×(1×2+16)
= 474
三.有关化学式的计算
计算相对分子质量
新课讲授
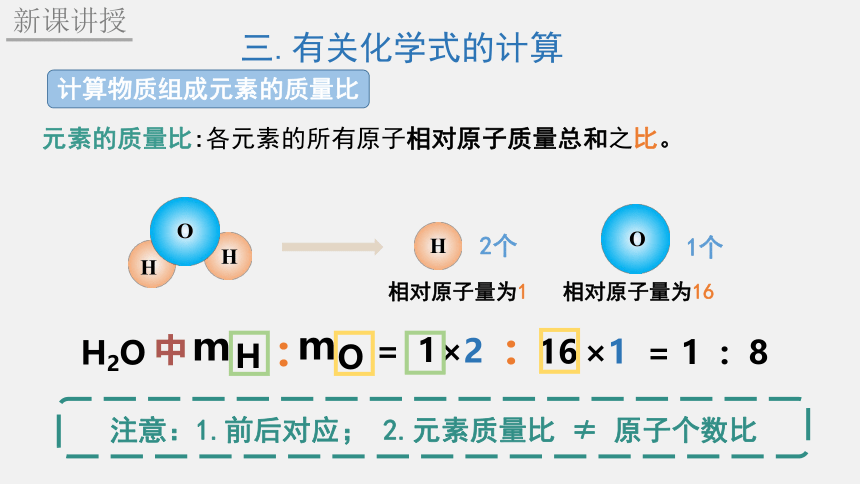
元素的质量比:各元素的所有原子相对原子质量总和之比。
H
H
O
H
O
相对原子量为1
相对原子量为16
2个
1个
H2O
= 1 : 8
1
×2
:
16
×1
H
O
中
m
m
:
=
注意:1.前后对应; 2.元素质量比 ≠ 原子个数比
三.有关化学式的计算
计算物质组成元素的质量比
新课讲授
1.硝酸铵(NH4NO3 )中,氮、氢、氧三种元素的质量比:
m(N) ∶ m(H) ∶ m(O)
=(14×2)∶ (1×4) ∶ (16×3)
= 7 ∶ 1 ∶ 12
2.氢氧化钙(Ca(OH)2 )中,钙、氢、氧三种元素的质量比:
m(Ca) ∶ m(H) ∶ m(O)
=(40×1)∶ (1×2) ∶ (16×2)
= 20 ∶ 16 ∶ 1
相对原子质量: H-1 N-14 O-16 Ca-40
新课讲授
三.有关化学式的计算
计算物质组成元素的质量比
相对分子质量
该元素的相对原子质量
×
该元素的原子个数
元素的质量分数
×
100%
=
元素的质量分数:该元素的质量与组成物质的元素总质量之比。
×100%
1
×2
1
×2
+
16
×1
×100%
H2O中氢元素的质量分数 =
=
新课讲授
三.有关化学式的计算
计算物质中某元素的质量分数
1.硝酸铵(NH4NO3 )中,氮元素的质量分数:
2.尿素(CO(NH2)2)中,氧元素的质量分数:
ω(O) =
16 × 1
12×1+16×1+14×2+1×4
×100%
ω(N) =
14 × 2
14×2+1×4+16×3
×100%
相对原子质量: H-1 C-12 N-14 O-16
新课讲授
三.有关化学式的计算
计算物质中某元素的质量分数
计算化合物中元素的质量比:
元素的质量比= (相对分子质量×原子个数)之比
计算化合物中某元素的质量分数:
某元素的质量分数
计算化合物中某元素的质量:某元素的质量=化合物的质量×
化合物中该元素的质量分数
物质的相对分子质量
该元素的相对原子质量
=
×
100%
×
该元素的原子个数
有关相对分子
质量的计算
计算相对分子质量:
相对分子质量=(相对原子质量×原子个数)之和
原子个数之比
课堂小结
课堂练习
1.某元素R的相对原子质量为32,在它的氧化物中,R显+6价,则该元素的氧化物的相对分子质量为( )
A. 48 B. 64 C. 80 D. 96
2.北京2008年第29届奥运会火炬是以符合环保要求的丙烷(C3H8)为燃料。请填写下列空格:
(1)丙烷的相对分子质量是________;
(2)丙烷分子中碳原子、氢原子的个数比是________;
(3)含有16 g氢元素的丙烷质量是________。
C
44
3:8
88g
课堂练习
3.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量。下列说法正确的是( )
A. K2Cr2O7中铬元素的化合价为+7
B. K2Cr2O7属于氧化物
C. C2H5OH的相对分子质量为46
D. C2H5OH中C、H、O的原子个数比为2∶5∶1
C
课堂练习
4.请根据资料回答下列问题:
(1)黑木耳中所含的铁是指______(填字母序号).
A.分子 B.原子 C.元素
(2)硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一,请根据其化学式计算:
①硫酸亚铁的相对分子质量为_______,
②硫酸亚铁中铁、硫、氧三种元素的质量比为_________;
③与200g干黑木耳中的铁元素质量相等的硫酸亚铁的质量为______mg.
C
152
7:4:8
532
课堂练习
5.在氧化物RO中含氧元素40%,则R的相对原子质量是( )
A.20 B.24 C.40 D.60
B
6.化肥对提高农作物的产量具有重要作用。硝酸铵(NH4NO3)是一种常见的氮肥。计算
(1)硝酸铵由_____种元素组成(填数字);
(2)硝酸铵中氮元素和氧元素的质量比为____(填最简比);
(3)若硝酸铵中含有2.8g氮元素,则该硝酸铵的质量为___g。
3
7:12
8
谢谢观看
第四单元 自然界的水
课题4 化学式与化合价
人教版
第三课时
1.会计算相对分子质量;
2.会计算化合物中各元素的质量比及某元素的质量分数;
3.能看懂某些商品标签或说明说明书上标示的物质含量。
教学目标
H
H
O
H
H
O
H2O
1个水分子是由 个氢原子和 个氧原子构成的。
1个水分子的质量= + 。
2
1
2个氢原子的质量
1个氧原子的质量
分子、原子质量都很小。为了方便,原子采用相对原子质量,那么分子呢?
相对分子质量
新课引入
相对分子质量:化学式中各原子的相对原子质量的总和,(符号为Mr)
H
H
O
H
O
相对原子量为1
相对原子量为16
Mr(H2O)=
= 18
1
×2
+
16
×1
2个
1个
g
关键:搞清楚组成元素的种类,及对应原子数目
H2O的相对分子质量=
相对分子质量也是比值,单位为1
三.有关化学式的计算
新课讲授
计算相对分子质量
相对原子质量: H-1 N-14 O-16 Al-27 S-32 K-39 Ca-40
1.计算 NH4NO3的相对分子质量
2.计算Al2(SO4)3的相对分子质量
Mr[Al2(SO4)3] = 27×2 + (32×1+16×4)×3
= 342
Mr[NH4NO3] = 14×2 + 1×4 + 16×3
= 80
3.计算KAl(SO4)2·12H2O的相对分子质量
Mr[KAl(SO4)2·12H2O] = 39 + 27 + (32+16×4)×2 + 12×(1×2+16)
= 474
三.有关化学式的计算
计算相对分子质量
新课讲授
元素的质量比:各元素的所有原子相对原子质量总和之比。
H
H
O
H
O
相对原子量为1
相对原子量为16
2个
1个
H2O
= 1 : 8
1
×2
:
16
×1
H
O
中
m
m
:
=
注意:1.前后对应; 2.元素质量比 ≠ 原子个数比
三.有关化学式的计算
计算物质组成元素的质量比
新课讲授
1.硝酸铵(NH4NO3 )中,氮、氢、氧三种元素的质量比:
m(N) ∶ m(H) ∶ m(O)
=(14×2)∶ (1×4) ∶ (16×3)
= 7 ∶ 1 ∶ 12
2.氢氧化钙(Ca(OH)2 )中,钙、氢、氧三种元素的质量比:
m(Ca) ∶ m(H) ∶ m(O)
=(40×1)∶ (1×2) ∶ (16×2)
= 20 ∶ 16 ∶ 1
相对原子质量: H-1 N-14 O-16 Ca-40
新课讲授
三.有关化学式的计算
计算物质组成元素的质量比
相对分子质量
该元素的相对原子质量
×
该元素的原子个数
元素的质量分数
×
100%
=
元素的质量分数:该元素的质量与组成物质的元素总质量之比。
×100%
1
×2
1
×2
+
16
×1
×100%
H2O中氢元素的质量分数 =
=
新课讲授
三.有关化学式的计算
计算物质中某元素的质量分数
1.硝酸铵(NH4NO3 )中,氮元素的质量分数:
2.尿素(CO(NH2)2)中,氧元素的质量分数:
ω(O) =
16 × 1
12×1+16×1+14×2+1×4
×100%
ω(N) =
14 × 2
14×2+1×4+16×3
×100%
相对原子质量: H-1 C-12 N-14 O-16
新课讲授
三.有关化学式的计算
计算物质中某元素的质量分数
计算化合物中元素的质量比:
元素的质量比= (相对分子质量×原子个数)之比
计算化合物中某元素的质量分数:
某元素的质量分数
计算化合物中某元素的质量:某元素的质量=化合物的质量×
化合物中该元素的质量分数
物质的相对分子质量
该元素的相对原子质量
=
×
100%
×
该元素的原子个数
有关相对分子
质量的计算
计算相对分子质量:
相对分子质量=(相对原子质量×原子个数)之和
原子个数之比
课堂小结
课堂练习
1.某元素R的相对原子质量为32,在它的氧化物中,R显+6价,则该元素的氧化物的相对分子质量为( )
A. 48 B. 64 C. 80 D. 96
2.北京2008年第29届奥运会火炬是以符合环保要求的丙烷(C3H8)为燃料。请填写下列空格:
(1)丙烷的相对分子质量是________;
(2)丙烷分子中碳原子、氢原子的个数比是________;
(3)含有16 g氢元素的丙烷质量是________。
C
44
3:8
88g
课堂练习
3.重铬酸钾(K2Cr2O7)可用于测定酒驾中的酒精(C2H5OH)含量。下列说法正确的是( )
A. K2Cr2O7中铬元素的化合价为+7
B. K2Cr2O7属于氧化物
C. C2H5OH的相对分子质量为46
D. C2H5OH中C、H、O的原子个数比为2∶5∶1
C
课堂练习
4.请根据资料回答下列问题:
(1)黑木耳中所含的铁是指______(填字母序号).
A.分子 B.原子 C.元素
(2)硫酸亚铁(FeSO4)是常见补铁类保健品中的有效成分之一,请根据其化学式计算:
①硫酸亚铁的相对分子质量为_______,
②硫酸亚铁中铁、硫、氧三种元素的质量比为_________;
③与200g干黑木耳中的铁元素质量相等的硫酸亚铁的质量为______mg.
C
152
7:4:8
532
课堂练习
5.在氧化物RO中含氧元素40%,则R的相对原子质量是( )
A.20 B.24 C.40 D.60
B
6.化肥对提高农作物的产量具有重要作用。硝酸铵(NH4NO3)是一种常见的氮肥。计算
(1)硝酸铵由_____种元素组成(填数字);
(2)硝酸铵中氮元素和氧元素的质量比为____(填最简比);
(3)若硝酸铵中含有2.8g氮元素,则该硝酸铵的质量为___g。
3
7:12
8
谢谢观看
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
