实验活动6 酸、碱的化学性质 同步练习 人教版化学九年级下册(含答案)
文档属性
| 名称 | 实验活动6 酸、碱的化学性质 同步练习 人教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 159.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-13 00:00:00 | ||
图片预览

文档简介
实验活动6 酸、碱的化学性质
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列关于硫酸的认识,正确的是
A.组成:硫酸溶液中H+和SO的数目相同
B.性质:能与CO2、SO3等非金属氧化物反应
C.用途:可用于实验室制备CuSO4等硫酸盐
D.生产:含硫酸废水用CaCl2处理后直接排放
2.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
3.小王同学往厨房的纯碱中滴加白醋,发现有气体生成。已知白醋里含3%~5%的醋酸(CH3COOH),醋酸与盐酸的化学性质相似,下列说法不正确的是
A.白醋里含有氢离子 B.生成的气体是二氧化碳
C.白醋能使紫色石蕊试液变红 D.白醋与纯碱的反应属于中和反应
4.下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的是
A.稀盐酸 B.二氧化碳 C.碳酸钙 D.石蕊溶液
5.下列化学方程式正确的是
A.
B.
C.
D.
6.下列“液体“中可能为纯净物的是
A.胃液
B.波尔多液
C.滤液
D.“84”消毒液
7.对下列事实的微观解释错误的是
A.氢氧化钠溶液能导电----溶液中存在自由移动的离子
B.汽油要密闭保存----分子不断运动
C.稀盐酸、稀硫酸均显酸性----溶液中都含有氢元素
D.金刚石和石墨的性质存在着明显差异----碳原子排列方式不同
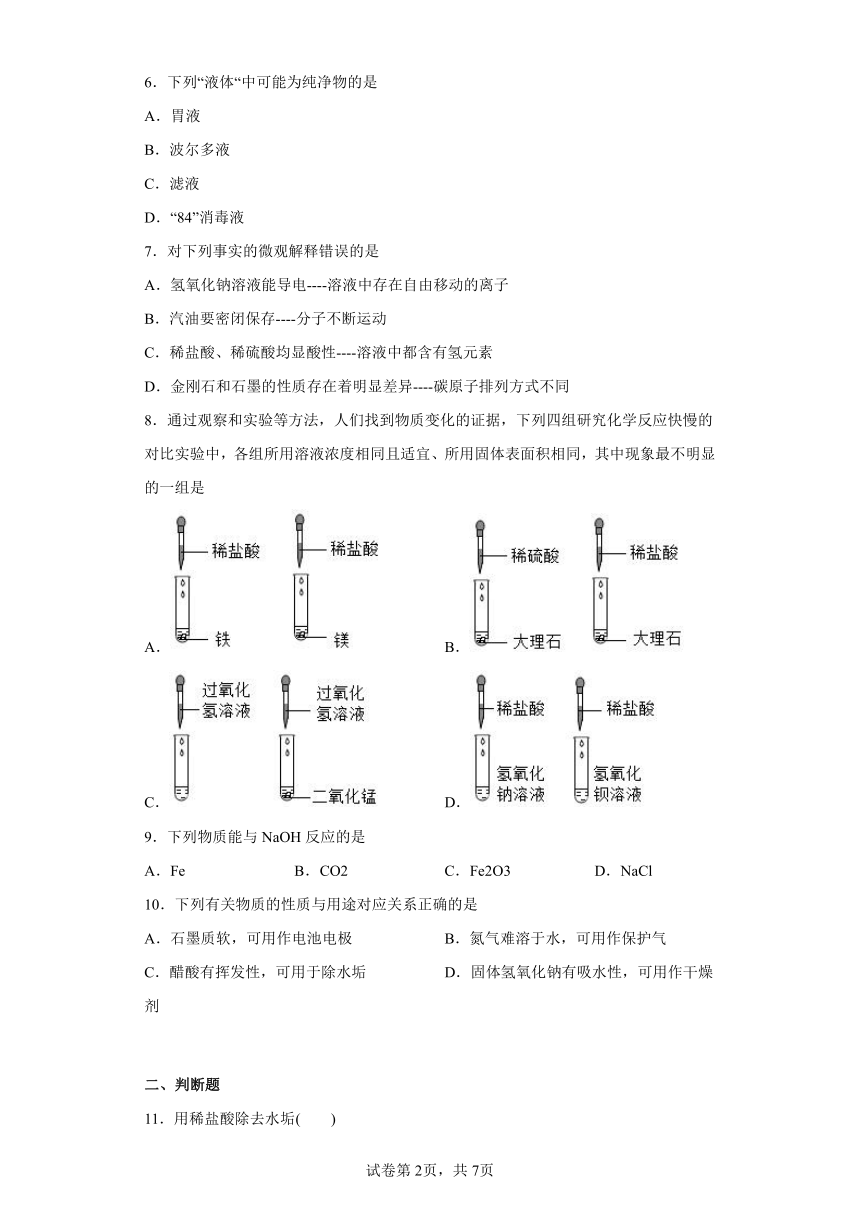
8.通过观察和实验等方法,人们找到物质变化的证据,下列四组研究化学反应快慢的对比实验中,各组所用溶液浓度相同且适宜、所用固体表面积相同,其中现象最不明显的一组是
A. B.
C. D.
9.下列物质能与NaOH反应的是
A.Fe B.CO2 C.Fe2O3 D.NaCl
10.下列有关物质的性质与用途对应关系正确的是
A.石墨质软,可用作电池电极 B.氮气难溶于水,可用作保护气
C.醋酸有挥发性,可用于除水垢 D.固体氢氧化钠有吸水性,可用作干燥剂
二、判断题
11.用稀盐酸除去水垢( )
12.CO2中含HCl,用NaOH溶液除去HCl。( )
13.稀盐酸、稀硫酸都能用于除锈( )
14.非金属氧化物和碱反应生成盐和水,所以可以用氢氧化钠溶液吸收CO( )
15.氧化铝和稀硫酸反应,固体逐渐溶解,溶液变为浅绿色( )
三、填空题
16.我国力争在2060年前实现“碳中和”(二氧化碳的排放与吸收平衡,实现“零排放”),保护环境。实现“碳中和”通常可采取如下措施:
(1)碳减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:,则X的化学式为______,B(OH)3中B的化合价为______。
(2)碳“捕捉”与封存:碳“捕捉”可用氢氧化钠溶液吸收空气中的二氧化碳,该反应的化学方程式为______。
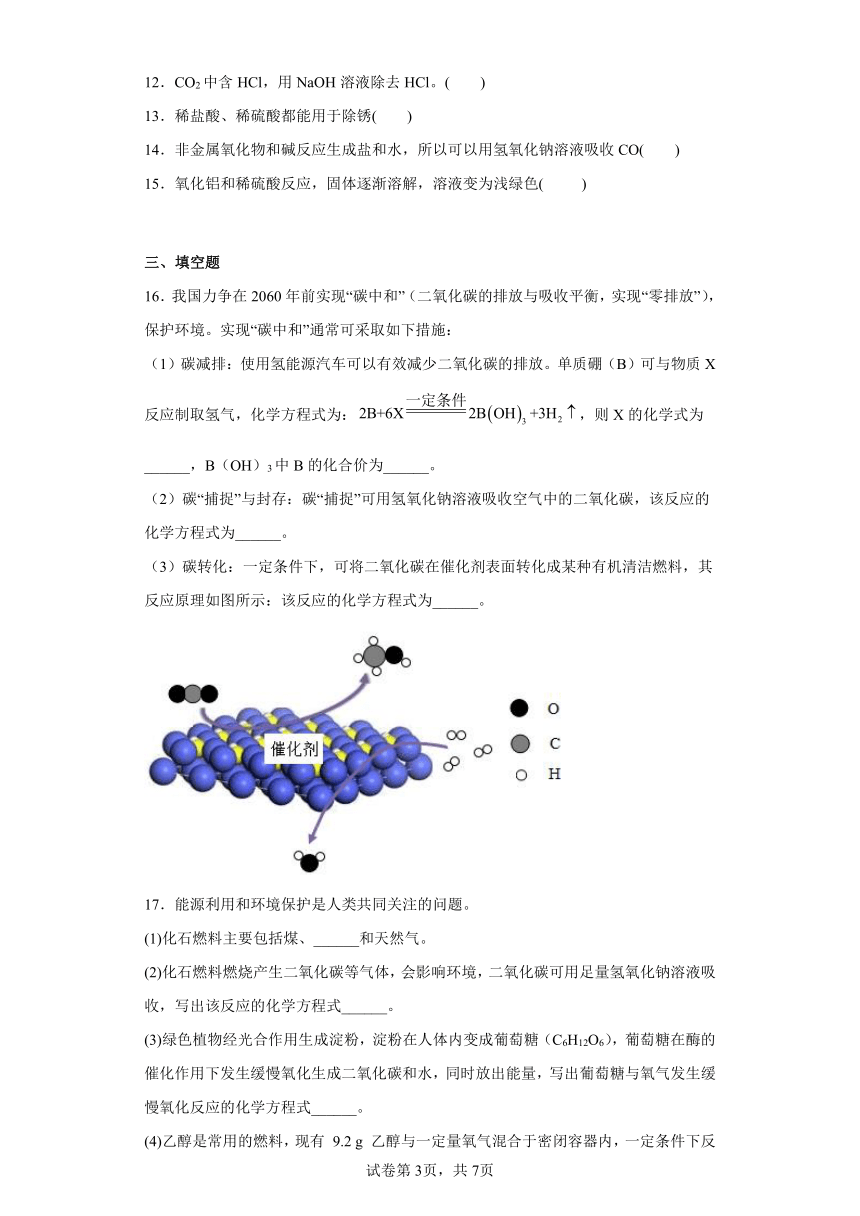
(3)碳转化:一定条件下,可将二氧化碳在催化剂表面转化成某种有机清洁燃料,其反应原理如图所示:该反应的化学方程式为______。
17.能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式______。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
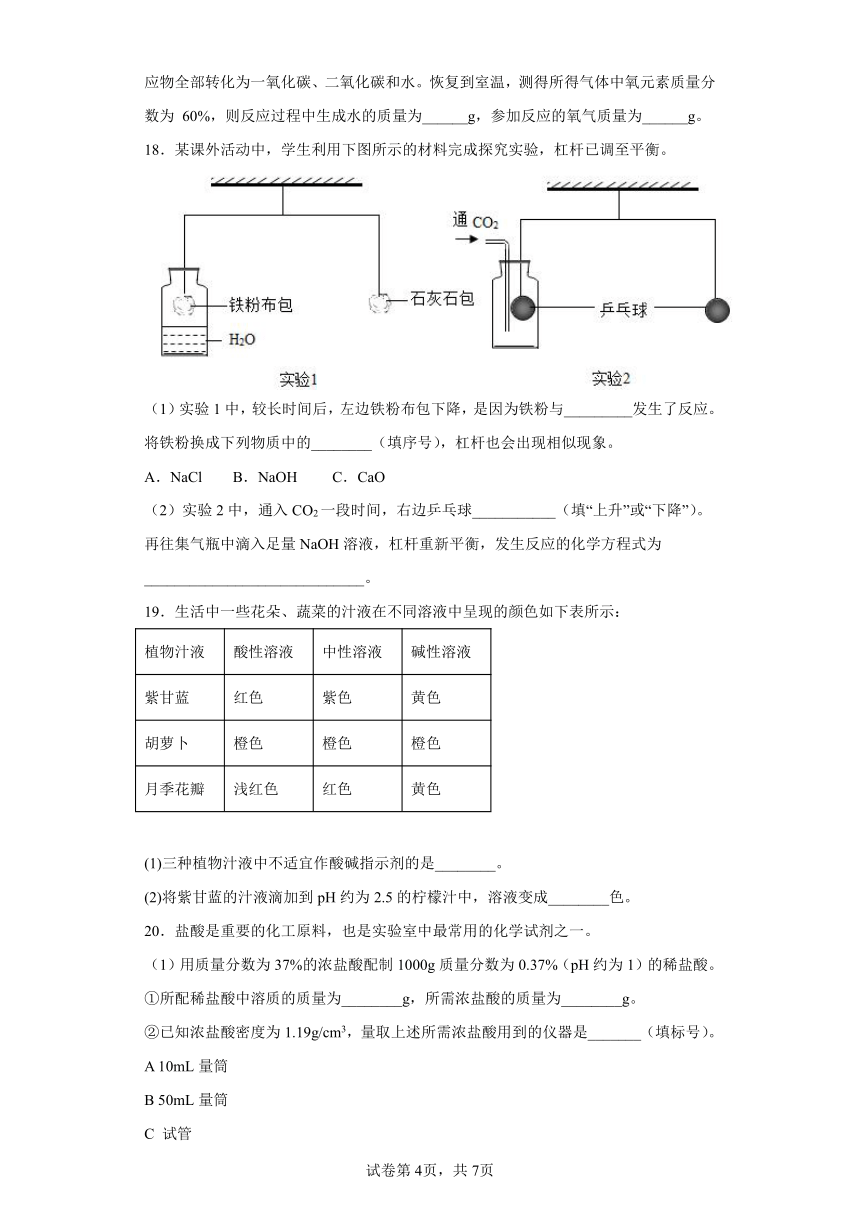
18.某课外活动中,学生利用下图所示的材料完成探究实验,杠杆已调至平衡。
(1)实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与_________发生了反应。将铁粉换成下列物质中的________(填序号),杠杆也会出现相似现象。
A.NaCl B.NaOH C.CaO
(2)实验2中,通入CO2一段时间,右边乒乓球___________(填“上升”或“下降”)。再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,发生反应的化学方程式为_____________________________。
19.生活中一些花朵、蔬菜的汁液在不同溶液中呈现的颜色如下表所示:
植物汁液 酸性溶液 中性溶液 碱性溶液
紫甘蓝 红色 紫色 黄色
胡萝卜 橙色 橙色 橙色
月季花瓣 浅红色 红色 黄色
(1)三种植物汁液中不适宜作酸碱指示剂的是________。
(2)将紫甘蓝的汁液滴加到pH约为2.5的柠檬汁中,溶液变成________色。
20.盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一。
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为________g,所需浓盐酸的质量为________g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是_______(填标号)。
A 10mL量筒
B 50mL量筒
C 试管
D 胶头滴管
③测定所配稀盐酸的酸碱度,应将pH试纸放置在__________上。
(2)取少量氢氧化钙粉末于试管中,加入2mL水,振荡,得到白色浑浊液,滴加1滴酚酞溶液,再滴加稀盐酸至反应完全,可观察到的现象是_________。
(3)取等质量的铁片和铁粉放入两支试管中,分别加入相同体积相同浓度的稀盐酸。
①铁与稀盐酸反应的化学方程式为________。
②下列示意图中,与实验结果相符的是_________(填标号)。
四、综合应用题
21.在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是________。
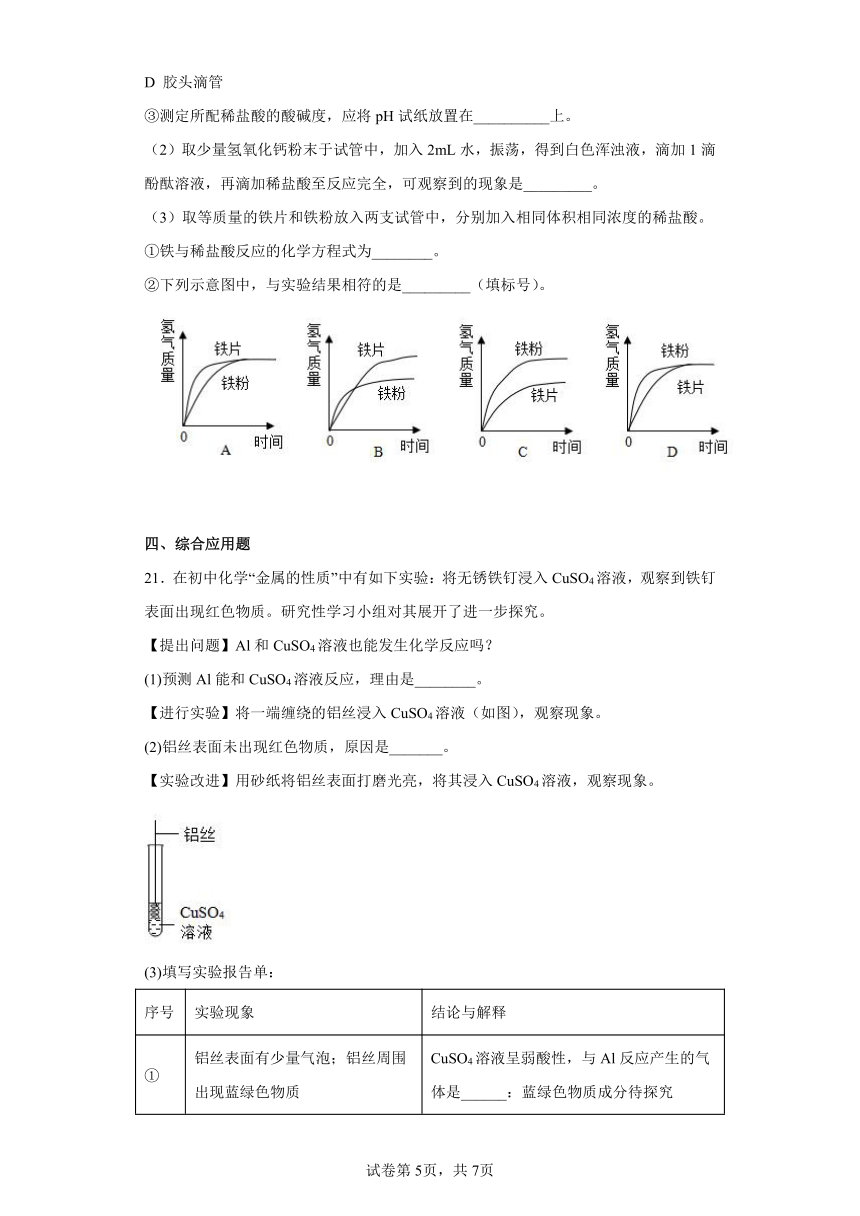
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
(2)铝丝表面未出现红色物质,原因是_______。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
序号 实验现象 结论与解释
① 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 CuSO4溶液呈弱酸性,与Al反应产生的气体是______:蓝绿色物质成分待探究
② 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 红色物质是_____,说明Al能和CuSO4溶液反应,但反应较慢
③ 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 反应生成的A12(SO4)3为无色;Al2(SO4)3溶液的密度____(填“>” 或“<”)CuSO4溶液
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为_______。
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是______。(填一种即可)
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是 (填序号)。A.食醋 B.食用油 C.面粉 D.咸菜
22.我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一、
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。
①捕捉室中NaOH溶液常喷成雾状,优点是_______。
②“反应分离”环节发生的复分解反应是_______(写化学方程式)。
③“反应分离”环节分离物质采用的方法是_______。
④CO2用途广泛,写出一种用途:_______。
(2)CaO固体也可以捕捉回收CO2.研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46g CaC2O4·H2O进行加热,固体质量随温度变化如下图。
①写出400~600℃范围内分解反应的化学方程式:_______。(CaC2O4·H2O的相对分子质量:146)
②据图分析,CaO捕捉CO2的反应温度应_______(填“高于”或“低于”)800℃。
23.酸碱盐在生活和生产中有广泛的应用。
(1)钠是人体必需的常量元素,它在人体内主要以_________形式存在。
A单质
B化合物
C离子
(2)根据生活经验推测,汗水中产生咸味的物质可能是____________(填化学式)。
(3)如图是浓盐酸试剂瓶上标签的部分内容。请回答:
①现要配制9%的稀盐酸160g,需要这种浓盐酸_______g。
②打开一段时间后,浓盐酸的溶质质量分数小于36%,原因是__________。
(4)为除去粗盐中CaCl2、MgCl2、Na2SO4、可溶性杂质,需进行如下操作:①溶解;②过量的Na2CO3溶液;③过量的NaOH溶液;④过量的BaCl2溶液;⑤过滤;⑥加适量稀盐酸;⑦蒸发、结晶。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀]
Ⅰ.写出此过程的正确操作顺序____________。
Ⅱ.写出此过程中加入过量Na2CO3溶液的目的_____________。
Ⅲ.经过提纯后得到NaCl固体的质量大于原样品中NaCl的质量,试分析其原因_____________。
(5)将一定量的Na2CO3溶液与50g稀盐酸混合,恰好完全反应,反应后测得溶液的总质量减少了4.4 g。求稀盐酸中溶质的质量分数_________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.D
4.D
5.A
6.C
7.C
8.D
9.B
10.D
11.正确
12.错误
13.正确
14.错误
15.错误
16.H2O +3
17.(1)石油
(2)
(3)
(4) 10.8 13.6
18.水和氧气(或H2O和O2) BC 下降 CO2+2NaOH===Na2CO3+H2O
19.胡萝卜 红
20.3.7 10 AD 玻璃片或白瓷板 溶液由红色变成无色 D
21.(1)Al比Cu活泼
(2)铝丝表面有一层致密的氧化铝膜
(3) H2##氢气 Cu##铜 <
(4)
(5)NaCl、CuCl2等
(6)AD
22.增大NaOH溶液与CO2气体的接触面积,使吸收CO2更充分、更快速 过滤 气体肥料/人工降雨 低于
23.C NaCl 40 浓盐酸具有挥发性 ①③④②⑤⑥⑦(或①④②③⑤⑥⑦或①④③②⑤⑥⑦) 除去溶液中的CaCl2及过量的BaCl2 在粗盐提纯的过程中有NaCl生成 14. 6%
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列关于硫酸的认识,正确的是
A.组成:硫酸溶液中H+和SO的数目相同
B.性质:能与CO2、SO3等非金属氧化物反应
C.用途:可用于实验室制备CuSO4等硫酸盐
D.生产:含硫酸废水用CaCl2处理后直接排放
2.稀HCl和NaOH溶液混合后无明显现象,要证明两者已发生化学反应,如图操作及实验现象(或结果),不能证明反应发生的是
A.在混合液中加金属Zn,无气泡产生
B.在混合液中加无色酚酞,溶液呈无色的
C.在混合液中加AgNO3溶液,有白色沉淀
D.用pH试纸测混合液的pH,测得pH等于7
3.小王同学往厨房的纯碱中滴加白醋,发现有气体生成。已知白醋里含3%~5%的醋酸(CH3COOH),醋酸与盐酸的化学性质相似,下列说法不正确的是
A.白醋里含有氢离子 B.生成的气体是二氧化碳
C.白醋能使紫色石蕊试液变红 D.白醋与纯碱的反应属于中和反应
4.下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的是
A.稀盐酸 B.二氧化碳 C.碳酸钙 D.石蕊溶液
5.下列化学方程式正确的是
A.
B.
C.
D.
6.下列“液体“中可能为纯净物的是
A.胃液
B.波尔多液
C.滤液
D.“84”消毒液
7.对下列事实的微观解释错误的是
A.氢氧化钠溶液能导电----溶液中存在自由移动的离子
B.汽油要密闭保存----分子不断运动
C.稀盐酸、稀硫酸均显酸性----溶液中都含有氢元素
D.金刚石和石墨的性质存在着明显差异----碳原子排列方式不同
8.通过观察和实验等方法,人们找到物质变化的证据,下列四组研究化学反应快慢的对比实验中,各组所用溶液浓度相同且适宜、所用固体表面积相同,其中现象最不明显的一组是
A. B.
C. D.
9.下列物质能与NaOH反应的是
A.Fe B.CO2 C.Fe2O3 D.NaCl
10.下列有关物质的性质与用途对应关系正确的是
A.石墨质软,可用作电池电极 B.氮气难溶于水,可用作保护气
C.醋酸有挥发性,可用于除水垢 D.固体氢氧化钠有吸水性,可用作干燥剂
二、判断题
11.用稀盐酸除去水垢( )
12.CO2中含HCl,用NaOH溶液除去HCl。( )
13.稀盐酸、稀硫酸都能用于除锈( )
14.非金属氧化物和碱反应生成盐和水,所以可以用氢氧化钠溶液吸收CO( )
15.氧化铝和稀硫酸反应,固体逐渐溶解,溶液变为浅绿色( )
三、填空题
16.我国力争在2060年前实现“碳中和”(二氧化碳的排放与吸收平衡,实现“零排放”),保护环境。实现“碳中和”通常可采取如下措施:
(1)碳减排:使用氢能源汽车可以有效减少二氧化碳的排放。单质硼(B)可与物质X反应制取氢气,化学方程式为:,则X的化学式为______,B(OH)3中B的化合价为______。
(2)碳“捕捉”与封存:碳“捕捉”可用氢氧化钠溶液吸收空气中的二氧化碳,该反应的化学方程式为______。
(3)碳转化:一定条件下,可将二氧化碳在催化剂表面转化成某种有机清洁燃料,其反应原理如图所示:该反应的化学方程式为______。
17.能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式______。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
18.某课外活动中,学生利用下图所示的材料完成探究实验,杠杆已调至平衡。
(1)实验1中,较长时间后,左边铁粉布包下降,是因为铁粉与_________发生了反应。将铁粉换成下列物质中的________(填序号),杠杆也会出现相似现象。
A.NaCl B.NaOH C.CaO
(2)实验2中,通入CO2一段时间,右边乒乓球___________(填“上升”或“下降”)。再往集气瓶中滴入足量NaOH溶液,杠杆重新平衡,发生反应的化学方程式为_____________________________。
19.生活中一些花朵、蔬菜的汁液在不同溶液中呈现的颜色如下表所示:
植物汁液 酸性溶液 中性溶液 碱性溶液
紫甘蓝 红色 紫色 黄色
胡萝卜 橙色 橙色 橙色
月季花瓣 浅红色 红色 黄色
(1)三种植物汁液中不适宜作酸碱指示剂的是________。
(2)将紫甘蓝的汁液滴加到pH约为2.5的柠檬汁中,溶液变成________色。
20.盐酸是重要的化工原料,也是实验室中最常用的化学试剂之一。
(1)用质量分数为37%的浓盐酸配制1000g质量分数为0.37%(pH约为1)的稀盐酸。
①所配稀盐酸中溶质的质量为________g,所需浓盐酸的质量为________g。
②已知浓盐酸密度为1.19g/cm3,量取上述所需浓盐酸用到的仪器是_______(填标号)。
A 10mL量筒
B 50mL量筒
C 试管
D 胶头滴管
③测定所配稀盐酸的酸碱度,应将pH试纸放置在__________上。
(2)取少量氢氧化钙粉末于试管中,加入2mL水,振荡,得到白色浑浊液,滴加1滴酚酞溶液,再滴加稀盐酸至反应完全,可观察到的现象是_________。
(3)取等质量的铁片和铁粉放入两支试管中,分别加入相同体积相同浓度的稀盐酸。
①铁与稀盐酸反应的化学方程式为________。
②下列示意图中,与实验结果相符的是_________(填标号)。
四、综合应用题
21.在初中化学“金属的性质”中有如下实验:将无锈铁钉浸入CuSO4溶液,观察到铁钉表面出现红色物质。研究性学习小组对其展开了进一步探究。
【提出问题】Al和CuSO4溶液也能发生化学反应吗?
(1)预测Al能和CuSO4溶液反应,理由是________。
【进行实验】将一端缠绕的铝丝浸入CuSO4溶液(如图),观察现象。
(2)铝丝表面未出现红色物质,原因是_______。
【实验改进】用砂纸将铝丝表面打磨光亮,将其浸入CuSO4溶液,观察现象。
(3)填写实验报告单:
序号 实验现象 结论与解释
① 铝丝表面有少量气泡;铝丝周围出现蓝绿色物质 CuSO4溶液呈弱酸性,与Al反应产生的气体是______:蓝绿色物质成分待探究
② 24h后,铝丝仍光亮;48h后,铝丝表面出现少量红色物质 红色物质是_____,说明Al能和CuSO4溶液反应,但反应较慢
③ 铝丝周围溶液逐渐变成无色,铝丝以下溶液仍为蓝色;两层溶液界面清晰 反应生成的A12(SO4)3为无色;Al2(SO4)3溶液的密度____(填“>” 或“<”)CuSO4溶液
【深入探究】为研究上述异常现象,同学们查阅了相关资料,继续开展探究。
资料:①Cu2(OH)2SO4呈蓝绿色,不溶于水;②Cl-可加快铝丝和其他物质的反应速率。
(4)取出铝丝,将试管中的混合物分离得到蓝绿色固体。加入稀硫酸,固体溶解形成蓝色溶液,该反应的化学方程式为_______。
(5)欲加快Al和CuSO4溶液的反应,可加入的物质是______。(填一种即可)
【拓展应用】通过探究,同学们提出了铝制品使用的注意事项。
(6)下列食品不能长时间用铝制炊具盛放的是 (填序号)。A.食醋 B.食用油 C.面粉 D.咸菜
22.我国将力争2060年前实现碳中和。CO2的捕捉是减少碳排放的措施之一、
(1)一种利用NaOH溶液捕捉回收CO2的过程如图所示。
①捕捉室中NaOH溶液常喷成雾状,优点是_______。
②“反应分离”环节发生的复分解反应是_______(写化学方程式)。
③“反应分离”环节分离物质采用的方法是_______。
④CO2用途广泛,写出一种用途:_______。
(2)CaO固体也可以捕捉回收CO2.研究表明CaC2O4·H2O热分解制得的CaO疏松多孔,具有良好的CO2捕捉性能。取1.46g CaC2O4·H2O进行加热,固体质量随温度变化如下图。
①写出400~600℃范围内分解反应的化学方程式:_______。(CaC2O4·H2O的相对分子质量:146)
②据图分析,CaO捕捉CO2的反应温度应_______(填“高于”或“低于”)800℃。
23.酸碱盐在生活和生产中有广泛的应用。
(1)钠是人体必需的常量元素,它在人体内主要以_________形式存在。
A单质
B化合物
C离子
(2)根据生活经验推测,汗水中产生咸味的物质可能是____________(填化学式)。
(3)如图是浓盐酸试剂瓶上标签的部分内容。请回答:
①现要配制9%的稀盐酸160g,需要这种浓盐酸_______g。
②打开一段时间后,浓盐酸的溶质质量分数小于36%,原因是__________。
(4)为除去粗盐中CaCl2、MgCl2、Na2SO4、可溶性杂质,需进行如下操作:①溶解;②过量的Na2CO3溶液;③过量的NaOH溶液;④过量的BaCl2溶液;⑤过滤;⑥加适量稀盐酸;⑦蒸发、结晶。[提示:Mg(OH)2、BaSO4、BaCO3难溶于水;微溶物不形成沉淀]
Ⅰ.写出此过程的正确操作顺序____________。
Ⅱ.写出此过程中加入过量Na2CO3溶液的目的_____________。
Ⅲ.经过提纯后得到NaCl固体的质量大于原样品中NaCl的质量,试分析其原因_____________。
(5)将一定量的Na2CO3溶液与50g稀盐酸混合,恰好完全反应,反应后测得溶液的总质量减少了4.4 g。求稀盐酸中溶质的质量分数_________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.D
4.D
5.A
6.C
7.C
8.D
9.B
10.D
11.正确
12.错误
13.正确
14.错误
15.错误
16.H2O +3
17.(1)石油
(2)
(3)
(4) 10.8 13.6
18.水和氧气(或H2O和O2) BC 下降 CO2+2NaOH===Na2CO3+H2O
19.胡萝卜 红
20.3.7 10 AD 玻璃片或白瓷板 溶液由红色变成无色 D
21.(1)Al比Cu活泼
(2)铝丝表面有一层致密的氧化铝膜
(3) H2##氢气 Cu##铜 <
(4)
(5)NaCl、CuCl2等
(6)AD
22.增大NaOH溶液与CO2气体的接触面积,使吸收CO2更充分、更快速 过滤 气体肥料/人工降雨 低于
23.C NaCl 40 浓盐酸具有挥发性 ①③④②⑤⑥⑦(或①④②③⑤⑥⑦或①④③②⑤⑥⑦) 除去溶液中的CaCl2及过量的BaCl2 在粗盐提纯的过程中有NaCl生成 14. 6%
答案第1页,共2页
答案第1页,共2页
同课章节目录
