【粤教版】化学九年级上册 5.2组成燃料的的主要元素---碳 课件(共17张PPT)
文档属性
| 名称 | 【粤教版】化学九年级上册 5.2组成燃料的的主要元素---碳 课件(共17张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-14 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
5.2 组成燃料的主要元素---碳
新课导学
中国文化源远流长,中国书法博大精深,是中华民族的瑰宝,是世界艺林的奇葩。几千年来,无数优秀书法作品把我国历史天空装点得绚烂辉煌!我国古代一些书法家用墨书写的字画历经了几百年甚至几千年,纸和布都已经破损,但其中的字画仍不变色,这说明了什么问题
金刚石和石墨
1.同一种元素可以组成不同的物质
白磷
红磷
金刚石
石墨
金刚石和石墨
2.根据物质的用途推断物质的性质
金刚石和石墨的应用 特性推断
无色透明的金刚石
深灰色金属光泽、 不透明的的片状石 墨固体
铅笔芯是用石墨粉 和黏土混合物制成
划玻璃刀头上镶一小粒金刚石,用来刻划玻璃
质硬(天然存在最硬的物质)
检测石墨电极芯的导电性
导电性强
比较6H和6B铅笔的软硬性能(信息提示:6B铅笔芯有较多石墨粉,6H铅笔芯含较多黏土)
6B铅笔芯色黑,质地软而滑腻
金刚石和石墨
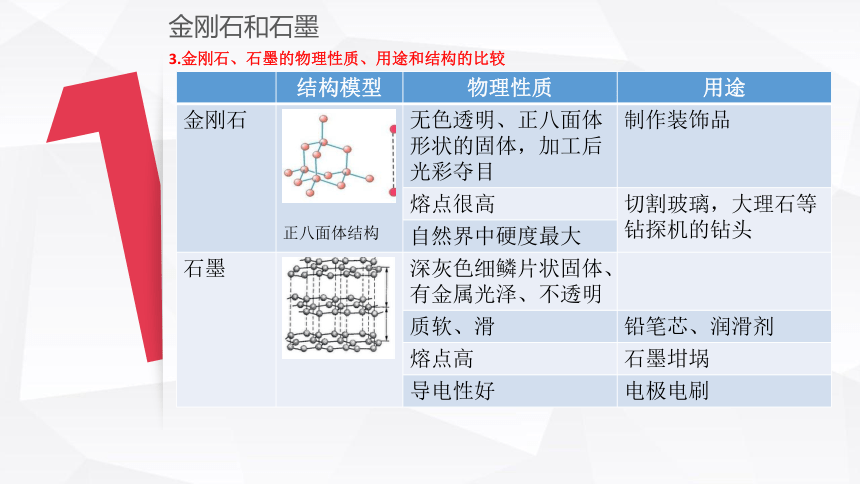
3.金刚石、石墨的物理性质、用途和结构的比较
结构模型 物理性质 用途
金刚石 正八面体结构 无色透明、正八面体形状的固体,加工后光彩夺目 制作装饰品
熔点很高 切割玻璃,大理石等钻探机的钻头
自然界中硬度最大 石墨 深灰色细鳞片状固体、有金属光泽、不透明
质软、滑 铅笔芯、润滑剂
熔点高 石墨坩埚
导电性好 电极电刷
金刚石和石墨
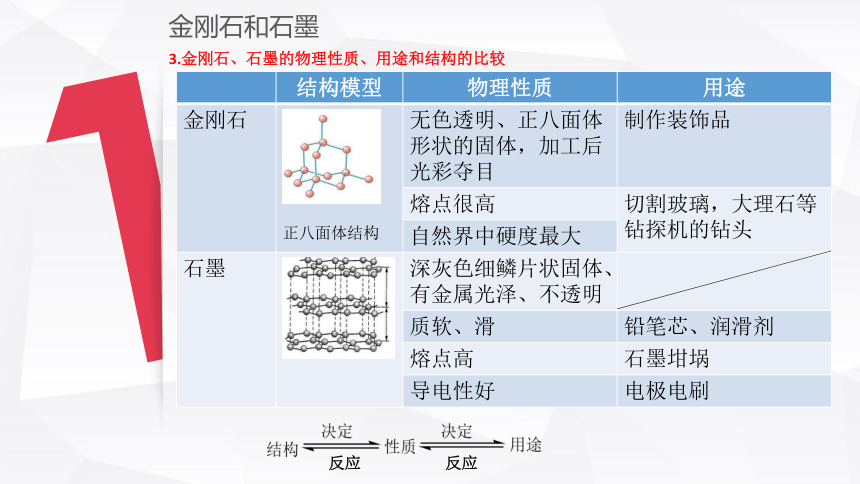
3.金刚石、石墨的物理性质、用途和结构的比较
结构模型 物理性质 用途
金刚石 正八面体结构 无色透明、正八面体形状的固体,加工后光彩夺目 制作装饰品
熔点很高 切割玻璃,大理石等钻探机的钻头
自然界中硬度最大 石墨 深灰色细鳞片状固体、有金属光泽、不透明
质软、滑 铅笔芯、润滑剂
熔点高 石墨坩埚
导电性好 电极电刷
反应
反应
金刚石和石墨
4.各种碳单质物理性质差异的原因
金刚石和石墨都是由碳元素组成的单质,但由于碳原子排列方式不同,所以两者物理性质有很大差异
无定型碳
1.木炭、活性炭、焦炭和炭黑的对比
无定形碳包括木炭、活性炭、焦炭、炭黑,它们都是由石墨的微小晶体和少量杂质构成的,无固定几何外形,所以叫无定形碳。
颜色、状态 制法 用途
木炭 灰黑色的多孔状固体 木材隔绝空气加强热 作燃料、冶炼金属、制黑火药、制活性炭等
活性炭 灰黑色多孔颗粒状固体 木炭在高温下用水蒸气处理 可净化多种气体和液体、制作防毒面具等
焦炭 浅灰色多孔状固体 烟煤隔绝空气加强热 冶炼金属等
炭黑 极细的黑色粉末 含碳物质不完全燃烧 制造油墨、油漆、鞋油、颜料等作橡胶制品的填料等
无定型碳
2.探究木炭、活性炭的吸附性
实验 在盛有半瓶水的小锥形瓶中,加入一滴红墨水,使水略显红色。投入几块烘烤过的木炭(或活性炭),轻轻振荡锥形瓶
现象 红色变为无色
分析 木炭具有疏松多孔的结构,具有吸附能力,色素被吸附在孔的表面
要点 (1)木炭、活性炭的吸附性是物理性质,吸附过程中发生的变化是物理变化
(2)活性炭结构孔内表面积比木炭大,吸附能力比木炭强
(3)吸附能力与物质的表面积有关表面积越大,吸附能力越强
无定型碳
3.碳单质的最新进展
结构 性质 用途
C60 稳定 应用于超导、催化、材料、医学及生物等领域
碳纳米管 机械强度高、导电性好 应用于材料、催化、信息等诸多领域中
单层石墨片 优异的导电、导热性 用途广泛
4.“碳”与“炭”的比较
含义 举例
碳 是指碳元素(即核电荷数为6的一类原子的总称),用来描述物质的组成 如二氧化碳、一氧化碳、碳酸钙等
炭 是指具体物质 如木炭、炭黑、焦炭和活性炭等
无定型碳
5.各种碳单质的性质和用途
木炭
活性
焦炭
炭黑
金刚石
石墨
制造油墨、墨汁
冶炼金属
用作防毒面具
制黑火药
用作电池的电极芯
地质勘测钻头
还原性
吸附性
导电性
硬度大
可燃性
常温下化学性质稳定
碳单质的化学性质
碳元素的单质物理性质差异很大,这是由于它们内部碳原子的排列方式不同。但参加化学反应的碳原子是相同的,故它们的化学性质相似。
1.常温下化学性质稳定
常温下,碳的化学性质稳定。中国古代字画大多是用墨(墨的主要成分是炭黑)书写或绘制的,历经千年而不褪色,是因为碳在常温下化学性质稳定。
碳单质的化学性质
2.碳与氧气反应
炭在点燃情况下可以与氧气反应,产生白光,放出热量,生成二氧化碳气体。但如果氧气不足,会发生不完全燃烧,生成一氧化碳。
碳发生不完全燃烧时,产生的热量远小于完全燃烧,这是对能源的浪费,因此要防止不完全燃烧的发生。同时,生成的一氧化碳有毒,是环境的污染性气体之一。从这个角度看,也应该防止不完全燃烧的发生。
比较事项 完全燃烧 不完全燃烧
燃烧条件 有充足的氧气 氧气不充足
燃烧速度 快 慢
释放热量 多 少
燃烧效率 高 低
以炭的燃烧为例
启示 从获取能量和保护环境等方面都体现了燃料完全燃烧的重要性 3.完全燃烧与不完全燃烧的比较
碳单质的化学性质
4.炽热的碳还能使二氧化碳还原成一氧化碳
5.注意事项
(1)CO与H2一样在与空气(或氧气)混合时,遇明火可能发生爆炸,因此点燃一氧化碳前必须验纯。
(2)因为CO有毒,排到空气中会污染大气,因此在用一氧化碳做实验时,一定要注意尾气处理装置。
一氧化碳(CO)
1.CO的物理性质
一氧化碳是无色、无味、难溶于水的气体,通常情况下密度略小于空气。
2.CO的可燃性
实验现象 ①一氧化碳燃烧火焰呈浅蓝色;
②烧杯内壁澄清石灰水变浑浊
分析 一氧化碳点燃时生成了二氧化碳,澄清石灰水遇二氧化碳变浑浊
(1)有人用炉火取暖,为防止煤
气中毒,在火炉上放一盆水,这样做行吗
(2)有人说他身强力壮,不会煤气中毒,等到一闻到煤气味就把火炉搬出去,这样做行吗
一氧化碳(CO)
3.CO的毒性
4.证明某气体是CO的方法
(1)CO能与血液中的血红蛋白结合,使之丧失输氧能力,人体因缺氧而室息死亡,是化学变化。
(2)冬天房间里用煤或木炭取暖时应该保持室内的空气流通。
(3)家用煤气中常常会添加一些具有难闻气味的气体(如乙硫醇)是为了让人们易于察觉一氧化碳泄,以免一氧化碳中毒。
(4)如发生煤气泄漏应迅速关上煤气总开关,打开门窗,并且不要使用家里的任何电器。
点燃待检测气体,先用干冷的小烧杯罩在火焰上方,无水珠,再用内壁涂有澄清石灰水的小烧杯罩在上方,若出现白色浑浊物,则该气体为CO。
感谢聆听
5.2 组成燃料的主要元素---碳
新课导学
中国文化源远流长,中国书法博大精深,是中华民族的瑰宝,是世界艺林的奇葩。几千年来,无数优秀书法作品把我国历史天空装点得绚烂辉煌!我国古代一些书法家用墨书写的字画历经了几百年甚至几千年,纸和布都已经破损,但其中的字画仍不变色,这说明了什么问题
金刚石和石墨
1.同一种元素可以组成不同的物质
白磷
红磷
金刚石
石墨
金刚石和石墨
2.根据物质的用途推断物质的性质
金刚石和石墨的应用 特性推断
无色透明的金刚石
深灰色金属光泽、 不透明的的片状石 墨固体
铅笔芯是用石墨粉 和黏土混合物制成
划玻璃刀头上镶一小粒金刚石,用来刻划玻璃
质硬(天然存在最硬的物质)
检测石墨电极芯的导电性
导电性强
比较6H和6B铅笔的软硬性能(信息提示:6B铅笔芯有较多石墨粉,6H铅笔芯含较多黏土)
6B铅笔芯色黑,质地软而滑腻
金刚石和石墨
3.金刚石、石墨的物理性质、用途和结构的比较
结构模型 物理性质 用途
金刚石 正八面体结构 无色透明、正八面体形状的固体,加工后光彩夺目 制作装饰品
熔点很高 切割玻璃,大理石等钻探机的钻头
自然界中硬度最大 石墨 深灰色细鳞片状固体、有金属光泽、不透明
质软、滑 铅笔芯、润滑剂
熔点高 石墨坩埚
导电性好 电极电刷
金刚石和石墨
3.金刚石、石墨的物理性质、用途和结构的比较
结构模型 物理性质 用途
金刚石 正八面体结构 无色透明、正八面体形状的固体,加工后光彩夺目 制作装饰品
熔点很高 切割玻璃,大理石等钻探机的钻头
自然界中硬度最大 石墨 深灰色细鳞片状固体、有金属光泽、不透明
质软、滑 铅笔芯、润滑剂
熔点高 石墨坩埚
导电性好 电极电刷
反应
反应
金刚石和石墨
4.各种碳单质物理性质差异的原因
金刚石和石墨都是由碳元素组成的单质,但由于碳原子排列方式不同,所以两者物理性质有很大差异
无定型碳
1.木炭、活性炭、焦炭和炭黑的对比
无定形碳包括木炭、活性炭、焦炭、炭黑,它们都是由石墨的微小晶体和少量杂质构成的,无固定几何外形,所以叫无定形碳。
颜色、状态 制法 用途
木炭 灰黑色的多孔状固体 木材隔绝空气加强热 作燃料、冶炼金属、制黑火药、制活性炭等
活性炭 灰黑色多孔颗粒状固体 木炭在高温下用水蒸气处理 可净化多种气体和液体、制作防毒面具等
焦炭 浅灰色多孔状固体 烟煤隔绝空气加强热 冶炼金属等
炭黑 极细的黑色粉末 含碳物质不完全燃烧 制造油墨、油漆、鞋油、颜料等作橡胶制品的填料等
无定型碳
2.探究木炭、活性炭的吸附性
实验 在盛有半瓶水的小锥形瓶中,加入一滴红墨水,使水略显红色。投入几块烘烤过的木炭(或活性炭),轻轻振荡锥形瓶
现象 红色变为无色
分析 木炭具有疏松多孔的结构,具有吸附能力,色素被吸附在孔的表面
要点 (1)木炭、活性炭的吸附性是物理性质,吸附过程中发生的变化是物理变化
(2)活性炭结构孔内表面积比木炭大,吸附能力比木炭强
(3)吸附能力与物质的表面积有关表面积越大,吸附能力越强
无定型碳
3.碳单质的最新进展
结构 性质 用途
C60 稳定 应用于超导、催化、材料、医学及生物等领域
碳纳米管 机械强度高、导电性好 应用于材料、催化、信息等诸多领域中
单层石墨片 优异的导电、导热性 用途广泛
4.“碳”与“炭”的比较
含义 举例
碳 是指碳元素(即核电荷数为6的一类原子的总称),用来描述物质的组成 如二氧化碳、一氧化碳、碳酸钙等
炭 是指具体物质 如木炭、炭黑、焦炭和活性炭等
无定型碳
5.各种碳单质的性质和用途
木炭
活性
焦炭
炭黑
金刚石
石墨
制造油墨、墨汁
冶炼金属
用作防毒面具
制黑火药
用作电池的电极芯
地质勘测钻头
还原性
吸附性
导电性
硬度大
可燃性
常温下化学性质稳定
碳单质的化学性质
碳元素的单质物理性质差异很大,这是由于它们内部碳原子的排列方式不同。但参加化学反应的碳原子是相同的,故它们的化学性质相似。
1.常温下化学性质稳定
常温下,碳的化学性质稳定。中国古代字画大多是用墨(墨的主要成分是炭黑)书写或绘制的,历经千年而不褪色,是因为碳在常温下化学性质稳定。
碳单质的化学性质
2.碳与氧气反应
炭在点燃情况下可以与氧气反应,产生白光,放出热量,生成二氧化碳气体。但如果氧气不足,会发生不完全燃烧,生成一氧化碳。
碳发生不完全燃烧时,产生的热量远小于完全燃烧,这是对能源的浪费,因此要防止不完全燃烧的发生。同时,生成的一氧化碳有毒,是环境的污染性气体之一。从这个角度看,也应该防止不完全燃烧的发生。
比较事项 完全燃烧 不完全燃烧
燃烧条件 有充足的氧气 氧气不充足
燃烧速度 快 慢
释放热量 多 少
燃烧效率 高 低
以炭的燃烧为例
启示 从获取能量和保护环境等方面都体现了燃料完全燃烧的重要性 3.完全燃烧与不完全燃烧的比较
碳单质的化学性质
4.炽热的碳还能使二氧化碳还原成一氧化碳
5.注意事项
(1)CO与H2一样在与空气(或氧气)混合时,遇明火可能发生爆炸,因此点燃一氧化碳前必须验纯。
(2)因为CO有毒,排到空气中会污染大气,因此在用一氧化碳做实验时,一定要注意尾气处理装置。
一氧化碳(CO)
1.CO的物理性质
一氧化碳是无色、无味、难溶于水的气体,通常情况下密度略小于空气。
2.CO的可燃性
实验现象 ①一氧化碳燃烧火焰呈浅蓝色;
②烧杯内壁澄清石灰水变浑浊
分析 一氧化碳点燃时生成了二氧化碳,澄清石灰水遇二氧化碳变浑浊
(1)有人用炉火取暖,为防止煤
气中毒,在火炉上放一盆水,这样做行吗
(2)有人说他身强力壮,不会煤气中毒,等到一闻到煤气味就把火炉搬出去,这样做行吗
一氧化碳(CO)
3.CO的毒性
4.证明某气体是CO的方法
(1)CO能与血液中的血红蛋白结合,使之丧失输氧能力,人体因缺氧而室息死亡,是化学变化。
(2)冬天房间里用煤或木炭取暖时应该保持室内的空气流通。
(3)家用煤气中常常会添加一些具有难闻气味的气体(如乙硫醇)是为了让人们易于察觉一氧化碳泄,以免一氧化碳中毒。
(4)如发生煤气泄漏应迅速关上煤气总开关,打开门窗,并且不要使用家里的任何电器。
点燃待检测气体,先用干冷的小烧杯罩在火焰上方,无水珠,再用内壁涂有澄清石灰水的小烧杯罩在上方,若出现白色浑浊物,则该气体为CO。
感谢聆听
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
