第七单元常见的酸和碱测试题(有答案)
图片预览



文档简介
第七单元 常见的酸和碱 测试题
一、单选题
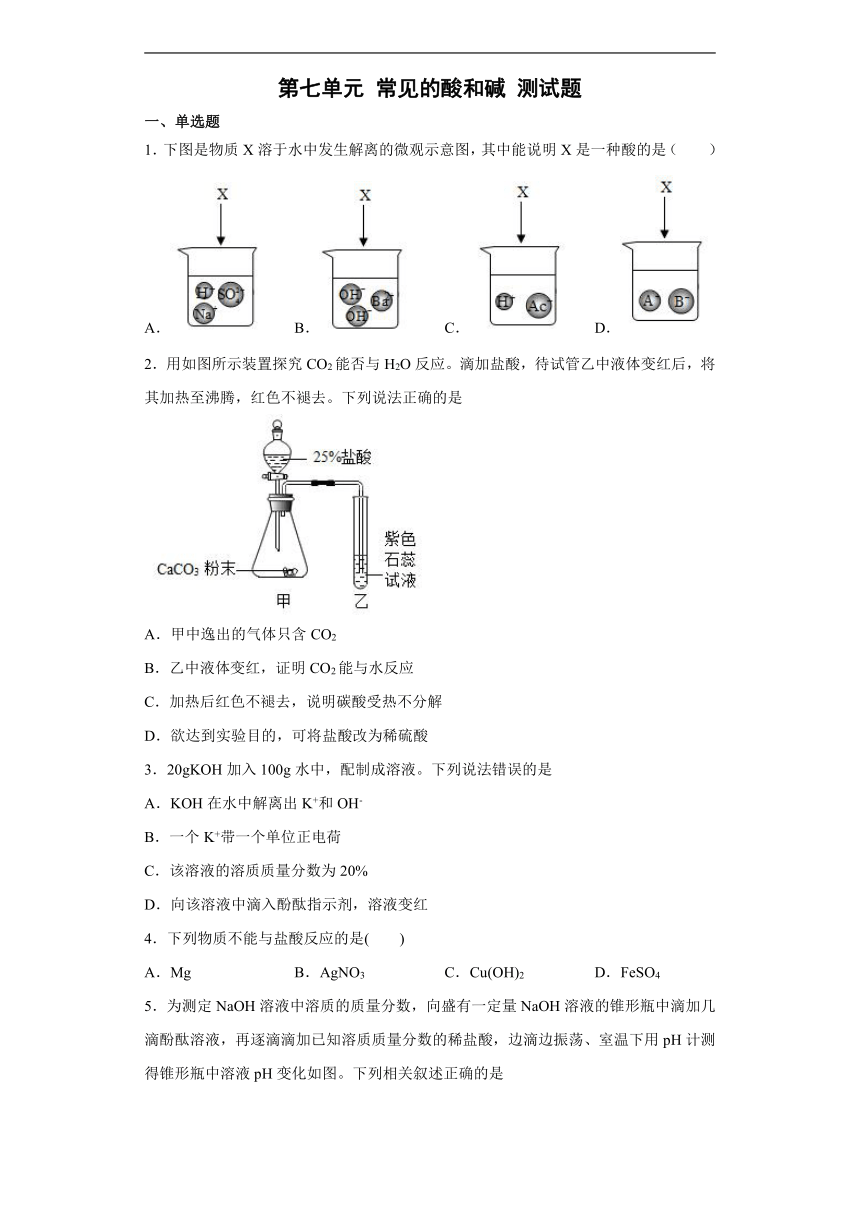
1.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A. B. C. D.
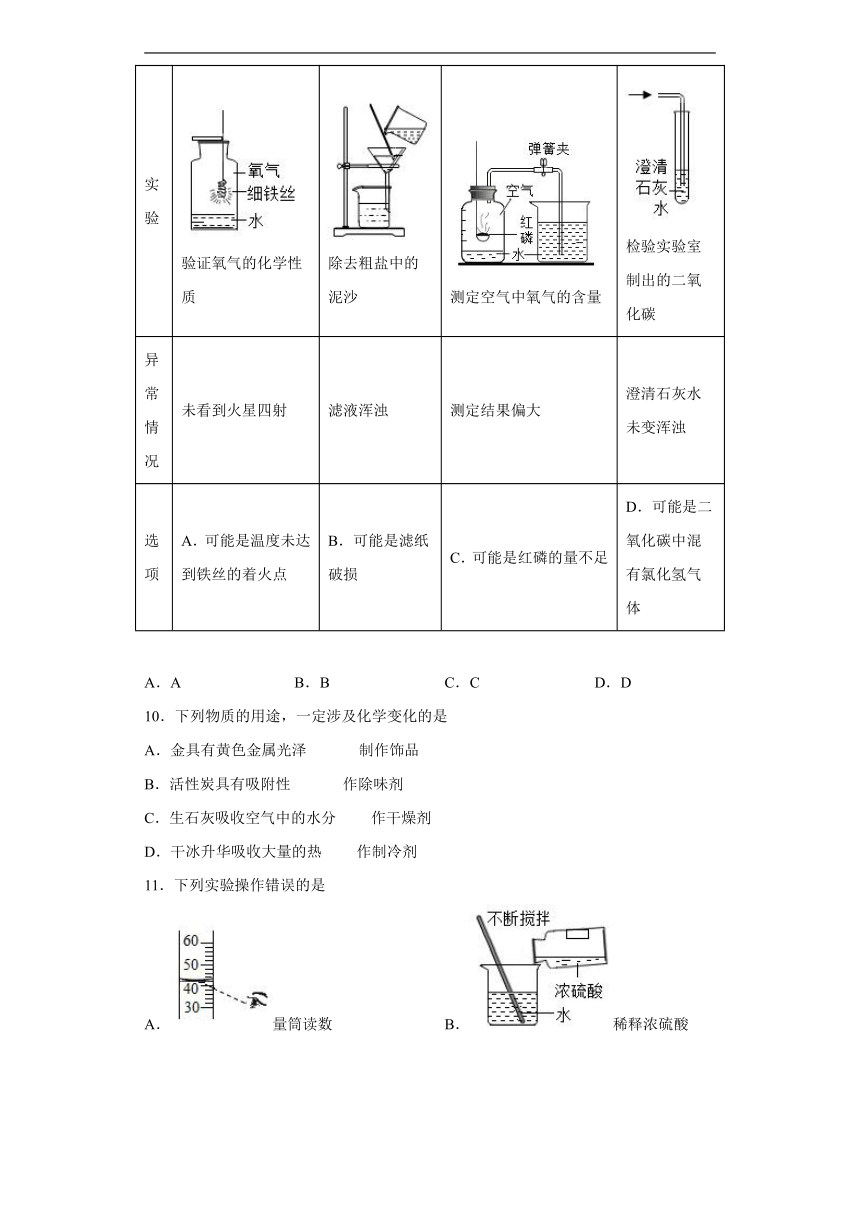
2.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
3.20gKOH加入100g水中,配制成溶液。下列说法错误的是
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
4.下列物质不能与盐酸反应的是( )
A.Mg B.AgNO3 C.Cu(OH)2 D.FeSO4
5.为测定NaOH溶液中溶质的质量分数,向盛有一定量NaOH溶液的锥形瓶中滴加几滴酚酞溶液,再逐滴滴加已知溶质质量分数的稀盐酸,边滴边振荡、室温下用pH计测得锥形瓶中溶液pH变化如图。下列相关叙述正确的是
A.锥形瓶中溶液为无色时其pH=7
B.a点溶液能使紫色石蕊溶液变红
C.b点时盐酸与NaOH恰好完全反应
D.c点溶液的溶质有NaCl和NaOH
6.元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价类二维图”,下列说法错误的是
A.A点对应的物质一定是金刚石
B.B点对应的物质与C点对应的物质可以相互转化
C.D点对应的物质很不稳定,容易分解
D.E点对应的物质可能是K2CO3
7.有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
8.下列实验操作或对意外事故的处理方法错误的
A.取液后的胶头滴管平放于实验台上
B.实验时,应穿好实验服,戴好防护眼镜
C.点燃氢气等可燃性气体前一定要检验其纯度
D.若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
9.化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
10.下列物质的用途,一定涉及化学变化的是
A.金具有黄色金属光泽 制作饰品
B.活性炭具有吸附性 作除味剂
C.生石灰吸收空气中的水分 作干燥剂
D.干冰升华吸收大量的热 作制冷剂
11.下列实验操作错误的是
A.量筒读数 B.稀释浓硫酸
C.滴加液体 D.过滤
12.下列关于氢氧化钠的描述中不正确的是
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
13.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO、CO D.H+、SO、CO
14.下列溶液酸性最强的是
A.pH=1 B.pH=5 C.pH=7 D.pH=14
15.下列关于硫酸的认识,正确的是
A.组成:硫酸溶液中H+和SO的数目相同
B.性质:能与CO2、SO3等非金属氧化物反应
C.用途:可用于实验室制备CuSO4等硫酸盐
D.生产:含硫酸废水用CaCl2处理后直接排放
二、填空题
16.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
n(H+)与n(OH-)的相对大小 溶液的酸碱性
n(H+)>n(OH-) 酸性
n(H+)=n(OH-) 中性
n(H+)<n(OH-) 碱性
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)______n(OH-)(填“>”或“=”或“<”,下同)。
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是____________,原因是该溶液中n(H+)______n(OH-)。
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)______n(OH-)。
17.在“宏观—微观-符号”之间建立联系,是化学学科特有的思维方式。请回答下列问题:
(1)从宏观角度看,地壳中含量最高的金属元素是____(写元素符号);从微观角度看,构成甲烷的分子符号是_____;硫酸亚铁中含有的阳离子是_____(写离子符号);氢氧化钠与盐酸发生中和反应的实质是____。
(2)某反应的微观示意图如下图所示。
①已知氟的元素符号为F(氟单质是气体),写出此反应的化学方程式_____。
②从微观、宏观任选一个角度简述,该反应前后____未发生改变。
18.能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式______。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
19.学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为____________。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为__________,属于___________(填基本反应类型)反应。
(4)图中⑤处应补充的文字是___________________(写一种,不能与图中已有信息重复)。
三、推断题
20.A~E是五种不同类别的常见物质:铁、二氧化碳、氢氧化钙、氯化铜、硫酸中的某一种,B常用于中和酸性土壤,E属于酸类物质,它们之间的相互关系如图所示(其中实线表示物质间可以相互反应,虚线表示物质间不能反应)。请回答下列问题:
(1)E的化学式为_____,B与E反应的化学方程式为__________,该反应的类型是_____。
(2)C和D反应的化学方程式为_______________。
(3)虚线相邻物质间存在转化关系的是__________。(填化学式)
21.如图所示,是初中化学常见的物质,和可发生中和反应,常用作食品干燥剂,为单质.根据图示回答下列问题.
(1)的俗称为______.
(2)的化学式为______.
(3)反应②的化学方程式为______.
四、实验题
22.用氢氧化钠溶液、稀盐酸和酚酞溶液按下图步骤进行实验。
回答下列问题:
(1)无色溶液A是________________,仪器C的名称是________;
(2)实验中滴入酚酞溶液的目的是________________________________;
(3)实验中反应的化学方程式是________________________________;
(4)步骤⑤的操作名称是____________,当出现较多量固体时应__________________________;
(5)实验步骤②和③两次使用了滴管,用完后需要洗涤的是________(填“②”或“③”)。
23.在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。
请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是_____。
(2)能产生气泡的是_____(填字母序号)。
(3)写出C烧杯中反应的化学方程式_____。
(4)D烧杯中,溶液由红色变为_____色,说明盐酸与氢氧化钠发生了反应。
五、计算题
24.实验室配制了 50 g 溶质质量分数为 8%的氢氧化钠溶液,将上述配制好的溶液分成 5 份,向其中一份中加入稀硫酸,随着稀硫酸的滴加,溶液的温度变化如图所示。试回答:
(1)C 点溶液中的阴离子是______。
(2)恰好完全反应时所得溶液中溶质的质量分数。
25.某造纸厂排放含NaOH的废水200吨,恰好需要含溶质4.9吨的硫酸溶液中和处理,求该废水中NaOH的溶质质量分数。
参考答案:
1.C 2.D 3.C 4.D 5.C 6.A 7.D 8.A 9.C 10.C 11.A 12.C 13.B 14.A 15.C
16. = 溶液变红 < >
17.(1) Al CH4 Fe2+ 氢离子与氢氧根离子结合生成水分子(或“H+和OH-结合生成H2O”或“H++OH-=H2O”)
(2) 元素种类(“原子的种类”或“原子的数目”或“氢元素化合价”)
18.(1)石油
(2)
(3)
(4) 10.8 13.6
19. ④⑥ 复分解 金属氧化物+酸(或非金属氧化物+碱)
20. H2SO4 Ca(OH)2+H2SO4=CaSO4+2H2O 复分解反应
Fe+CuCl2=FeCl2+Cu H2SO4→CO2
21. 熟石灰(或消石灰)
22. 氢氧化钠溶液 酒精灯 证明盐酸能与氢氧化钠发生化学反应
HCl+NaOH===NaCl+H2O 蒸发结晶 停止加热,用余热蒸干滤液 ③
23. 在金属活动性顺序表中铜排在氢的后面 BE 无
24.(1)SO42-
(2)参加反应的氢氧化钠的质量:,恰好完全反应时所得溶液的质量:+20g=30g;
设反应后所得溶液中溶质的质量分数为x
x≈4.7 3%
答:恰好完全反应时所得溶液中溶质的质量分数为4.7 3%。
25.解:设该废水中NaOH的溶质质量分数为x
x=2%
答:该废水中NaOH的溶质质量分数为2%。
一、单选题
1.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
A. B. C. D.
2.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
3.20gKOH加入100g水中,配制成溶液。下列说法错误的是
A.KOH在水中解离出K+和OH-
B.一个K+带一个单位正电荷
C.该溶液的溶质质量分数为20%
D.向该溶液中滴入酚酞指示剂,溶液变红
4.下列物质不能与盐酸反应的是( )
A.Mg B.AgNO3 C.Cu(OH)2 D.FeSO4
5.为测定NaOH溶液中溶质的质量分数,向盛有一定量NaOH溶液的锥形瓶中滴加几滴酚酞溶液,再逐滴滴加已知溶质质量分数的稀盐酸,边滴边振荡、室温下用pH计测得锥形瓶中溶液pH变化如图。下列相关叙述正确的是
A.锥形瓶中溶液为无色时其pH=7
B.a点溶液能使紫色石蕊溶液变红
C.b点时盐酸与NaOH恰好完全反应
D.c点溶液的溶质有NaCl和NaOH
6.元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是碳元素的“价类二维图”,下列说法错误的是
A.A点对应的物质一定是金刚石
B.B点对应的物质与C点对应的物质可以相互转化
C.D点对应的物质很不稳定,容易分解
D.E点对应的物质可能是K2CO3
7.有关中和反应的说法一定正确的是( )
A.反应物均须溶于水 B.有沉淀生成
C.有气体生成 D.有盐生成
8.下列实验操作或对意外事故的处理方法错误的
A.取液后的胶头滴管平放于实验台上
B.实验时,应穿好实验服,戴好防护眼镜
C.点燃氢气等可燃性气体前一定要检验其纯度
D.若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,再涂上3%~5%的碳酸氢钠溶液
9.化学实验中常会出现一些“出乎意料”的现象或结果,下列各项对相关异常情况的解释不合理的是
实验 验证氧气的化学性质 除去粗盐中的泥沙 测定空气中氧气的含量 检验实验室制出的二氧化碳
异常情况 未看到火星四射 滤液浑浊 测定结果偏大 澄清石灰水未变浑浊
选项 A.可能是温度未达到铁丝的着火点 B.可能是滤纸破损 C.可能是红磷的量不足 D.可能是二氧化碳中混有氯化氢气体
A.A B.B C.C D.D
10.下列物质的用途,一定涉及化学变化的是
A.金具有黄色金属光泽 制作饰品
B.活性炭具有吸附性 作除味剂
C.生石灰吸收空气中的水分 作干燥剂
D.干冰升华吸收大量的热 作制冷剂
11.下列实验操作错误的是
A.量筒读数 B.稀释浓硫酸
C.滴加液体 D.过滤
12.下列关于氢氧化钠的描述中不正确的是
A.曝露在空气中易潮解 B.能与酸发生中和反应
C.其水溶液能使石蕊溶液变红 D.对皮肤有强烈的腐蚀作用
13.河道两旁有甲、乙两厂,它们排放的工业废水中共含有H+、Na+、Ba2+、Cl-、SO、CO六种离子。两厂废水中各含三种离子,其中甲厂的废水明显呈酸性,甲厂废水中的离子是( )
A.H+、Na+、Ba2+ B.H+、Ba2+、Cl-
C.Na+、SO、CO D.H+、SO、CO
14.下列溶液酸性最强的是
A.pH=1 B.pH=5 C.pH=7 D.pH=14
15.下列关于硫酸的认识,正确的是
A.组成:硫酸溶液中H+和SO的数目相同
B.性质:能与CO2、SO3等非金属氧化物反应
C.用途:可用于实验室制备CuSO4等硫酸盐
D.生产:含硫酸废水用CaCl2处理后直接排放
二、填空题
16.经测定,在任何水溶液中,均存在一定数量的H+〔用n(H+)表示〕和一定数量的OH-〔用n(OH-)表示〕,n(H+)与n(OH-)的相对大小对应溶液的酸碱性如表所示:
n(H+)与n(OH-)的相对大小 溶液的酸碱性
n(H+)>n(OH-) 酸性
n(H+)=n(OH-) 中性
n(H+)<n(OH-) 碱性
据此分析
(1)常温下测得水中pH=7,可知水中n(H+)______n(OH-)(填“>”或“=”或“<”,下同)。
(2)向盛有碳酸钠溶液的试管中滴入几滴酚酞,现象是____________,原因是该溶液中n(H+)______n(OH-)。
(3)往上述试管中再滴入适量的硫酸氢钠溶液,溶液颜色褪去,说明硫酸氢钠溶液中n(H+)______n(OH-)。
17.在“宏观—微观-符号”之间建立联系,是化学学科特有的思维方式。请回答下列问题:
(1)从宏观角度看,地壳中含量最高的金属元素是____(写元素符号);从微观角度看,构成甲烷的分子符号是_____;硫酸亚铁中含有的阳离子是_____(写离子符号);氢氧化钠与盐酸发生中和反应的实质是____。
(2)某反应的微观示意图如下图所示。
①已知氟的元素符号为F(氟单质是气体),写出此反应的化学方程式_____。
②从微观、宏观任选一个角度简述,该反应前后____未发生改变。
18.能源利用和环境保护是人类共同关注的问题。
(1)化石燃料主要包括煤、______和天然气。
(2)化石燃料燃烧产生二氧化碳等气体,会影响环境,二氧化碳可用足量氢氧化钠溶液吸收,写出该反应的化学方程式______。
(3)绿色植物经光合作用生成淀粉,淀粉在人体内变成葡萄糖(C6H12O6),葡萄糖在酶的催化作用下发生缓慢氧化生成二氧化碳和水,同时放出能量,写出葡萄糖与氧气发生缓慢氧化反应的化学方程式______。
(4)乙醇是常用的燃料,现有 9.2 g 乙醇与一定量氧气混合于密闭容器内,一定条件下反应物全部转化为一氧化碳、二氧化碳和水。恢复到室温,测得所得气体中氧元素质量分数为 60%,则反应过程中生成水的质量为______g,参加反应的氧气质量为______g。
19.学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为____________。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)若盐是硝酸铜,则由⑦来实现的化学方程式为__________,属于___________(填基本反应类型)反应。
(4)图中⑤处应补充的文字是___________________(写一种,不能与图中已有信息重复)。
三、推断题
20.A~E是五种不同类别的常见物质:铁、二氧化碳、氢氧化钙、氯化铜、硫酸中的某一种,B常用于中和酸性土壤,E属于酸类物质,它们之间的相互关系如图所示(其中实线表示物质间可以相互反应,虚线表示物质间不能反应)。请回答下列问题:
(1)E的化学式为_____,B与E反应的化学方程式为__________,该反应的类型是_____。
(2)C和D反应的化学方程式为_______________。
(3)虚线相邻物质间存在转化关系的是__________。(填化学式)
21.如图所示,是初中化学常见的物质,和可发生中和反应,常用作食品干燥剂,为单质.根据图示回答下列问题.
(1)的俗称为______.
(2)的化学式为______.
(3)反应②的化学方程式为______.
四、实验题
22.用氢氧化钠溶液、稀盐酸和酚酞溶液按下图步骤进行实验。
回答下列问题:
(1)无色溶液A是________________,仪器C的名称是________;
(2)实验中滴入酚酞溶液的目的是________________________________;
(3)实验中反应的化学方程式是________________________________;
(4)步骤⑤的操作名称是____________,当出现较多量固体时应__________________________;
(5)实验步骤②和③两次使用了滴管,用完后需要洗涤的是________(填“②”或“③”)。
23.在学习了酸的化学性质之后,某实验小组选用稀盐酸做了如下图所示实验。
请回答下列问题:
(1)A烧杯中,铜不与稀盐酸发生反应的原因是_____。
(2)能产生气泡的是_____(填字母序号)。
(3)写出C烧杯中反应的化学方程式_____。
(4)D烧杯中,溶液由红色变为_____色,说明盐酸与氢氧化钠发生了反应。
五、计算题
24.实验室配制了 50 g 溶质质量分数为 8%的氢氧化钠溶液,将上述配制好的溶液分成 5 份,向其中一份中加入稀硫酸,随着稀硫酸的滴加,溶液的温度变化如图所示。试回答:
(1)C 点溶液中的阴离子是______。
(2)恰好完全反应时所得溶液中溶质的质量分数。
25.某造纸厂排放含NaOH的废水200吨,恰好需要含溶质4.9吨的硫酸溶液中和处理,求该废水中NaOH的溶质质量分数。
参考答案:
1.C 2.D 3.C 4.D 5.C 6.A 7.D 8.A 9.C 10.C 11.A 12.C 13.B 14.A 15.C
16. = 溶液变红 < >
17.(1) Al CH4 Fe2+ 氢离子与氢氧根离子结合生成水分子(或“H+和OH-结合生成H2O”或“H++OH-=H2O”)
(2) 元素种类(“原子的种类”或“原子的数目”或“氢元素化合价”)
18.(1)石油
(2)
(3)
(4) 10.8 13.6
19. ④⑥ 复分解 金属氧化物+酸(或非金属氧化物+碱)
20. H2SO4 Ca(OH)2+H2SO4=CaSO4+2H2O 复分解反应
Fe+CuCl2=FeCl2+Cu H2SO4→CO2
21. 熟石灰(或消石灰)
22. 氢氧化钠溶液 酒精灯 证明盐酸能与氢氧化钠发生化学反应
HCl+NaOH===NaCl+H2O 蒸发结晶 停止加热,用余热蒸干滤液 ③
23. 在金属活动性顺序表中铜排在氢的后面 BE 无
24.(1)SO42-
(2)参加反应的氢氧化钠的质量:,恰好完全反应时所得溶液的质量:+20g=30g;
设反应后所得溶液中溶质的质量分数为x
x≈4.7 3%
答:恰好完全反应时所得溶液中溶质的质量分数为4.7 3%。
25.解:设该废水中NaOH的溶质质量分数为x
x=2%
答:该废水中NaOH的溶质质量分数为2%。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
