2022-2023学年上学期高一化学人教版(2019)必修第一册4.2.元素周期律 教学课件(17张ppt)
文档属性
| 名称 | 2022-2023学年上学期高一化学人教版(2019)必修第一册4.2.元素周期律 教学课件(17张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-17 00:00:00 | ||
图片预览



文档简介
第二节 元素周期律
元素性质的周期性变化规律
元素周期表和元素周期律的应用
通过对碱金属元素、卤素的原子结构和性质的研究,我们已经知道元素周期表中同主族元素的性质有着相似性和递变性。那么,周期表中同周期元素的性质有什么变化规律呢?
新课导入
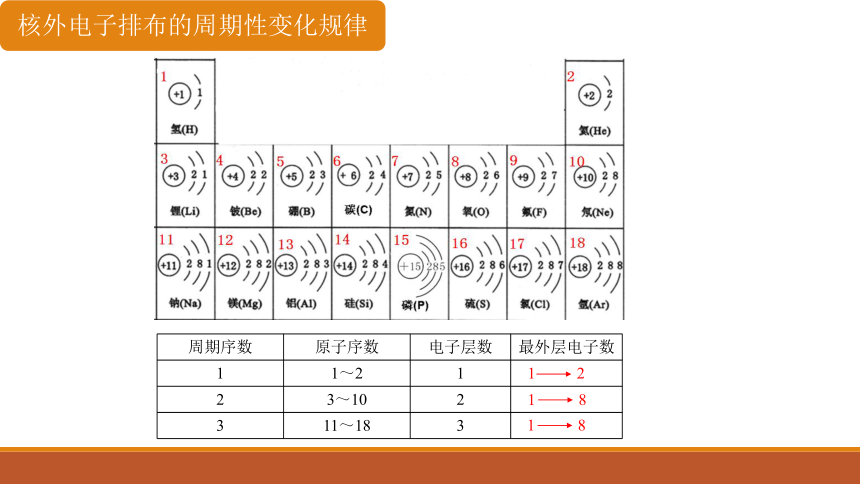
周期序数 原子序数 电子层数 最外层电子数
1 1~2 1
2 3~10 2
3 11~18 3
1
2
1
8
1
8
核外电子排布的周期性变化规律
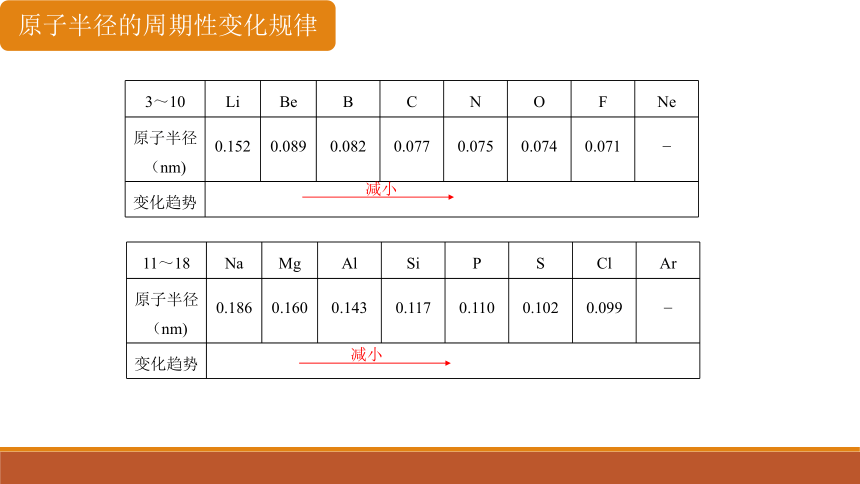
3~10 Li Be B C N O F Ne
原子半径 (nm) 0.152 0.089 0.082 0.077 0.075 0.074 0.071 _
变化趋势 11~18 Na Mg Al Si P S Cl Ar
原子半径 (nm) 0.186 0.160 0.143 0.117 0.110 0.102 0.099 _
变化趋势 减小
减小
原子半径的周期性变化规律
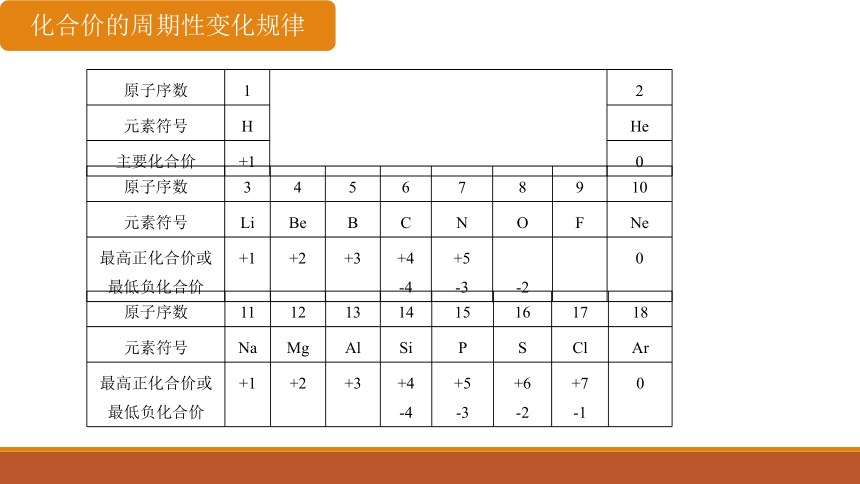
原子序数 3 4 5 6 7 8 9 10
元素符号 Li Be B C N O F Ne
最高正化合价或最低负化合价 +1 +2 +3 +4 -4 +5 -3 -2 0
原子序数 11 12 13 14 15 16 17 18
元素符号 Na Mg Al Si P S Cl Ar
最高正化合价或最低负化合价 +1 +2 +3 +4 -4 +5 -3 +6 -2 +7 -1 0
化合价的周期性变化规律
原子序数 1 2
元素符号 H He
主要化合价 +1 0
元素性质的周期性变化规律
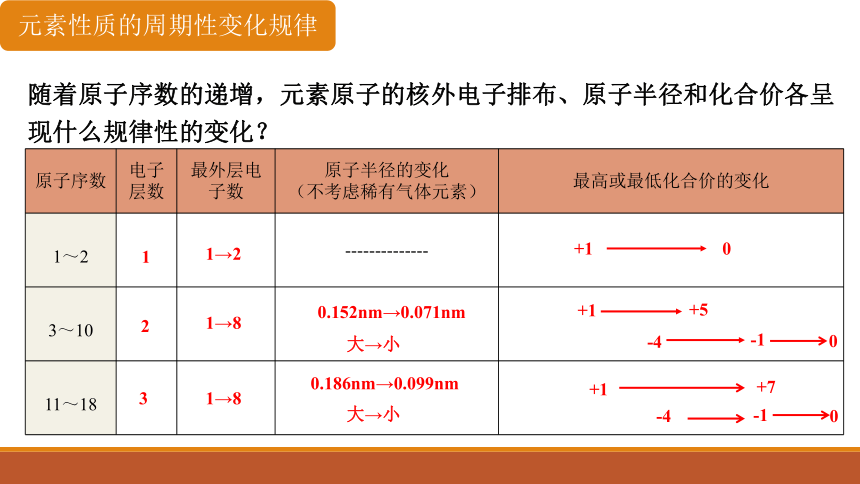
随着原子序数的递增,元素原子的核外电子排布、原子半径和化合价各呈现什么规律性的变化?
原子序数 电子层数 最外层电子数 原子半径的变化 (不考虑稀有气体元素) 最高或最低化合价的变化
1~2 --------------
3~10
11~18
1
2
3
1→8
1→8
1→2
0.152nm→0.071nm
0.186nm→0.099nm
+1
0
+1
+5
-4
-1
0
+1
+7
-4
-1
0
大→小
大→小
元素性质的周期性变化规律
随着原子序数的递增,元素的原子半径呈现由大到小的周期性变化。
随着原子序数的递增,元素原子的最外层电子数呈现
1 8周期性变化(第一周期除外)。
结论
最高正价= 最外层电子数=主族序数(O、F除外)
最高正价+|最低负价|= 8
问题讨论
根据第三周期元素原子的核外电子排布规律,推测出该周期元素金属性和非金属的变化规律。
原子半径逐渐减小
核电荷数依次增多
失电子能力减弱,得电子能力增强
金属性减弱,非金属性增强
实验比较
第三周期元素性质的递变
金属元素 Na Mg Al
单质与水反应
最高价氧化物对应水化物的碱性强弱
结论 与冷水反应缓慢,与沸水反应迅速
2Na+2H2O=2NaOH+H2
Mg+2H2O=Mg(OH)2+H2
NaOH
强碱
Mg(OH)2
中强碱
Al(OH)3
两性氢氧化物
与冷水反应剧烈
金属性:Na>Mg>Al
金属性的周期性变化规律
与热水也不反应
金属性的周期性变化规律
A1(OH)3在酸或强碱溶液中都能溶解,表明它既能与酸发生反应,又能与强溶液发生反应。反应的离子方程式分别如下:
钠、镁、铝是金属元素,都能形成氢氧化物。NaOH是强碱,Mg(OH)2是中强碱,而Al(OH)3是两性氢氧化物。这说明铝虽是金属,但已表现出一定的非金属性。
Al(OH)3 + 3H+ =Al3+ + 3H2O
Al(OH)3 +OH- =AlO2-+ 2H2O
信息获取
Al(OH)3 + 3HCl =AlCl3+ 3H2O
Al(OH)3 +NaOH =Na AlO2+ 2H2O
第三周期元素性质的递变
非金属元素 Si P S Cl
最高价氧化物对应水化物酸性强弱
结论 非金属性:Si
H2SiO3
弱酸
H3PO4
中强酸
H2SO4
强酸
HClO4
强酸
非金属性的周期性变化规律
结论分析
Na Mg Al Si P S Cl
金属性逐渐减弱,非金属性逐渐增强
元素周期律的内容:
元素原子的核外电子排布的周期性的变化
元素周期律的实质:
元素的性质随着原子序数的递增而呈现周期性的变化
元素周期律
01BAlSiGeAsSbTe234567ⅠAⅡAⅢAⅣAⅤAⅥAⅦAPoAt非金属性逐渐增强金属性逐渐增强金属性逐渐增强非金属性逐渐增强非金属区金属区CsF周期表中元素金属性与非金属性的递变规律2.下列各组元素性质的递变规律错误的是 ( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. Na、K、Rb的电子层数依次增多
D. N、O、F原子半径依次增大
练一练
D
1.下列性质的递变关系正确的是( )。
A. 氢化物稳定性:NH3>H2O>HF
B. 碱性:NaOH>KOH>Mg(OH)2
C. 离子半径:O2->F->Al3+ >Mg2+ >Na+
D. 最高正价:Cl>Si>Al>Na
D
3、A、B、C、D四种元素在元素周期表中的位置如图所示。则下列说法正确的是( )
A. 原子半径:A>B>C>D
B. 最外层电子数:A>B>C>D
C. 单质氧化性:C>D
D. 非金属性:A>B>C>D
C
4、X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示。
若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
A. X的最常见气态氢化物的水溶液显酸性
B. 最高价氧化物对应水化物的酸性W比Z强
C. Z的单质与氢气反应比Y单质与氢气反应剧烈
D. X的原子半径小于Y
B
