人教版九年级下册 第九单元 课题3 溶液的浓度 课件(46张ppt)
文档属性
| 名称 | 人教版九年级下册 第九单元 课题3 溶液的浓度 课件(46张ppt) |
|
|
| 格式 | zip | ||
| 文件大小 | 214.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-01-15 00:00:00 | ||
图片预览







文档简介
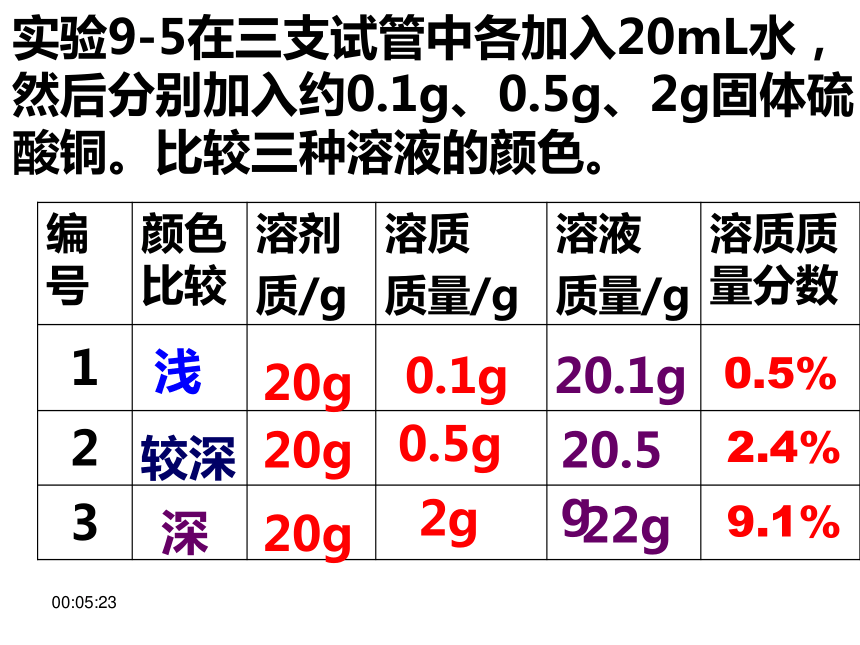
课件46张PPT。10:01:37实验9-5在三支试管中各加入10mL水,
然后分别加入约0.5g、1g、1.5g固体硫酸铜。比较三种溶液的颜色。浅较深深20g20g20g0.1g0.5g2g20.1g20.5g22g10:01:37课题3 溶质的质量分数
10:01:37溶质质量分数的意义:
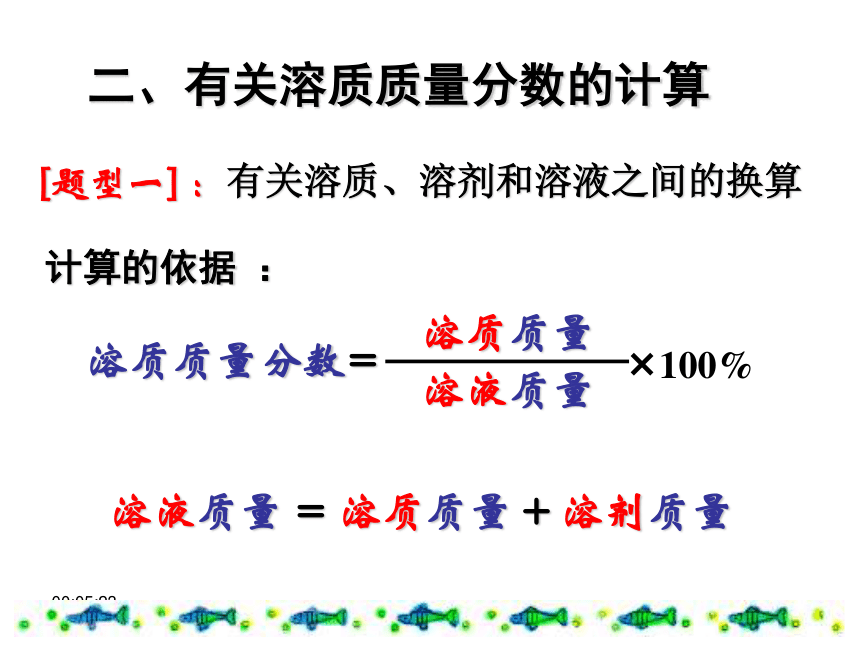
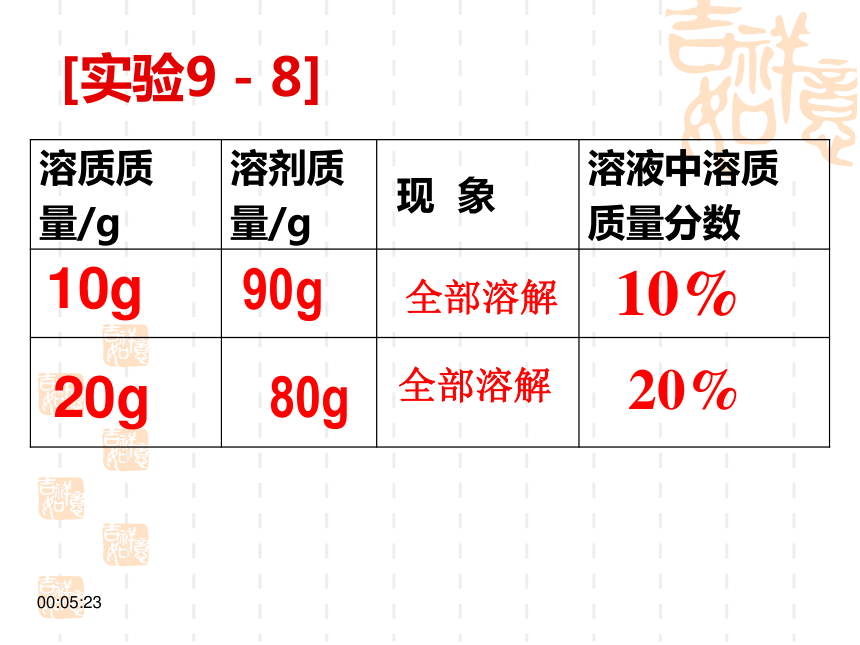
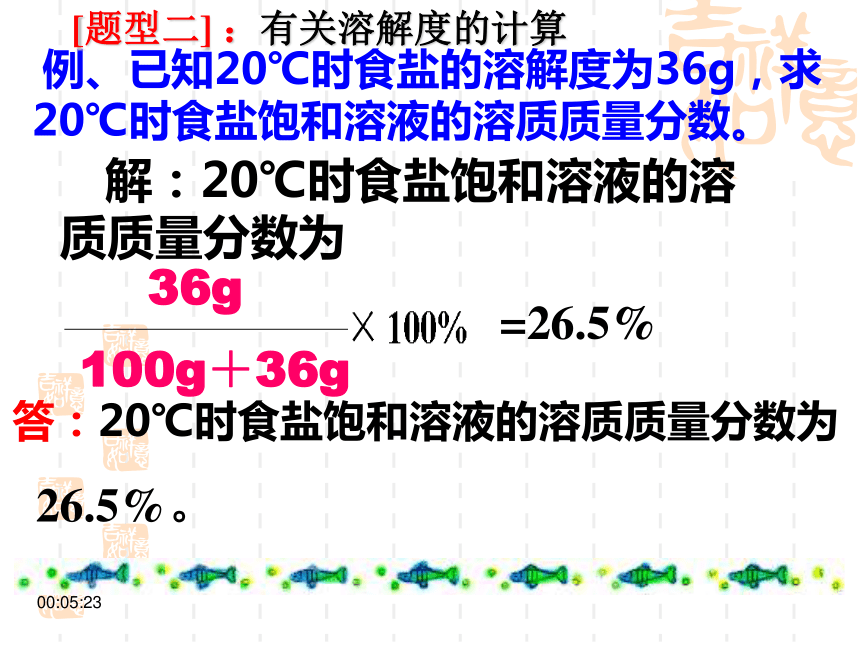
表示一定量溶液中含有溶质的多少溶液的质量=溶质的质量+溶剂的质量溶质的质量分数=10:01:37实验9-5在三支试管中各加入20mL水, 然后分别加入约0.1g、0.5g、2g固体硫酸铜。比较三种溶液的颜色。浅较深深20g20g20g0.1g0.5g2g20.1g20.5g22g0.5%2.4%9.1%10:01:37[题型一] :有关溶质、溶剂和溶液之间的换算 二、有关溶质质量分数的计算溶质质量溶液质量?100% 溶质质量分数=溶液质量 = 溶质质量 + 溶剂质量计算的依据 :10:01:37[实验9-8]10g20g90g80g10%20%全部溶解全部溶解10:01:37 例、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%答:20℃时食盐饱和溶液的溶质质量分数为
26.5%。
? [题型二] :有关溶解度的计算10:01:37 饱和溶液的
溶质质量分数= 溶质的质量分数36% 是指:100g溶液中含有36g溶质。
溶质T℃时溶解度36g是指: 在T℃时,100g水最多溶解该溶质36g。溶质质量分数与溶解度的比较10:01:37[例题] :200C时,氯化钠溶解度为36克, (1)若将32克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
(2)若将36克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
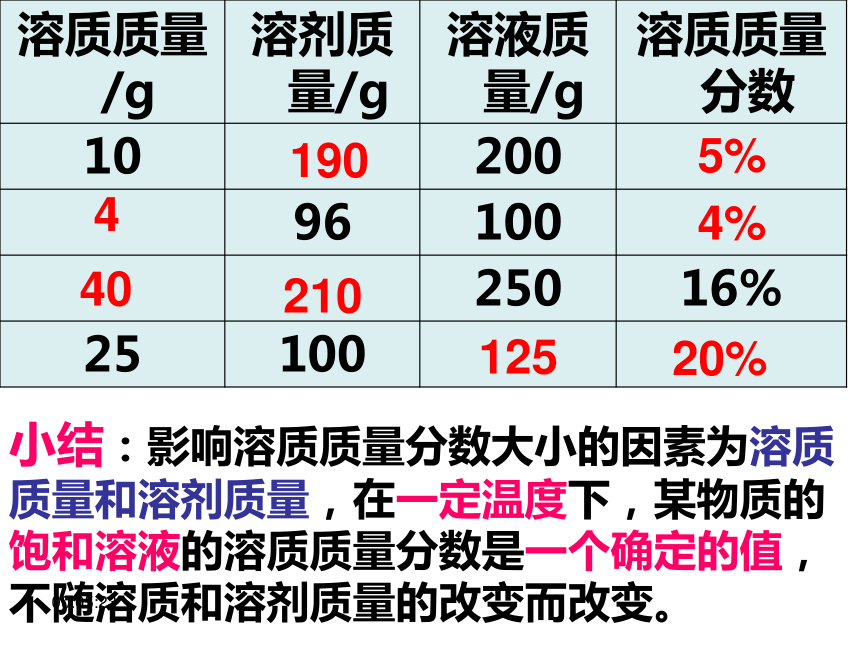
(3)若将38克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少? 从上面例题中你得到什么启示?说明什么问题? 10:01:37基本公式溶液的质量=溶质质量+溶剂质量溶质质量=溶液的质量×溶质的质量分数10:01:371905%4%4021012520%4小结:影响溶质质量分数大小的因素为溶质
质量和溶剂质量,在一定温度下,某物质的
饱和溶液的溶质质量分数是一个确定的值,
不随溶质和溶剂质量的改变而改变。10:01:37 例: 冬天,人们常给皮肤抹上一点甘油溶液,使皮肤保持湿润。用400克甘油溶解在100克水中,配制的甘油溶液效果最佳。该甘油溶液的溶质的质量分数是多少? 解:=80%答:该甘油溶液的溶质的质量分数是80 %甘油溶液中溶质的质量分数为10:01:37例题1:在农业生产上,常需要用质量分数为16%
的氯化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各多少?解:所需氯化钠的质量为:
150kg ?16% = 24kg需要水的质量为:150kg - 24kg = 126kg答:配150kg质量分数为16%的氯化钠溶液
需24kg 氯化钠和126kg水10:01:37 1、20g食盐溶液中含有2g食盐,求:该溶液中溶质质量分数2、40g 2%的食盐溶液中含有多少g食盐和水? 含食盐:40g×2%=0.8g 解:答:该溶液的溶质质量分数是10%。解:答:40g 2%的食盐溶液中含有 0.8g食盐和39.2g水。
含水:40g–0.8g=39.2g该溶液中溶质质量分数为10:01:37 3、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。4、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。剩余溶液的溶质质量分数不变,仍是 10 %解:加水:加盐:10:01:37练习:将100克10%的硝酸钾溶液进行以下变化,求变化后溶液的溶质质量分数?(1)加100克水 (2)加12.5克硝酸钾(3)蒸发掉50克水 要使溶液中溶质的质量分数扩大一倍,蒸发溶剂的质量是原溶液质量的一半。要使溶液中溶质的质量分数变为原来的一半,所加水的质量为原溶液溶液质量的一倍。小结 :10:01:37例题:有50g质量分数为5%的硝酸钾溶液,若将其溶质质量分数提高到10%,可采用的方法是:( )
A、蒸发掉23.75g
B、水蒸发掉25g水
C、加入2g硝酸钾晶体
D、加入50g溶质质量分数为5%的硝酸钾溶液 B10:01:37练习 配制100mL密度为1.1g/mL的20%的NaCl溶液
需要多少克NaCl和多少mL水?解:溶液质量= 100mL?1.1g/mL=110g
所需NaCl的质量为: 110g?20% = 22g所需水的质量为:100mL? 1.1g/mL – 22g = 88g答:略基本公式: m=ρV V=10:01:37 向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算? ? [题型三] :有关溶液稀释或浓缩的计算计算的依据 : 稀释前溶质质量 = 稀释后溶质质量 浓缩前溶质质量 = 浓缩后溶质质量基本公式: m(浓)·c (浓) =m (稀) ·c (稀)10:01:37例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的 硫酸溶液需要多少克水?解:设稀释后溶液的质量为x50g ?98% = X ?20%X = 答:略需要水的质量= 245 g– 50g = 195g10:01:37例3:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?解:设需要98%硫酸的体积为V V?1.84g/mL ?98% = 98g ?10%V = 答:略10:01:37练习:配制500mL质量分数为20%的H2SO4溶液,需要质量分数为98%的H2SO4多少mL?[ρ(浓硫酸)=1.84g/cm3 ρ(20%H2SO4)=1.14g/cm3]1.14g/cm3 ×500mL×20% = 1.84g/cm3 · V × 98%稀释前后溶质的质量不变V= 63.2mL加水多少毫升?解:设需要质量分数为98%的浓硫酸的体积为V1.14g/cm3 × 500mL – 1.84g/cm3 × 63.2mL = 453.7gV水 = 453.7mL10:01:37三、溶液的配制:步骤: 1,计算:2,称量、量取3,溶解所需仪器: 托盘天平,药匙、
量筒、玻璃棒、
烧杯、胶头滴管10:01:37例1: 配制50g6%的氯化钠溶液计算:需食盐:50g×6%=3g 需 水:50g–3g=47g称量:用天平称量3g食盐
用量筒量取47mL水溶解:烧杯、玻璃棒实验仪器:天平(砝码)、药匙、量 筒、胶头滴管、烧杯、玻璃棒10:01:37练习:下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。1、2、3、4、10:01:372、配制质量分数为3%的氯化钠溶液1、计算 用已配好的质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制50g质量分数为3%的溶液设需6%的氯化钠溶液的质量为x
x·6%=50g×3%
x=25g
氯化钠溶液的体积=25g/1.04g/cm3=24.0cm3
水的质量=50g-25g=25g
水的体积=25cm32、量取 用量筒量取24.0cm3的氯化钠溶液,
水25cm3 3、混匀 4、装瓶、贴标签10:01:37
1、 100g9.8%硫酸跟多少克锌反应?同时 生成多少克氢气?(H:1 S:32 O:16 Zn:65)四、溶质质量分数在化学方程式中应用注意点:
溶液是混合物,溶液的质量不能直接代入化学方程式中计算;必须计算成溶质的质量。10:01:37练习:要使50g质量分数为16%的硫酸铜完全反
应,至少需要铁粉的质量是多少g?
(Fe:56 S:32 O:16 Cu:64)解:硫酸铜的质量=50g×16%=8g设:需要铁粉的质量为X
Fe+CuSO4=Cu+FeSO4
56 160
X 8g答:需要铁粉的质量为2.8g10:01:37例2: 50g盐酸与6.5g锌恰好完全反应,求这种盐酸中溶质的质量分数?(H:1 Cl:36.5 Zn:65) 10:01:37练习1:实验室用200g稀硫酸和一定量的锌完全反应,
制得0.8g氢气。求该稀硫酸中溶质的质量分数。解:设稀硫酸中溶质的质量为xH2SO4 + Zn = ZnSO4 + H2?98 2 x 0.8g答:稀硫酸中溶质的质量为19.6%10:01:37例3、某硫酸溶液200g,与13g含杂质10%的锌完全反应,这种硫酸的溶质质量分数是多少?10:01:37 例4:3.25克锌刚好跟100g盐酸完全反应,求:
(1)盐酸中溶质的质量分数。
(2)反应后所得溶液的溶质质量分数6.6%3.65%10:01:37Zn + 2HCl= ZnCl2 + H2 ↑(1) 解:设盐酸溶液中溶质的质量为X,65 73 3.25g X X = 3.65g10:01:37Zn + 2HCl= ZnCl2 + H2 ↑(2) 解: ZnCl2的质量为Y,氢气质量为Z65 136 23.25g Y ZY = 6.8gZ = 0.1g或10:01:37 例4.32.5克锌粒与280克稀硫酸恰好完全反应。试求:
(1)生成氢气的质量。
(2)稀硫酸中溶质的质量分数。
(3)所得溶液中溶质的质量分数。(1)1克
(2)17.5%
10:01:37注意点:
溶液是混合物,溶液的质量不能直接代入化学方程式中计算;必须换算成溶质的质量。
换算方法:
溶质质量 = 溶液的质量× 溶质的质量分数10:01:37 例4.32.5克锌粒与280克稀硫酸恰好完全反应。试求:
(1)生成氢气的质量。
(2)稀硫酸中溶质的质量分数。
(3)所得溶液中溶质的质量分数。10:01:37反应后溶液的质量确定:(1)根据溶液组成:
溶液质量=溶质质量+溶剂质量(水)(2)根据质量守恒:
反应后溶液质量
=反应物1+反应物2-生成的气体-生成的沉淀
(不溶物)10:01:37反馈练习 4.5g不纯的铁粉恰好与75g质量分数为16%的硫酸铜溶液反应,求
(1)铁粉的纯度
(2)反应后所得溶液中溶质的质量分数93.3%15.3%10:01:37练习1:为了测定某黄铜样品中铜的质量分数,取10g该黄铜样品加入到50g稀硫酸中,恰好完全反应,产生氢气0.1g。试求:
(1)该黄铜样品中铜的质量分数;
(2)原稀硫酸溶液中溶质的质量分数。
(3)反应后所得溶液的溶质质量分数。67.5%9.8%15.1%10:01:37练习4:某学校的学习小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。根据实验数据计算:(1)表中 n的数值为 。
(2)样品中碳酸钙的质量分数是 。
(3)求盐酸中溶质的质量分数。2.8g82.5%18.25%10:01:37??1、100克40%的氢氧化钠溶液恰好与200克硫酸铜溶液完全反应,求:
(1)生成沉淀多少克?
(2)硫酸铜溶液中溶质质量分数?
*(3)生成物溶液中溶质质量分数?
拓展练习 1:10:01:371、3.25克锌刚好跟100g盐酸完全反应,求:(1)盐酸溶质的质量分数。(2)反应后所得溶液的溶质质量分数巩固练习 :2、5.6克铁与多少克10%的硫酸铜溶液恰好完全反应?反应后所得溶液的溶质质量分数是多少?3、含碳酸钙80%的石灰石200克可跟多少克10%的盐酸完全反应?生成多少克二氧化碳?反应后所得溶液的溶质质量分数10:01:37??2、100克40%的氢氧化钠溶液恰好与200克
硫酸溶液完全反应,生成硫酸钠和水。求:
(1)生成硫酸钠多少克?
(2)硫酸溶液中溶质质量分数?
*(3)生成溶液中溶质质量分数?
拓展练习 2:10:01:37巩固练习:40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?解:设稀盐酸的质量为X,反应后生成的NaCl的质量为YNaOH + HCl = NaCl + H2O40g?10% X ?10% Y40 36.5 58.5 X = 36.5gY=5.85gNaCl% = 答:略 (NaOH + HCl = NaCl + H2O)10:01:373、配制溶质质量分数一定的溶液⑴计算 ⑵称量 ⑶溶解 ⑷装瓶药匙 天平 烧杯 量筒 滴管 玻璃棒
10:01:37溶质质量分数的意义:
表示一定量溶液中含有溶质的多少溶液的质量=溶质的质量+溶剂的质量溶质的质量分数=10:01:37实验9-5在三支试管中各加入20mL水, 然后分别加入约0.1g、0.5g、2g固体硫酸铜。比较三种溶液的颜色。浅较深深20g20g20g0.1g0.5g2g20.1g20.5g22g0.5%2.4%9.1%10:01:37[题型一] :有关溶质、溶剂和溶液之间的换算 二、有关溶质质量分数的计算溶质质量溶液质量?100% 溶质质量分数=溶液质量 = 溶质质量 + 溶剂质量计算的依据 :10:01:37[实验9-8]10g20g90g80g10%20%全部溶解全部溶解10:01:37 例、已知20℃时食盐的溶解度为36g,求20℃时食盐饱和溶液的溶质质量分数。 解:20℃时食盐饱和溶液的溶质质量分数为=26.5%答:20℃时食盐饱和溶液的溶质质量分数为
26.5%。
? [题型二] :有关溶解度的计算10:01:37 饱和溶液的
溶质质量分数= 溶质的质量分数36% 是指:100g溶液中含有36g溶质。
溶质T℃时溶解度36g是指: 在T℃时,100g水最多溶解该溶质36g。溶质质量分数与溶解度的比较10:01:37[例题] :200C时,氯化钠溶解度为36克, (1)若将32克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
(2)若将36克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少?
(3)若将38克氯化钠溶于100克水里,所得溶液中溶质的质量分数是多少? 从上面例题中你得到什么启示?说明什么问题? 10:01:37基本公式溶液的质量=溶质质量+溶剂质量溶质质量=溶液的质量×溶质的质量分数10:01:371905%4%4021012520%4小结:影响溶质质量分数大小的因素为溶质
质量和溶剂质量,在一定温度下,某物质的
饱和溶液的溶质质量分数是一个确定的值,
不随溶质和溶剂质量的改变而改变。10:01:37 例: 冬天,人们常给皮肤抹上一点甘油溶液,使皮肤保持湿润。用400克甘油溶解在100克水中,配制的甘油溶液效果最佳。该甘油溶液的溶质的质量分数是多少? 解:=80%答:该甘油溶液的溶质的质量分数是80 %甘油溶液中溶质的质量分数为10:01:37例题1:在农业生产上,常需要用质量分数为16%
的氯化钠溶液来选种。现要配制150kg这种溶液,
需要氯化钠和水的质量各多少?解:所需氯化钠的质量为:
150kg ?16% = 24kg需要水的质量为:150kg - 24kg = 126kg答:配150kg质量分数为16%的氯化钠溶液
需24kg 氯化钠和126kg水10:01:37 1、20g食盐溶液中含有2g食盐,求:该溶液中溶质质量分数2、40g 2%的食盐溶液中含有多少g食盐和水? 含食盐:40g×2%=0.8g 解:答:该溶液的溶质质量分数是10%。解:答:40g 2%的食盐溶液中含有 0.8g食盐和39.2g水。
含水:40g–0.8g=39.2g该溶液中溶质质量分数为10:01:37 3、20g 10%的盐水中放入 2g水或2g食盐,求:所得溶液的溶质质量分数。4、20g 10%的盐水中倒出一半,求:剩余溶液的溶质的质量分数。剩余溶液的溶质质量分数不变,仍是 10 %解:加水:加盐:10:01:37练习:将100克10%的硝酸钾溶液进行以下变化,求变化后溶液的溶质质量分数?(1)加100克水 (2)加12.5克硝酸钾(3)蒸发掉50克水 要使溶液中溶质的质量分数扩大一倍,蒸发溶剂的质量是原溶液质量的一半。要使溶液中溶质的质量分数变为原来的一半,所加水的质量为原溶液溶液质量的一倍。小结 :10:01:37例题:有50g质量分数为5%的硝酸钾溶液,若将其溶质质量分数提高到10%,可采用的方法是:( )
A、蒸发掉23.75g
B、水蒸发掉25g水
C、加入2g硝酸钾晶体
D、加入50g溶质质量分数为5%的硝酸钾溶液 B10:01:37练习 配制100mL密度为1.1g/mL的20%的NaCl溶液
需要多少克NaCl和多少mL水?解:溶液质量= 100mL?1.1g/mL=110g
所需NaCl的质量为: 110g?20% = 22g所需水的质量为:100mL? 1.1g/mL – 22g = 88g答:略基本公式: m=ρV V=10:01:37 向20%的某浓溶液中加水后溶液、溶质和溶剂的质量如何变化? 如何解决有关溶液稀释的计算? ? [题型三] :有关溶液稀释或浓缩的计算计算的依据 : 稀释前溶质质量 = 稀释后溶质质量 浓缩前溶质质量 = 浓缩后溶质质量基本公式: m(浓)·c (浓) =m (稀) ·c (稀)10:01:37例题2:化学实验室现有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的 硫酸溶液需要多少克水?解:设稀释后溶液的质量为x50g ?98% = X ?20%X = 答:略需要水的质量= 245 g– 50g = 195g10:01:37例3:配制10%硫酸98g,要98%硫酸(密度为1.84g/m L )多少mL ?解:设需要98%硫酸的体积为V V?1.84g/mL ?98% = 98g ?10%V = 答:略10:01:37练习:配制500mL质量分数为20%的H2SO4溶液,需要质量分数为98%的H2SO4多少mL?[ρ(浓硫酸)=1.84g/cm3 ρ(20%H2SO4)=1.14g/cm3]1.14g/cm3 ×500mL×20% = 1.84g/cm3 · V × 98%稀释前后溶质的质量不变V= 63.2mL加水多少毫升?解:设需要质量分数为98%的浓硫酸的体积为V1.14g/cm3 × 500mL – 1.84g/cm3 × 63.2mL = 453.7gV水 = 453.7mL10:01:37三、溶液的配制:步骤: 1,计算:2,称量、量取3,溶解所需仪器: 托盘天平,药匙、
量筒、玻璃棒、
烧杯、胶头滴管10:01:37例1: 配制50g6%的氯化钠溶液计算:需食盐:50g×6%=3g 需 水:50g–3g=47g称量:用天平称量3g食盐
用量筒量取47mL水溶解:烧杯、玻璃棒实验仪器:天平(砝码)、药匙、量 筒、胶头滴管、烧杯、玻璃棒10:01:37练习:下面是一位同学配制一定溶质质量分数的氯化钠溶液时的流程图,请找出其中的错误,并说明理由。1、2、3、4、10:01:372、配制质量分数为3%的氯化钠溶液1、计算 用已配好的质量分数为6%的氯化钠溶液(密度为1.04g/cm3),配制50g质量分数为3%的溶液设需6%的氯化钠溶液的质量为x
x·6%=50g×3%
x=25g
氯化钠溶液的体积=25g/1.04g/cm3=24.0cm3
水的质量=50g-25g=25g
水的体积=25cm32、量取 用量筒量取24.0cm3的氯化钠溶液,
水25cm3 3、混匀 4、装瓶、贴标签10:01:37
1、 100g9.8%硫酸跟多少克锌反应?同时 生成多少克氢气?(H:1 S:32 O:16 Zn:65)四、溶质质量分数在化学方程式中应用注意点:
溶液是混合物,溶液的质量不能直接代入化学方程式中计算;必须计算成溶质的质量。10:01:37练习:要使50g质量分数为16%的硫酸铜完全反
应,至少需要铁粉的质量是多少g?
(Fe:56 S:32 O:16 Cu:64)解:硫酸铜的质量=50g×16%=8g设:需要铁粉的质量为X
Fe+CuSO4=Cu+FeSO4
56 160
X 8g答:需要铁粉的质量为2.8g10:01:37例2: 50g盐酸与6.5g锌恰好完全反应,求这种盐酸中溶质的质量分数?(H:1 Cl:36.5 Zn:65) 10:01:37练习1:实验室用200g稀硫酸和一定量的锌完全反应,
制得0.8g氢气。求该稀硫酸中溶质的质量分数。解:设稀硫酸中溶质的质量为xH2SO4 + Zn = ZnSO4 + H2?98 2 x 0.8g答:稀硫酸中溶质的质量为19.6%10:01:37例3、某硫酸溶液200g,与13g含杂质10%的锌完全反应,这种硫酸的溶质质量分数是多少?10:01:37 例4:3.25克锌刚好跟100g盐酸完全反应,求:
(1)盐酸中溶质的质量分数。
(2)反应后所得溶液的溶质质量分数6.6%3.65%10:01:37Zn + 2HCl= ZnCl2 + H2 ↑(1) 解:设盐酸溶液中溶质的质量为X,65 73 3.25g X X = 3.65g10:01:37Zn + 2HCl= ZnCl2 + H2 ↑(2) 解: ZnCl2的质量为Y,氢气质量为Z65 136 23.25g Y ZY = 6.8gZ = 0.1g或10:01:37 例4.32.5克锌粒与280克稀硫酸恰好完全反应。试求:
(1)生成氢气的质量。
(2)稀硫酸中溶质的质量分数。
(3)所得溶液中溶质的质量分数。(1)1克
(2)17.5%
10:01:37注意点:
溶液是混合物,溶液的质量不能直接代入化学方程式中计算;必须换算成溶质的质量。
换算方法:
溶质质量 = 溶液的质量× 溶质的质量分数10:01:37 例4.32.5克锌粒与280克稀硫酸恰好完全反应。试求:
(1)生成氢气的质量。
(2)稀硫酸中溶质的质量分数。
(3)所得溶液中溶质的质量分数。10:01:37反应后溶液的质量确定:(1)根据溶液组成:
溶液质量=溶质质量+溶剂质量(水)(2)根据质量守恒:
反应后溶液质量
=反应物1+反应物2-生成的气体-生成的沉淀
(不溶物)10:01:37反馈练习 4.5g不纯的铁粉恰好与75g质量分数为16%的硫酸铜溶液反应,求
(1)铁粉的纯度
(2)反应后所得溶液中溶质的质量分数93.3%15.3%10:01:37练习1:为了测定某黄铜样品中铜的质量分数,取10g该黄铜样品加入到50g稀硫酸中,恰好完全反应,产生氢气0.1g。试求:
(1)该黄铜样品中铜的质量分数;
(2)原稀硫酸溶液中溶质的质量分数。
(3)反应后所得溶液的溶质质量分数。67.5%9.8%15.1%10:01:37练习4:某学校的学习小组对当地的石灰石矿区进行调查,欲测定石灰石中碳酸钙的质量分数,采用的方法如下:取该石灰石样品16g,把80g稀盐酸分四次加入,实验过程所得数据如下表(已知石灰石样品中含有的二氧化硅等杂质不溶于水,不与稀盐酸反应)。根据实验数据计算:(1)表中 n的数值为 。
(2)样品中碳酸钙的质量分数是 。
(3)求盐酸中溶质的质量分数。2.8g82.5%18.25%10:01:37??1、100克40%的氢氧化钠溶液恰好与200克硫酸铜溶液完全反应,求:
(1)生成沉淀多少克?
(2)硫酸铜溶液中溶质质量分数?
*(3)生成物溶液中溶质质量分数?
拓展练习 1:10:01:371、3.25克锌刚好跟100g盐酸完全反应,求:(1)盐酸溶质的质量分数。(2)反应后所得溶液的溶质质量分数巩固练习 :2、5.6克铁与多少克10%的硫酸铜溶液恰好完全反应?反应后所得溶液的溶质质量分数是多少?3、含碳酸钙80%的石灰石200克可跟多少克10%的盐酸完全反应?生成多少克二氧化碳?反应后所得溶液的溶质质量分数10:01:37??2、100克40%的氢氧化钠溶液恰好与200克
硫酸溶液完全反应,生成硫酸钠和水。求:
(1)生成硫酸钠多少克?
(2)硫酸溶液中溶质质量分数?
*(3)生成溶液中溶质质量分数?
拓展练习 2:10:01:37巩固练习:40g10%NaOH溶液跟多少克10%盐酸完全反应?反应后溶液的溶质的质量分数是多少?解:设稀盐酸的质量为X,反应后生成的NaCl的质量为YNaOH + HCl = NaCl + H2O40g?10% X ?10% Y40 36.5 58.5 X = 36.5gY=5.85gNaCl% = 答:略 (NaOH + HCl = NaCl + H2O)10:01:373、配制溶质质量分数一定的溶液⑴计算 ⑵称量 ⑶溶解 ⑷装瓶药匙 天平 烧杯 量筒 滴管 玻璃棒
同课章节目录
