2022-2023高中化学人教版必修2 5.1硫的转化——揭开硫磺熏蒸的秘密说课(共53张PPT)
文档属性
| 名称 | 2022-2023高中化学人教版必修2 5.1硫的转化——揭开硫磺熏蒸的秘密说课(共53张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 72.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-18 00:00:00 | ||
图片预览








文档简介
(共53张PPT)
硫
的
转
化
揭开硫磺熏蒸的秘密
目 录
CATALOG
01
02
04
05
教学分析
教学目标
教学过程
教学反思
Teaching Anlysis
Teaching Design
Teaching Process
Teaching Refletion
03
教学设计
Teaching Process
教学分析
Teaching Process
PART 03
教学分析
课标分析
【内容要求】
结合真实情境中的应用实例或通过实验探究,了解硫及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。结合实例认识硫及其化合物的多样性,了解通过化学反应可以探索含硫物质性质、实现含硫物质转化
【学业要求】
1.能列举、描述、辨识典型含硫物质重要的物理和化学性质及实验现象。能用化学方程式、离子方程式正确表示典型含硫物质的主要化学性质。
2.能从物质类别、元素价态的角度,依据复分解反应和氧化还原反应原理,预测含硫物质的化学性质和变化,设计实验进行初步验证,并能分析、解释有关实验现象。能参与社会性议题的讨论(如食品安全等)。
已具备:初步掌握了从“价-类”两个角度预测典型物质的性质,具备初步设计实验方案的能力
障碍点:是否灵活调用价类二维模型解决转化问题
发展点:通过硫的转化探究,提升利用价类二维模型实现物质间转化,解决实际问题的能力
教学分析
学情分析
教学目标
Teaching Object
PART 02
【学习目标】
1. 通过实验探究,掌握固定硫磺熏蒸证据的方法,探究硫的物理性质和化学性质,学会从物质类别和化合价两个维度预测硫及其化合物的性质。认识硫单质的用途,能说明硫及化合物对社会发展的价值和对环境的影响。
2、通过预测性质、设计方案和实施实验,以价态变化为主线,运用氧化还原反应知识探究不同价态硫元素之间的转化,掌握实现不同价态元素之间转化的思路和方法。
3、能够使用“价—类”二维模型从元素找到物质,运用“价—类”两个角度设计含硫物质的相互转化并进行实验验证。总结二氧化硫、硫化钠的部分化学性质,并学会从价态的角度认识物质群的化学性质。
教学目标
项目学习目标
【评价目标】
1. 能绘出硫及其化合物的“价-类”二维图,了解硫元素在自然界中的转化,能举例说明含硫元素物质及其在自然界中的存在,能用化学方程式、离子方程式正确表示典型含硫物质的主要化学性质。
2、能够使用“价—类”二维模型从元素找到物质,运用“价—类”两个角度设计含硫物质的相互转化并进行实验验证。诊断并发展证据推理与模型认知素养。
3、学会从价态的角度认识含硫物质群的化学性质。诊断并发展科学探究与创新意识素养
教学目标
项目评价目标
教学设计
Teaching Design
PART 04
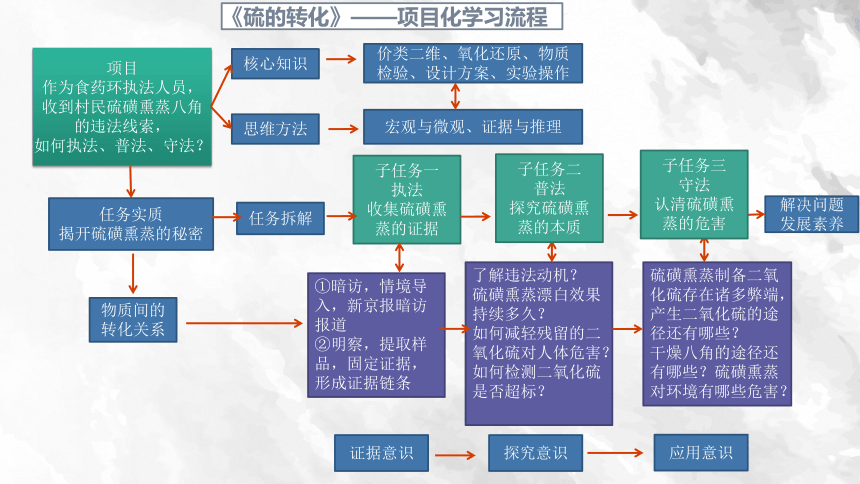
项目
作为食药环执法人员,收到村民硫磺熏蒸八角的违法线索,
如何执法、普法、守法?
任务实质
揭开硫磺熏蒸的秘密
任务拆解
子任务一
执法
收集硫磺熏蒸的证据
①暗访,情境导入,新京报暗访报道
②明察,提取样品,固定证据,形成证据链条
了解违法动机?
硫磺熏蒸漂白效果持续多久?
如何减轻残留的二氧化硫对人体危害?
如何检测二氧化硫是否超标?
硫磺熏蒸制备二氧化硫存在诸多弊端,产生二氧化硫的途径还有哪些?
干燥八角的途径还有哪些?硫磺熏蒸对环境有哪些危害?
物质间的转化关系
核心知识
思维方法
价类二维、氧化还原、物质检验、设计方案、实验操作
宏观与微观、证据与推理
解决问题
发展素养
证据意识
探究意识
应用意识
《硫的转化》——项目化学习流程
子任务二
普法
探究硫磺熏蒸的本质
子任务三
守法
认清硫磺熏蒸的危害
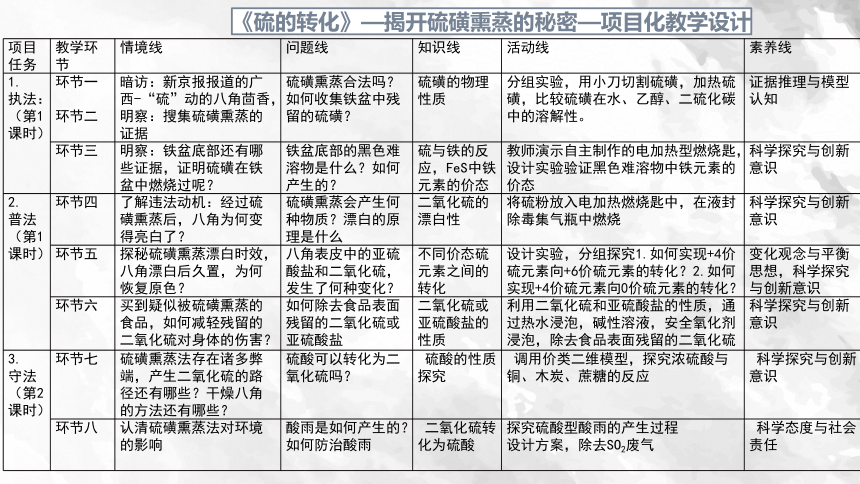
《硫的转化》—揭开硫磺熏蒸的秘密—项目化教学设计
项目 任务 教学环节 情境线 问题线 知识线 活动线 素养线
1. 执法: (第1课时) 环节一 环节二 暗访:新京报报道的广西-“硫”动的八角茴香, 明察:搜集硫磺熏蒸的证据 硫磺熏蒸合法吗?如何收集铁盆中残留的硫磺? 硫磺的物理性质 分组实验,用小刀切割硫磺,加热硫磺,比较硫磺在水、乙醇、二硫化碳中的溶解性。 证据推理与模型认知
环节三 明察:铁盆底部还有哪些证据,证明硫磺在铁盆中燃烧过呢? 铁盆底部的黑色难溶物是什么?如何产生的? 硫与铁的反应,FeS中铁元素的价态 教师演示自主制作的电加热型燃烧匙,设计实验验证黑色难溶物中铁元素的价态 科学探究与创新意识
2. 普法 (第1课时) 环节四 了解违法动机:经过硫磺熏蒸后,八角为何变得亮白了? 硫磺熏蒸会产生何种物质?漂白的原理是什么 二氧化硫的漂白性 将硫粉放入电加热燃烧匙中,在液封除毒集气瓶中燃烧 科学探究与创新意识
环节五 探秘硫磺熏蒸漂白时效,八角漂白后久置,为何恢复原色? 八角表皮中的亚硫酸盐和二氧化硫,发生了何种变化? 不同价态硫元素之间的转化 设计实验,分组探究1.如何实现+4价硫元素向+6价硫元素的转化?2.如何实现+4价硫元素向0价硫元素的转化? 变化观念与平衡思想,科学探究与创新意识
环节六 买到疑似被硫磺熏蒸的食品,如何减轻残留的二氧化硫对身体的伤害? 如何除去食品表面残留的二氧化硫或亚硫酸盐 二氧化硫或亚硫酸盐的性质 利用二氧化硫和亚硫酸盐的性质,通过热水浸泡,碱性溶液,安全氧化剂浸泡,除去食品表面残留的二氧化硫 科学探究与创新意识
3. 守法 (第2课时) 环节七 硫磺熏蒸法存在诸多弊端,产生二氧化硫的路径还有哪些?干燥八角的方法还有哪些? 硫酸可以转化为二氧化硫吗? 硫酸的性质探究 调用价类二维模型,探究浓硫酸与铜、木炭、蔗糖的反应 科学探究与创新意识
环节八 认清硫磺熏蒸法对环境的影响 酸雨是如何产生的? 如何防治酸雨 二氧化硫转化为硫酸 探究硫酸型酸雨的产生过程 设计方案,除去SO2废气 科学态度与社会责任
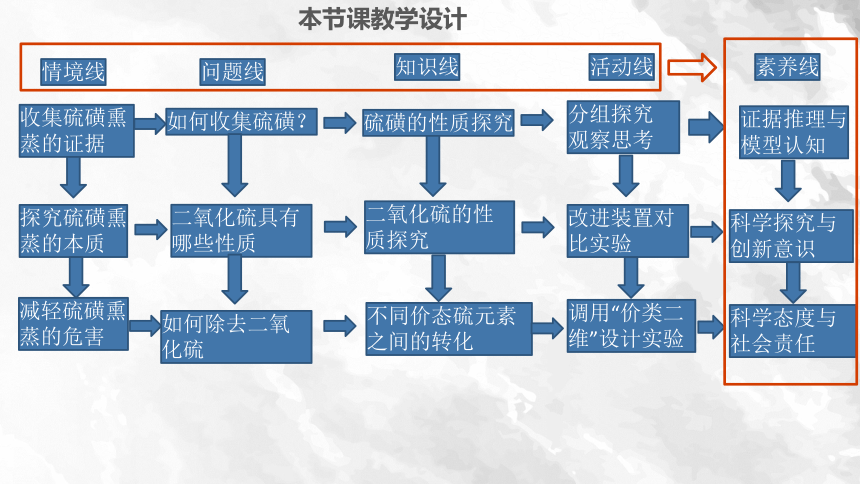
情境线
减轻硫磺熏蒸的危害
问题线
知识线
活动线
收集硫磺熏蒸的证据
探究硫磺熏蒸的本质
本节课教学设计
素养线
如何收集硫磺?
二氧化硫具有哪些性质
如何除去二氧化硫
硫磺的性质探究
二氧化硫的性质探究
不同价态硫元素之间的转化
分组探究
观察思考
改进装置对比实验
调用“价类二维”设计实验
证据推理与模型认知
科学探究与创新意识
科学态度与社会责任
教学过程
Teaching Process
PART 04
播放新京报报道—“硫”动的八角
暗访:广西地区盛产八角茴香,八角采摘后需要晾晒风干,但阴雨天气会使得晾晒的八角发霉腐烂,为了防止晾晒过程中损耗,当地人用硫磺熏蒸八角,将八角晾晒一两天后,撑起一个塑料布棚,把硫磺粉放进铁盆点燃后再放进塑料布棚内熏蒸八角。
问题1 用硫磺熏蒸八角茴香合法吗?如何利用化学知识
①搜集硫磺熏蒸的证据、
②认清硫磺熏蒸的本质,
③减轻硫磺熏蒸的危害?
项目1 执法
环节一: 创设情境
设计意图:引出本节课的三个主要问题:
①硫磺的性质探究
②二氧化硫的性质探究,
③不同价态硫元素之间转化
提取样本:给学生展示两种从农贸市场购买的八角实物,一种色泽鲜艳,一种黑褐色,让同学自主选择会购买哪一种,学生从颜色方面,选择颜色鲜艳的第一种。教师提醒学生,挑选食品不仅要观其色,还要闻其味,学生闻过后发现色鲜艳的八角有刺鼻的酸味,于是对颜色鲜艳的八角为何有股刺激性酸味感到好奇,激发学生兴趣,明确研究任务—揭开硫磺熏蒸的秘密
刺激性酸味
正常气味
设计目的:持续强化情境,由新闻走进现实生活,为后续检测食品中二氧化硫埋下伏笔
问题2 村民用铁盆盛放硫磺熏蒸,铁盆底部沾附少量淡黄色固体,如何收集残留的硫磺从而固定证据?探究硫磺的物理性质
①可以用小刀刮下硫磺固体放入广口瓶中
②可以加热熔化后倒出自然冷却,或倒入冷水中
③可以加入溶剂溶解后倒出,再结晶析出
环节二:从所需原料角度,搜集硫磺熏蒸的证据
设计意图:归纳硫磺的物理性质,硬而脆,熔点低,引入探究硫磺的溶解性实验
项目1 执法
模拟从铁盆中回收硫磺,小火加热至熔化立即撤去酒精灯,防止硫磺燃烧或与铁反应
实验药品:
1.请同学们结合课本,观察事先研磨好的硫粉,观察试管中硫粉的颜色、状态,并将少量且等量硫粉装在三个试管中分别加入蒸馏水、酒精、二硫化碳,小组交流总结硫的颜色、状态、脆度、溶解性。取①、②、③号三支试管(已加入等量硫粉),分别加入0.5mL(约10滴)水,0.5mL无水乙醇、0.5mL二硫化碳(CS2),振荡,观察现象,填写下面表格。
让学生说出硫磺的溶解性差异并说明判断依据
1.根据剩余硫磺质量
2.根据溶液颜色深浅,溶液黄色越深,溶解度越大
颜色 状态 脆度 熔沸点 溶解性
黄色或
淡黄色
固体
很脆
不溶于水
微溶于酒精
易溶于CS2
不高
设计意图:从铁盆中提取硫磺,探究硫磺的物理性质,培养学生的证据推理意识和语言表达能力
同素异形体:由 组成的性质不同的几种 ,叫作该元素的同素异形体
同一种元素
单质
2.加热熔化硫磺,凝固后回收固定违法证据,发现快速冷却凝固后的硫磺具有弹性,变为弹性硫
设计意图:搜集硫磺熏蒸证据,冷却液态硫过程中的“异常现象”,可以作为同素异形体的素材
问题3 盛放硫磺的铁盆底部的黑色难溶物是什么?如何产生的?
设计意图:引导学生结合氧化还原反应,从硫元素的化合价角度分析,推测单质硫具有怎样的化学性质?
学生推测黑色难溶物为FeS
硫单质化合价为0价,有氧化性和还原性
环节三:从硫磺熏蒸器底部残留的副产物,寻找硫磺熏蒸的证据
项目1 执法
设计实验:如何确定铁质硫磺熏蒸器底部,黑色固体中铁元素的价态是+2价或者+3价?(已知硫与铁的反应的黑色产物难溶于水,易溶于稀硫酸)
将黑色固体溶于稀硫酸,加入KSCN溶液不变红,再加入H2O2溶液变红
学生方案
设计意图:培养学生设计实验和语言表达能力
演示硫粉与铁粉实验:展示我自己设计焊接的电加热型燃烧匙(电烙铁+燃烧匙),通电加热至红热状态后断电,放入混合好的硫粉和铁粉,观察硫粉和铁粉在液封除毒集气瓶中的现象。同时提问学生,与传统集气瓶和燃烧匙相比,该仪器的优点?
调温旋钮
加热丝
燃烧匙
电源插头
密封橡胶圈
实验 实验现象 结论
硫粉与铁 粉的反应
切断电源,停止加热后,混合物仍保持红热状态;
硫单质具有氧化性
Fe+ S === FeS
△
设计意图:
1.进一步解释了铁质硫磺熏蒸器底部黑色难溶物产生的原因
2.教师改装仪器,为学生作引领示范,电加热型燃烧匙避免在空气中加热硫粉产生污染气体,通过调温旋钮随时调节温度,液封除毒集气瓶防止气体泄漏到空气中,培养学生的科学探究与创新意识,科学态度与社会责任
2.从物质类别的角度分析,预测单质硫可能与哪几类物质反应?(类比Cl2)
单质硫与Cu Na等金属,与H2 、O2等非金属
评价任务
1. Cl2与S谁的氧化性更强?请用方程式证明:
Cl2的氧化性更强
2Fe+3Cl2 点燃 2FeCl3
Fe+S 点燃 FeS
2.已知Cu的主要化合价:0、+1、+2,写出硫粉与铜粉加热反应的化学方程式2Cu+S Cu2S
设计意图:
1.引导学生从类别角度预测硫磺性质
2.回扣氧化还原,氧化性还原性比较等知识
矿泉水瓶
塑料导管
环节四: 探究硫磺熏蒸,产生的何种物质发挥漂白性?
问题4 八角被何种物质漂白了呢
在电加热型燃烧匙基础上再改进为
通气型电加热燃烧匙
设计意图:探究熏蒸产生具有漂白性的物质
项目2 普法
预测性质 实验现象 结论及化学反应方程式
O2 + S === SO2
点燃
硫元素化合从 ,硫单质具有 还原性.
硫单质在空气中燃烧,发出淡蓝色火焰;硫单质在氧气中燃烧,发出明亮的蓝紫色火焰。品红褪色
硫单质具有还原性,产生二氧化硫具有漂白性
0→+4
教师质疑:该实验能否证明,产生具有漂白性的物质一定是二氧化硫?若为硫蒸气,如何设计对照实验,排除干扰因素
学生向硫粉中加入品红,观察是否褪色
设计意图:培养学生严谨的科学态度,掌握对比参照的思想
问题5 为何硫磺熏蒸的物品久置后恢复原来颜色?
含硫物质中硫元素之间如何转化的?发生氧化反应还是还原反应?
资料卡片:二氧化硫与有色物质结合,生成不稳定的化合物
+4价硫元素转化为+6价硫元素
+4价硫元素转化为0价硫元素
设计意图:引导学生自主调用价类二维图分析,培养模型认知素养
环节五:探秘硫磺熏蒸漂白时效
项目2 普法
实验药品:
SO2水溶液,Na2SO3溶液,Na2S溶液,H2S溶液,酸性KMnO4溶液,石蕊,氯水,稀硫酸
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
【活动1】根据提供的实验药品设计实验,验证转化,并描述实验设计思路。
展示汇报内容
基于价态找物质
基于氧还找原理
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
价降低,被还原,加还原剂
SO2 S
H2SO3 SO42-
1、+4价硫元素存在于哪些物质中?
2、如何实现+4价到0价的转化?
实验方案设计及实施(实验1)
预期转化 选取试剂 预期实验现象 微观分析
S
+4
S
0
Na2SO3溶液,
Na2S溶液
反应生成淡黄色沉淀
S2-→S
SO32-→S
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
预期转化 选取试剂 预期实验现象 微观分析
实验方案设计及实施(实验2)
SO2水溶液,
Na2S溶液
反应生成淡黄色沉淀
S
+4
S
0
S2-→S,
SO2→S
学生方案
实验方案设计及实施(实验1)
预期转化 选取试剂 实验现象 微观分析
S
+4
S
0
Na2SO3溶液,
Na2S溶液
稀硫酸
肉眼观测到微量沉淀,但无法判断沉淀颜色,用数码显微镜放大后,观测到沉淀为淡黄色
【深度思考1】从物质群的角度分析,实验1和实验2氧化还原反应原理相同,为什么实验1未出现预期的实验现象呢?(较少的硫单质)
S2-→S
SO32-→S
在H+条件下反应
数码显微镜
实验1改进再探究:向Na2S和Na2SO3的混合溶液中加入0.2mL稀硫酸,并观察实验现象。
产生大量淡黄色沉淀
2S2- + SO32- + 6H+= 3S↓ + 3H2O
设计意图:“价类二维”模型预测物质性质不是万能的,反应需要一定的条件,培养学生严谨的思维
实验药品:
SO2水溶液,Na2SO3溶液,Na2S溶液,H2S溶液,酸性KMnO4溶液,石蕊,氯水,稀硫酸
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
【活动2】根据提供的实验药品设计实验,验证转化,并描述实验设计思路。
展示汇报内容
基于价态找物质
基于氧还找原理
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
价升高,被氧化,加氧化剂
SO2 SO3
H2SO3 H2SO4
SO32- SO42-
1、+4价硫元素存在于哪些物质中?
2、如何实现+4价到+6价的转化?
预期转化 选取试剂 预期实验现象 微观分析
实验方案设计及实施(实验3)
SO2水溶液,
KMnO4溶液
KMnO4溶液紫色
褪去
S
+4
S
+6
实验方案设计及实施(实验4)
预期转化 选取试剂 预期实验现象 微观分析
S
+4
S
+6
SO2水溶液,氯水
氯水浅黄绿色褪去
BaCl2溶液
MnO4-→Mn2+,
SO2→SO42-
白色沉淀
【深度思考1】若现象不明显,我们该如何证明反应发生?
Cl2→Cl-,SO2→SO42-
Ba2++SO42-= BaSO4
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
【合作探究】请同学们分别将石蕊、氯水、高锰酸钾、氯化铁放入微型试剂盒中,按照气流顺序并联装置,连接完装置后,再打开并挤压二氧化硫的矿泉水瓶
收集二氧化硫
的矿泉水瓶
医用输液管
尾气处理
设计意图:①落实课标必做实验②将多根医用输液管粘合,用矿泉水瓶作为供气装置,与微型密封反应装置结合,培养学生跨学科思维和废品利用的意识
归纳总结1
含+4价硫元素的物质(SO2、SO32-)具有 氧化 性;能与H2S、Na2S反应生成硫单质。
基于转化研究性质:
+6 SO3 H2SO4 Na2SO4
+4 SO2 H2SO3 Na2SO3
0 S
-2 H2S FeS
氢化物 单质 氧化物 含氧酸 盐
归纳总结2
含+4价硫元素的物质具有 还原 性;SO2体现较强的还原性,能与O2 、酸性KMnO4溶液、氯水、H2O2 、 Na2O2 、 Fe3+等氧化剂反应生成SO3/SO42-。
基于转化研究性质:
+6 SO3 H2SO4 Na2SO4
+4 SO2 H2SO3 Na2SO3
0 S
-2 H2S FeS
氢化物 单质 氧化物 含氧酸 盐
实现+4→+6价转化
设计实验并实施
含+4价硫元素物质
SO2、H2SO3、Na2SO3
S
S
+4
+6
价升高,失电子,被氧化
需要加氧化剂
还原性
提供证据
探究不同价态硫元素之间相互转化的思路
归纳总结3
基于价态
找物质
基于氧还
找原理
现象明显看现象
现象不明辨微粒
“类”角度:
①SO2为酸性氧化物,能与碱性物质反应用NaHCO3等溶液浸泡、NaOH溶液(不可取)
②亚硫酸或亚硫酸盐不稳定易分解,热水浸泡
环节六:买到疑似被硫磺熏蒸的食品,如何减小对身体的伤害?
问题6 买到疑似被硫磺熏蒸的食品,如何减小二氧化硫残留的危害?
设计除去二氧化硫或亚硫酸盐的方案
“价”角度:
SO2具有还原性,可用生活中常见的无毒氧化剂浸泡
物理性质角度:SO2和亚硫酸盐易溶于水,可用大量清水浸泡
项目2 普法
验证判断:提供食品二氧化硫检测管,检测疑似被漂白的八角中二氧化硫残余量
设计意图:回扣情境,判断二氧化硫是否超标
应用实践
1、根据现有知识,如何评价 SO2的“功”与“过”?
应用实践
SO2
NaHSO3
(NH4)2SO3
CaSO3
物质类别
氢化物
氧化物
酸
盐
单质
CaSO4
-2
0
+4
+6
SO42-
物理吸附
S
亚硫酸钠
氨水
石灰石
元素价态
氧化法
还原法
复
分
解
法
循环利用
2、依据SO2的性质,可有哪些方式实现SO2的改“过”自新?
教学反思
Teaching Refletion
PART 05
教学反思
1.以探究硫磺熏蒸的奥秘为情境主线,真实背景下的模拟任务更能激发学生兴趣
2.注意运用信息化教学手段,本节课采用数码显微镜实时观察肉眼较难观测到的硫磺沉淀,丰富证据来源
3.注重实验创新,教师亲自动手改装实验装置,将物理学科的电烙铁、生物学科的点滴输液装置与化学融合,是培养学生科学探究与创新意识的最好示范
4.讨论过程中的思路方法要通过课堂小结不断外显,让学生完整叙述实验方案,提升学生说明论证能力,本节课基于“价-类”两个角度建立的实现物质间转化的思路,后期要不断强化应用
硫
的
转
化
揭开硫磺熏蒸的秘密
目 录
CATALOG
01
02
04
05
教学分析
教学目标
教学过程
教学反思
Teaching Anlysis
Teaching Design
Teaching Process
Teaching Refletion
03
教学设计
Teaching Process
教学分析
Teaching Process
PART 03
教学分析
课标分析
【内容要求】
结合真实情境中的应用实例或通过实验探究,了解硫及其重要化合物的主要性质,认识这些物质在生产中的应用和对生态环境的影响。结合实例认识硫及其化合物的多样性,了解通过化学反应可以探索含硫物质性质、实现含硫物质转化
【学业要求】
1.能列举、描述、辨识典型含硫物质重要的物理和化学性质及实验现象。能用化学方程式、离子方程式正确表示典型含硫物质的主要化学性质。
2.能从物质类别、元素价态的角度,依据复分解反应和氧化还原反应原理,预测含硫物质的化学性质和变化,设计实验进行初步验证,并能分析、解释有关实验现象。能参与社会性议题的讨论(如食品安全等)。
已具备:初步掌握了从“价-类”两个角度预测典型物质的性质,具备初步设计实验方案的能力
障碍点:是否灵活调用价类二维模型解决转化问题
发展点:通过硫的转化探究,提升利用价类二维模型实现物质间转化,解决实际问题的能力
教学分析
学情分析
教学目标
Teaching Object
PART 02
【学习目标】
1. 通过实验探究,掌握固定硫磺熏蒸证据的方法,探究硫的物理性质和化学性质,学会从物质类别和化合价两个维度预测硫及其化合物的性质。认识硫单质的用途,能说明硫及化合物对社会发展的价值和对环境的影响。
2、通过预测性质、设计方案和实施实验,以价态变化为主线,运用氧化还原反应知识探究不同价态硫元素之间的转化,掌握实现不同价态元素之间转化的思路和方法。
3、能够使用“价—类”二维模型从元素找到物质,运用“价—类”两个角度设计含硫物质的相互转化并进行实验验证。总结二氧化硫、硫化钠的部分化学性质,并学会从价态的角度认识物质群的化学性质。
教学目标
项目学习目标
【评价目标】
1. 能绘出硫及其化合物的“价-类”二维图,了解硫元素在自然界中的转化,能举例说明含硫元素物质及其在自然界中的存在,能用化学方程式、离子方程式正确表示典型含硫物质的主要化学性质。
2、能够使用“价—类”二维模型从元素找到物质,运用“价—类”两个角度设计含硫物质的相互转化并进行实验验证。诊断并发展证据推理与模型认知素养。
3、学会从价态的角度认识含硫物质群的化学性质。诊断并发展科学探究与创新意识素养
教学目标
项目评价目标
教学设计
Teaching Design
PART 04
项目
作为食药环执法人员,收到村民硫磺熏蒸八角的违法线索,
如何执法、普法、守法?
任务实质
揭开硫磺熏蒸的秘密
任务拆解
子任务一
执法
收集硫磺熏蒸的证据
①暗访,情境导入,新京报暗访报道
②明察,提取样品,固定证据,形成证据链条
了解违法动机?
硫磺熏蒸漂白效果持续多久?
如何减轻残留的二氧化硫对人体危害?
如何检测二氧化硫是否超标?
硫磺熏蒸制备二氧化硫存在诸多弊端,产生二氧化硫的途径还有哪些?
干燥八角的途径还有哪些?硫磺熏蒸对环境有哪些危害?
物质间的转化关系
核心知识
思维方法
价类二维、氧化还原、物质检验、设计方案、实验操作
宏观与微观、证据与推理
解决问题
发展素养
证据意识
探究意识
应用意识
《硫的转化》——项目化学习流程
子任务二
普法
探究硫磺熏蒸的本质
子任务三
守法
认清硫磺熏蒸的危害
《硫的转化》—揭开硫磺熏蒸的秘密—项目化教学设计
项目 任务 教学环节 情境线 问题线 知识线 活动线 素养线
1. 执法: (第1课时) 环节一 环节二 暗访:新京报报道的广西-“硫”动的八角茴香, 明察:搜集硫磺熏蒸的证据 硫磺熏蒸合法吗?如何收集铁盆中残留的硫磺? 硫磺的物理性质 分组实验,用小刀切割硫磺,加热硫磺,比较硫磺在水、乙醇、二硫化碳中的溶解性。 证据推理与模型认知
环节三 明察:铁盆底部还有哪些证据,证明硫磺在铁盆中燃烧过呢? 铁盆底部的黑色难溶物是什么?如何产生的? 硫与铁的反应,FeS中铁元素的价态 教师演示自主制作的电加热型燃烧匙,设计实验验证黑色难溶物中铁元素的价态 科学探究与创新意识
2. 普法 (第1课时) 环节四 了解违法动机:经过硫磺熏蒸后,八角为何变得亮白了? 硫磺熏蒸会产生何种物质?漂白的原理是什么 二氧化硫的漂白性 将硫粉放入电加热燃烧匙中,在液封除毒集气瓶中燃烧 科学探究与创新意识
环节五 探秘硫磺熏蒸漂白时效,八角漂白后久置,为何恢复原色? 八角表皮中的亚硫酸盐和二氧化硫,发生了何种变化? 不同价态硫元素之间的转化 设计实验,分组探究1.如何实现+4价硫元素向+6价硫元素的转化?2.如何实现+4价硫元素向0价硫元素的转化? 变化观念与平衡思想,科学探究与创新意识
环节六 买到疑似被硫磺熏蒸的食品,如何减轻残留的二氧化硫对身体的伤害? 如何除去食品表面残留的二氧化硫或亚硫酸盐 二氧化硫或亚硫酸盐的性质 利用二氧化硫和亚硫酸盐的性质,通过热水浸泡,碱性溶液,安全氧化剂浸泡,除去食品表面残留的二氧化硫 科学探究与创新意识
3. 守法 (第2课时) 环节七 硫磺熏蒸法存在诸多弊端,产生二氧化硫的路径还有哪些?干燥八角的方法还有哪些? 硫酸可以转化为二氧化硫吗? 硫酸的性质探究 调用价类二维模型,探究浓硫酸与铜、木炭、蔗糖的反应 科学探究与创新意识
环节八 认清硫磺熏蒸法对环境的影响 酸雨是如何产生的? 如何防治酸雨 二氧化硫转化为硫酸 探究硫酸型酸雨的产生过程 设计方案,除去SO2废气 科学态度与社会责任
情境线
减轻硫磺熏蒸的危害
问题线
知识线
活动线
收集硫磺熏蒸的证据
探究硫磺熏蒸的本质
本节课教学设计
素养线
如何收集硫磺?
二氧化硫具有哪些性质
如何除去二氧化硫
硫磺的性质探究
二氧化硫的性质探究
不同价态硫元素之间的转化
分组探究
观察思考
改进装置对比实验
调用“价类二维”设计实验
证据推理与模型认知
科学探究与创新意识
科学态度与社会责任
教学过程
Teaching Process
PART 04
播放新京报报道—“硫”动的八角
暗访:广西地区盛产八角茴香,八角采摘后需要晾晒风干,但阴雨天气会使得晾晒的八角发霉腐烂,为了防止晾晒过程中损耗,当地人用硫磺熏蒸八角,将八角晾晒一两天后,撑起一个塑料布棚,把硫磺粉放进铁盆点燃后再放进塑料布棚内熏蒸八角。
问题1 用硫磺熏蒸八角茴香合法吗?如何利用化学知识
①搜集硫磺熏蒸的证据、
②认清硫磺熏蒸的本质,
③减轻硫磺熏蒸的危害?
项目1 执法
环节一: 创设情境
设计意图:引出本节课的三个主要问题:
①硫磺的性质探究
②二氧化硫的性质探究,
③不同价态硫元素之间转化
提取样本:给学生展示两种从农贸市场购买的八角实物,一种色泽鲜艳,一种黑褐色,让同学自主选择会购买哪一种,学生从颜色方面,选择颜色鲜艳的第一种。教师提醒学生,挑选食品不仅要观其色,还要闻其味,学生闻过后发现色鲜艳的八角有刺鼻的酸味,于是对颜色鲜艳的八角为何有股刺激性酸味感到好奇,激发学生兴趣,明确研究任务—揭开硫磺熏蒸的秘密
刺激性酸味
正常气味
设计目的:持续强化情境,由新闻走进现实生活,为后续检测食品中二氧化硫埋下伏笔
问题2 村民用铁盆盛放硫磺熏蒸,铁盆底部沾附少量淡黄色固体,如何收集残留的硫磺从而固定证据?探究硫磺的物理性质
①可以用小刀刮下硫磺固体放入广口瓶中
②可以加热熔化后倒出自然冷却,或倒入冷水中
③可以加入溶剂溶解后倒出,再结晶析出
环节二:从所需原料角度,搜集硫磺熏蒸的证据
设计意图:归纳硫磺的物理性质,硬而脆,熔点低,引入探究硫磺的溶解性实验
项目1 执法
模拟从铁盆中回收硫磺,小火加热至熔化立即撤去酒精灯,防止硫磺燃烧或与铁反应
实验药品:
1.请同学们结合课本,观察事先研磨好的硫粉,观察试管中硫粉的颜色、状态,并将少量且等量硫粉装在三个试管中分别加入蒸馏水、酒精、二硫化碳,小组交流总结硫的颜色、状态、脆度、溶解性。取①、②、③号三支试管(已加入等量硫粉),分别加入0.5mL(约10滴)水,0.5mL无水乙醇、0.5mL二硫化碳(CS2),振荡,观察现象,填写下面表格。
让学生说出硫磺的溶解性差异并说明判断依据
1.根据剩余硫磺质量
2.根据溶液颜色深浅,溶液黄色越深,溶解度越大
颜色 状态 脆度 熔沸点 溶解性
黄色或
淡黄色
固体
很脆
不溶于水
微溶于酒精
易溶于CS2
不高
设计意图:从铁盆中提取硫磺,探究硫磺的物理性质,培养学生的证据推理意识和语言表达能力
同素异形体:由 组成的性质不同的几种 ,叫作该元素的同素异形体
同一种元素
单质
2.加热熔化硫磺,凝固后回收固定违法证据,发现快速冷却凝固后的硫磺具有弹性,变为弹性硫
设计意图:搜集硫磺熏蒸证据,冷却液态硫过程中的“异常现象”,可以作为同素异形体的素材
问题3 盛放硫磺的铁盆底部的黑色难溶物是什么?如何产生的?
设计意图:引导学生结合氧化还原反应,从硫元素的化合价角度分析,推测单质硫具有怎样的化学性质?
学生推测黑色难溶物为FeS
硫单质化合价为0价,有氧化性和还原性
环节三:从硫磺熏蒸器底部残留的副产物,寻找硫磺熏蒸的证据
项目1 执法
设计实验:如何确定铁质硫磺熏蒸器底部,黑色固体中铁元素的价态是+2价或者+3价?(已知硫与铁的反应的黑色产物难溶于水,易溶于稀硫酸)
将黑色固体溶于稀硫酸,加入KSCN溶液不变红,再加入H2O2溶液变红
学生方案
设计意图:培养学生设计实验和语言表达能力
演示硫粉与铁粉实验:展示我自己设计焊接的电加热型燃烧匙(电烙铁+燃烧匙),通电加热至红热状态后断电,放入混合好的硫粉和铁粉,观察硫粉和铁粉在液封除毒集气瓶中的现象。同时提问学生,与传统集气瓶和燃烧匙相比,该仪器的优点?
调温旋钮
加热丝
燃烧匙
电源插头
密封橡胶圈
实验 实验现象 结论
硫粉与铁 粉的反应
切断电源,停止加热后,混合物仍保持红热状态;
硫单质具有氧化性
Fe+ S === FeS
△
设计意图:
1.进一步解释了铁质硫磺熏蒸器底部黑色难溶物产生的原因
2.教师改装仪器,为学生作引领示范,电加热型燃烧匙避免在空气中加热硫粉产生污染气体,通过调温旋钮随时调节温度,液封除毒集气瓶防止气体泄漏到空气中,培养学生的科学探究与创新意识,科学态度与社会责任
2.从物质类别的角度分析,预测单质硫可能与哪几类物质反应?(类比Cl2)
单质硫与Cu Na等金属,与H2 、O2等非金属
评价任务
1. Cl2与S谁的氧化性更强?请用方程式证明:
Cl2的氧化性更强
2Fe+3Cl2 点燃 2FeCl3
Fe+S 点燃 FeS
2.已知Cu的主要化合价:0、+1、+2,写出硫粉与铜粉加热反应的化学方程式2Cu+S Cu2S
设计意图:
1.引导学生从类别角度预测硫磺性质
2.回扣氧化还原,氧化性还原性比较等知识
矿泉水瓶
塑料导管
环节四: 探究硫磺熏蒸,产生的何种物质发挥漂白性?
问题4 八角被何种物质漂白了呢
在电加热型燃烧匙基础上再改进为
通气型电加热燃烧匙
设计意图:探究熏蒸产生具有漂白性的物质
项目2 普法
预测性质 实验现象 结论及化学反应方程式
O2 + S === SO2
点燃
硫元素化合从 ,硫单质具有 还原性.
硫单质在空气中燃烧,发出淡蓝色火焰;硫单质在氧气中燃烧,发出明亮的蓝紫色火焰。品红褪色
硫单质具有还原性,产生二氧化硫具有漂白性
0→+4
教师质疑:该实验能否证明,产生具有漂白性的物质一定是二氧化硫?若为硫蒸气,如何设计对照实验,排除干扰因素
学生向硫粉中加入品红,观察是否褪色
设计意图:培养学生严谨的科学态度,掌握对比参照的思想
问题5 为何硫磺熏蒸的物品久置后恢复原来颜色?
含硫物质中硫元素之间如何转化的?发生氧化反应还是还原反应?
资料卡片:二氧化硫与有色物质结合,生成不稳定的化合物
+4价硫元素转化为+6价硫元素
+4价硫元素转化为0价硫元素
设计意图:引导学生自主调用价类二维图分析,培养模型认知素养
环节五:探秘硫磺熏蒸漂白时效
项目2 普法
实验药品:
SO2水溶液,Na2SO3溶液,Na2S溶液,H2S溶液,酸性KMnO4溶液,石蕊,氯水,稀硫酸
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
【活动1】根据提供的实验药品设计实验,验证转化,并描述实验设计思路。
展示汇报内容
基于价态找物质
基于氧还找原理
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
价降低,被还原,加还原剂
SO2 S
H2SO3 SO42-
1、+4价硫元素存在于哪些物质中?
2、如何实现+4价到0价的转化?
实验方案设计及实施(实验1)
预期转化 选取试剂 预期实验现象 微观分析
S
+4
S
0
Na2SO3溶液,
Na2S溶液
反应生成淡黄色沉淀
S2-→S
SO32-→S
探究一、如何在实验室实现+4价硫元素向0价硫元素的转化?
预期转化 选取试剂 预期实验现象 微观分析
实验方案设计及实施(实验2)
SO2水溶液,
Na2S溶液
反应生成淡黄色沉淀
S
+4
S
0
S2-→S,
SO2→S
学生方案
实验方案设计及实施(实验1)
预期转化 选取试剂 实验现象 微观分析
S
+4
S
0
Na2SO3溶液,
Na2S溶液
稀硫酸
肉眼观测到微量沉淀,但无法判断沉淀颜色,用数码显微镜放大后,观测到沉淀为淡黄色
【深度思考1】从物质群的角度分析,实验1和实验2氧化还原反应原理相同,为什么实验1未出现预期的实验现象呢?(较少的硫单质)
S2-→S
SO32-→S
在H+条件下反应
数码显微镜
实验1改进再探究:向Na2S和Na2SO3的混合溶液中加入0.2mL稀硫酸,并观察实验现象。
产生大量淡黄色沉淀
2S2- + SO32- + 6H+= 3S↓ + 3H2O
设计意图:“价类二维”模型预测物质性质不是万能的,反应需要一定的条件,培养学生严谨的思维
实验药品:
SO2水溶液,Na2SO3溶液,Na2S溶液,H2S溶液,酸性KMnO4溶液,石蕊,氯水,稀硫酸
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
【活动2】根据提供的实验药品设计实验,验证转化,并描述实验设计思路。
展示汇报内容
基于价态找物质
基于氧还找原理
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
价升高,被氧化,加氧化剂
SO2 SO3
H2SO3 H2SO4
SO32- SO42-
1、+4价硫元素存在于哪些物质中?
2、如何实现+4价到+6价的转化?
预期转化 选取试剂 预期实验现象 微观分析
实验方案设计及实施(实验3)
SO2水溶液,
KMnO4溶液
KMnO4溶液紫色
褪去
S
+4
S
+6
实验方案设计及实施(实验4)
预期转化 选取试剂 预期实验现象 微观分析
S
+4
S
+6
SO2水溶液,氯水
氯水浅黄绿色褪去
BaCl2溶液
MnO4-→Mn2+,
SO2→SO42-
白色沉淀
【深度思考1】若现象不明显,我们该如何证明反应发生?
Cl2→Cl-,SO2→SO42-
Ba2++SO42-= BaSO4
探究二、如何在实验室实现+4价硫元素向+6价硫元素的转化?
【合作探究】请同学们分别将石蕊、氯水、高锰酸钾、氯化铁放入微型试剂盒中,按照气流顺序并联装置,连接完装置后,再打开并挤压二氧化硫的矿泉水瓶
收集二氧化硫
的矿泉水瓶
医用输液管
尾气处理
设计意图:①落实课标必做实验②将多根医用输液管粘合,用矿泉水瓶作为供气装置,与微型密封反应装置结合,培养学生跨学科思维和废品利用的意识
归纳总结1
含+4价硫元素的物质(SO2、SO32-)具有 氧化 性;能与H2S、Na2S反应生成硫单质。
基于转化研究性质:
+6 SO3 H2SO4 Na2SO4
+4 SO2 H2SO3 Na2SO3
0 S
-2 H2S FeS
氢化物 单质 氧化物 含氧酸 盐
归纳总结2
含+4价硫元素的物质具有 还原 性;SO2体现较强的还原性,能与O2 、酸性KMnO4溶液、氯水、H2O2 、 Na2O2 、 Fe3+等氧化剂反应生成SO3/SO42-。
基于转化研究性质:
+6 SO3 H2SO4 Na2SO4
+4 SO2 H2SO3 Na2SO3
0 S
-2 H2S FeS
氢化物 单质 氧化物 含氧酸 盐
实现+4→+6价转化
设计实验并实施
含+4价硫元素物质
SO2、H2SO3、Na2SO3
S
S
+4
+6
价升高,失电子,被氧化
需要加氧化剂
还原性
提供证据
探究不同价态硫元素之间相互转化的思路
归纳总结3
基于价态
找物质
基于氧还
找原理
现象明显看现象
现象不明辨微粒
“类”角度:
①SO2为酸性氧化物,能与碱性物质反应用NaHCO3等溶液浸泡、NaOH溶液(不可取)
②亚硫酸或亚硫酸盐不稳定易分解,热水浸泡
环节六:买到疑似被硫磺熏蒸的食品,如何减小对身体的伤害?
问题6 买到疑似被硫磺熏蒸的食品,如何减小二氧化硫残留的危害?
设计除去二氧化硫或亚硫酸盐的方案
“价”角度:
SO2具有还原性,可用生活中常见的无毒氧化剂浸泡
物理性质角度:SO2和亚硫酸盐易溶于水,可用大量清水浸泡
项目2 普法
验证判断:提供食品二氧化硫检测管,检测疑似被漂白的八角中二氧化硫残余量
设计意图:回扣情境,判断二氧化硫是否超标
应用实践
1、根据现有知识,如何评价 SO2的“功”与“过”?
应用实践
SO2
NaHSO3
(NH4)2SO3
CaSO3
物质类别
氢化物
氧化物
酸
盐
单质
CaSO4
-2
0
+4
+6
SO42-
物理吸附
S
亚硫酸钠
氨水
石灰石
元素价态
氧化法
还原法
复
分
解
法
循环利用
2、依据SO2的性质,可有哪些方式实现SO2的改“过”自新?
教学反思
Teaching Refletion
PART 05
教学反思
1.以探究硫磺熏蒸的奥秘为情境主线,真实背景下的模拟任务更能激发学生兴趣
2.注意运用信息化教学手段,本节课采用数码显微镜实时观察肉眼较难观测到的硫磺沉淀,丰富证据来源
3.注重实验创新,教师亲自动手改装实验装置,将物理学科的电烙铁、生物学科的点滴输液装置与化学融合,是培养学生科学探究与创新意识的最好示范
4.讨论过程中的思路方法要通过课堂小结不断外显,让学生完整叙述实验方案,提升学生说明论证能力,本节课基于“价-类”两个角度建立的实现物质间转化的思路,后期要不断强化应用
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
