2022-2023学年高中化学人教版必修1-3.1.2铁的重要化合物(共25张PPT)
文档属性
| 名称 | 2022-2023学年高中化学人教版必修1-3.1.2铁的重要化合物(共25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-19 00:00:00 | ||
图片预览




文档简介
(共25张PPT)
铁及其化合物
IRON AND THE COMPOUNDS OF IRON
激光打印机
墨粉(碳粉)
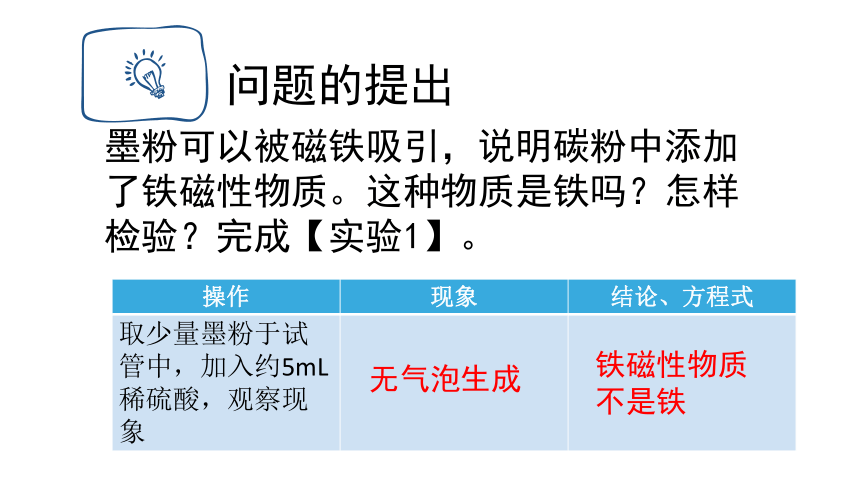
问题的提出
墨粉可以被磁铁吸引,说明碳粉中添加了铁磁性物质。这种物质是铁吗?怎样检验?完成【实验1】。
操作 现象 结论、方程式
取少量墨粉于试管中,加入约5mL稀硫酸,观察现象
无气泡生成
铁磁性物质
不是铁
二、
铁的重要化合物
The important compounds of Iron
单质
盐
氢氧化物
氧化物
1.铁的氧化物
阅读课本66-67页“铁的氧化物”部分
列表对比铁的氧化物的性质及用途
【学习任务 1】
铁的氧化物
氧化亚铁 氧化铁 四氧化三铁
化学式
铁的价态
俗 名
外 观
主 要 性 质
用 途
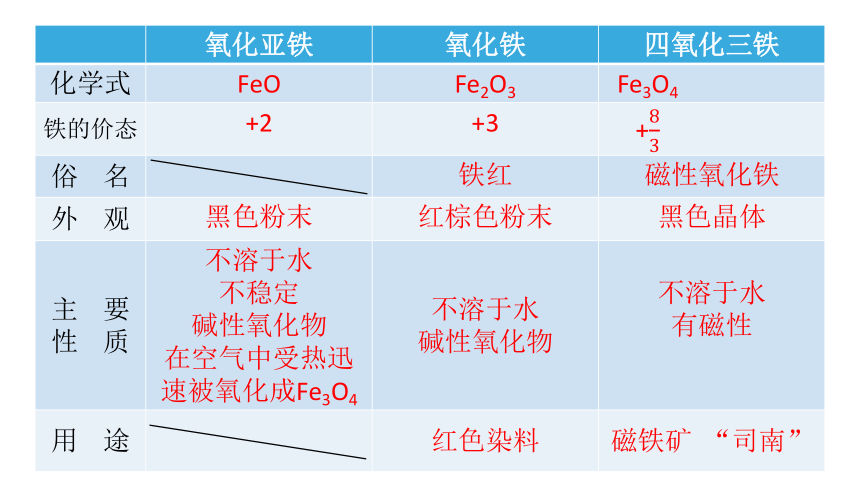
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4
铁的价态 +2 +3 +
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
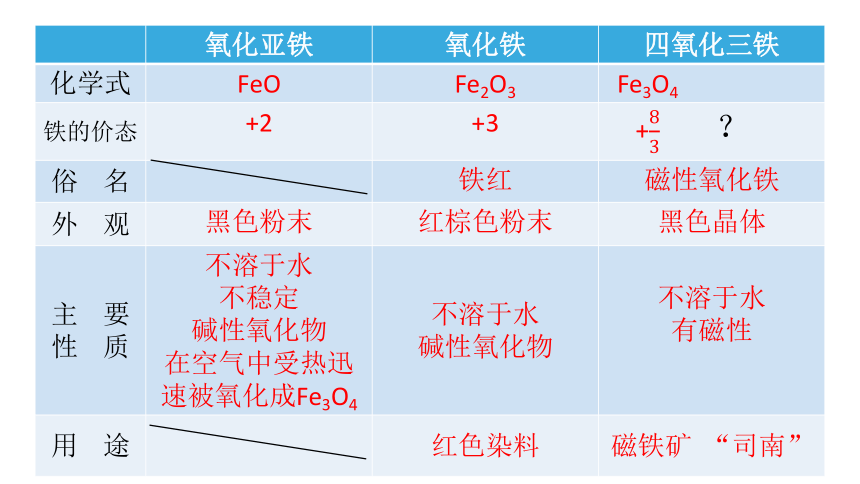
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4
铁的价态 +2 +3 + ?
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
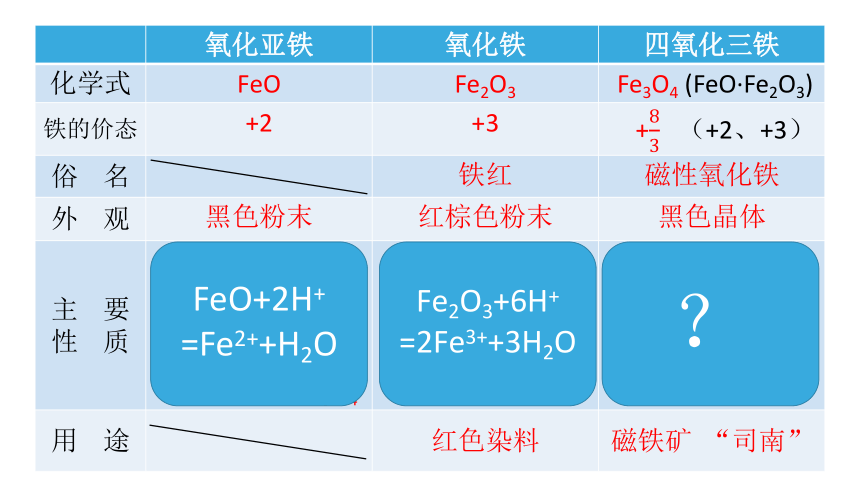
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4 (FeO·Fe2O3)
铁的价态 +2 +3 + (+2、+3)
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
FeO+2H+ =Fe2++H2O
Fe2O3+6H+ =2Fe3++3H2O
?
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4 (FeO·Fe2O3)
铁的价态 +2 +3 + (+2、+3)
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
FeO+2H+ =Fe2++H2O
Fe2O3+6H+ =2Fe3++3H2O
Fe3O4+8H+ =Fe2++2Fe3+
+3H2O
问题1:提出猜想
墨粉中的铁磁性物质可能是哪种物质?
Fe3O4
观察墨粉浸取液和FeSO4、FeCl3溶液,
结合物质分类、转化的思想提出可能
的检验方案。
问题2
方案1: 将离子转化为氢氧化物沉淀进行鉴别
2.铁的氢氧化物
【实验2】分别取2mLFeSO4和FeCl3溶液试管中,
向其中分别加入NaOH溶液,观察并记录现象。
操作 现象 结论、方程式
取2mLFeSO4溶液试管中,向其中滴加NaOH溶液
取2mLFeCl3溶液试管中,向其中滴加NaOH溶液
【学习任务 2】
生成白绿色沉淀,
沉淀迅速变为灰绿色,
最终变为红褐色
生成红褐色沉淀
Fe3++3OH- =Fe(OH)3↓
Fe2++2OH- =Fe(OH)2↓
4Fe(OH)2+O2+2H2O=
4Fe(OH)3
盐+碱—→新碱+新盐
问题3
(1)在实验室里,如何得到“白色”的Fe(OH)2
在各个环节中避免或减少接触氧气。油封隔离,煮沸除氧……
(2)此方法可用于常量Fe2+和Fe3+的检验,是否适用于检验墨粉中的Fe2+和Fe3+?
不适合,一是墨粉浸取液接近无色,铁元素含量可能不高,
二是Fe3+会对Fe2+的检验有干扰作用
方案2:寻找更加灵敏的特效试剂
资料:在含有Fe3+的溶液加入硫氰化钾(KSCN)溶液,
溶液变成红色, 化学上常利用这一反应检验Fe3+的
存在。
【实验3】
操作 现象 结论、方程式
分别取2mLFeSO4、FeCl3溶液于试管中,向其中各加1-2滴KSCN 溶液,观察现象。
取打印墨粉上层浸取液1-2mL,向其中各加1-2滴KSCN溶液
Fe3+的盐溶液遇KSCN
溶液变为红色
Fe2+与KSCN反应不显色
可用KSCN溶液
检验Fe3+
溶液变为红色
墨粉浸取液中
含有Fe3+
【学习任务3】
问题4
如何检验墨粉浸取液中的Fe2+?
3.铁盐和亚铁盐
从氧化还原反应的角度,预测Fe2+和Fe3+的性质。
Fe3+:化合价最高,只有氧化性,也是Fe的最稳定价态
Fe2+:中间价态,既有氧化性又有还原性,更容易变化
到+3价,以还原性为主
【学习任务4】
化合价升降
最高价:只有氧化性
最低价:只有还原性
中间价:既有氧化性,
又有还原性
问题4
如何检验墨粉浸出液中的Fe2+?
利用Fe2+的还原性来检验
【实验4】
操作 现象 结论、方程式
取FeSO4溶液1-2mL,加入1-2滴KSCN溶液, 再加新制氯水2-3滴 ,振荡
取1-2mL墨粉浸取液,加入硫酸酸化的KMnO4溶液3滴,振荡
开始无明显现象,
滴加氯水后溶液
变为红色
2Fe2++Cl2=2Fe3++2Cl-
KMnO4溶液褪色
墨粉浸取液中
含有Fe2+
结论
墨粉浸取液中检出了Fe2+和Fe3+,
结合墨粉的物理性质,
我们确定:
墨粉中添加的磁性物质为Fe3O4。
激光打印机用磁性调色剂(碳粉)的主要成分
F-Fe3O4晶体粉(PLGMENT):
占20-30%
聚丙烯酸脂-苯乙烯共聚物:50-60%
电荷调节剂CCA:占10-20%
流动化剂SiO2等
表面改性剂聚乙烯/聚丙烯 石蜡
激光打印机
硒鼓
墨粉(碳粉)
磁辊
3.铁盐和亚铁盐
亚铁盐
铁盐
Cl2、KMnO4等氧化剂
还原剂
【实验5】
操作 现象 结论、方程式
取FeCl3溶液2mL,加1-2滴KSCN溶液, 再加入少量铁粉,振荡
(金属单质,如Zn、Fe、Cu;
其他还原剂,如I-,VC等)
滴加KSCN后变红
加入铁粉振荡后
褪色
2Fe3++Fe=3Fe2+
总结:铁及其化合物
化合价
物质类别
+3
+2
0
单质
氢氧化物
盐
氧化物
Fe
FeO
Fe2O3
Fe3O4
Fe3+
Fe2+
Fe(OH)3
Fe(OH)2
H+
H+
NaOH
NaOH
H+
H+
H+
Δ
O2或H2O(g)
Cl2
H+
O2
Cl2
O2
O2,H2O
Fe
Cu
检验:KSCN溶液
检验:
①NaOH溶液(常量)
②KSCN溶液,新制氯水
③硫酸酸化的KMnO4 溶液
化学家的“元素组成”应当是 C3H3,
即:Clear Head + Clever Hands + Clean Habits。
卢嘉锡(1915.10.26—2001.6.4),
台湾省台南市人,祖籍福建省永定县 ,
物理化学家、教育家、社会活动家和科
技组织领导者。
卢嘉锡工作涉及物理化学、结构化学、
核化学和材料科学等多种学科领域。在结
构化学研究工作中有杰出贡献,对中国原子
簇化学的发展起了重要推动作用,他所指导
的新技术晶体材料科学研究,也取得了重大
成绩。
卢嘉锡先生
自我评价
请从以下维度对自己本节课的学习做出评价,
如果做的满意,请奖励自己一个五星好评;
如果有所欠缺,这就是我们努力的方向。
评价维度 评价等级
对简单问题的解决提出可能的假设
设计并选择实验仪器,与同学合作完成实验操作
依据证据分析问题,推出合理的结论
正确使用化学语言表征结论
会使用物质分类观、价态观推测物质的性质
THANK YOU
感谢聆听,敬请批评指导!
铁及其化合物
IRON AND THE COMPOUNDS OF IRON
激光打印机
墨粉(碳粉)
问题的提出
墨粉可以被磁铁吸引,说明碳粉中添加了铁磁性物质。这种物质是铁吗?怎样检验?完成【实验1】。
操作 现象 结论、方程式
取少量墨粉于试管中,加入约5mL稀硫酸,观察现象
无气泡生成
铁磁性物质
不是铁
二、
铁的重要化合物
The important compounds of Iron
单质
盐
氢氧化物
氧化物
1.铁的氧化物
阅读课本66-67页“铁的氧化物”部分
列表对比铁的氧化物的性质及用途
【学习任务 1】
铁的氧化物
氧化亚铁 氧化铁 四氧化三铁
化学式
铁的价态
俗 名
外 观
主 要 性 质
用 途
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4
铁的价态 +2 +3 +
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4
铁的价态 +2 +3 + ?
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4 (FeO·Fe2O3)
铁的价态 +2 +3 + (+2、+3)
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
FeO+2H+ =Fe2++H2O
Fe2O3+6H+ =2Fe3++3H2O
?
氧化亚铁 氧化铁 四氧化三铁
化学式 FeO Fe2O3 Fe3O4 (FeO·Fe2O3)
铁的价态 +2 +3 + (+2、+3)
俗 名 铁红 磁性氧化铁
外 观 黑色粉末 红棕色粉末 黑色晶体
主 要 性 质 不溶于水 不稳定 碱性氧化物 在空气中受热迅速被氧化成Fe3O4 不溶于水 碱性氧化物 不溶于水
有磁性
用 途 红色染料 磁铁矿 “司南”
FeO+2H+ =Fe2++H2O
Fe2O3+6H+ =2Fe3++3H2O
Fe3O4+8H+ =Fe2++2Fe3+
+3H2O
问题1:提出猜想
墨粉中的铁磁性物质可能是哪种物质?
Fe3O4
观察墨粉浸取液和FeSO4、FeCl3溶液,
结合物质分类、转化的思想提出可能
的检验方案。
问题2
方案1: 将离子转化为氢氧化物沉淀进行鉴别
2.铁的氢氧化物
【实验2】分别取2mLFeSO4和FeCl3溶液试管中,
向其中分别加入NaOH溶液,观察并记录现象。
操作 现象 结论、方程式
取2mLFeSO4溶液试管中,向其中滴加NaOH溶液
取2mLFeCl3溶液试管中,向其中滴加NaOH溶液
【学习任务 2】
生成白绿色沉淀,
沉淀迅速变为灰绿色,
最终变为红褐色
生成红褐色沉淀
Fe3++3OH- =Fe(OH)3↓
Fe2++2OH- =Fe(OH)2↓
4Fe(OH)2+O2+2H2O=
4Fe(OH)3
盐+碱—→新碱+新盐
问题3
(1)在实验室里,如何得到“白色”的Fe(OH)2
在各个环节中避免或减少接触氧气。油封隔离,煮沸除氧……
(2)此方法可用于常量Fe2+和Fe3+的检验,是否适用于检验墨粉中的Fe2+和Fe3+?
不适合,一是墨粉浸取液接近无色,铁元素含量可能不高,
二是Fe3+会对Fe2+的检验有干扰作用
方案2:寻找更加灵敏的特效试剂
资料:在含有Fe3+的溶液加入硫氰化钾(KSCN)溶液,
溶液变成红色, 化学上常利用这一反应检验Fe3+的
存在。
【实验3】
操作 现象 结论、方程式
分别取2mLFeSO4、FeCl3溶液于试管中,向其中各加1-2滴KSCN 溶液,观察现象。
取打印墨粉上层浸取液1-2mL,向其中各加1-2滴KSCN溶液
Fe3+的盐溶液遇KSCN
溶液变为红色
Fe2+与KSCN反应不显色
可用KSCN溶液
检验Fe3+
溶液变为红色
墨粉浸取液中
含有Fe3+
【学习任务3】
问题4
如何检验墨粉浸取液中的Fe2+?
3.铁盐和亚铁盐
从氧化还原反应的角度,预测Fe2+和Fe3+的性质。
Fe3+:化合价最高,只有氧化性,也是Fe的最稳定价态
Fe2+:中间价态,既有氧化性又有还原性,更容易变化
到+3价,以还原性为主
【学习任务4】
化合价升降
最高价:只有氧化性
最低价:只有还原性
中间价:既有氧化性,
又有还原性
问题4
如何检验墨粉浸出液中的Fe2+?
利用Fe2+的还原性来检验
【实验4】
操作 现象 结论、方程式
取FeSO4溶液1-2mL,加入1-2滴KSCN溶液, 再加新制氯水2-3滴 ,振荡
取1-2mL墨粉浸取液,加入硫酸酸化的KMnO4溶液3滴,振荡
开始无明显现象,
滴加氯水后溶液
变为红色
2Fe2++Cl2=2Fe3++2Cl-
KMnO4溶液褪色
墨粉浸取液中
含有Fe2+
结论
墨粉浸取液中检出了Fe2+和Fe3+,
结合墨粉的物理性质,
我们确定:
墨粉中添加的磁性物质为Fe3O4。
激光打印机用磁性调色剂(碳粉)的主要成分
F-Fe3O4晶体粉(PLGMENT):
占20-30%
聚丙烯酸脂-苯乙烯共聚物:50-60%
电荷调节剂CCA:占10-20%
流动化剂SiO2等
表面改性剂聚乙烯/聚丙烯 石蜡
激光打印机
硒鼓
墨粉(碳粉)
磁辊
3.铁盐和亚铁盐
亚铁盐
铁盐
Cl2、KMnO4等氧化剂
还原剂
【实验5】
操作 现象 结论、方程式
取FeCl3溶液2mL,加1-2滴KSCN溶液, 再加入少量铁粉,振荡
(金属单质,如Zn、Fe、Cu;
其他还原剂,如I-,VC等)
滴加KSCN后变红
加入铁粉振荡后
褪色
2Fe3++Fe=3Fe2+
总结:铁及其化合物
化合价
物质类别
+3
+2
0
单质
氢氧化物
盐
氧化物
Fe
FeO
Fe2O3
Fe3O4
Fe3+
Fe2+
Fe(OH)3
Fe(OH)2
H+
H+
NaOH
NaOH
H+
H+
H+
Δ
O2或H2O(g)
Cl2
H+
O2
Cl2
O2
O2,H2O
Fe
Cu
检验:KSCN溶液
检验:
①NaOH溶液(常量)
②KSCN溶液,新制氯水
③硫酸酸化的KMnO4 溶液
化学家的“元素组成”应当是 C3H3,
即:Clear Head + Clever Hands + Clean Habits。
卢嘉锡(1915.10.26—2001.6.4),
台湾省台南市人,祖籍福建省永定县 ,
物理化学家、教育家、社会活动家和科
技组织领导者。
卢嘉锡工作涉及物理化学、结构化学、
核化学和材料科学等多种学科领域。在结
构化学研究工作中有杰出贡献,对中国原子
簇化学的发展起了重要推动作用,他所指导
的新技术晶体材料科学研究,也取得了重大
成绩。
卢嘉锡先生
自我评价
请从以下维度对自己本节课的学习做出评价,
如果做的满意,请奖励自己一个五星好评;
如果有所欠缺,这就是我们努力的方向。
评价维度 评价等级
对简单问题的解决提出可能的假设
设计并选择实验仪器,与同学合作完成实验操作
依据证据分析问题,推出合理的结论
正确使用化学语言表征结论
会使用物质分类观、价态观推测物质的性质
THANK YOU
感谢聆听,敬请批评指导!
