第12章盐基础练习题九年级化学京改版(2013)下册(含答案)
文档属性
| 名称 | 第12章盐基础练习题九年级化学京改版(2013)下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 95.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-19 00:00:00 | ||
图片预览


文档简介
第12章盐基础练习题九年级化学京改版(2013)下册
一、单选题
1.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
2.下列物质放在空气中易潮解的是
A.碳酸钙 B.纯碱 C.烧碱 D.生石灰
3.下列有关NaCl的叙述,错误的是
A.不溶于水 B.溶液呈中性
C.是食盐的主要成分 D.可用于配制生理盐水
4.下列关于酸、碱、盐在生产和生活中的应用,说法不合理的是
A.KNO3是一种复合肥料 B.高温煅烧石灰石可制得生石灰
C.小苏打可用于治疗胃酸过多 D.将氯化铵和草木灰混合使用
5.在pH=3的溶液中,下列离子可以大量共存的是
A.Cu2+ K+ NO
B.Ag+ Na+ Cl-
C.Na+ Ba2+ OH-
D.K+ Ba 2+ SO
6.磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( )
A.属于金属元素
B.原子核外有16个电子
C.相对原子质量为30.97 g
D.是农作物必需的营养元素
7.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
8.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
9.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
10.今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )
A.尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿
B.磷酸二氢铵(NH4H2PO4)属于复合肥
C.含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物
D.化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
11.下列说法正确的是
A.洗洁精和汽油都能清洗油污,其原理相同
B.不饱和溶液转化为饱和溶液,溶质质量分数一定增大
C.某物质与熟石灰研磨,无刺激性气味,该物质一定不是氮肥
D.合金的硬度一般比各成分金属大,熔点一般比各成分金属低
12.某钠盐溶液中含有Cl﹣、OH﹣、CO32﹣三种阴离子,仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液。
A.①②④②③ B.④②①②③ C.③②①②④ D.④②③②①
二、简答题
13.一瓶氢氧化钠溶液较长时间敞口放置,取出少量溶液于试管中,滴入氯化钡溶液,发现试管中出现白色沉淀,加入少量稀盐酸,白色沉淀溶解,并有气泡产生。解释上述现象(用化学方程式表示):
(1)___
(2)___
(3)___
14.怎样鉴别石灰水和氢氧化钠溶液?
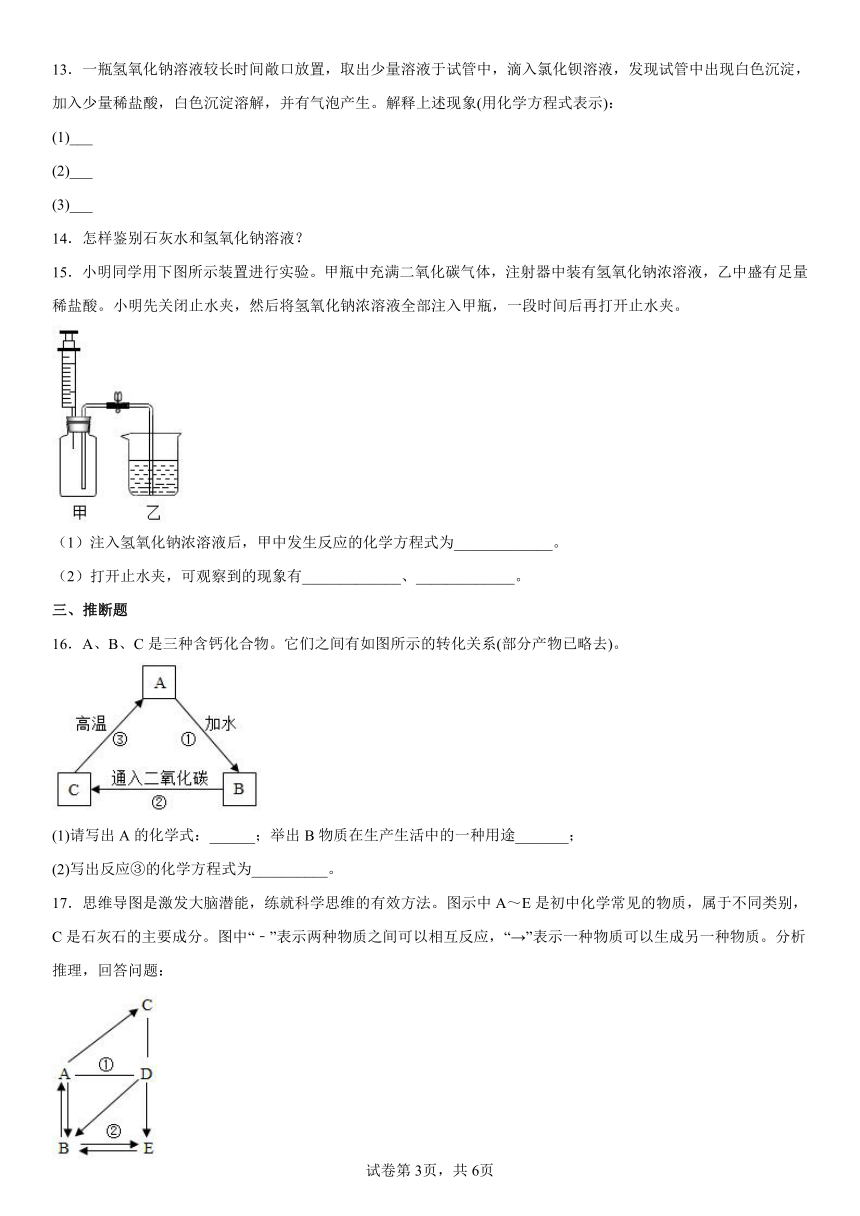
15.小明同学用下图所示装置进行实验。甲瓶中充满二氧化碳气体,注射器中装有氢氧化钠浓溶液,乙中盛有足量稀盐酸。小明先关闭止水夹,然后将氢氧化钠浓溶液全部注入甲瓶,一段时间后再打开止水夹。
(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_____________。
(2)打开止水夹,可观察到的现象有_____________、_____________。
三、推断题
16.A、B、C是三种含钙化合物。它们之间有如图所示的转化关系(部分产物已略去)。
(1)请写出A的化学式:______;举出B物质在生产生活中的一种用途_______;
(2)写出反应③的化学方程式为__________。
17.思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
(1)物质C的化学式 _______。
(2)反应①的化学方程式 __________。
(3)反应②的化学方程式__________。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
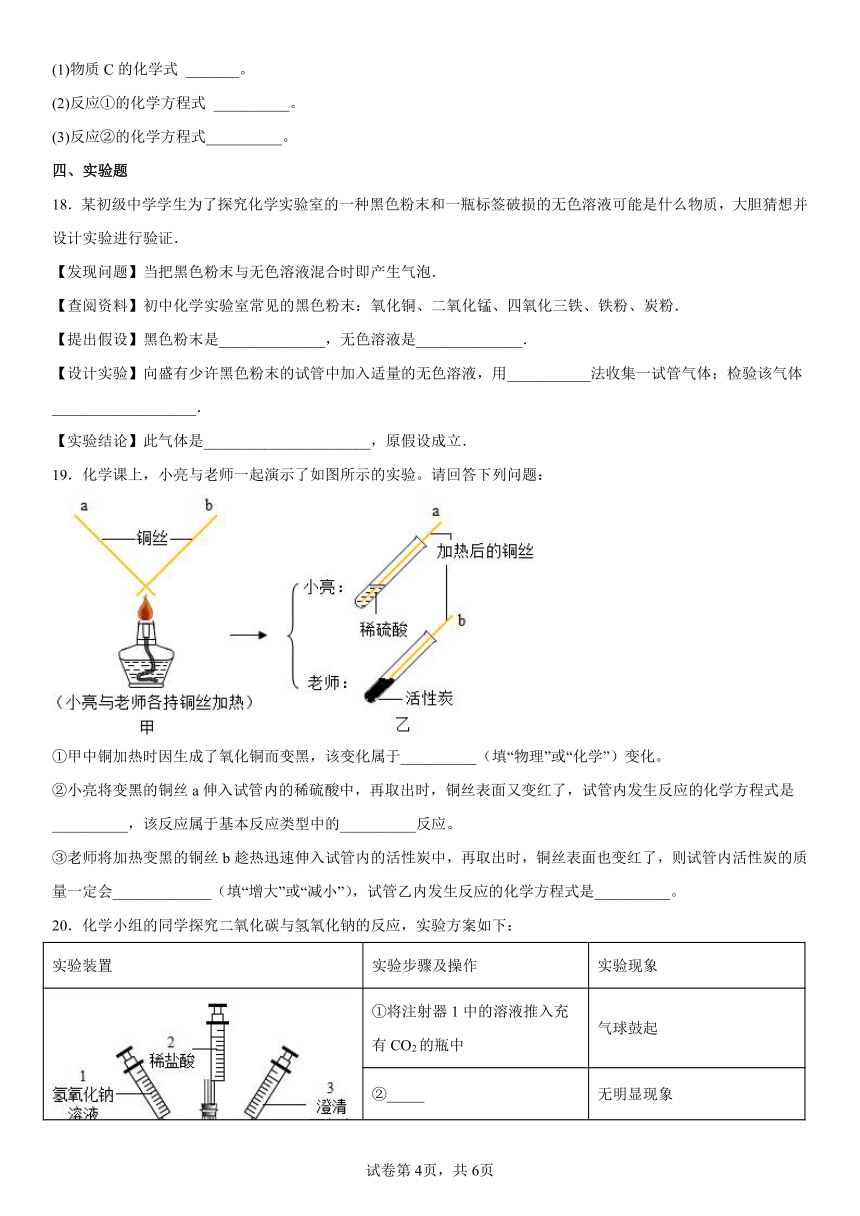
19.化学课上,小亮与老师一起演示了如图所示的实验。请回答下列问题:
①甲中铜加热时因生成了氧化铜而变黑,该变化属于__________(填“物理”或“化学”)变化。
②小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是__________,该反应属于基本反应类型中的__________反应。
③老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会_____________(填“增大”或“减小”),试管乙内发生反应的化学方程式是__________。
20.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液推入充有CO2的瓶中 气球鼓起
②_____ 无明显现象
③将注射器2中的溶液推入瓶中 溶液中有气泡产生,气球变瘪
④向外拉注射器3 澄清石灰水变浑浊
(1)步骤①中气球鼓起的原因可能是_____.
(2)步骤②中的操作是_____,其目的是验证瓶内_____是否完全反应.
(3)本实验的结论是_____.
五、计算题
21.某同学发现张大爷家菜园中的蔬菜生长迟缓,便帮他购买施用了一包化肥,如图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(商品的标签或说明书上常常用质量分数来表示某物质的成分或纯度):
(1)硝酸铵中氮元素和氢元素的质量比为 (填最简整数比)。
(2)硝酸铵中氮元素的质量分数为 ,因此证明这包氮肥包装标签的说明 (填“有”或“没有” )虚假之处。
(3)经化验证明这包化肥的纯度为96%(其余成分中无氮元素),则这包化肥中共含有多少kg的氮元素。(写出计算过程)
22.将10g碳酸氢钠固体加热一段时间后,冷却,称量剩余固体的质量为6.9g。
(1)写出碳酸氢钠加热分解的化学方程式?
(2)分解的碳酸氢钠占总碳酸氢钠固体的质量分数是?
23.某工业品盐酸的溶质的质量分数为37%.请回答:
(1)将该盐酸敞口露置于空气中,一段时间后,其溶质的质量分数______37%(填“大于”“小于”或“等于”);
(2)该盐酸因含有少量Fe3+而显黄色(其他杂质忽略不计)。现取少量样品,与适量硝酸银溶液恰好完全反应。经实验测得,反应后溶液中的H+和NO3-的个数比为91:94,则该盐酸中Fe3+和Cl-的个数比为______。
24.为测定实验室中某硫酸铜样品中硫酸铜的质量分数(所含杂质溶于水,但不参与反应),进行了图所示的实验。请计算:
(1)a=______。
(2)该样品中硫酸铜的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.A
4.D
5.A
6.D
7.C
8.B
9.C
10.C
11.D
12.B
13. 2NaOH+CO2=Na2CO3+H2O Na2CO3+BaCl2=BaCO3↓+2NaCl BaCO3+2HCl=BaCl2+H2O+CO2↑
14.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
15. 2NaOH + CO2Na2CO3 + H2O 乙中液体倒吸入甲中, 甲中产生无色气体
16.(1) CaO 建筑材料
(2)CaCO3CaO+CO2↑
17.(1)CaCO3
(2)(合理即可)
(3)
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19. 化学 复分解 减小
20. 氢氧化钠与二氧化碳反应,消耗瓶内二氧化碳,气压减小 向外拉注射器 3 二氧化碳 二氧化碳能与氢氧化钠反应
21.(1)7:1;(2)35% ;有;(3)50kg×96%×35%=16.8kg
22.碳酸氢钠加热分解生成碳酸钠、二氧化碳和水,其化学方程式为:2NaHCO3Na2CO3+H2O+CO2↑;根据质量守恒定律,H2O+CO2的质量=l0g-6.9g=3.1g;
设:原混合物中碳酸氢钠的质量为x。
x=8.4g
分解的碳酸氢钠占总碳酸氢钠固体的质量分数=。
23.(1)小于(2)1:94
24.(1)10
(2)96%
解:由题意知,硫酸铜样品中所含杂质溶于水,所以滤渣的质量为氢氧化铜的质量,
设参加反应的硫酸铜质量为x,
样品中硫酸铜的质量分数为×100%=96%;
答:样品中硫酸铜的质量分数为96%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质属于盐的是
A.NaOH B.CaO C.Cu D.CaCO3
2.下列物质放在空气中易潮解的是
A.碳酸钙 B.纯碱 C.烧碱 D.生石灰
3.下列有关NaCl的叙述,错误的是
A.不溶于水 B.溶液呈中性
C.是食盐的主要成分 D.可用于配制生理盐水
4.下列关于酸、碱、盐在生产和生活中的应用,说法不合理的是
A.KNO3是一种复合肥料 B.高温煅烧石灰石可制得生石灰
C.小苏打可用于治疗胃酸过多 D.将氯化铵和草木灰混合使用
5.在pH=3的溶液中,下列离子可以大量共存的是
A.Cu2+ K+ NO
B.Ag+ Na+ Cl-
C.Na+ Ba2+ OH-
D.K+ Ba 2+ SO
6.磷元素对生命活动具有重要意义,其相关信息如图所示。下列有关磷元素的说法正确的是( )
A.属于金属元素
B.原子核外有16个电子
C.相对原子质量为30.97 g
D.是农作物必需的营养元素
7.下列物质间的转化一步就能实现的是
A.CaCO3→Na2CO3 B. C.CO2→O2 D.H2O2→H2
8.下列关于碳酸钙的说法错误的是
A.大理石的主要成分是碳酸钙
B.实验室常用碳酸钙与稀硫酸反应制取CO2
C.碳酸钙可用作补钙剂
D.石灰浆粉刷墙壁,“出汗”后变成碳酸钙
9.向烧杯中逐渐加入x溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
选项 烧杯中的物质 x溶液
A 稀硫酸 氯化钡溶液
B 氯化钠溶液 硝酸银溶液
C 硫酸和硫酸铜混合溶液 氢氧化钠溶液
D 碳酸氢钠溶液 稀盐酸
A.A B.B C.C D.D
10.今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )
A.尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿
B.磷酸二氢铵(NH4H2PO4)属于复合肥
C.含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物
D.化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
11.下列说法正确的是
A.洗洁精和汽油都能清洗油污,其原理相同
B.不饱和溶液转化为饱和溶液,溶质质量分数一定增大
C.某物质与熟石灰研磨,无刺激性气味,该物质一定不是氮肥
D.合金的硬度一般比各成分金属大,熔点一般比各成分金属低
12.某钠盐溶液中含有Cl﹣、OH﹣、CO32﹣三种阴离子,仅用一份样品溶液,利用下面的试剂与操作就可将溶液中的三种阴离子依次检验出来,正确的实验操作顺序是
①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液。
A.①②④②③ B.④②①②③ C.③②①②④ D.④②③②①
二、简答题
13.一瓶氢氧化钠溶液较长时间敞口放置,取出少量溶液于试管中,滴入氯化钡溶液,发现试管中出现白色沉淀,加入少量稀盐酸,白色沉淀溶解,并有气泡产生。解释上述现象(用化学方程式表示):
(1)___
(2)___
(3)___
14.怎样鉴别石灰水和氢氧化钠溶液?
15.小明同学用下图所示装置进行实验。甲瓶中充满二氧化碳气体,注射器中装有氢氧化钠浓溶液,乙中盛有足量稀盐酸。小明先关闭止水夹,然后将氢氧化钠浓溶液全部注入甲瓶,一段时间后再打开止水夹。
(1)注入氢氧化钠浓溶液后,甲中发生反应的化学方程式为_____________。
(2)打开止水夹,可观察到的现象有_____________、_____________。
三、推断题
16.A、B、C是三种含钙化合物。它们之间有如图所示的转化关系(部分产物已略去)。
(1)请写出A的化学式:______;举出B物质在生产生活中的一种用途_______;
(2)写出反应③的化学方程式为__________。
17.思维导图是激发大脑潜能,练就科学思维的有效方法。图示中A~E是初中化学常见的物质,属于不同类别,C是石灰石的主要成分。图中“﹣”表示两种物质之间可以相互反应,“→”表示一种物质可以生成另一种物质。分析推理,回答问题:
(1)物质C的化学式 _______。
(2)反应①的化学方程式 __________。
(3)反应②的化学方程式__________。
四、实验题
18.某初级中学学生为了探究化学实验室的一种黑色粉末和一瓶标签破损的无色溶液可能是什么物质,大胆猜想并设计实验进行验证.
【发现问题】当把黑色粉末与无色溶液混合时即产生气泡.
【查阅资料】初中化学实验室常见的黑色粉末:氧化铜、二氧化锰、四氧化三铁、铁粉、炭粉.
【提出假设】黑色粉末是______________,无色溶液是______________.
【设计实验】向盛有少许黑色粉末的试管中加入适量的无色溶液,用___________法收集一试管气体;检验该气体___________________.
【实验结论】此气体是______________________,原假设成立.
19.化学课上,小亮与老师一起演示了如图所示的实验。请回答下列问题:
①甲中铜加热时因生成了氧化铜而变黑,该变化属于__________(填“物理”或“化学”)变化。
②小亮将变黑的铜丝a伸入试管内的稀硫酸中,再取出时,铜丝表面又变红了,试管内发生反应的化学方程式是__________,该反应属于基本反应类型中的__________反应。
③老师将加热变黑的铜丝b趁热迅速伸入试管内的活性炭中,再取出时,铜丝表面也变红了,则试管内活性炭的质量一定会_____________(填“增大”或“减小”),试管乙内发生反应的化学方程式是__________。
20.化学小组的同学探究二氧化碳与氢氧化钠的反应,实验方案如下:
实验装置 实验步骤及操作 实验现象
①将注射器1中的溶液推入充有CO2的瓶中 气球鼓起
②_____ 无明显现象
③将注射器2中的溶液推入瓶中 溶液中有气泡产生,气球变瘪
④向外拉注射器3 澄清石灰水变浑浊
(1)步骤①中气球鼓起的原因可能是_____.
(2)步骤②中的操作是_____,其目的是验证瓶内_____是否完全反应.
(3)本实验的结论是_____.
五、计算题
21.某同学发现张大爷家菜园中的蔬菜生长迟缓,便帮他购买施用了一包化肥,如图为该包化肥的外包装标签上的部分说明,请仔细阅读标签并回答下列问题(商品的标签或说明书上常常用质量分数来表示某物质的成分或纯度):
(1)硝酸铵中氮元素和氢元素的质量比为 (填最简整数比)。
(2)硝酸铵中氮元素的质量分数为 ,因此证明这包氮肥包装标签的说明 (填“有”或“没有” )虚假之处。
(3)经化验证明这包化肥的纯度为96%(其余成分中无氮元素),则这包化肥中共含有多少kg的氮元素。(写出计算过程)
22.将10g碳酸氢钠固体加热一段时间后,冷却,称量剩余固体的质量为6.9g。
(1)写出碳酸氢钠加热分解的化学方程式?
(2)分解的碳酸氢钠占总碳酸氢钠固体的质量分数是?
23.某工业品盐酸的溶质的质量分数为37%.请回答:
(1)将该盐酸敞口露置于空气中,一段时间后,其溶质的质量分数______37%(填“大于”“小于”或“等于”);
(2)该盐酸因含有少量Fe3+而显黄色(其他杂质忽略不计)。现取少量样品,与适量硝酸银溶液恰好完全反应。经实验测得,反应后溶液中的H+和NO3-的个数比为91:94,则该盐酸中Fe3+和Cl-的个数比为______。
24.为测定实验室中某硫酸铜样品中硫酸铜的质量分数(所含杂质溶于水,但不参与反应),进行了图所示的实验。请计算:
(1)a=______。
(2)该样品中硫酸铜的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.A
4.D
5.A
6.D
7.C
8.B
9.C
10.C
11.D
12.B
13. 2NaOH+CO2=Na2CO3+H2O Na2CO3+BaCl2=BaCO3↓+2NaCl BaCO3+2HCl=BaCl2+H2O+CO2↑
14.取少量溶液于试管中,加入适量碳酸钠溶液,产生白色沉淀,则是石灰水,无明显现象,则是氢氧化钠溶液。
15. 2NaOH + CO2Na2CO3 + H2O 乙中液体倒吸入甲中, 甲中产生无色气体
16.(1) CaO 建筑材料
(2)CaCO3CaO+CO2↑
17.(1)CaCO3
(2)(合理即可)
(3)
18. MnO2 H2O2 排水集气法 用带火星的木条伸入试管中,带火星的木条复燃 O2
19. 化学 复分解 减小
20. 氢氧化钠与二氧化碳反应,消耗瓶内二氧化碳,气压减小 向外拉注射器 3 二氧化碳 二氧化碳能与氢氧化钠反应
21.(1)7:1;(2)35% ;有;(3)50kg×96%×35%=16.8kg
22.碳酸氢钠加热分解生成碳酸钠、二氧化碳和水,其化学方程式为:2NaHCO3Na2CO3+H2O+CO2↑;根据质量守恒定律,H2O+CO2的质量=l0g-6.9g=3.1g;
设:原混合物中碳酸氢钠的质量为x。
x=8.4g
分解的碳酸氢钠占总碳酸氢钠固体的质量分数=。
23.(1)小于(2)1:94
24.(1)10
(2)96%
解:由题意知,硫酸铜样品中所含杂质溶于水,所以滤渣的质量为氢氧化铜的质量,
设参加反应的硫酸铜质量为x,
样品中硫酸铜的质量分数为×100%=96%;
答:样品中硫酸铜的质量分数为96%。
答案第1页,共2页
答案第1页,共2页
