浙教版2022学年九上科学期末复习课件三:物质的转化(课件 20张ppt)
文档属性
| 名称 | 浙教版2022学年九上科学期末复习课件三:物质的转化(课件 20张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-12-20 00:00:00 | ||
图片预览




文档简介
(共20张PPT)
浙教版 科学(初中)
九上期末复习课(三)
物质的转化
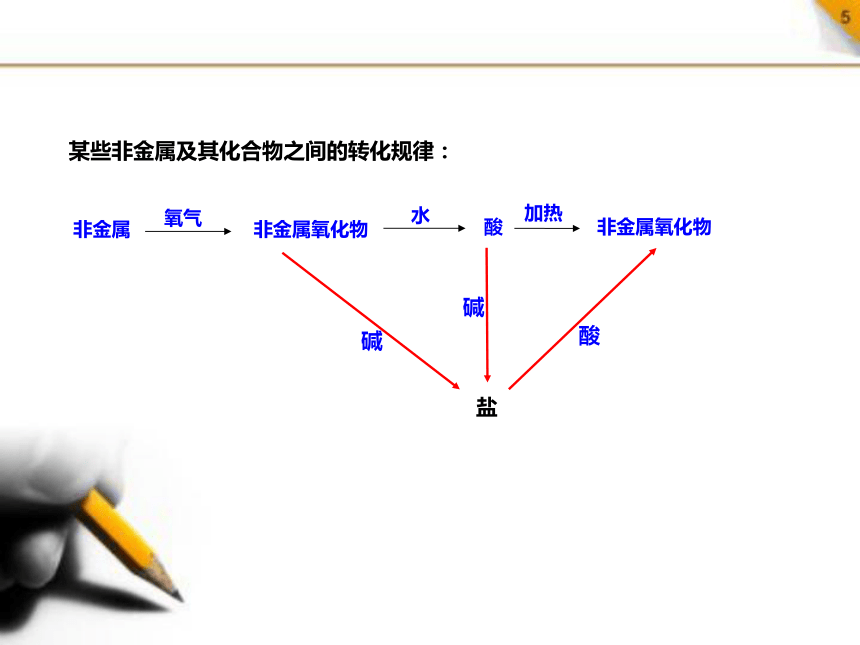
某些非金属及其化合物之间的转化规律:
盐
碱
酸
碱
非金属
氧气
非金属氧化物
水
酸
加热
非金属氧化物
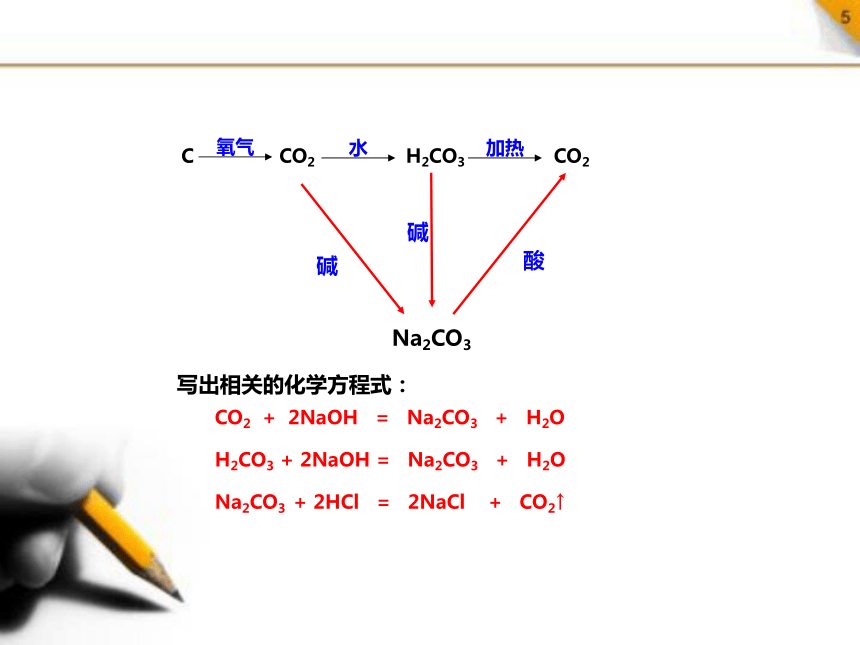
CO2 + 2NaOH = Na2CO3 + H2O
H2CO3 + 2NaOH = Na2CO3 + H2O
Na2CO3 + 2HCl = 2NaCl + CO2↑
C CO2 H2CO3 CO2
氧气
水
加热
Na2CO3
碱
酸
碱
写出相关的化学方程式:
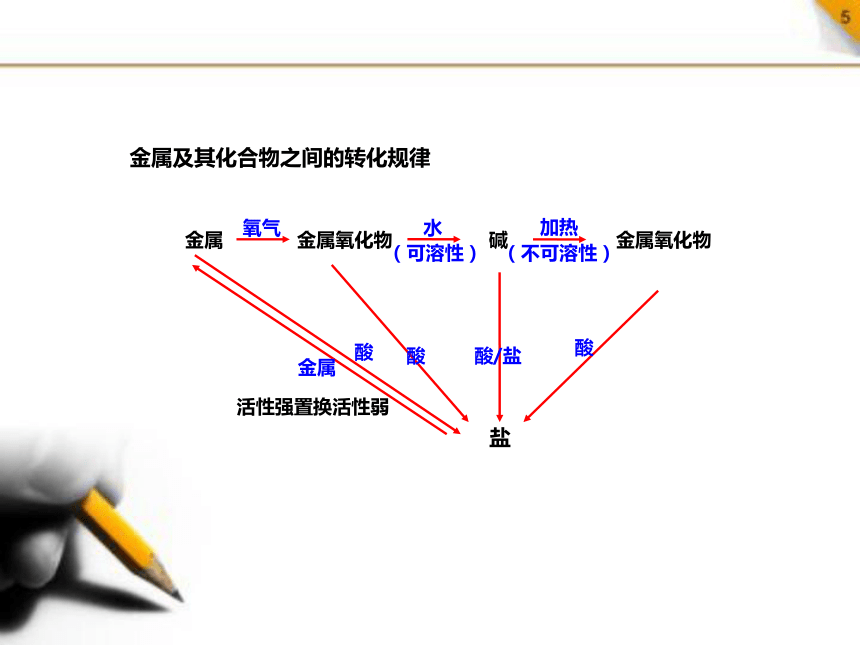
金属及其化合物之间的转化规律
金属 金属氧化物 碱 金属氧化物
活性强置换活性弱
氧气
水
加热
(不可溶性)
盐
酸
酸/盐
酸
(可溶性)
酸
金属
怎样才能从矿石中得到金属呢?
金属冶炼:
把金属从化合态变成游离态
为了得到金属单质,把金属从化合态变成游离态叫金属的冶炼。
常用的金属冶炼方法:
碳与金属氧化物在高温下反应,碳能夺取金属氧化物中的氧,从而得到金属单质。如:
C
+
CuO
Cu
+
CO2
2
2
高温
碳与氧化铜反应后可以得到单质铜,化学方程式为:
冶炼方法一:碳与金属氧化物在高温下进行反应
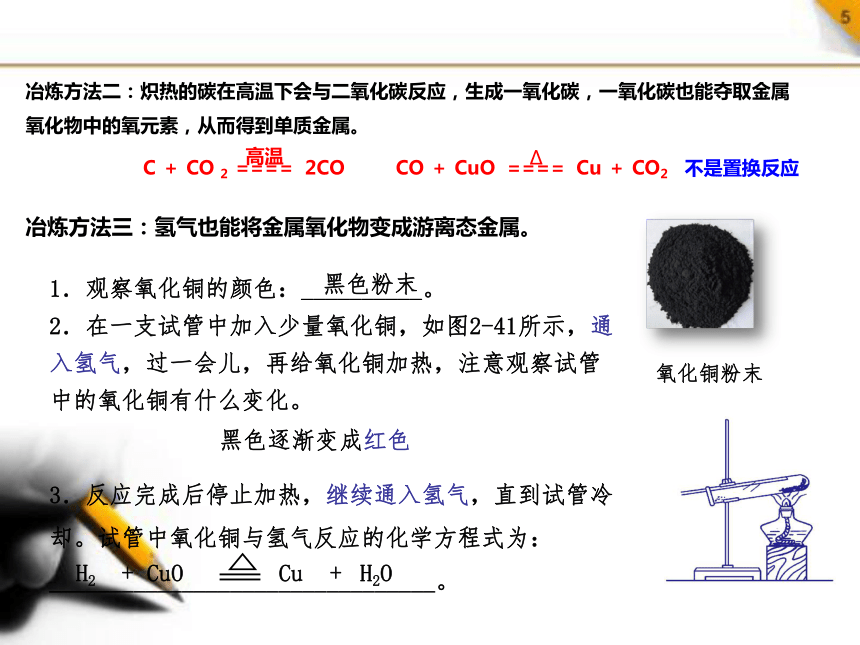
冶炼方法二:炽热的碳在高温下会与二氧化碳反应,生成一氧化碳,一氧化碳也能夺取金属氧化物中的氧元素,从而得到单质金属。
C + CO 2 ==== 2CO CO + CuO ==== Cu + CO2
高温
Δ
不是置换反应
冶炼方法三:氢气也能将金属氧化物变成游离态金属。
1.观察氧化铜的颜色:__________。
2.在一支试管中加入少量氧化铜,如图2-41所示,通入氢气,过一会儿,再给氧化铜加热,注意观察试管中的氧化铜有什么变化。
3.反应完成后停止加热,继续通入氢气,直到试管冷却。试管中氧化铜与氢气反应的化学方程式为:________________________________。
黑色粉末
黑色逐渐变成红色
H2
+
CuO
Cu
+
H2O
氧化铜粉末
冶炼方法四:一氧化碳也能将金属氧化物变成游离态金属。
(2)现象:
①玻璃管中的粉末由红色逐渐变为黑色;
②试管中的澄清石灰水变浑浊;
(3)化学方程式
(4)注意事项:
因CO有毒性,故要用点燃的方法进行尾气处理;
(1)装置
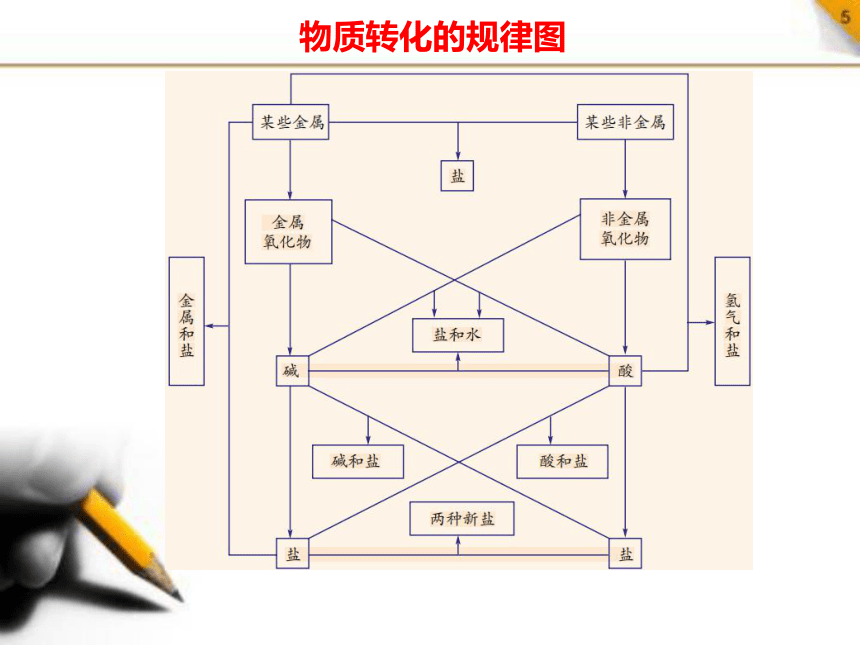
物质转化的规律图
1.C、H2、CO三种物质有如下转化关系:①C→CO2;②H2→H2O;③CO→CO2 下列有关说法正确的是( )
A. 上述转化均说明三种物质具有还原性
B. 三种物质都跟氧气发生反应才能实现以上转化
C. 反应前后元素的化合价均发生改变
D. 若三种物质都用来冶炼金属,则以上转化中的反应均为置换反应
A
基础过关
基础过关
2. 某同学在学习了金属及其化合物之间的转化规律后,绘制了可以通过一步反应制取MgSO4的思维导图,其中所选用的物质错误的是( )
A. ①—Mg B. ②—MgCl2
C. ③—H2SO4 D. ④—Mg(OH)2
B
基础过关
3.下列选项所示的物质转化均能一步实现的是( )
D
基础过关
4.构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
(1)C的化学式________________,A的化学式________________.
(2)写出由B生成硫酸铜的化学方程式____________________________________________________.
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有________
A、单质 B、氧化物 C、酸 D、碱 E、盐.
Cu
Cu(OH)2
CuO+H2SO4=CuSO4+H2O
ADE
基础过关
5.采用“双碱法”使烟气(含SO2)脱硫是我国目前环保领域的的经济、实用、高效的一种方法。其脱硫(除去烟气中的二氧化硫)的工业流程如下,试回答:
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水。NaOH溶液喷洒成雾状来吸收SO2的好处是______________________________________________________________。
(2)写出沉淀室中发生的反应化学方程式_____________________________________________。
(3)“双碱法”中实际使用的碱原料只有________________(填名称或化学式)。
增大与二氧化硫的接触面积,从而充分吸收二氧化碳
Ca(OH)2+Na2SO3=CaSO3↓+2NaOH
氢氧化钙
提高训练
1.如图给出了三种物质可能存在的转化关系。根据所学的物质性质及化学变化规律,判断下列选项正确的是( )
A.不能一步实现转化的有①②
B.实现③转化,可将二氧化碳通入氯化钠溶液中
C.实现⑤转化,可加入碳酸钙粉末
D.实现⑥转化,可加入氢氧化钾溶液
A
提高训练
2.氯化镁在化工、冶金、食品、医药等领域都有广泛的应用,是一种重要的原材料。某学习小组在学习了相关知识后,对生成氯化镁的方法加以归纳和整理,如图所示,其中A、B、C、D均为含镁元素的不同类别的物质,都能与X溶液反应生成氯化镁。A为单质,B为氧化物,D与硫酸镁、氯化镁属同一类物质。下列说法不正确的是( )
A.①③发生反应的基本类型分别是置换反应和复分解反应
B.X是盐酸,A是镁,B是氧化镁
C.如果D、Y是常见的同类物质,Y可能是氯化钠
D.C是氢氧化镁,所以③的化学方程式为Mg(OH)2+2HCl===MgCl2+2H2O
C
基础过关
3.如图中的a、b、c、d是初中科学中常见的四种不同类别的物质,连线的两物质(或其水溶液)都能发生化学反应,分别生成甲、乙、丙、丁四种物质(部分生成物已经略去)。其中甲是标准状况下密度最小的气体;
乙为氯化物,是家庭做菜时必要的调味品;
a为常见的单质,它的制品在生活中应用极广,
其组成元素是合成人体血红蛋白所必需的;
c中含有三种元素,c和d相混时会产生蓝色絮状
沉淀物丙。
(1)c的化学式是_______。
(2)a与b反应的化学方程式是_________________________。
(3)c与d反应的基本类型属于_____________。
NaOH
Fe+2HCl=== FeCl2+H2↑
复分解反应
提高训练
4. A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“——”表示相连两物质能发生化学反应,部分反应物、生成物
及反应条件已略去。请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化
学方程式是____________________________________。
(2)若C是锌,A和B都属于酸,写出D可能的化学式
_____________________________________________
_________________________________(物质类别不同的两种即可)。
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
Na2CO3、CuO、NaOH(三种中的任意两种或其他
提高训练
5. 小科以化合价为纵坐标,以物 质类别为横坐标绘制了题示图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均 表示初中科学中的常见物质,
其中“→ ”表示物质 间的转化关系。
已 知A中氧元素 的质量分数为 60%,
C、D、E、F均含有铜元素。请回答:
(1)“A+H2O=== B”的反应属于基本反
应类型中的___________。
(2)写出B和D反应得到C和水的化学方程式
为__________________________________ 。
(3)列举3种能与E反应得到F的物质
__________________________________ 。
化合反应
H2SO4+Cu(OH)2=== CuSO4+2H2O
H2、C、CO(或氢气、碳、一氧化碳)
提高训练
6.A H是初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G﹣H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:
3C+2Fe2O3 ===== 4Fe+3CO2↑
C+CO2 ====2CO
Cl2+2FeCl2=2FeCl3
(1)B的化学式为____________,F的化学式为____________.
(2)反应①的化学方程式为______________________________________.
(3)反应②的化学方程式为______________________________________.
(4)反应③的化学方程式为______________________________________.
(5)某同学认为“图中每一步转化均有元素化合价的变化”,他的判断____________ (填“正确”或“不正确”).
不正确
Fe2O3
HCl
高温
高温
提高训练
7.小明为了测定铜和氧化铜混合物中氧化铜的质量分数,设计组装了如图的实验装置:
(1)仪器识别:a________;b________。
(2)装置A中发生反应的化学方程式 ________________________________ 。
(3)能除去H2中混有少量HCl气体的装置是________(填装置序号)。
(4)装置E中硫酸铜粉末变蓝色,说明硬质试管中反应后有________生成。
(5)实验前硬质试管中混合物的质量为5g,实验后剩余固体质量为4.2g,求混合物中氧化铜的质量分数________ %。
锥形瓶
酒精灯
Zn+2HCl=ZnCl2+H2↑
B
水蒸气
80
浙教版 科学(初中)
九上期末复习课(三)
物质的转化
某些非金属及其化合物之间的转化规律:
盐
碱
酸
碱
非金属
氧气
非金属氧化物
水
酸
加热
非金属氧化物
CO2 + 2NaOH = Na2CO3 + H2O
H2CO3 + 2NaOH = Na2CO3 + H2O
Na2CO3 + 2HCl = 2NaCl + CO2↑
C CO2 H2CO3 CO2
氧气
水
加热
Na2CO3
碱
酸
碱
写出相关的化学方程式:
金属及其化合物之间的转化规律
金属 金属氧化物 碱 金属氧化物
活性强置换活性弱
氧气
水
加热
(不可溶性)
盐
酸
酸/盐
酸
(可溶性)
酸
金属
怎样才能从矿石中得到金属呢?
金属冶炼:
把金属从化合态变成游离态
为了得到金属单质,把金属从化合态变成游离态叫金属的冶炼。
常用的金属冶炼方法:
碳与金属氧化物在高温下反应,碳能夺取金属氧化物中的氧,从而得到金属单质。如:
C
+
CuO
Cu
+
CO2
2
2
高温
碳与氧化铜反应后可以得到单质铜,化学方程式为:
冶炼方法一:碳与金属氧化物在高温下进行反应
冶炼方法二:炽热的碳在高温下会与二氧化碳反应,生成一氧化碳,一氧化碳也能夺取金属氧化物中的氧元素,从而得到单质金属。
C + CO 2 ==== 2CO CO + CuO ==== Cu + CO2
高温
Δ
不是置换反应
冶炼方法三:氢气也能将金属氧化物变成游离态金属。
1.观察氧化铜的颜色:__________。
2.在一支试管中加入少量氧化铜,如图2-41所示,通入氢气,过一会儿,再给氧化铜加热,注意观察试管中的氧化铜有什么变化。
3.反应完成后停止加热,继续通入氢气,直到试管冷却。试管中氧化铜与氢气反应的化学方程式为:________________________________。
黑色粉末
黑色逐渐变成红色
H2
+
CuO
Cu
+
H2O
氧化铜粉末
冶炼方法四:一氧化碳也能将金属氧化物变成游离态金属。
(2)现象:
①玻璃管中的粉末由红色逐渐变为黑色;
②试管中的澄清石灰水变浑浊;
(3)化学方程式
(4)注意事项:
因CO有毒性,故要用点燃的方法进行尾气处理;
(1)装置
物质转化的规律图
1.C、H2、CO三种物质有如下转化关系:①C→CO2;②H2→H2O;③CO→CO2 下列有关说法正确的是( )
A. 上述转化均说明三种物质具有还原性
B. 三种物质都跟氧气发生反应才能实现以上转化
C. 反应前后元素的化合价均发生改变
D. 若三种物质都用来冶炼金属,则以上转化中的反应均为置换反应
A
基础过关
基础过关
2. 某同学在学习了金属及其化合物之间的转化规律后,绘制了可以通过一步反应制取MgSO4的思维导图,其中所选用的物质错误的是( )
A. ①—Mg B. ②—MgCl2
C. ③—H2SO4 D. ④—Mg(OH)2
B
基础过关
3.下列选项所示的物质转化均能一步实现的是( )
D
基础过关
4.构建知识网络是学习化学的重要方法,如图是不同物质相互转化关系图.其中A、B、C、D属于不同类别的物质,且都含有铜元素,B为黑色粉末,C为红色粉末.“→”表示一种物质一步转化成另一种物质(部分反应物、生成物及反应条件未标出),请回答问题:
(1)C的化学式________________,A的化学式________________.
(2)写出由B生成硫酸铜的化学方程式____________________________________________________.
(3)在该知识网络所涉及的化学反应中,可以归纳出能与盐发生反应的物质类别有________
A、单质 B、氧化物 C、酸 D、碱 E、盐.
Cu
Cu(OH)2
CuO+H2SO4=CuSO4+H2O
ADE
基础过关
5.采用“双碱法”使烟气(含SO2)脱硫是我国目前环保领域的的经济、实用、高效的一种方法。其脱硫(除去烟气中的二氧化硫)的工业流程如下,试回答:
(1)吸收塔中,用NaOH溶液吸收SO2生成亚硫酸钠(Na2SO3)和水。NaOH溶液喷洒成雾状来吸收SO2的好处是______________________________________________________________。
(2)写出沉淀室中发生的反应化学方程式_____________________________________________。
(3)“双碱法”中实际使用的碱原料只有________________(填名称或化学式)。
增大与二氧化硫的接触面积,从而充分吸收二氧化碳
Ca(OH)2+Na2SO3=CaSO3↓+2NaOH
氢氧化钙
提高训练
1.如图给出了三种物质可能存在的转化关系。根据所学的物质性质及化学变化规律,判断下列选项正确的是( )
A.不能一步实现转化的有①②
B.实现③转化,可将二氧化碳通入氯化钠溶液中
C.实现⑤转化,可加入碳酸钙粉末
D.实现⑥转化,可加入氢氧化钾溶液
A
提高训练
2.氯化镁在化工、冶金、食品、医药等领域都有广泛的应用,是一种重要的原材料。某学习小组在学习了相关知识后,对生成氯化镁的方法加以归纳和整理,如图所示,其中A、B、C、D均为含镁元素的不同类别的物质,都能与X溶液反应生成氯化镁。A为单质,B为氧化物,D与硫酸镁、氯化镁属同一类物质。下列说法不正确的是( )
A.①③发生反应的基本类型分别是置换反应和复分解反应
B.X是盐酸,A是镁,B是氧化镁
C.如果D、Y是常见的同类物质,Y可能是氯化钠
D.C是氢氧化镁,所以③的化学方程式为Mg(OH)2+2HCl===MgCl2+2H2O
C
基础过关
3.如图中的a、b、c、d是初中科学中常见的四种不同类别的物质,连线的两物质(或其水溶液)都能发生化学反应,分别生成甲、乙、丙、丁四种物质(部分生成物已经略去)。其中甲是标准状况下密度最小的气体;
乙为氯化物,是家庭做菜时必要的调味品;
a为常见的单质,它的制品在生活中应用极广,
其组成元素是合成人体血红蛋白所必需的;
c中含有三种元素,c和d相混时会产生蓝色絮状
沉淀物丙。
(1)c的化学式是_______。
(2)a与b反应的化学方程式是_________________________。
(3)c与d反应的基本类型属于_____________。
NaOH
Fe+2HCl=== FeCl2+H2↑
复分解反应
提高训练
4. A、B、C、D是初中科学常见的四种物质,其中A、B属于相同物质类别的化合物,C、D物质类别不同,它们之间的转化和反应关系如图。图中“→”表示某一种物质经一步反应可转化为另一种物质,“——”表示相连两物质能发生化学反应,部分反应物、生成物
及反应条件已略去。请回答:
(1)若C是二氧化碳,B是氢氧化钙,则B→A的化
学方程式是____________________________________。
(2)若C是锌,A和B都属于酸,写出D可能的化学式
_____________________________________________
_________________________________(物质类别不同的两种即可)。
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
Na2CO3、CuO、NaOH(三种中的任意两种或其他
提高训练
5. 小科以化合价为纵坐标,以物 质类别为横坐标绘制了题示图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均 表示初中科学中的常见物质,
其中“→ ”表示物质 间的转化关系。
已 知A中氧元素 的质量分数为 60%,
C、D、E、F均含有铜元素。请回答:
(1)“A+H2O=== B”的反应属于基本反
应类型中的___________。
(2)写出B和D反应得到C和水的化学方程式
为__________________________________ 。
(3)列举3种能与E反应得到F的物质
__________________________________ 。
化合反应
H2SO4+Cu(OH)2=== CuSO4+2H2O
H2、C、CO(或氢气、碳、一氧化碳)
提高训练
6.A H是初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G﹣H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:
3C+2Fe2O3 ===== 4Fe+3CO2↑
C+CO2 ====2CO
Cl2+2FeCl2=2FeCl3
(1)B的化学式为____________,F的化学式为____________.
(2)反应①的化学方程式为______________________________________.
(3)反应②的化学方程式为______________________________________.
(4)反应③的化学方程式为______________________________________.
(5)某同学认为“图中每一步转化均有元素化合价的变化”,他的判断____________ (填“正确”或“不正确”).
不正确
Fe2O3
HCl
高温
高温
提高训练
7.小明为了测定铜和氧化铜混合物中氧化铜的质量分数,设计组装了如图的实验装置:
(1)仪器识别:a________;b________。
(2)装置A中发生反应的化学方程式 ________________________________ 。
(3)能除去H2中混有少量HCl气体的装置是________(填装置序号)。
(4)装置E中硫酸铜粉末变蓝色,说明硬质试管中反应后有________生成。
(5)实验前硬质试管中混合物的质量为5g,实验后剩余固体质量为4.2g,求混合物中氧化铜的质量分数________ %。
锥形瓶
酒精灯
Zn+2HCl=ZnCl2+H2↑
B
水蒸气
80
同课章节目录
