9.1常见的金属材料同步练习鲁教版化学九年级下册(有答案)
文档属性
| 名称 | 9.1常见的金属材料同步练习鲁教版化学九年级下册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 234.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-20 00:00:00 | ||
图片预览




文档简介
9.1常见的金属材料
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.推理是学习化学的一种重要方法,但推理必须科学、严谨。下列推理正确的是( )
A.氧化物中含有氧元素,所以含有氧元素的物质就是氧化物
B.由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成
C.原子核是由质子和中子构成的,故所有原子核中都一定含有质子和中子
D.不锈钢虽然是金属材料,但它属于混合物而不是金属单质
2.区别下列各组物质,所选择的方法或试剂错误的是
待区分的物质 区分方法或试剂
A 两瓶无色气体:氧气和氮气 分别用手轻扇闻气味
B 两种无色溶液:水和过氧化氢溶液 分别加入少量二氧化锰
C 两种黑色粉末:木炭粉和氧化铜 分别在空气中灼烧
D 两种常用金属:铁丝和铜片 打磨观察颜色
A.A B.B C.C D.D
3.我国科学家率先用铝合金和石墨烯按一定比例混合制成“烯合金”,该材料有望生产出“一分钟充满电的电池”。下列关于“烯合金”的说法不正确的是
A.常温下稳定 B.是一种纯净物
C.具有导电性 D.含碳元素和铝元素
4.下列有关合金的叙述,正确的有
①合金中至少含有两种金属
②合金一定是混合物
③合金中的元素以化合物的形式存在
④合金一般比组成它们的纯金属硬度更高,熔点更低
⑤合金中各成分保持自己原有的化学性质
A.①②④ B.②④⑤ C.②③⑤ D.①③④
5.物质的组成结构决定性质是化学基本思想。下列说法不正确的是
A 生铁和钢机械性能不同 含碳量不同
B 氧气和液氧颜色不同 氧分子之间的间隔不同
C 金刚石和石墨物理性质不同 碳原子的排列方式不同
D 食盐在人体中能生成胃酸 食盐中有钠离子缘故
A.A B.B C.C D.D
6.下列有关金属的说法中正确的是( )
A.金属在自然界中都以单质形式存在
B.地壳中含量最高的金属元素是铁元素
C.武德合金熔点高,常用作保险丝
D.黄铜(锌铜合金)比纯铜的硬度大
7.下列对于“一定”说法正确的是( )
A.化合物一定由分子构成 B.单质一定由原子构成
C.溶液和合金一定是混合物 D.固体和液体构成的一定是混合物
8.下列物质名称与其主要成分不相匹配的是
A.大理石――SiO2 B.赤铁矿――Fe2O3
C.铝土矿――Al2O3 D.辉铜矿――Cu2S
9.下列合金(金属)的比较,不正确的是
A.含碳量:生铁>钢 B.抗腐蚀性:纯铝>纯铁
C.硬度:生铁>纯铁 D.熔点:焊锡>锡
10.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 除去N2中的O2 将混合气体通过红热的铜网
B 除去Cu粉中少量的Fe粉 用磁铁吸引
C 除去CO2中少量的CO 点燃
D 区分硬水和软水 加肥皂水,振荡
A.A B.B C.C D.D
二、判断题
11.钙是人体含量最高的金属元素。( )
12.生铁和钢的性质和用途的差别主要是因为含碳量不同。( )
13.日常是生活中常用的金属材料,大多数是合金。____
14.金属是一类重要的材料,人类的生活和生产都离不开金属。( )
15.合金是一种金属和其它金属熔合形成的具有金属特性的物质( )
三、填空题
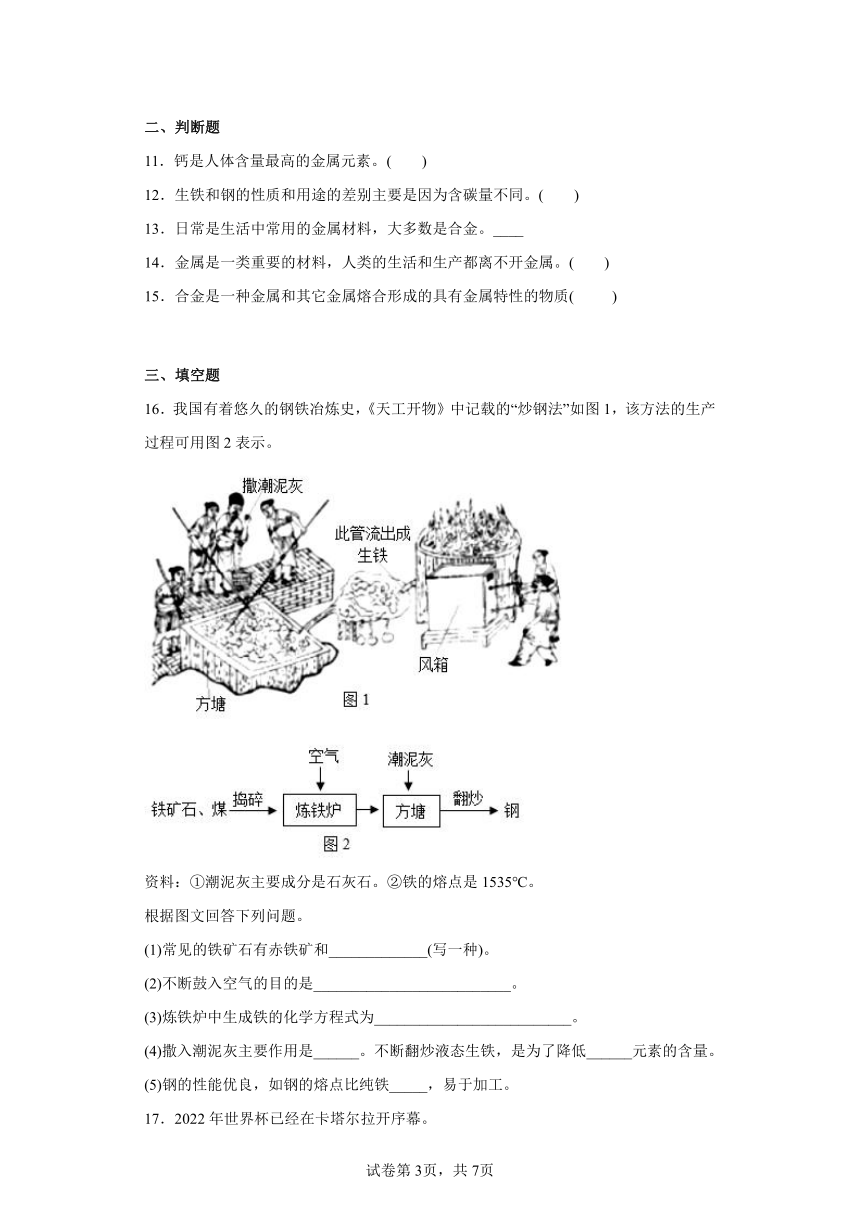
16.我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”如图1,该方法的生产过程可用图2表示。
资料:①潮泥灰主要成分是石灰石。②铁的熔点是1535℃。
根据图文回答下列问题。
(1)常见的铁矿石有赤铁矿和_____________(写一种)。
(2)不断鼓入空气的目的是__________________________。
(3)炼铁炉中生成铁的化学方程式为__________________________。
(4)撒入潮泥灰主要作用是______。不断翻炒液态生铁,是为了降低______元素的含量。
(5)钢的性能优良,如钢的熔点比纯铁_____,易于加工。
17.2022年世界杯已经在卡塔尔拉开序幕。
(1)世界杯场馆建设使用了大量金属材料—钢。钢属于___________(填“合金”或“金属”),主要含有的元素是___________(填元素符号),钢的含碳量___________生铁(填“>”、“=”、“<”)
(2)世界杯中的足球。化学上有一种物质叫足球烯,其分子是由60个碳原子构成,因结构形似足球而得名,它的化学式为___________。
(3)卡塔尔水资源缺乏,是一个水比汽油贵的国家,主要依靠海水净化获得淡水。海水属于硬水,因为里面含有较多___________、___________(填离子符号),生活中可以用___________鉴别硬水,现象是___________。写出一个节约用水或者保护水资源措施___________
(4)世界杯比赛中经常会出现运动员受伤倒地,医生对着伤口喷射一种药水—氯乙烷(C2H5Cl),不用多久运动员便能继续投入比赛。工业上常用乙烯(C2H4)和氯化氢在催化剂作用下反应得到氯乙烷,请写出反应的化学方程式___________。
18.工业上炼铁炼钢和轧制钢材的主要流程如下图:
已知:生铁的含碳量为2%~4.3%,钢的含碳量为 0.03%~2%。
(1)反应:①Fe2O3+3CO[Math Processing Error] 2Fe+3CO,②Fe2O3+3C[Math Processing Error]2Fe+3CO。属于置换反应的是________,用于高炉炼铁的原理是______________(填序号)。
(2)炼铁的固体原料需经过粉碎,其目的是__________________________。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是______________。炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是______________。
(4)炼钢炉中,通入纯氧的目的是_______________。将钢锭轧成钢板,体现了金属的______________性。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式:______________。
19.选择下列适当的物质填空(选填序号):
A.活性炭 B.盐酸 C.石灰石 D.镁粉 E.洗洁精F.食盐G.硝酸铵H.武德合金
(1)可用作制保险丝的是___________;
(2)生活中作乳化剂的是___________;
(3)溶于水温度降低的是___________;
(4)可除去冰箱异味的是___________;
(5)可用作制照明弹的是___________;
(6)可用于工业炼铁的是___________。
20.用下图装置进行实验(夹持仪器略去)。
(1)玻璃管中的现象是______,反应的化学方程式为______。
(2)澄清石灰水的作用是______。
(3)尾气中主要含有 CO2和______,应处理后再排放。
四、综合应用题
21.化学是一门以实验为基础的学科,实验是学习化学进行科学探究的重要途径。
(1)下列关于实验现象的描述中正确的是______。
A.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.将氯化铵和熟石灰混合后研磨,有刺激性气味气体产生
C.将铜丝插入稀盐酸中,产生气泡,溶液逐渐变为蓝色
D.向盛有块状石灰石的试管中倒入稀硫酸,有气泡持续冒出
(2)下列是实验室制取气体的装置图。
①实验室利用A、C装置制取氧气,则A中发生反应的化学方程式为______;利用G装置收集到氧气的最佳时刻是______。
②B装置的球形管内固体为大理石,烧杯内 盛有稀盐酸反应的化学方程式为______,若要用F装置收集一瓶干燥的CO2(气体从导管h进入集气瓶内),并检验CO2的性质则所选用装置的导管接口从左到右的正确连接顺序为:a接______、______接______、______接______、______接______;与F装置匹配最合适的带导管的橡皮塞是图2中的______。
(3)图3是化学小组设计的模拟炼铁微型实验装置。
①实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的气体已纯净的方法是______。
②我国是世界钢铁产量最大的国家,某冶炼厂按计划冶炼含铁质量分数为98%的生铁1000吨,试计算:若用含杂质质量分数为20%的赤铁矿冶炼,最少需要该赤铁矿多少吨?______
22.钢铁是目前世界上使用最多的金属材料。我国早在春秋战国时期就开始炼铁、应用金属铁。
炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料放入高炉,在高温条件下,炼铁,反应过程如下图所示。则回答:
(1)原料中焦炭在第①②步中都要用到,则焦炭的作用是______________。在冶炼反应过程中应先__________ (填“加热”或“通入CO”),其目的___________。
(2)当反应进行一段时间后,第③步中出现的现象为___________________,该反应化学方程式为______________。冶炼铁时除CO外,还可用_______等物质来还原赤铁矿中的氧化铁。
(3)中国钢铁公司为了测定朝鲜茂山铁矿的优质赤铁矿中氧化铁的质量分数。公司实验室取该赤铁矿样品10g与足量的一氧化碳充分反应,测得反应后固体物质的质量为7.6g(假设赤铁矿中的杂质不参加反应)。则赤铁矿样品中氧化铁的质量分数为_____。
23.2019年底,徐宿淮盐铁路将建成通车,淮安人可实现高铁出行。
(1)高铁在建造时使用了大量的新材料,下列属于金属材料的是 ______ (填序号)。
A生产高铁车头的玻璃钢
B制造高铁车身的镁铝合金
C制造轨道枕木的聚氨酯材料
D建筑高铁路基的钢筋混凝土
(2)高铁刹车制动盘使用合金锻钢制作,主要利用该合金耐高温、 ______ 等特性。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.B
4.B
5.D
6.D
7.C
8.A
9.D
10.C
11.正确
12.正确
13.正确
14.正确
15.错误
16.(1)磁铁矿(或菱铁矿)
(2)提高炉温
(3)(或)
(4) 除杂 碳##C
(5)低
17.(1) 合金 Fe和C <
(2)C60
(3) Ca2+ Mg2+ 肥皂水 生成浮渣多 生活污染处理后再排放(或洗衣服的水拖地或淘米水浇花等,合理即可)
(4)
18. ② ① 增大反应接触面积,加快反应速率 N2 +4 使生铁中的碳转化为二氧化碳,降低生铁中碳含量 延展 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
19.(1)H
(2)E
(3)G
(4)A
(5)D
(6)C
20. 红色固体变黑色 检验生成的二氧化碳气体 CO
21.(1)B
(2) 导管口气泡连续均匀产生时 g f b c h m e 丙
(3) 在右端导气管口用排水法收集一试管气体,移近火焰点火,若发出轻微的爆鸣声,证明气体已纯净 设需要Fe2O3的质量为x
解得:x=1440t;
最少需要亦铁矿的质量为。
答:理论上可炼出纯铁1750吨。
22. 作燃料提供高温并生成还原剂CO 通入CO 排出空气,防止加热时发生爆炸 红色固体变为黑色 C或H2 80%
23. B 耐磨。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.推理是学习化学的一种重要方法,但推理必须科学、严谨。下列推理正确的是( )
A.氧化物中含有氧元素,所以含有氧元素的物质就是氧化物
B.由同种分子构成的物质是纯净物,所以纯净物一定由同种分子构成
C.原子核是由质子和中子构成的,故所有原子核中都一定含有质子和中子
D.不锈钢虽然是金属材料,但它属于混合物而不是金属单质
2.区别下列各组物质,所选择的方法或试剂错误的是
待区分的物质 区分方法或试剂
A 两瓶无色气体:氧气和氮气 分别用手轻扇闻气味
B 两种无色溶液:水和过氧化氢溶液 分别加入少量二氧化锰
C 两种黑色粉末:木炭粉和氧化铜 分别在空气中灼烧
D 两种常用金属:铁丝和铜片 打磨观察颜色
A.A B.B C.C D.D
3.我国科学家率先用铝合金和石墨烯按一定比例混合制成“烯合金”,该材料有望生产出“一分钟充满电的电池”。下列关于“烯合金”的说法不正确的是
A.常温下稳定 B.是一种纯净物
C.具有导电性 D.含碳元素和铝元素
4.下列有关合金的叙述,正确的有
①合金中至少含有两种金属
②合金一定是混合物
③合金中的元素以化合物的形式存在
④合金一般比组成它们的纯金属硬度更高,熔点更低
⑤合金中各成分保持自己原有的化学性质
A.①②④ B.②④⑤ C.②③⑤ D.①③④
5.物质的组成结构决定性质是化学基本思想。下列说法不正确的是
A 生铁和钢机械性能不同 含碳量不同
B 氧气和液氧颜色不同 氧分子之间的间隔不同
C 金刚石和石墨物理性质不同 碳原子的排列方式不同
D 食盐在人体中能生成胃酸 食盐中有钠离子缘故
A.A B.B C.C D.D
6.下列有关金属的说法中正确的是( )
A.金属在自然界中都以单质形式存在
B.地壳中含量最高的金属元素是铁元素
C.武德合金熔点高,常用作保险丝
D.黄铜(锌铜合金)比纯铜的硬度大
7.下列对于“一定”说法正确的是( )
A.化合物一定由分子构成 B.单质一定由原子构成
C.溶液和合金一定是混合物 D.固体和液体构成的一定是混合物
8.下列物质名称与其主要成分不相匹配的是
A.大理石――SiO2 B.赤铁矿――Fe2O3
C.铝土矿――Al2O3 D.辉铜矿――Cu2S
9.下列合金(金属)的比较,不正确的是
A.含碳量:生铁>钢 B.抗腐蚀性:纯铝>纯铁
C.硬度:生铁>纯铁 D.熔点:焊锡>锡
10.下列实验操作不能达到实验目的的是
选项 实验目的 实验操作
A 除去N2中的O2 将混合气体通过红热的铜网
B 除去Cu粉中少量的Fe粉 用磁铁吸引
C 除去CO2中少量的CO 点燃
D 区分硬水和软水 加肥皂水,振荡
A.A B.B C.C D.D
二、判断题
11.钙是人体含量最高的金属元素。( )
12.生铁和钢的性质和用途的差别主要是因为含碳量不同。( )
13.日常是生活中常用的金属材料,大多数是合金。____
14.金属是一类重要的材料,人类的生活和生产都离不开金属。( )
15.合金是一种金属和其它金属熔合形成的具有金属特性的物质( )
三、填空题
16.我国有着悠久的钢铁冶炼史,《天工开物》中记载的“炒钢法”如图1,该方法的生产过程可用图2表示。
资料:①潮泥灰主要成分是石灰石。②铁的熔点是1535℃。
根据图文回答下列问题。
(1)常见的铁矿石有赤铁矿和_____________(写一种)。
(2)不断鼓入空气的目的是__________________________。
(3)炼铁炉中生成铁的化学方程式为__________________________。
(4)撒入潮泥灰主要作用是______。不断翻炒液态生铁,是为了降低______元素的含量。
(5)钢的性能优良,如钢的熔点比纯铁_____,易于加工。
17.2022年世界杯已经在卡塔尔拉开序幕。
(1)世界杯场馆建设使用了大量金属材料—钢。钢属于___________(填“合金”或“金属”),主要含有的元素是___________(填元素符号),钢的含碳量___________生铁(填“>”、“=”、“<”)
(2)世界杯中的足球。化学上有一种物质叫足球烯,其分子是由60个碳原子构成,因结构形似足球而得名,它的化学式为___________。
(3)卡塔尔水资源缺乏,是一个水比汽油贵的国家,主要依靠海水净化获得淡水。海水属于硬水,因为里面含有较多___________、___________(填离子符号),生活中可以用___________鉴别硬水,现象是___________。写出一个节约用水或者保护水资源措施___________
(4)世界杯比赛中经常会出现运动员受伤倒地,医生对着伤口喷射一种药水—氯乙烷(C2H5Cl),不用多久运动员便能继续投入比赛。工业上常用乙烯(C2H4)和氯化氢在催化剂作用下反应得到氯乙烷,请写出反应的化学方程式___________。
18.工业上炼铁炼钢和轧制钢材的主要流程如下图:
已知:生铁的含碳量为2%~4.3%,钢的含碳量为 0.03%~2%。
(1)反应:①Fe2O3+3CO[Math Processing Error] 2Fe+3CO,②Fe2O3+3C[Math Processing Error]2Fe+3CO。属于置换反应的是________,用于高炉炼铁的原理是______________(填序号)。
(2)炼铁的固体原料需经过粉碎,其目的是__________________________。
(3)热空气和高炉气体的主要成分有一种相同,这种气体的化学式是______________。炉渣中含有硅酸钙(CaSiO3),其中硅元素的化合价是______________。
(4)炼钢炉中,通入纯氧的目的是_______________。将钢锭轧成钢板,体现了金属的______________性。
(5)钢铁制品可能会生锈,写出用稀硫酸除锈反应的化学方程式:______________。
19.选择下列适当的物质填空(选填序号):
A.活性炭 B.盐酸 C.石灰石 D.镁粉 E.洗洁精F.食盐G.硝酸铵H.武德合金
(1)可用作制保险丝的是___________;
(2)生活中作乳化剂的是___________;
(3)溶于水温度降低的是___________;
(4)可除去冰箱异味的是___________;
(5)可用作制照明弹的是___________;
(6)可用于工业炼铁的是___________。
20.用下图装置进行实验(夹持仪器略去)。
(1)玻璃管中的现象是______,反应的化学方程式为______。
(2)澄清石灰水的作用是______。
(3)尾气中主要含有 CO2和______,应处理后再排放。
四、综合应用题
21.化学是一门以实验为基础的学科,实验是学习化学进行科学探究的重要途径。
(1)下列关于实验现象的描述中正确的是______。
A.铁丝在氧气中剧烈燃烧,火星四射,生成四氧化三铁
B.将氯化铵和熟石灰混合后研磨,有刺激性气味气体产生
C.将铜丝插入稀盐酸中,产生气泡,溶液逐渐变为蓝色
D.向盛有块状石灰石的试管中倒入稀硫酸,有气泡持续冒出
(2)下列是实验室制取气体的装置图。
①实验室利用A、C装置制取氧气,则A中发生反应的化学方程式为______;利用G装置收集到氧气的最佳时刻是______。
②B装置的球形管内固体为大理石,烧杯内 盛有稀盐酸反应的化学方程式为______,若要用F装置收集一瓶干燥的CO2(气体从导管h进入集气瓶内),并检验CO2的性质则所选用装置的导管接口从左到右的正确连接顺序为:a接______、______接______、______接______、______接______;与F装置匹配最合适的带导管的橡皮塞是图2中的______。
(3)图3是化学小组设计的模拟炼铁微型实验装置。
①实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的气体已纯净的方法是______。
②我国是世界钢铁产量最大的国家,某冶炼厂按计划冶炼含铁质量分数为98%的生铁1000吨,试计算:若用含杂质质量分数为20%的赤铁矿冶炼,最少需要该赤铁矿多少吨?______
22.钢铁是目前世界上使用最多的金属材料。我国早在春秋战国时期就开始炼铁、应用金属铁。
炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料放入高炉,在高温条件下,炼铁,反应过程如下图所示。则回答:
(1)原料中焦炭在第①②步中都要用到,则焦炭的作用是______________。在冶炼反应过程中应先__________ (填“加热”或“通入CO”),其目的___________。
(2)当反应进行一段时间后,第③步中出现的现象为___________________,该反应化学方程式为______________。冶炼铁时除CO外,还可用_______等物质来还原赤铁矿中的氧化铁。
(3)中国钢铁公司为了测定朝鲜茂山铁矿的优质赤铁矿中氧化铁的质量分数。公司实验室取该赤铁矿样品10g与足量的一氧化碳充分反应,测得反应后固体物质的质量为7.6g(假设赤铁矿中的杂质不参加反应)。则赤铁矿样品中氧化铁的质量分数为_____。
23.2019年底,徐宿淮盐铁路将建成通车,淮安人可实现高铁出行。
(1)高铁在建造时使用了大量的新材料,下列属于金属材料的是 ______ (填序号)。
A生产高铁车头的玻璃钢
B制造高铁车身的镁铝合金
C制造轨道枕木的聚氨酯材料
D建筑高铁路基的钢筋混凝土
(2)高铁刹车制动盘使用合金锻钢制作,主要利用该合金耐高温、 ______ 等特性。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.A
3.B
4.B
5.D
6.D
7.C
8.A
9.D
10.C
11.正确
12.正确
13.正确
14.正确
15.错误
16.(1)磁铁矿(或菱铁矿)
(2)提高炉温
(3)(或)
(4) 除杂 碳##C
(5)低
17.(1) 合金 Fe和C <
(2)C60
(3) Ca2+ Mg2+ 肥皂水 生成浮渣多 生活污染处理后再排放(或洗衣服的水拖地或淘米水浇花等,合理即可)
(4)
18. ② ① 增大反应接触面积,加快反应速率 N2 +4 使生铁中的碳转化为二氧化碳,降低生铁中碳含量 延展 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
19.(1)H
(2)E
(3)G
(4)A
(5)D
(6)C
20. 红色固体变黑色 检验生成的二氧化碳气体 CO
21.(1)B
(2) 导管口气泡连续均匀产生时 g f b c h m e 丙
(3) 在右端导气管口用排水法收集一试管气体,移近火焰点火,若发出轻微的爆鸣声,证明气体已纯净 设需要Fe2O3的质量为x
解得:x=1440t;
最少需要亦铁矿的质量为。
答:理论上可炼出纯铁1750吨。
22. 作燃料提供高温并生成还原剂CO 通入CO 排出空气,防止加热时发生爆炸 红色固体变为黑色 C或H2 80%
23. B 耐磨。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
