九年级化学京改版(2013)下册 第10章金属检测题(有答案)
文档属性
| 名称 | 九年级化学京改版(2013)下册 第10章金属检测题(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 177.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-22 00:00:00 | ||
图片预览



文档简介
第10章《金属》检测题
一、单选题
1.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是
A.银白色 B.密度较大 C.导电性良好 D.能被氧化
2.下列属于纯净物的是
A.汽水 B.氢气 C.黄铜 D.空气
3.下列对实验现象的描述正确的是
A.铁丝在空气中燃烧,有黑色固体生成 B.光亮的铜丝放入稀硫酸中,产生大量气泡
C.红磷在氧气中燃烧,产生大量白烟 D.硫粉在氧气中燃烧,产生淡蓝色火焰
4.有关金属与金属材料的说法中错误的是
A.银的导电性比铜好,但电线一般用铜制,主要与价格和资源等因素有关
B.生铁和钢都是铁合金,但钢中的含碳量比生铁中高
C.铝合金门窗耐腐蚀性好,硬度高
D.焊锡是锡和铅的合金,其熔点低,可以用于焊接金属
5.化学知识可以指导生活实践。下列说法不正确的是
A.加热煮沸不能降低水的硬度 B.用肥皂水区分硬水和软水
C.不锈钢抗锈蚀性能比铁好 D.炒菜时油锅着火可用锅盖盖灭
6.某工业尾气中可能含有H2、CO和CO2中的一种或几种,为检验其成分,小明同学按下图装置进行实验时,观察到黑色固体变红,澄清石灰水变浑浊,由此实验现象得出尾气的组成情况可能有
A.2种 B.3种 C.4种 D.5种
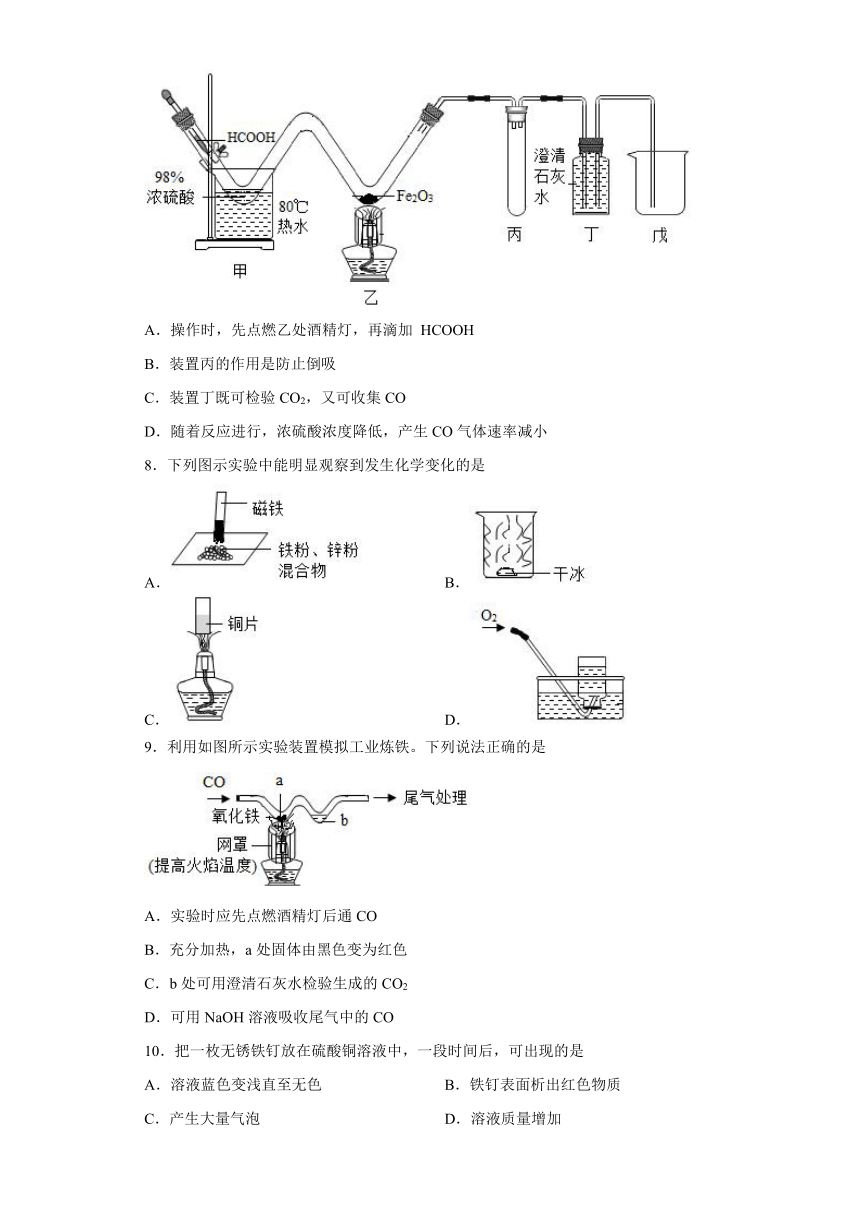
7.利用甲酸( HCOOH)与浓硫酸制备CO,并用如下实验装置验证CO的有关性质。已知: ,下列说法不正确的是
A.操作时,先点燃乙处酒精灯,再滴加 HCOOH
B.装置丙的作用是防止倒吸
C.装置丁既可检验CO2,又可收集CO
D.随着反应进行,浓硫酸浓度降低,产生CO气体速率减小
8.下列图示实验中能明显观察到发生化学变化的是
A. B.
C. D.
9.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
10.把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是
A.溶液蓝色变浅直至无色 B.铁钉表面析出红色物质
C.产生大量气泡 D.溶液质量增加
11.下列有关金属材料的说法错误的是
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
二、简答题
12.化学实验是学习化学的重要方法.请完成下列金属性质的实验.
(1)实验一:比较铁、铜的金属活动性强弱.请你设计实验完成下表内容.
实验步骤 实验现象 结 论
________________ ________________ 金属活动性:Fe>Cu
(2)实验二:镁、锌、铁三种金属与酸的反应.
[实验]取一定量的镁、锌、铁三种金属分别加入到溶质质量分数相同的稀硫酸中,充分反应,观察现象.
[结论]活泼金属能与酸反应.
[分析]
①三个反应的共同特点是_________,写出其中一个反应的化学方程式__________________.
②若完全反应后,三个反应生成氢气的质量相等,原因是__________________.
13.金属用途广泛,金属的用途与其性质密切相关。
(1)如图中将两块金属片相互刻画,该实验的目的是什么?
(2)某同学在Cu(NO3)2和AgNO3的混合溶液中加入一定质量的锌粉,充分反应后过滤,发现滤液仍呈蓝色。分析滤液中溶质的成分,并写出Zn与AgNO3溶液反应的化学方程式。
14.A、B、C、D为金属活动顺序表中常见的四种金属。已知:①A+BSO4===ASO4+B;②C+H2SO4===CSO4+H2↑;③B+2DNO3===B(NO3)2+2D。请完成以下填空:
(1)金属C在金属活动顺序表中排在氢________(填“前面”或“后面”)。
(2)根据上述反应能判断出其中三种金属的活动性,其金属活动性由强到弱的顺序是
____________(填字母)。
(3)若A、B、C、D分别为锌、铁、铜、银中的一种,金属C与H2SO4反应后所得溶液呈浅绿色,则金属A为________,反应③的化学方程式为________________________________。
三、推断题
15.A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件,部分反应物及生成物已略去),请回答下列问题:
(1)A的化学式为____________;
(2)B的一种用途是____________;
(3)反应③的化学方程式为:_________________;
(4)E、F、G三种金属的活动性由强到弱的顺序为_______________。(用元素符号表示)
16.如图是铁元素循环的关系图,箭号表示能实现一步转化。
(1)反应①中可观察到__________现象。
(2)①~⑤五个反应中,铁元素的化合价不变的反应是__________(填序号)。
(3)反应③的化学方程式为__________,该反应属于__________反应(填基本反应类型)。
17.从ZnSO4、CuSO4和FeSO4的混合液中回收金属铜,设计了如下方案:
①操作a的名称是______,加入锌后,写出发生反应的一个化学方程式__,该反应体现了铜的金属活动性比锌____(选填“强”或“弱”)。
②操作a后的固体中一定有的物质是____,生成气体的化学式是_____。
四、实验题
18.某化学兴趣小组利用下图装置进行实验。探究工业炼铁的化学原理,试按要求填空。
(1)硬质玻璃管中观察到的现象是__________,写出一氧化碳和氧化铁反应的化学方程式________;
(2)实验中首先通入一氧化碳的目的是__________;
(3)装置中导管末端加一点燃的酒精灯目的是______________。
19.有三瓶失去标签的溶质质量分数为15%、10%、5%的盐酸。选择下列仪器和药品,设计两种不同的方案,辨别出三瓶盐酸
实验仪器:温度计、量筒、秒表、烧杯、试管、剪刀、镊子
药品:镁条
提示:镁条和盐酸反应速度很快,通过观察放出气泡的速度很难准确判断盐酸浓度的大小。
(1)写出镁与盐酸反应的化学方程式:_______________。
(2)实验的关键是控制三个变量:
①在的环境温度下进行实验。
②取相同质量的镁条。
③取_____________________。
(3)你的方案是:
方案一:测定_________________。
方案—:测定____________________。
20.铁是应用最广泛的金属,通过冶炼铁矿可以得到铁。
(1)高炉是工业炼铁的主要设备(如图1)。
①高炉炼铁中,焦炭的作用是_______(用化学方程式表示)。
②写出高炉中以赤铁矿为原料得到铁的化学方程式:_______。
(2)实验室用氧化铁粉末模拟炼铁(如图2),并探究产物成分。
①实验中观察到硬质玻璃管内固体全部变为黑色,澄清石灰水变浑浊:实验结束时,硬质玻璃管内物质冷却后才停止通一氧化碳的主要原因是________;该装置的一个明显缺陷是________。
②查阅资料发现:
一氧化碳还原氧化铁后剩余固体可能由四氧化三铁、氧化亚铁、铁粉和未反应的氧化铁中的一种或几种组成;进一步查得三种铁的氧化物的某些性质如下表:
氧化亚铁 氧化铁 四氧化三铁
颜色 黑色 红棕色 黑色
磁性 无 无 有
与硫酸铜溶液 不反应
与稀盐酸 反应生成可溶性物质,无气体放出
由实验中_________的现象,确认剩余固体中已无氧化铁。
③继续探究剩余固体的组成:
步骤 实验操作 实验现象 实验结论
1 用磁铁吸引剩余固体 a_________ 剩余固体中没有氧化亚铁
2 b_________ c_________ 剩余固体中只有铁粉
五、计算题
21.某铁矿粉,主要成分为铁的氧化物(FeXOy),一学生利用实验作进一步分析,过程及数据如下。(注:铁矿粉中杂质不参与下列过程中的反应)
Ⅰ.取30g该铁矿粉在CO气流中充分加热,将反应后的气体用烧碱溶液充分吸收,烧碱溶液增重17.6g
Ⅱ.将上述加热后的固体取出后,再向固体逐滴加入稀硫酸,测得产生气体与滴入稀硫酸的质量关系如图:
通过计算回答下列问题:
(1)30g铁矿粉所含铁的氧化物中,铁元素的质量为______g,氧元素的质量为______g。
(2)该铁的氧化物化学式中,x、y的最简整数比x:y=______。
22.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下:
第一次 第二次 第三次 第四次 第五次 第六次
加入稀硫酸的质量(g) 10 10 10 10 10 10
剩余固体的质量(g) 9.35 8.7 8.05 7.4 6.75 6.75
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
参考答案:
1.D 2.B 3.C 4.B 5.A 6.D 7.A 8.C 9.C 10.B 11.C
12. 向硫酸铜溶液中投入铁钉 铁钉表面有红色固体析出,溶液由蓝色变为浅绿色 都是置换反应 Mg+H2SO4=MgSO4+H2↑或Zn+H2SO4=ZnSO4+H2↑或Fe+H2SO4=FeSO4+H2↑; 当三种金属过量,硫酸完全反应时,则生成氢气质量相等;当硫酸过量,三种金属完全反应,且质量比为mMg:mZn:mFe=24:65:56时,则生成氢气质量相等.
13.(1)比较黄铜和纯铜的硬度
(2)一定含Cu(NO3)2和Zn(NO3)2,可能含AgNO3;Zn+2AgNO3=Zn(NO3)2+2Ag
14. 前面 A>B>D Zn Cu+2AgNO3===Cu(NO3)2+2Ag
15. Fe2O3 冶炼金属 Fe+CuSO4=FeSO4+Cu 铁>铜>银
16.(1)铁溶解,产生气泡,溶液变为浅绿色
(2)③④##④③
(3) 复分解
17. 过滤 弱 Fe、Cu H2
18. 红色固体变为黑色 排尽装置中的空气,防止加热时发生爆炸 将尾气CO燃烧掉,防止污染空气
19.(1)Mg+2HCl=MgCl2+H2↑
(2)相同体积的盐酸
(3) 不同浓度盐酸和镁条反应所需时间 不同浓度盐酸和镁条反应后所得溶液的温度
20.(1) 和
(2) 防止生成的铁在高温条件下再次被氧化 没有尾气处理装置 红棕色粉末完全转化为黑色 黑色固体被全部吸引 往剩余固体中加足量硝酸铜 黑色固体全部变成红色
21. 16.8 6.4 3:4
22.(1)32.5%; (2)9.8%
一、单选题
1.银是一种银白色金属,密度较大,具有良好的导电性,长期放置会被氧化而发黑。其中属于银的化学性质的是
A.银白色 B.密度较大 C.导电性良好 D.能被氧化
2.下列属于纯净物的是
A.汽水 B.氢气 C.黄铜 D.空气
3.下列对实验现象的描述正确的是
A.铁丝在空气中燃烧,有黑色固体生成 B.光亮的铜丝放入稀硫酸中,产生大量气泡
C.红磷在氧气中燃烧,产生大量白烟 D.硫粉在氧气中燃烧,产生淡蓝色火焰
4.有关金属与金属材料的说法中错误的是
A.银的导电性比铜好,但电线一般用铜制,主要与价格和资源等因素有关
B.生铁和钢都是铁合金,但钢中的含碳量比生铁中高
C.铝合金门窗耐腐蚀性好,硬度高
D.焊锡是锡和铅的合金,其熔点低,可以用于焊接金属
5.化学知识可以指导生活实践。下列说法不正确的是
A.加热煮沸不能降低水的硬度 B.用肥皂水区分硬水和软水
C.不锈钢抗锈蚀性能比铁好 D.炒菜时油锅着火可用锅盖盖灭
6.某工业尾气中可能含有H2、CO和CO2中的一种或几种,为检验其成分,小明同学按下图装置进行实验时,观察到黑色固体变红,澄清石灰水变浑浊,由此实验现象得出尾气的组成情况可能有
A.2种 B.3种 C.4种 D.5种
7.利用甲酸( HCOOH)与浓硫酸制备CO,并用如下实验装置验证CO的有关性质。已知: ,下列说法不正确的是
A.操作时,先点燃乙处酒精灯,再滴加 HCOOH
B.装置丙的作用是防止倒吸
C.装置丁既可检验CO2,又可收集CO
D.随着反应进行,浓硫酸浓度降低,产生CO气体速率减小
8.下列图示实验中能明显观察到发生化学变化的是
A. B.
C. D.
9.利用如图所示实验装置模拟工业炼铁。下列说法正确的是
A.实验时应先点燃酒精灯后通CO
B.充分加热,a处固体由黑色变为红色
C.b处可用澄清石灰水检验生成的CO2
D.可用NaOH溶液吸收尾气中的CO
10.把一枚无锈铁钉放在硫酸铜溶液中,一段时间后,可出现的是
A.溶液蓝色变浅直至无色 B.铁钉表面析出红色物质
C.产生大量气泡 D.溶液质量增加
11.下列有关金属材料的说法错误的是
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
二、简答题
12.化学实验是学习化学的重要方法.请完成下列金属性质的实验.
(1)实验一:比较铁、铜的金属活动性强弱.请你设计实验完成下表内容.
实验步骤 实验现象 结 论
________________ ________________ 金属活动性:Fe>Cu
(2)实验二:镁、锌、铁三种金属与酸的反应.
[实验]取一定量的镁、锌、铁三种金属分别加入到溶质质量分数相同的稀硫酸中,充分反应,观察现象.
[结论]活泼金属能与酸反应.
[分析]
①三个反应的共同特点是_________,写出其中一个反应的化学方程式__________________.
②若完全反应后,三个反应生成氢气的质量相等,原因是__________________.
13.金属用途广泛,金属的用途与其性质密切相关。
(1)如图中将两块金属片相互刻画,该实验的目的是什么?
(2)某同学在Cu(NO3)2和AgNO3的混合溶液中加入一定质量的锌粉,充分反应后过滤,发现滤液仍呈蓝色。分析滤液中溶质的成分,并写出Zn与AgNO3溶液反应的化学方程式。
14.A、B、C、D为金属活动顺序表中常见的四种金属。已知:①A+BSO4===ASO4+B;②C+H2SO4===CSO4+H2↑;③B+2DNO3===B(NO3)2+2D。请完成以下填空:
(1)金属C在金属活动顺序表中排在氢________(填“前面”或“后面”)。
(2)根据上述反应能判断出其中三种金属的活动性,其金属活动性由强到弱的顺序是
____________(填字母)。
(3)若A、B、C、D分别为锌、铁、铜、银中的一种,金属C与H2SO4反应后所得溶液呈浅绿色,则金属A为________,反应③的化学方程式为________________________________。
三、推断题
15.A~G表示初中化学常见物质,其中A、B、C、D都是氧化物,E、F、G都是金属单质,A和G均为红色,它们之间的转化关系如图所示(反应条件,部分反应物及生成物已略去),请回答下列问题:
(1)A的化学式为____________;
(2)B的一种用途是____________;
(3)反应③的化学方程式为:_________________;
(4)E、F、G三种金属的活动性由强到弱的顺序为_______________。(用元素符号表示)
16.如图是铁元素循环的关系图,箭号表示能实现一步转化。
(1)反应①中可观察到__________现象。
(2)①~⑤五个反应中,铁元素的化合价不变的反应是__________(填序号)。
(3)反应③的化学方程式为__________,该反应属于__________反应(填基本反应类型)。
17.从ZnSO4、CuSO4和FeSO4的混合液中回收金属铜,设计了如下方案:
①操作a的名称是______,加入锌后,写出发生反应的一个化学方程式__,该反应体现了铜的金属活动性比锌____(选填“强”或“弱”)。
②操作a后的固体中一定有的物质是____,生成气体的化学式是_____。
四、实验题
18.某化学兴趣小组利用下图装置进行实验。探究工业炼铁的化学原理,试按要求填空。
(1)硬质玻璃管中观察到的现象是__________,写出一氧化碳和氧化铁反应的化学方程式________;
(2)实验中首先通入一氧化碳的目的是__________;
(3)装置中导管末端加一点燃的酒精灯目的是______________。
19.有三瓶失去标签的溶质质量分数为15%、10%、5%的盐酸。选择下列仪器和药品,设计两种不同的方案,辨别出三瓶盐酸
实验仪器:温度计、量筒、秒表、烧杯、试管、剪刀、镊子
药品:镁条
提示:镁条和盐酸反应速度很快,通过观察放出气泡的速度很难准确判断盐酸浓度的大小。
(1)写出镁与盐酸反应的化学方程式:_______________。
(2)实验的关键是控制三个变量:
①在的环境温度下进行实验。
②取相同质量的镁条。
③取_____________________。
(3)你的方案是:
方案一:测定_________________。
方案—:测定____________________。
20.铁是应用最广泛的金属,通过冶炼铁矿可以得到铁。
(1)高炉是工业炼铁的主要设备(如图1)。
①高炉炼铁中,焦炭的作用是_______(用化学方程式表示)。
②写出高炉中以赤铁矿为原料得到铁的化学方程式:_______。
(2)实验室用氧化铁粉末模拟炼铁(如图2),并探究产物成分。
①实验中观察到硬质玻璃管内固体全部变为黑色,澄清石灰水变浑浊:实验结束时,硬质玻璃管内物质冷却后才停止通一氧化碳的主要原因是________;该装置的一个明显缺陷是________。
②查阅资料发现:
一氧化碳还原氧化铁后剩余固体可能由四氧化三铁、氧化亚铁、铁粉和未反应的氧化铁中的一种或几种组成;进一步查得三种铁的氧化物的某些性质如下表:
氧化亚铁 氧化铁 四氧化三铁
颜色 黑色 红棕色 黑色
磁性 无 无 有
与硫酸铜溶液 不反应
与稀盐酸 反应生成可溶性物质,无气体放出
由实验中_________的现象,确认剩余固体中已无氧化铁。
③继续探究剩余固体的组成:
步骤 实验操作 实验现象 实验结论
1 用磁铁吸引剩余固体 a_________ 剩余固体中没有氧化亚铁
2 b_________ c_________ 剩余固体中只有铁粉
五、计算题
21.某铁矿粉,主要成分为铁的氧化物(FeXOy),一学生利用实验作进一步分析,过程及数据如下。(注:铁矿粉中杂质不参与下列过程中的反应)
Ⅰ.取30g该铁矿粉在CO气流中充分加热,将反应后的气体用烧碱溶液充分吸收,烧碱溶液增重17.6g
Ⅱ.将上述加热后的固体取出后,再向固体逐滴加入稀硫酸,测得产生气体与滴入稀硫酸的质量关系如图:
通过计算回答下列问题:
(1)30g铁矿粉所含铁的氧化物中,铁元素的质量为______g,氧元素的质量为______g。
(2)该铁的氧化物化学式中,x、y的最简整数比x:y=______。
22.某化学兴趣小组为了测定某黄铜(铜、锌合金)样品中锌的质量分数,取10克样品放入烧杯中,再取60克稀硫酸分六次加入烧杯中,均充分反应,实验数据如下:
第一次 第二次 第三次 第四次 第五次 第六次
加入稀硫酸的质量(g) 10 10 10 10 10 10
剩余固体的质量(g) 9.35 8.7 8.05 7.4 6.75 6.75
(1)黄铜样品中锌的质量分数为多少?(写出计算步骤,下同)
(2)所用稀硫酸的质量分数为多少?
参考答案:
1.D 2.B 3.C 4.B 5.A 6.D 7.A 8.C 9.C 10.B 11.C
12. 向硫酸铜溶液中投入铁钉 铁钉表面有红色固体析出,溶液由蓝色变为浅绿色 都是置换反应 Mg+H2SO4=MgSO4+H2↑或Zn+H2SO4=ZnSO4+H2↑或Fe+H2SO4=FeSO4+H2↑; 当三种金属过量,硫酸完全反应时,则生成氢气质量相等;当硫酸过量,三种金属完全反应,且质量比为mMg:mZn:mFe=24:65:56时,则生成氢气质量相等.
13.(1)比较黄铜和纯铜的硬度
(2)一定含Cu(NO3)2和Zn(NO3)2,可能含AgNO3;Zn+2AgNO3=Zn(NO3)2+2Ag
14. 前面 A>B>D Zn Cu+2AgNO3===Cu(NO3)2+2Ag
15. Fe2O3 冶炼金属 Fe+CuSO4=FeSO4+Cu 铁>铜>银
16.(1)铁溶解,产生气泡,溶液变为浅绿色
(2)③④##④③
(3) 复分解
17. 过滤 弱 Fe、Cu H2
18. 红色固体变为黑色 排尽装置中的空气,防止加热时发生爆炸 将尾气CO燃烧掉,防止污染空气
19.(1)Mg+2HCl=MgCl2+H2↑
(2)相同体积的盐酸
(3) 不同浓度盐酸和镁条反应所需时间 不同浓度盐酸和镁条反应后所得溶液的温度
20.(1) 和
(2) 防止生成的铁在高温条件下再次被氧化 没有尾气处理装置 红棕色粉末完全转化为黑色 黑色固体被全部吸引 往剩余固体中加足量硝酸铜 黑色固体全部变成红色
21. 16.8 6.4 3:4
22.(1)32.5%; (2)9.8%
