2023化学苏教版选择性必修一 3.3.1 盐类水解的原理 课件(共20张ppt)
文档属性
| 名称 | 2023化学苏教版选择性必修一 3.3.1 盐类水解的原理 课件(共20张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-22 22:31:26 | ||
图片预览





文档简介
(共20张PPT)
第1课时 盐类水解的原理
专题3 水溶液中的离子反应
第三单元 盐类的水解
氯化铵溶液可除铁锈
纯碱可去油污
①Na2CO3和氯化铵属于哪类物质?
②Na2CO3溶液能去油污说明了什么?
③氯化铵溶液可以除铁锈说明什么?
盐类
Na2CO3溶液显碱性
氯化铵溶液显酸性
思考与讨论
Ⅰ.盐溶液的酸碱性
实验内容:测定NaCl、Na2SO4、NH4Cl、 (NH4 )2SO4、CH3COONa、Na2CO3溶液的pH。
中性
中性
酸性
酸性
碱性
碱性
活动与探究
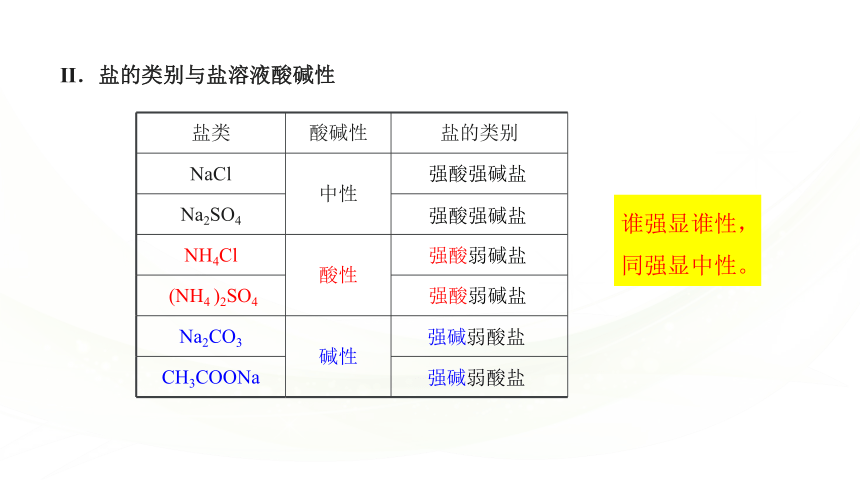
盐类 酸碱性 盐的类别
NaCl 中性
Na2SO4
NH4Cl 酸性
(NH4 )2SO4
Na2CO3 碱性
CH3COONa
强酸强碱盐
强酸强碱盐
强酸弱碱盐
强酸弱碱盐
强碱弱酸盐
强碱弱酸盐
谁强显谁性,同强显中性。
Ⅱ.盐的类别与盐溶液酸碱性
分析CH3COONa水溶液显碱性的原因:
④最终会引起溶液中的c(H+)和c(OH-)如何变化?
①CH3COONa水溶液中存在哪些电离?
②CH3COONa水溶液中存在哪些粒子?
③离子相互作用时对水的电离平衡有何影响?
CH3COONa === CH3COO- + Na+
+
CH3COOH
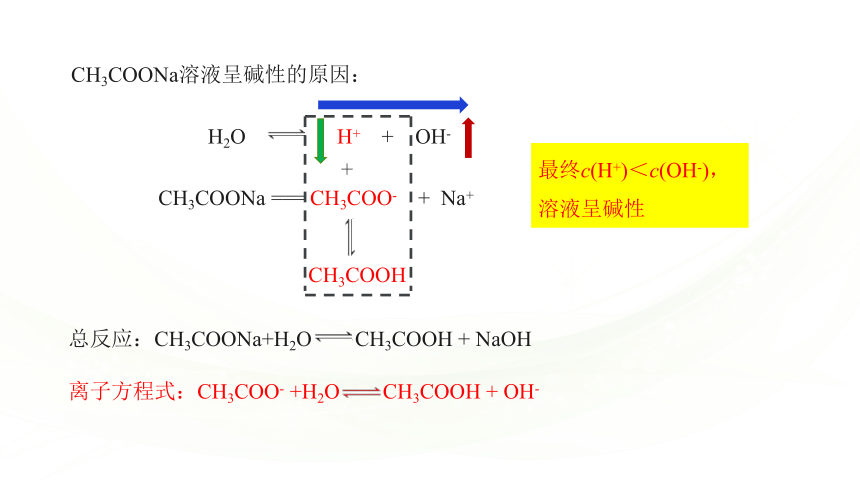
CH3COONa溶液呈碱性的原因:
最终c(H+)<c(OH-),
溶液呈碱性
H2O H+ + OH-
总反应:CH3COONa+H2O CH3COOH + NaOH
离子方程式:CH3COO- +H2O CH3COOH + OH-
H2O OH- + H+
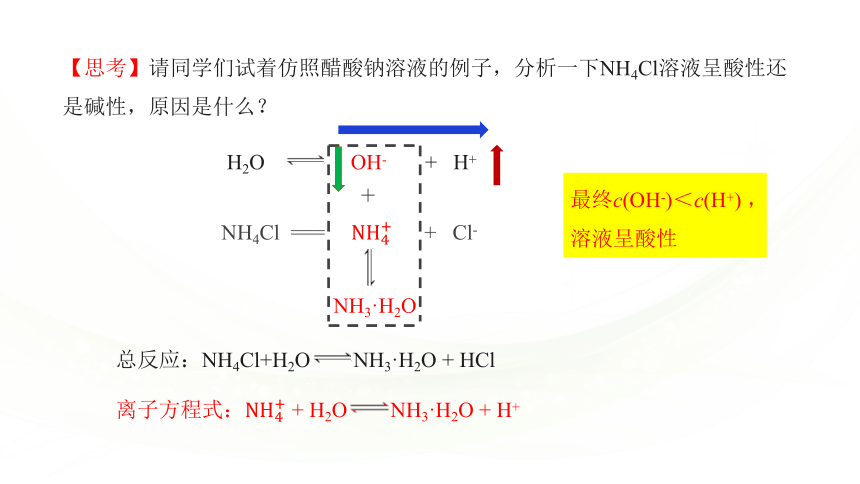
【思考】请同学们试着仿照醋酸钠溶液的例子,分析一下NH4Cl溶液呈酸性还是碱性,原因是什么?
NH4Cl === + Cl-
+
NH3·H2O
总反应:NH4Cl+H2O NH3·H2O + HCl
离子方程式: + H2O NH3·H2O + H+
最终c(OH-)<c(H+) ,
溶液呈酸性
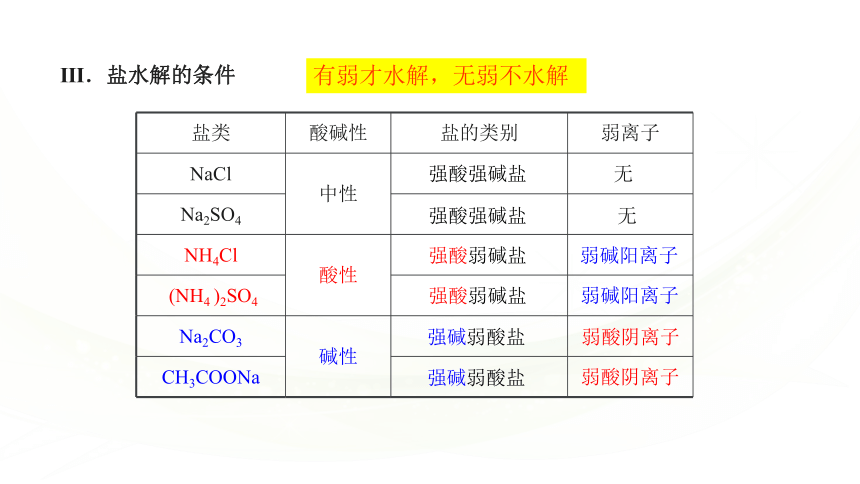
Ⅲ.盐水解的条件
盐类 酸碱性 盐的类别 弱离子
NaCl 中性
Na2SO4
NH4Cl 酸性
(NH4 )2SO4
Na2CO3 碱性
CH3COONa
强酸强碱盐
强酸强碱盐
强酸弱碱盐
强酸弱碱盐
强碱弱酸盐
强碱弱酸盐
无
弱碱阳离子
弱碱阳离子
弱酸阴离子
弱酸阴离子
无
有弱才水解,无弱不水解
常见的“弱”离子
①弱碱阳离子:
②弱酸阴离子:
、Mg2+、Al3+、 Fe3+等
、、 、 、S2- 、HS- 、 ClO- 、 、 CH3COO-、 F- 、 等
2.实质
促进水的电离平衡,使溶液呈现一定的酸性或碱性。
一、盐类的水解
1.定义
盐在水溶液中电离出的离子跟水电离出的H+或OH-结合生成弱电解质的反应,叫做盐类的水解。
知识梳理
(3)盐类的水解程度一般比较小。
(1)盐类的水解是酸碱中和反应的逆反应。
(2)酸碱中和为放热反应,故水解反应为吸热反应。
故温度越高,盐的水解程度增大。
(4)盐类的水解是可逆的,其平衡状态属于动态平衡。
3.水解的特点
有弱才水解,无弱不水解,
谁弱谁水解,都弱都水解;
谁强显谁性, 同强显中性。
4.水解的规律
2.一般盐类水解的程度很小,水解产物很少。通常不生成沉淀或气体,一般不标“↓”或“↑”,也不把生成物(如H2CO3、NH3·H2O等)写成分解产物的形式。
水解方程式:盐 + 水 酸 + 碱
水解离子方程式:盐的离子 + 水 酸(或碱) + OH-(或H+)
二、盐类水解离子方程式
1.盐类水解是可逆反应,反应方程式中要写“ ”。
例: Na2CO3的水解
Fe3+的水解
4.多元弱碱的阳离子水解复杂,可一步写出。
3.多元弱酸根的水解是分步水解的,其中第一步水解程度远远大于第二步水解的程度,以第一步水解为主。
第一步:+H2O +OH- (主要)
第二步:+H2O H2CO3+OH- (次要)
Fe3++3H2O Fe(OH)3+3H+
【练习】书写下列物质的水解离子方程式
①NaHSO3
②Na2S
③(NH4)2SO4
④AlCl3
⑤NH4Cl
⑥ NaClO
+H2O H2SO3+OH-
+H2O NH3·H2O+H+
+H2O NH3·H2O+H+
S2-+H2O HS-+OH-
Al3++3H2O Al(OH)3+3H+
ClO-+H2O HClO +OH-
1.下列溶液pH小于7的是( )
A.溴化钾 B.硫酸铜 C.硫化钠 D.硝酸钡
2.下列溶液能使酚酞指示剂显红色的是( )
A.氯化钾 B. 硫酸氢钠 C. 碳酸钠 D. 氯化铁
B
C
当堂检测
3.在溶液中,不能发生水解的离子是( )
A.ClO – B. C.Fe 3+ D.
D
4.下列盐的水溶液中,哪些呈酸性( )哪些呈碱性( )
① FeCl3 ② NaClO ③ (NH4)2SO4 ④ AgNO3 ⑤ Na2S ⑥ K2SO4
①③④
②⑤
AD
5.下列水解离子方程式正确的是( )
A.Fe3+ + 3H2O Fe(OH)3 + 3H+
B.Br- + H2O HBr + OH-
C.+ 2H2O H2CO3 + 2OH-
D.+2H2O NH3·H2O + H3O+
6.下列各离子方程式中,属于水解反应的是( )
A.H2O + H2O H3O+ + OH-
B.OH- + === +H2O
C.+ H2O NH3·H2O + H+
D.CH3COOH + H2O CH3COO- + H3O+
C
本节内容结束
第1课时 盐类水解的原理
专题3 水溶液中的离子反应
第三单元 盐类的水解
氯化铵溶液可除铁锈
纯碱可去油污
①Na2CO3和氯化铵属于哪类物质?
②Na2CO3溶液能去油污说明了什么?
③氯化铵溶液可以除铁锈说明什么?
盐类
Na2CO3溶液显碱性
氯化铵溶液显酸性
思考与讨论
Ⅰ.盐溶液的酸碱性
实验内容:测定NaCl、Na2SO4、NH4Cl、 (NH4 )2SO4、CH3COONa、Na2CO3溶液的pH。
中性
中性
酸性
酸性
碱性
碱性
活动与探究
盐类 酸碱性 盐的类别
NaCl 中性
Na2SO4
NH4Cl 酸性
(NH4 )2SO4
Na2CO3 碱性
CH3COONa
强酸强碱盐
强酸强碱盐
强酸弱碱盐
强酸弱碱盐
强碱弱酸盐
强碱弱酸盐
谁强显谁性,同强显中性。
Ⅱ.盐的类别与盐溶液酸碱性
分析CH3COONa水溶液显碱性的原因:
④最终会引起溶液中的c(H+)和c(OH-)如何变化?
①CH3COONa水溶液中存在哪些电离?
②CH3COONa水溶液中存在哪些粒子?
③离子相互作用时对水的电离平衡有何影响?
CH3COONa === CH3COO- + Na+
+
CH3COOH
CH3COONa溶液呈碱性的原因:
最终c(H+)<c(OH-),
溶液呈碱性
H2O H+ + OH-
总反应:CH3COONa+H2O CH3COOH + NaOH
离子方程式:CH3COO- +H2O CH3COOH + OH-
H2O OH- + H+
【思考】请同学们试着仿照醋酸钠溶液的例子,分析一下NH4Cl溶液呈酸性还是碱性,原因是什么?
NH4Cl === + Cl-
+
NH3·H2O
总反应:NH4Cl+H2O NH3·H2O + HCl
离子方程式: + H2O NH3·H2O + H+
最终c(OH-)<c(H+) ,
溶液呈酸性
Ⅲ.盐水解的条件
盐类 酸碱性 盐的类别 弱离子
NaCl 中性
Na2SO4
NH4Cl 酸性
(NH4 )2SO4
Na2CO3 碱性
CH3COONa
强酸强碱盐
强酸强碱盐
强酸弱碱盐
强酸弱碱盐
强碱弱酸盐
强碱弱酸盐
无
弱碱阳离子
弱碱阳离子
弱酸阴离子
弱酸阴离子
无
有弱才水解,无弱不水解
常见的“弱”离子
①弱碱阳离子:
②弱酸阴离子:
、Mg2+、Al3+、 Fe3+等
、、 、 、S2- 、HS- 、 ClO- 、 、 CH3COO-、 F- 、 等
2.实质
促进水的电离平衡,使溶液呈现一定的酸性或碱性。
一、盐类的水解
1.定义
盐在水溶液中电离出的离子跟水电离出的H+或OH-结合生成弱电解质的反应,叫做盐类的水解。
知识梳理
(3)盐类的水解程度一般比较小。
(1)盐类的水解是酸碱中和反应的逆反应。
(2)酸碱中和为放热反应,故水解反应为吸热反应。
故温度越高,盐的水解程度增大。
(4)盐类的水解是可逆的,其平衡状态属于动态平衡。
3.水解的特点
有弱才水解,无弱不水解,
谁弱谁水解,都弱都水解;
谁强显谁性, 同强显中性。
4.水解的规律
2.一般盐类水解的程度很小,水解产物很少。通常不生成沉淀或气体,一般不标“↓”或“↑”,也不把生成物(如H2CO3、NH3·H2O等)写成分解产物的形式。
水解方程式:盐 + 水 酸 + 碱
水解离子方程式:盐的离子 + 水 酸(或碱) + OH-(或H+)
二、盐类水解离子方程式
1.盐类水解是可逆反应,反应方程式中要写“ ”。
例: Na2CO3的水解
Fe3+的水解
4.多元弱碱的阳离子水解复杂,可一步写出。
3.多元弱酸根的水解是分步水解的,其中第一步水解程度远远大于第二步水解的程度,以第一步水解为主。
第一步:+H2O +OH- (主要)
第二步:+H2O H2CO3+OH- (次要)
Fe3++3H2O Fe(OH)3+3H+
【练习】书写下列物质的水解离子方程式
①NaHSO3
②Na2S
③(NH4)2SO4
④AlCl3
⑤NH4Cl
⑥ NaClO
+H2O H2SO3+OH-
+H2O NH3·H2O+H+
+H2O NH3·H2O+H+
S2-+H2O HS-+OH-
Al3++3H2O Al(OH)3+3H+
ClO-+H2O HClO +OH-
1.下列溶液pH小于7的是( )
A.溴化钾 B.硫酸铜 C.硫化钠 D.硝酸钡
2.下列溶液能使酚酞指示剂显红色的是( )
A.氯化钾 B. 硫酸氢钠 C. 碳酸钠 D. 氯化铁
B
C
当堂检测
3.在溶液中,不能发生水解的离子是( )
A.ClO – B. C.Fe 3+ D.
D
4.下列盐的水溶液中,哪些呈酸性( )哪些呈碱性( )
① FeCl3 ② NaClO ③ (NH4)2SO4 ④ AgNO3 ⑤ Na2S ⑥ K2SO4
①③④
②⑤
AD
5.下列水解离子方程式正确的是( )
A.Fe3+ + 3H2O Fe(OH)3 + 3H+
B.Br- + H2O HBr + OH-
C.+ 2H2O H2CO3 + 2OH-
D.+2H2O NH3·H2O + H3O+
6.下列各离子方程式中,属于水解反应的是( )
A.H2O + H2O H3O+ + OH-
B.OH- + === +H2O
C.+ H2O NH3·H2O + H+
D.CH3COOH + H2O CH3COO- + H3O+
C
本节内容结束
