3.1.2 铁及其化合物 课件 (20张ppt) 2022-2023学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 3.1.2 铁及其化合物 课件 (20张ppt) 2022-2023学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | zip | ||
| 文件大小 | 13.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-23 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
3.1.2 铁及其化合物
铁有两种氢氧化物,可以分别由相对应的可溶性盐与碱溶液反应制得。
【实验3-1】在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
FeCl3溶液 FeSO4溶液
加入NaOH溶液
离子方程式
生成红褐色沉淀
白色沉淀迅速变成灰绿色,最后变成红褐色
Fe3++3OH- = Fe(OH)3 ↓
Fe2++2OH- = Fe(OH)2 ↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3
应用:可利用以上原理检验Fe3+ 或 Fe2+离子的存在。
铁的氢氧化物
上述实验在制备Fe(OH)2过程中,胶头滴管的使用是否正确?这样操作的目的是什么?怎样才能使制得的Fe(OH)2较长时间存在?
成功的关键:
①溶液中不含O2等氧化性物质;
②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气的体系中。
①使用新配制的FeSO4溶液和NaOH溶液。
②把NaOH溶液或配制溶液用的蒸馏水事先加热煮沸一下。
③如果在试管中FeSO4溶液液面上预先注入一层植物油,则生
成的Fe(OH)2保存的时间会更长一些。
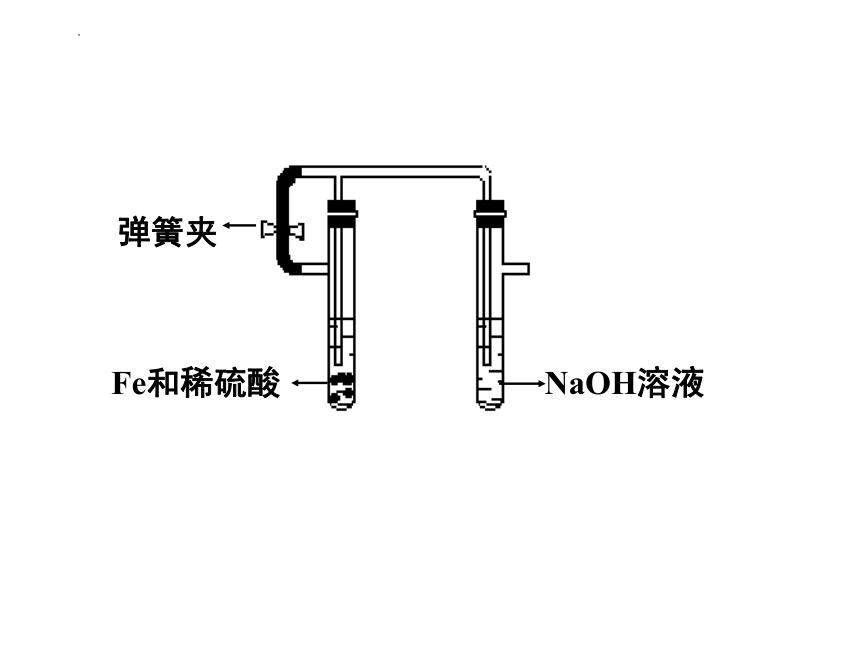
④改进实验装置
弹簧夹
Fe和稀硫酸
NaOH溶液
化学式 Fe(OH)2 Fe(OH)3
色态
溶解性
制备
与O2反应
稳定性
与酸反应
白色固体
红褐色固体
难溶
难溶
Fe3++3OH- ==Fe(OH)3↓
Fe2++2OH- ==Fe(OH)2↓
4Fe(OH)2+2H2O+O2== 4Fe(OH)3
白色→灰绿色→红褐色
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
不稳定,易被空气氧化,
加热易分解
2Fe(OH)3 == Fe2O3+3H2O
△
小结
常见的铁盐有Fe2(SO4)3、 FeCl3等,常见的亚铁盐有FeSO4、 FeCl2等。
铁盐和亚铁盐
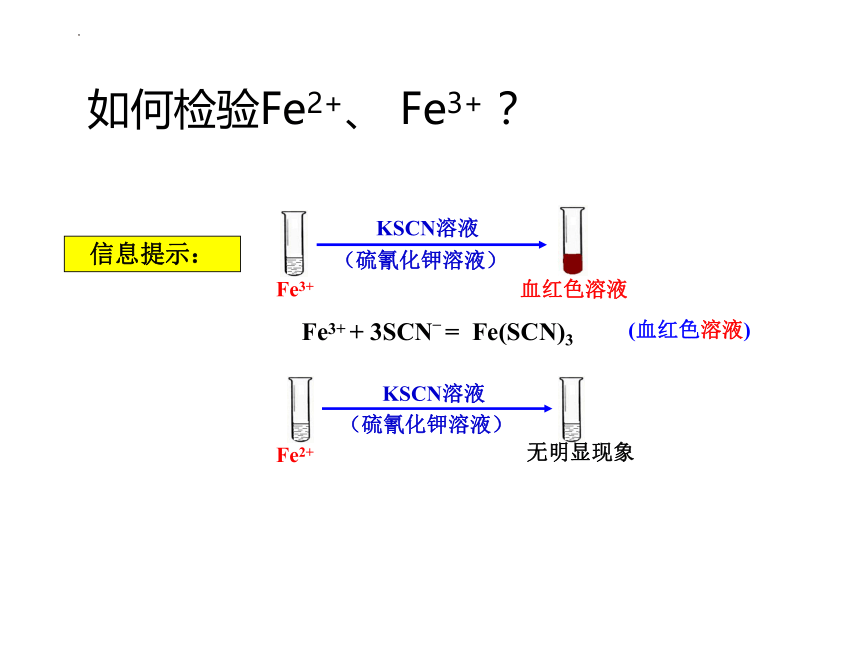
如何检验Fe2+、 Fe3+ ?
信息提示:
KSCN溶液
Fe3+
(硫氰化钾溶液)
KSCN溶液
(硫氰化钾溶液)
Fe2+
血红色溶液
无明显现象
Fe3+ + 3SCN– = Fe(SCN)3
(血红色溶液)
白色沉淀
灰绿色沉淀
红褐色沉淀
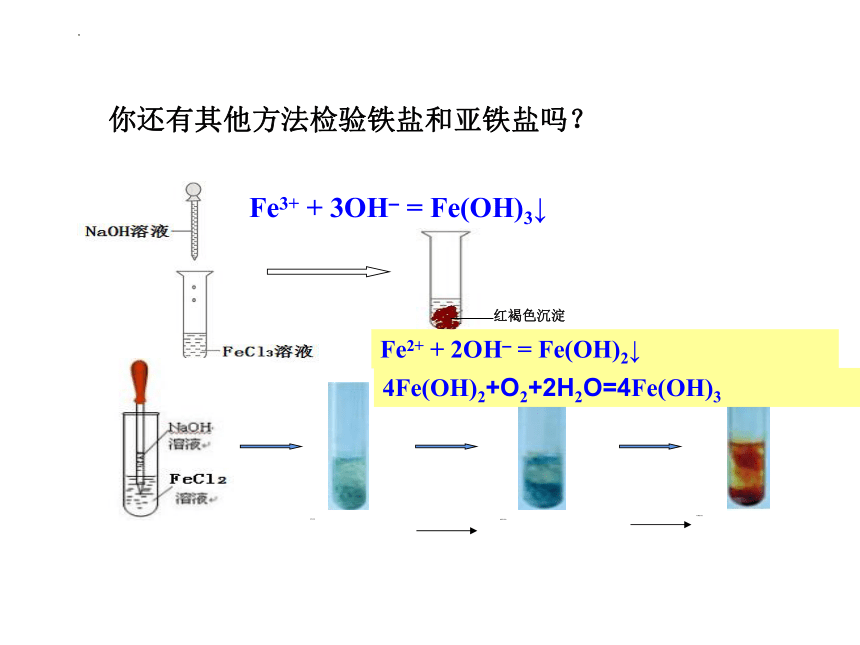
你还有其他方法检验铁盐和亚铁盐吗?
红褐色沉淀
Fe3+ + 3OH– = Fe(OH)3↓
Fe2+ + 2OH– = Fe(OH)2↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3
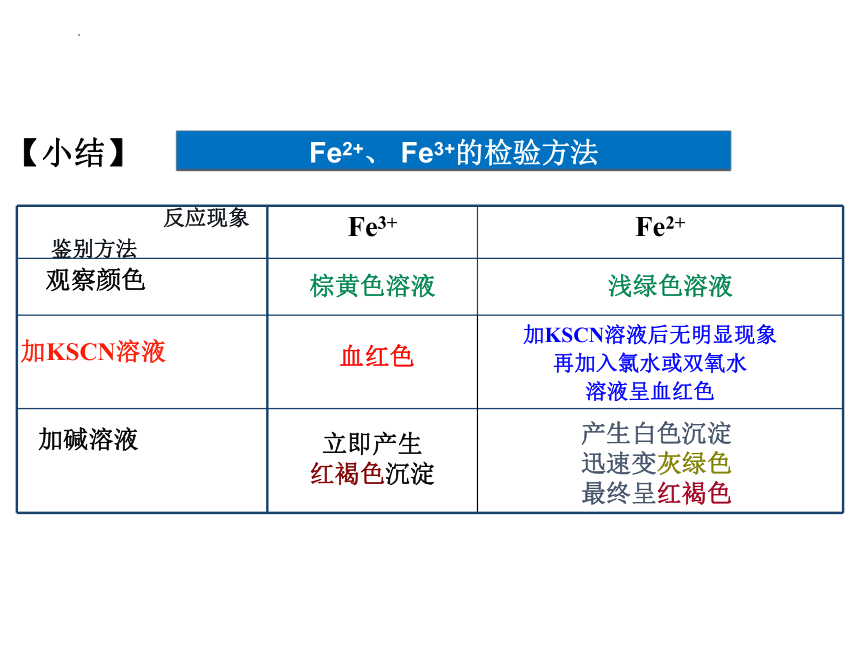
鉴别方法
反应现象
Fe3+ Fe2+
Fe2+、 Fe3+的检验方法
浅绿色溶液
棕黄色溶液
立即产生
红褐色沉淀
加KSCN溶液后无明显现象
再加入氯水或双氧水
溶液呈血红色
血红色
加KSCN溶液
加碱溶液
观察颜色
【小结】
产生白色沉淀
迅速变灰绿色
最终呈红褐色
Fe2+
Fe3+
??
氧化剂
请同学们讨论探究Fe2+转化为Fe3+实验方案。
可选试剂:FeCl2溶液、FeCl3溶液、KSCN溶液、新制氯水、H2O2溶液、铁粉、铜粉。
1、将讨论好的实验方案记载下来
2、动手实验并记录实验现象
Fe2+、 Fe3+相互转化的条件
实验3-2 滴入KSCN溶液
FeCl2溶液
FeCl3溶液
解释及结论
无明显变化
黄色溶液变成血红色
FeCl3+3KSCN =Fe(SCN)3+3KCl
【Fe3++3SCN— =Fe(SCN)3】
KSCN可用来检验Fe3+的存在
实验3-3 现象 解释及结论
①FeCl3溶液中加入铁粉,振荡,滴入KSCN溶液
②接着加入氯水,振荡
①溶液由黄变成浅绿色,加入KSCN无变化
②加氯水后,溶液由浅绿色变为红色
①Fe3+具有氧化性
2Fe3++Fe=3Fe2+
②Fe2+具有还原性
2Fe2++Cl2=2Fe3++2Cl-
还原剂:金属单质,如铁、铜、S2-、I- 等
氧化剂:Cl2、H2O2、 O2 、 HNO3、
浓H2SO4 、 KMnO4 、 KClO3
Fe2+ Fe3+
氧化剂
还原剂
2Fe3++ Fe = 3Fe2+
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++Cl2 = 2Fe3+ +2Cl—
还原性 氧化性
(1)如何证明FeCl2是否变质?
变质分为3种情况,即完全变质;部分变质;完全未变质
取样溶于水
讨论
(2)为什么存放亚铁盐溶液时,向溶液中加入少量铁屑?
防止Fe2+被氧化
(1)除去FeCl3中的FeCl2应滴加氯水;
(2)除去FeSO4中的Fe2(SO4)3应加铁屑。
(3)除去Fe2+中的Cu2+应该用铁屑
如何除去Fe2+中的Cu2+
如何证明四氧化三铁中铁元素的化合价为+2、+3价?
1.加热的盐酸溶解
Fe3O4+8H+=Fe2++2Fe3++4H2O
2.用KSCN检验Fe3+
3.......
Fe2+有强还原性,可以使强氧化性的酸性高锰酸钾溶液褪色
利用图铜板制作图案
(1)2FeCl3 +Cu = 2FeCl2 + CuCl2
小魔术:用毛笔在铜片上刻字
如何从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液?
分别写出步骤①、⑤中反应的离子方程式① 、 。
⑤ 。
2Fe2++Cl2=2Fe3++2Cl-
Cu
Fe+2Fe3+=3Fe2+
Fe+Cu 2+=Fe2++Cu
铁粉
Fe Cl2
Fe、Cu
FeCl3、FeCl2、CuCl2
盐酸
氯气
再见
3.1.2 铁及其化合物
铁有两种氢氧化物,可以分别由相对应的可溶性盐与碱溶液反应制得。
【实验3-1】在两支试管中分别加入少量的FeCl3溶液和FeSO4溶液,然后各滴入NaOH溶液。观察并描述发生的现象。
FeCl3溶液 FeSO4溶液
加入NaOH溶液
离子方程式
生成红褐色沉淀
白色沉淀迅速变成灰绿色,最后变成红褐色
Fe3++3OH- = Fe(OH)3 ↓
Fe2++2OH- = Fe(OH)2 ↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3
应用:可利用以上原理检验Fe3+ 或 Fe2+离子的存在。
铁的氢氧化物
上述实验在制备Fe(OH)2过程中,胶头滴管的使用是否正确?这样操作的目的是什么?怎样才能使制得的Fe(OH)2较长时间存在?
成功的关键:
①溶液中不含O2等氧化性物质;
②制备过程中,保证生成的Fe(OH)2在密闭的隔绝空气的体系中。
①使用新配制的FeSO4溶液和NaOH溶液。
②把NaOH溶液或配制溶液用的蒸馏水事先加热煮沸一下。
③如果在试管中FeSO4溶液液面上预先注入一层植物油,则生
成的Fe(OH)2保存的时间会更长一些。
④改进实验装置
弹簧夹
Fe和稀硫酸
NaOH溶液
化学式 Fe(OH)2 Fe(OH)3
色态
溶解性
制备
与O2反应
稳定性
与酸反应
白色固体
红褐色固体
难溶
难溶
Fe3++3OH- ==Fe(OH)3↓
Fe2++2OH- ==Fe(OH)2↓
4Fe(OH)2+2H2O+O2== 4Fe(OH)3
白色→灰绿色→红褐色
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
不稳定,易被空气氧化,
加热易分解
2Fe(OH)3 == Fe2O3+3H2O
△
小结
常见的铁盐有Fe2(SO4)3、 FeCl3等,常见的亚铁盐有FeSO4、 FeCl2等。
铁盐和亚铁盐
如何检验Fe2+、 Fe3+ ?
信息提示:
KSCN溶液
Fe3+
(硫氰化钾溶液)
KSCN溶液
(硫氰化钾溶液)
Fe2+
血红色溶液
无明显现象
Fe3+ + 3SCN– = Fe(SCN)3
(血红色溶液)
白色沉淀
灰绿色沉淀
红褐色沉淀
你还有其他方法检验铁盐和亚铁盐吗?
红褐色沉淀
Fe3+ + 3OH– = Fe(OH)3↓
Fe2+ + 2OH– = Fe(OH)2↓
4Fe(OH)2+O2+2H2O=4Fe(OH)3
鉴别方法
反应现象
Fe3+ Fe2+
Fe2+、 Fe3+的检验方法
浅绿色溶液
棕黄色溶液
立即产生
红褐色沉淀
加KSCN溶液后无明显现象
再加入氯水或双氧水
溶液呈血红色
血红色
加KSCN溶液
加碱溶液
观察颜色
【小结】
产生白色沉淀
迅速变灰绿色
最终呈红褐色
Fe2+
Fe3+
??
氧化剂
请同学们讨论探究Fe2+转化为Fe3+实验方案。
可选试剂:FeCl2溶液、FeCl3溶液、KSCN溶液、新制氯水、H2O2溶液、铁粉、铜粉。
1、将讨论好的实验方案记载下来
2、动手实验并记录实验现象
Fe2+、 Fe3+相互转化的条件
实验3-2 滴入KSCN溶液
FeCl2溶液
FeCl3溶液
解释及结论
无明显变化
黄色溶液变成血红色
FeCl3+3KSCN =Fe(SCN)3+3KCl
【Fe3++3SCN— =Fe(SCN)3】
KSCN可用来检验Fe3+的存在
实验3-3 现象 解释及结论
①FeCl3溶液中加入铁粉,振荡,滴入KSCN溶液
②接着加入氯水,振荡
①溶液由黄变成浅绿色,加入KSCN无变化
②加氯水后,溶液由浅绿色变为红色
①Fe3+具有氧化性
2Fe3++Fe=3Fe2+
②Fe2+具有还原性
2Fe2++Cl2=2Fe3++2Cl-
还原剂:金属单质,如铁、铜、S2-、I- 等
氧化剂:Cl2、H2O2、 O2 、 HNO3、
浓H2SO4 、 KMnO4 、 KClO3
Fe2+ Fe3+
氧化剂
还原剂
2Fe3++ Fe = 3Fe2+
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++Cl2 = 2Fe3+ +2Cl—
还原性 氧化性
(1)如何证明FeCl2是否变质?
变质分为3种情况,即完全变质;部分变质;完全未变质
取样溶于水
讨论
(2)为什么存放亚铁盐溶液时,向溶液中加入少量铁屑?
防止Fe2+被氧化
(1)除去FeCl3中的FeCl2应滴加氯水;
(2)除去FeSO4中的Fe2(SO4)3应加铁屑。
(3)除去Fe2+中的Cu2+应该用铁屑
如何除去Fe2+中的Cu2+
如何证明四氧化三铁中铁元素的化合价为+2、+3价?
1.加热的盐酸溶解
Fe3O4+8H+=Fe2++2Fe3++4H2O
2.用KSCN检验Fe3+
3.......
Fe2+有强还原性,可以使强氧化性的酸性高锰酸钾溶液褪色
利用图铜板制作图案
(1)2FeCl3 +Cu = 2FeCl2 + CuCl2
小魔术:用毛笔在铜片上刻字
如何从使用过的腐蚀废液中回收铜,并重新制得纯净的FeCl3溶液?
分别写出步骤①、⑤中反应的离子方程式① 、 。
⑤ 。
2Fe2++Cl2=2Fe3++2Cl-
Cu
Fe+2Fe3+=3Fe2+
Fe+Cu 2+=Fe2++Cu
铁粉
Fe Cl2
Fe、Cu
FeCl3、FeCl2、CuCl2
盐酸
氯气
再见
