【寒假备课精选】2013-2014下学期高中化学同步配套辅导与检测(人教版,必修2):第三章第二节 第1课时 乙烯(55张ppt)
文档属性
| 名称 | 【寒假备课精选】2013-2014下学期高中化学同步配套辅导与检测(人教版,必修2):第三章第二节 第1课时 乙烯(55张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 876.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2014-01-23 00:00:00 | ||
图片预览








文档简介
课件55张PPT。第二节 来自石油和煤的两种基本化工原料
第1课时 乙 烯有机化合物第1课时 乙 烯 2009年8月,山东电视台“生活帮”栏目报导了这样一件事情:市面上的很多葡萄看起来又红又紫,但吃起来却酸涩无比。根据记者的调查才知,葡萄种植者在未成熟的葡萄上喷洒了乙烯利,促进葡萄成熟,但这种催熟的葡萄没有正常成熟的葡萄甘甜。乙烯利是一种水剂,在一定条件下能放出乙烯,乙烯能促进果实成熟。
乙烯是从石油中提取的,它有哪些性质呢?1.了解烯烃的概念。
2.了解乙烯的物理性质、工业制取原理及其在化工生产中的作用。
3.掌握乙烯的分子结构,初步体会其结构特点对性质的影响。
4.掌握乙烯的化学性质,认识加成反应的特点。烯烃1.概念
分子中含有________的一类链烃,属于不饱和烃。
2.分子通式
CnH2n(n≥2)。碳碳双键乙烯1.乙烯的来源
从______中获得乙烯,已成为目前工业上生产乙烯的主要途径,乙烯是石油的裂解产物。
2.乙烯的制取
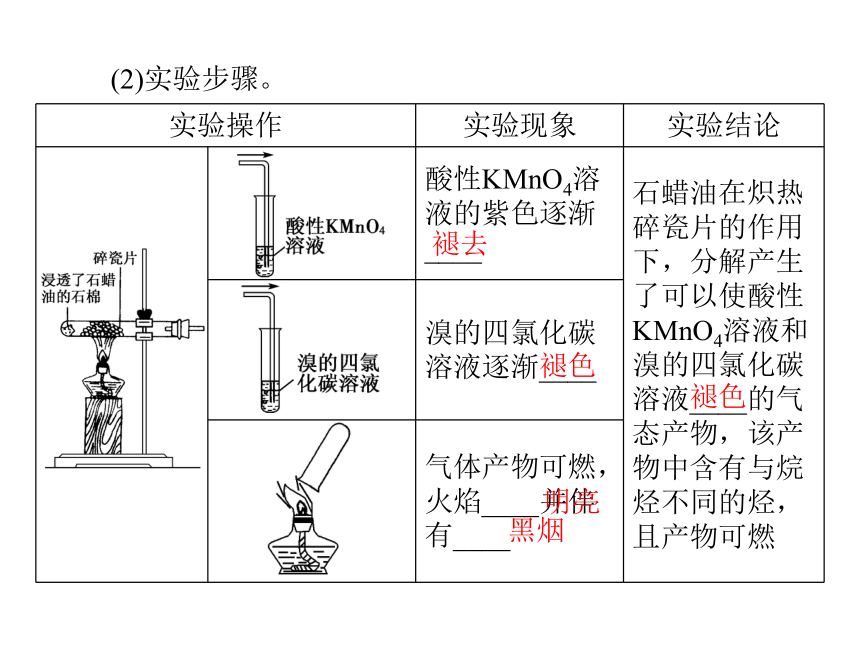
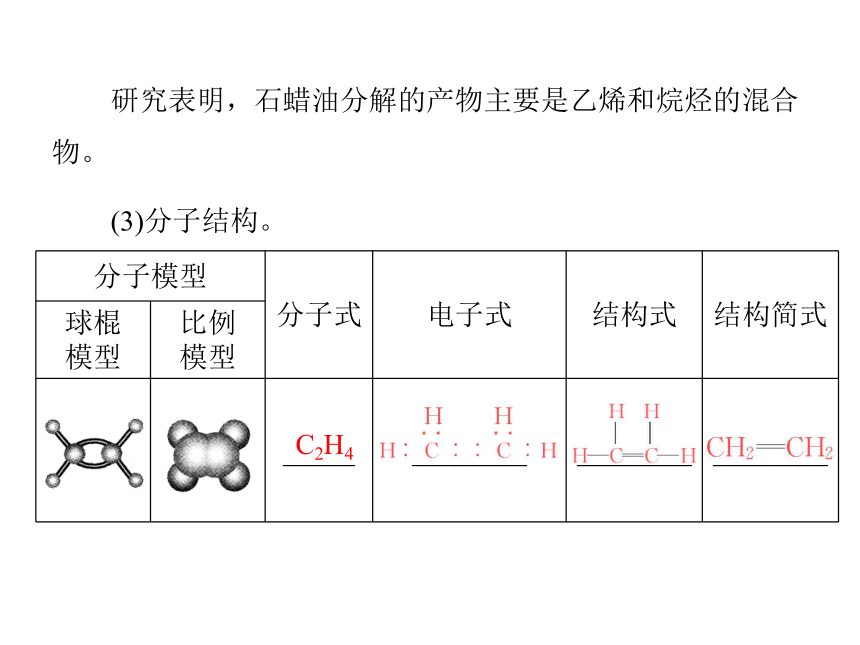
(1)实验原理。石蜡油 乙烯等(石蜡油是含17个C以上的液态烷烃混合物)。石油(2)实验步骤。褪去褪色明亮黑烟褪色研究表明,石蜡油分解的产物主要是乙烯和烷烃的混合物。
(3)分子结构。C2H43.乙烯的化学性质
(1)氧化反应。(2)加成反应。
①概念:有机物分子中的______(或______)两端的碳原子与其他原子或原子团________生成新的化合物的反应。
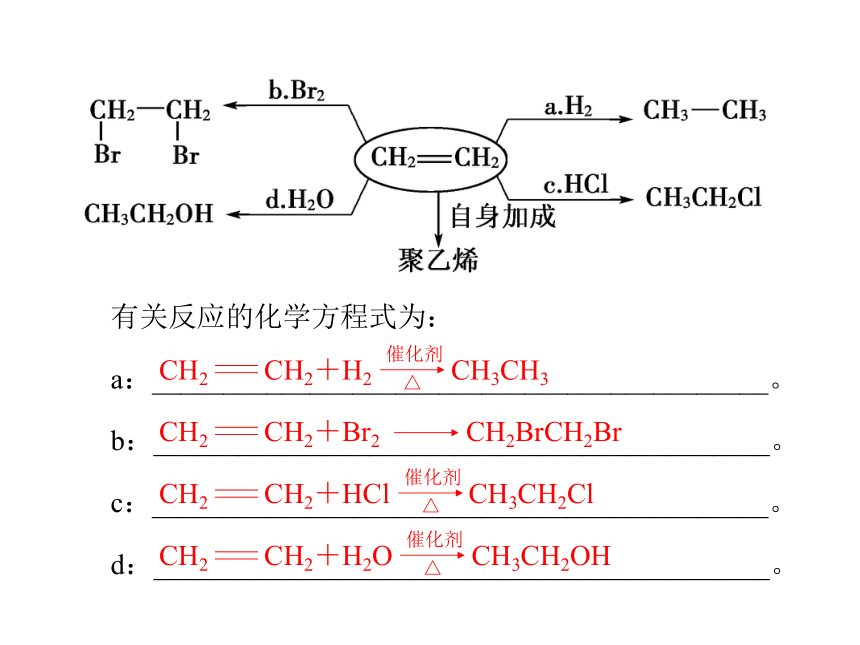
②乙烯的加成反应。褪色明亮黑烟双键 三键直接结合有关反应的化学方程式为:
a:___________________________________________。
b:___________________________________________。
c:___________________________________________。
d:___________________________________________。4.乙烯的用途
(1)______的产量可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中用作______________。乙烯植物生长调节剂应用思考:1.乙烯燃烧时为什么火焰明亮并伴有黑烟?提示:乙烯燃烧时火焰明亮并伴有黑烟的原因是乙烯的含碳量高。乙烯燃烧不充分时,一部分碳呈游离态,所以冒黑烟,又因该部分碳被烧成炙热状态,所以乙烯的火焰很明亮。 2.检验甲烷和乙烯气体可以采用什么方法?除去甲烷气体中的乙烯可以采用什么方法?提示:检验甲烷和乙烯可以选择溴水或酸性KMnO4溶液,出现褪色现象的为乙烯;但是除去甲烷中的乙烯只能用溴水,因为酸性KMnO4溶液可以将乙烯氧化成CO2气体而引入新的杂质。综合拓展一、乙烯与酸性高锰酸钾溶液、溴水、溴的四氯化碳溶液反应的比较特别关注:(1)利用乙烯(或烯烃)能使溴水褪色而甲烷(或烷烃)不能使溴水褪色,既可以区别乙烯(或烯烃)和甲烷(或烷烃),也可以除去甲烷(或烷烃)中混有的乙烯(或烯烃)气体以提纯甲烷(或烷烃)。
(2)为制得纯净的氯乙烷,应用乙烯与HCl的加成反应而不宜用乙烷与Cl2的取代反应。因为乙烯与HCl的加成产物只有一种,而乙烷与Cl2的取代产物是多种氯代烷的混合物。 二、乙烷、乙烯的结构和性质比较(续上表)(续上表)三、取代反应与加成反应的比较尝试应用1.下列物质的分子中,所有的原子都在同一平面上的是( )
A.氨气 B.乙烷 C.甲烷 D.乙烯解析:NH3的结构为三角锥型,N原子位于锥顶;C2H6是由两个四面体组成的不规则结构;CH4是正四面体结构;C2H4是平面结构。
答案:D 2.(双选题)下列各反应中属于加成反应的是( )解析:掌握加成反应的特点是解答本题的关键。C项是乙炔与H2的加成反应,根据加成反应的定义知C项也符合题意。
答案:AC3.下列关于乙烯的叙述中,不正确的是( )
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,同时冒出黑烟
C.乙烯可作香蕉果实的催熟剂
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应D一、乙烯的结构 由乙烯推测丙烯(CH3CH===CH2)的结构或性质正确的是( )
A.分子中3个碳原子在同一条直线上
B.分子中所有原子都在同一平面上
C.能使溴的四氯化碳溶液褪色
D.与HCl加成只生成一种产物代替,所以3个碳原子以及连在双键碳上的氢原子是在同一平面上,显然3个碳原子不在同一条直线上。由于甲基中4个原子不在同一平面上,所以CH2===CH—CH3分子中不可能所有原子都在同一平面上;既然丙烯中有不饱和键,就和乙烯的性质相似,能使溴的四氯化碳溶液褪色。丙烯与HCl加成可得 。答案:C名师点睛:乙烷、乙烯的比较:
(1)结构的区别,乙烷分子中含C—C键,碳原子的化合价达到“饱和”,乙烯分子中含C===C键,碳原子的化合价未达到“饱和”。
(2)与酸性KMnO4溶液反应,乙烷不能使酸性KMnO4溶液褪色,乙烯能使酸性KMnO4溶液褪色。
(3)只要有机物分子中有碳碳双键,化学性质就与乙烯的相似,能发生氧化反应和加成反应。变式应用1.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数比为1:2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯容易与溴水发生加成反应,且1 mol乙烯完全加成消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色解析:乙烯分子里碳氢原子个数比是由有机物的结构决定的,烯烃和环烷烃分子中碳氢原子个数比均为1∶2;乙烯的燃烧产物不能证明双键的个数;乙烯的加成反应与双键有直接关系,1 mol双键消耗1 mol溴单质;不饱和键均能使酸性KMnO4溶液褪色。
答案:C二、乙烯的化学性质 足球比赛中,当运动员肌肉挫伤或扭伤时,队医随即对准球员的受伤部位喷射药剂氯乙烷(沸点12.27 ℃),进行局部冷冻麻醉应急处理。
(1)制取氯乙烷(CH3—CH2Cl)的最好方法是( )
A.乙烷与氯气发生取代反应
B.乙烯与氯气发生加成反应
C.乙烷与氯化氢混合
D.乙烯与氯化氢发生加成反应(2)写出所选反应的化学方程式___________________________________________________,
该反应的反应类型为________反应。
(3)决定氯乙烷能用于冷冻麻醉应急处理的理由是___________________________________________________。 解析:(1)A中乙烷可以与氯气发生取代反应,但是反应可以得到CH3—CH2Cl、CH2Cl—CH2Cl、CH3—CHCl2…CCl3—CCl3等一系列取代产物,不能得到纯净的氯乙烷。B中乙烯与氯气加成得到二氯乙烷CH2Cl—CH2Cl,不能得到氯乙烷。C中乙烷与氯化氢不能反应。只有D中乙烯和氯化氢加成可以得到纯净的氯乙烷。
答案:(1)D
(2)CH2===CH2+HCl―→CH3—CH2Cl 加成
(3)其沸点低,极易挥发而吸收大量的热
名师点睛:乙烯分子中含有碳碳双键,化学性质活泼,双键中有一个键容易断裂,从而在两个碳原子上各连接一个原子或原子团而发生加成反应;双键也容易被强氧化剂如酸性KMnO4溶液氧化。变式应用2.下列说法中,错误的是( )
A.无论乙烯与Br2的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷解析:答案:C水平测试1.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应能使其褪色
C.乙烯分子没有同分异构体
D.乙烯分子的一氯代物只有一种结构B2.下列不属于乙烯用途的是( )
A.制造塑料 B.制有机溶剂
C.做灭火剂 D.做果实催熟剂解析:乙烯易燃烧,不能做灭火剂。
答案:C3.甲烷是最简单的烷烃,乙烯是最简单的烯烃,下列物质中,不能用来鉴别二者的是( )
A.水 B.溴水
C.溴的四氯化碳溶液 D.酸性高锰酸钾溶液A 4.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )A5.(双选题)在120 ℃ 101 kPa时,下列物质与足量的氧气混合,充分燃烧后恢复到原来的条件,反应前后气体体积不变化的是( )
A.乙烯 B.丙烯 C.甲烷 D.乙烷解析:推断本题的正确选项,可利用差量法(体积)。根据烃燃烧的化学方程式:由此可知燃烧后气体体积的变化量只与烃分子中的H原子数有关,与C原子数无关。当温度大于100 ℃时,H2O为气态,ΔV=1- 。本题要求是反应前后气体体积不变,即ΔV=0,所以1- =0,则y=4。这表明在烃分子中的H原子数为4的均符合题意。如CH4、C2H4等。
答案:AC 6.石蜡油(主要是含17个以上碳原子的液态烷烃混合物)分解实验按照下图进行:(1)石蜡油分解实验产生的气体的主要成分是________。
①只有甲烷 ②只有乙烯 ③烷烃跟烯烃的混合物
(2)将石蜡油分解所得生成物通入溴水中,现象是______________________;通入酸性高锰酸钾溶液中,现象是______________________。
(3)碎瓷片的作用是________。
①防止暴沸 ②有催化功能 ③积蓄热量 ④作反应物
(4)写出含有18个碳原子的烷烃分解为乙烷与最多乙烯的化学方程式:__________________________________。能力提升7.使1 mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应,则两个过程中消耗氯气的总物质的量最多是( )
A.3 mol B.4 mol C.5 mol D.6 mol解析:1 mol乙烯能与1 mol Cl2发生加成反应,而1 mol加成产物中含4 mol氢原子,被氯原子完全取代,消耗4 mol Cl2,所以共消耗Cl2 5 mol,故选C项。
答案:C8.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
A.将混合气体通过盛有酸性高锰酸钾溶液的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体跟氯化氢混合解析:鉴别乙烷和乙烯,可以选A操作或B操作,能使酸性高锰酸钾溶液或溴水褪色的气体是乙烯。除去乙烷中的乙烯,只能选B操作,因为乙烷可被酸性高锰酸钾溶液氧化为二氧化碳和水,二氧化碳会混入乙烷中,所以不能选A操作。
答案:B 9.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计实验如下图所示以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:(1)在图中①②③④装置中可盛放的试剂是:①__________________________________________________;
②________;③________;④________。
A.品红溶液 B.NaOH溶液
C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明二氧化硫气体存在的现象是__________________________________________________。(3)使用装置②的目的是__________________________________________________。
(4)使用装置③的目的是__________________________________________________。
(5)确认含有乙烯的现象是__________________________________________________。答案:(1)①A ②B ③A ④D
(2)装置①中品红溶液褪色
(3)除去SO2,以免干扰乙烯的检验
(4)检验SO2是否除净
(5)装置③中的品红溶液不褪色,装置④中的酸性高锰酸钾溶液褪色10.乙烯和乙烷的混合气体共a mol,与b mol的氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45 g水。试求:
(1)CO和CO2混合气体的物质的量为________,生成的水的物质的量为________。
(2)当a=1时,乙烯和乙烷的物质的量之比:n(乙烯):n(乙烷)=________。(3)当a=1,且反应后CO和CO2混合气体的物质的量为反应前氧气的2/3时,则b=________;得到的CO和CO2的物质的量之比:n(CO):n(CO2)=________。
(4)a的取值范围是________;b的取值范围是________。感谢您的使用,退出请按ESC键本小节结束
第1课时 乙 烯有机化合物第1课时 乙 烯 2009年8月,山东电视台“生活帮”栏目报导了这样一件事情:市面上的很多葡萄看起来又红又紫,但吃起来却酸涩无比。根据记者的调查才知,葡萄种植者在未成熟的葡萄上喷洒了乙烯利,促进葡萄成熟,但这种催熟的葡萄没有正常成熟的葡萄甘甜。乙烯利是一种水剂,在一定条件下能放出乙烯,乙烯能促进果实成熟。
乙烯是从石油中提取的,它有哪些性质呢?1.了解烯烃的概念。
2.了解乙烯的物理性质、工业制取原理及其在化工生产中的作用。
3.掌握乙烯的分子结构,初步体会其结构特点对性质的影响。
4.掌握乙烯的化学性质,认识加成反应的特点。烯烃1.概念
分子中含有________的一类链烃,属于不饱和烃。
2.分子通式
CnH2n(n≥2)。碳碳双键乙烯1.乙烯的来源
从______中获得乙烯,已成为目前工业上生产乙烯的主要途径,乙烯是石油的裂解产物。
2.乙烯的制取
(1)实验原理。石蜡油 乙烯等(石蜡油是含17个C以上的液态烷烃混合物)。石油(2)实验步骤。褪去褪色明亮黑烟褪色研究表明,石蜡油分解的产物主要是乙烯和烷烃的混合物。
(3)分子结构。C2H43.乙烯的化学性质
(1)氧化反应。(2)加成反应。
①概念:有机物分子中的______(或______)两端的碳原子与其他原子或原子团________生成新的化合物的反应。
②乙烯的加成反应。褪色明亮黑烟双键 三键直接结合有关反应的化学方程式为:
a:___________________________________________。
b:___________________________________________。
c:___________________________________________。
d:___________________________________________。4.乙烯的用途
(1)______的产量可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中用作______________。乙烯植物生长调节剂应用思考:1.乙烯燃烧时为什么火焰明亮并伴有黑烟?提示:乙烯燃烧时火焰明亮并伴有黑烟的原因是乙烯的含碳量高。乙烯燃烧不充分时,一部分碳呈游离态,所以冒黑烟,又因该部分碳被烧成炙热状态,所以乙烯的火焰很明亮。 2.检验甲烷和乙烯气体可以采用什么方法?除去甲烷气体中的乙烯可以采用什么方法?提示:检验甲烷和乙烯可以选择溴水或酸性KMnO4溶液,出现褪色现象的为乙烯;但是除去甲烷中的乙烯只能用溴水,因为酸性KMnO4溶液可以将乙烯氧化成CO2气体而引入新的杂质。综合拓展一、乙烯与酸性高锰酸钾溶液、溴水、溴的四氯化碳溶液反应的比较特别关注:(1)利用乙烯(或烯烃)能使溴水褪色而甲烷(或烷烃)不能使溴水褪色,既可以区别乙烯(或烯烃)和甲烷(或烷烃),也可以除去甲烷(或烷烃)中混有的乙烯(或烯烃)气体以提纯甲烷(或烷烃)。
(2)为制得纯净的氯乙烷,应用乙烯与HCl的加成反应而不宜用乙烷与Cl2的取代反应。因为乙烯与HCl的加成产物只有一种,而乙烷与Cl2的取代产物是多种氯代烷的混合物。 二、乙烷、乙烯的结构和性质比较(续上表)(续上表)三、取代反应与加成反应的比较尝试应用1.下列物质的分子中,所有的原子都在同一平面上的是( )
A.氨气 B.乙烷 C.甲烷 D.乙烯解析:NH3的结构为三角锥型,N原子位于锥顶;C2H6是由两个四面体组成的不规则结构;CH4是正四面体结构;C2H4是平面结构。
答案:D 2.(双选题)下列各反应中属于加成反应的是( )解析:掌握加成反应的特点是解答本题的关键。C项是乙炔与H2的加成反应,根据加成反应的定义知C项也符合题意。
答案:AC3.下列关于乙烯的叙述中,不正确的是( )
A.乙烯的化学性质比乙烷活泼
B.乙烯燃烧时火焰明亮,同时冒出黑烟
C.乙烯可作香蕉果实的催熟剂
D.乙烯双键中的一个键可以断裂,容易发生加成反应和取代反应D一、乙烯的结构 由乙烯推测丙烯(CH3CH===CH2)的结构或性质正确的是( )
A.分子中3个碳原子在同一条直线上
B.分子中所有原子都在同一平面上
C.能使溴的四氯化碳溶液褪色
D.与HCl加成只生成一种产物代替,所以3个碳原子以及连在双键碳上的氢原子是在同一平面上,显然3个碳原子不在同一条直线上。由于甲基中4个原子不在同一平面上,所以CH2===CH—CH3分子中不可能所有原子都在同一平面上;既然丙烯中有不饱和键,就和乙烯的性质相似,能使溴的四氯化碳溶液褪色。丙烯与HCl加成可得 。答案:C名师点睛:乙烷、乙烯的比较:
(1)结构的区别,乙烷分子中含C—C键,碳原子的化合价达到“饱和”,乙烯分子中含C===C键,碳原子的化合价未达到“饱和”。
(2)与酸性KMnO4溶液反应,乙烷不能使酸性KMnO4溶液褪色,乙烯能使酸性KMnO4溶液褪色。
(3)只要有机物分子中有碳碳双键,化学性质就与乙烯的相似,能发生氧化反应和加成反应。变式应用1.能证明乙烯分子里含有一个碳碳双键的事实是( )
A.乙烯分子里碳氢原子个数比为1:2
B.乙烯完全燃烧生成的CO2和H2O的物质的量相等
C.乙烯容易与溴水发生加成反应,且1 mol乙烯完全加成消耗1 mol溴单质
D.乙烯能使酸性KMnO4溶液褪色解析:乙烯分子里碳氢原子个数比是由有机物的结构决定的,烯烃和环烷烃分子中碳氢原子个数比均为1∶2;乙烯的燃烧产物不能证明双键的个数;乙烯的加成反应与双键有直接关系,1 mol双键消耗1 mol溴单质;不饱和键均能使酸性KMnO4溶液褪色。
答案:C二、乙烯的化学性质 足球比赛中,当运动员肌肉挫伤或扭伤时,队医随即对准球员的受伤部位喷射药剂氯乙烷(沸点12.27 ℃),进行局部冷冻麻醉应急处理。
(1)制取氯乙烷(CH3—CH2Cl)的最好方法是( )
A.乙烷与氯气发生取代反应
B.乙烯与氯气发生加成反应
C.乙烷与氯化氢混合
D.乙烯与氯化氢发生加成反应(2)写出所选反应的化学方程式___________________________________________________,
该反应的反应类型为________反应。
(3)决定氯乙烷能用于冷冻麻醉应急处理的理由是___________________________________________________。 解析:(1)A中乙烷可以与氯气发生取代反应,但是反应可以得到CH3—CH2Cl、CH2Cl—CH2Cl、CH3—CHCl2…CCl3—CCl3等一系列取代产物,不能得到纯净的氯乙烷。B中乙烯与氯气加成得到二氯乙烷CH2Cl—CH2Cl,不能得到氯乙烷。C中乙烷与氯化氢不能反应。只有D中乙烯和氯化氢加成可以得到纯净的氯乙烷。
答案:(1)D
(2)CH2===CH2+HCl―→CH3—CH2Cl 加成
(3)其沸点低,极易挥发而吸收大量的热
名师点睛:乙烯分子中含有碳碳双键,化学性质活泼,双键中有一个键容易断裂,从而在两个碳原子上各连接一个原子或原子团而发生加成反应;双键也容易被强氧化剂如酸性KMnO4溶液氧化。变式应用2.下列说法中,错误的是( )
A.无论乙烯与Br2的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
B.用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷
C.相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同
D.利用燃烧的方法可以鉴别乙烯和甲烷解析:答案:C水平测试1.下列关于乙烯结构与性质的叙述中,错误的是( )
A.乙烯分子中6个原子在同一平面内
B.乙烯与酸性KMnO4溶液发生加成反应能使其褪色
C.乙烯分子没有同分异构体
D.乙烯分子的一氯代物只有一种结构B2.下列不属于乙烯用途的是( )
A.制造塑料 B.制有机溶剂
C.做灭火剂 D.做果实催熟剂解析:乙烯易燃烧,不能做灭火剂。
答案:C3.甲烷是最简单的烷烃,乙烯是最简单的烯烃,下列物质中,不能用来鉴别二者的是( )
A.水 B.溴水
C.溴的四氯化碳溶液 D.酸性高锰酸钾溶液A 4.下列各组物质之间的化学反应,反应产物一定为纯净物的是( )A5.(双选题)在120 ℃ 101 kPa时,下列物质与足量的氧气混合,充分燃烧后恢复到原来的条件,反应前后气体体积不变化的是( )
A.乙烯 B.丙烯 C.甲烷 D.乙烷解析:推断本题的正确选项,可利用差量法(体积)。根据烃燃烧的化学方程式:由此可知燃烧后气体体积的变化量只与烃分子中的H原子数有关,与C原子数无关。当温度大于100 ℃时,H2O为气态,ΔV=1- 。本题要求是反应前后气体体积不变,即ΔV=0,所以1- =0,则y=4。这表明在烃分子中的H原子数为4的均符合题意。如CH4、C2H4等。
答案:AC 6.石蜡油(主要是含17个以上碳原子的液态烷烃混合物)分解实验按照下图进行:(1)石蜡油分解实验产生的气体的主要成分是________。
①只有甲烷 ②只有乙烯 ③烷烃跟烯烃的混合物
(2)将石蜡油分解所得生成物通入溴水中,现象是______________________;通入酸性高锰酸钾溶液中,现象是______________________。
(3)碎瓷片的作用是________。
①防止暴沸 ②有催化功能 ③积蓄热量 ④作反应物
(4)写出含有18个碳原子的烷烃分解为乙烷与最多乙烯的化学方程式:__________________________________。能力提升7.使1 mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与氯气在光照的条件下发生取代反应,则两个过程中消耗氯气的总物质的量最多是( )
A.3 mol B.4 mol C.5 mol D.6 mol解析:1 mol乙烯能与1 mol Cl2发生加成反应,而1 mol加成产物中含4 mol氢原子,被氯原子完全取代,消耗4 mol Cl2,所以共消耗Cl2 5 mol,故选C项。
答案:C8.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
A.将混合气体通过盛有酸性高锰酸钾溶液的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体跟氯化氢混合解析:鉴别乙烷和乙烯,可以选A操作或B操作,能使酸性高锰酸钾溶液或溴水褪色的气体是乙烯。除去乙烷中的乙烯,只能选B操作,因为乙烷可被酸性高锰酸钾溶液氧化为二氧化碳和水,二氧化碳会混入乙烷中,所以不能选A操作。
答案:B 9.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。有人设计实验如下图所示以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:(1)在图中①②③④装置中可盛放的试剂是:①__________________________________________________;
②________;③________;④________。
A.品红溶液 B.NaOH溶液
C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明二氧化硫气体存在的现象是__________________________________________________。(3)使用装置②的目的是__________________________________________________。
(4)使用装置③的目的是__________________________________________________。
(5)确认含有乙烯的现象是__________________________________________________。答案:(1)①A ②B ③A ④D
(2)装置①中品红溶液褪色
(3)除去SO2,以免干扰乙烯的检验
(4)检验SO2是否除净
(5)装置③中的品红溶液不褪色,装置④中的酸性高锰酸钾溶液褪色10.乙烯和乙烷的混合气体共a mol,与b mol的氧气共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45 g水。试求:
(1)CO和CO2混合气体的物质的量为________,生成的水的物质的量为________。
(2)当a=1时,乙烯和乙烷的物质的量之比:n(乙烯):n(乙烷)=________。(3)当a=1,且反应后CO和CO2混合气体的物质的量为反应前氧气的2/3时,则b=________;得到的CO和CO2的物质的量之比:n(CO):n(CO2)=________。
(4)a的取值范围是________;b的取值范围是________。感谢您的使用,退出请按ESC键本小节结束
