4.3质量守恒定律同步练习(含答案)科粤版化学九年级上册
文档属性
| 名称 | 4.3质量守恒定律同步练习(含答案)科粤版化学九年级上册 |
|
|
| 格式 | docx | ||
| 文件大小 | 163.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-24 00:00:00 | ||
图片预览



文档简介
4.3质量守恒定律同步练习科粤版化学九年级上册
学校:___________姓名:___________班级:___________考号:___________
一、单选题
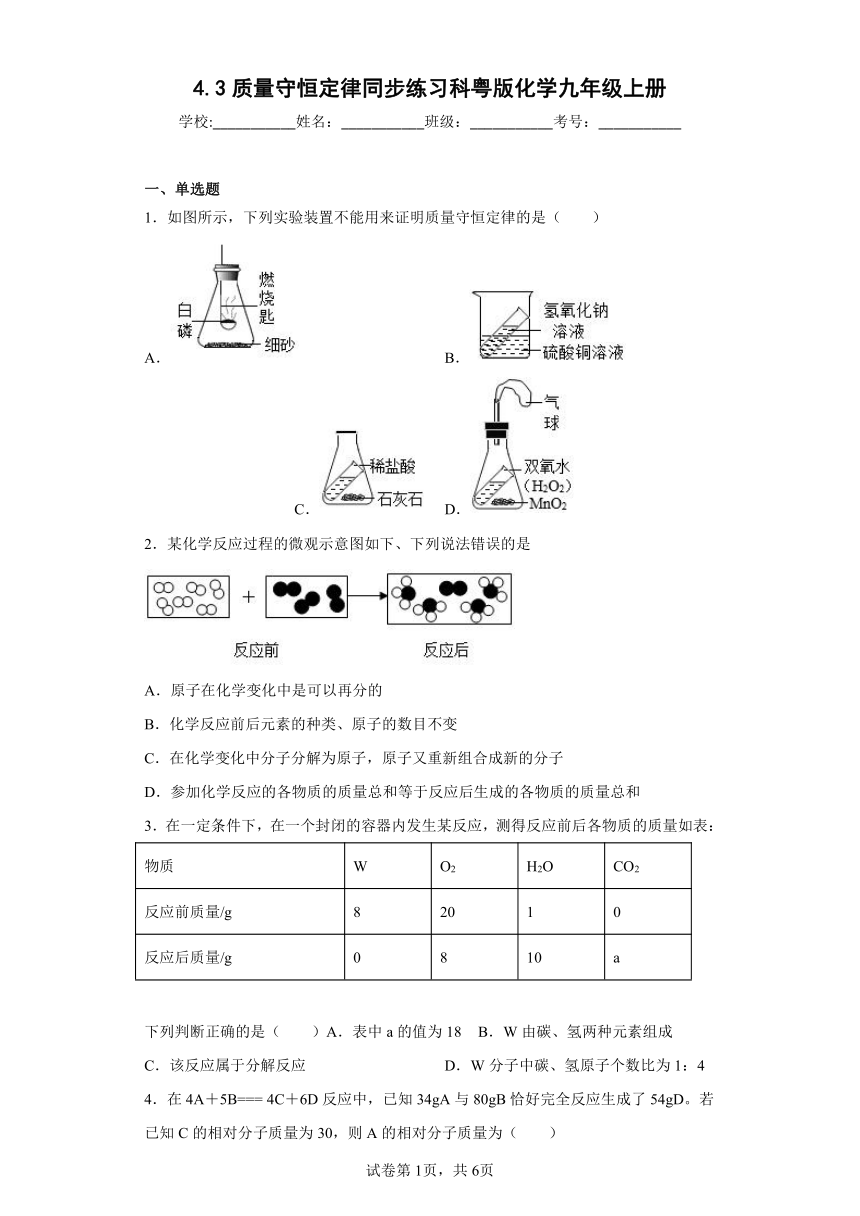
1.如图所示,下列实验装置不能用来证明质量守恒定律的是( )
A. B. C. D.
2.某化学反应过程的微观示意图如下、下列说法错误的是
A.原子在化学变化中是可以再分的
B.化学反应前后元素的种类、原子的数目不变
C.在化学变化中分子分解为原子,原子又重新组合成新的分子
D.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
3.在一定条件下,在一个封闭的容器内发生某反应,测得反应前后各物质的质量如表:
物质 W O2 H2O CO2
反应前质量/g 8 20 1 0
反应后质量/g 0 8 10 a
下列判断正确的是( )A.表中a的值为18 B.W由碳、氢两种元素组成
C.该反应属于分解反应 D.W分子中碳、氢原子个数比为1:4
4.在4A+5B=== 4C+6D反应中,已知34gA与80gB恰好完全反应生成了54gD。若已知C的相对分子质量为30,则A的相对分子质量为( )
A.68 B.34 C.17 D.5
5.香烟的烟气中含有CO和尼古丁(C10H14N2)等有害健康的物质。下列有关尼古丁的说法正确的是
A.完全燃烧只生成CO2和H2O
B.碳、氢、氮元素的质量比为5:7:1
C.162g尼古丁中含氢元素的质量为14g
D.氮元素的质量分数最小
6.某化学反应的微观示意图如下图所示,下列说法正确的是镁原子
A.该反应生成了3种物质
B.反应涉及的物质中,是由原子构成的单质
C.参加反应的和的微粒个数比是4:3
D.反应前后元素的种类及化合价均未发生改变
7.山茶油是一种绿色保健食品,其主要成分是柠檬醛。现从山茶油中提取15.2柠檬醛,使其在氧气中充分燃烧,生成44二氧化碳和14.4水,则柠檬醛中
A.只含碳、氢元素 B.一定含有碳、氢、氧元素
C.一定含碳、氢元素,可能含有氧元素 D.含有的元素种类无法判断
8.近年,科学家找到从月球岩石制取氧气的方法。下列有关叙述正确的是
A.制取过程只发生了物理变化 B.月球岩石中肯定含有高锰酸钾
C.月球岩石中一定含有氧元素 D.月球岩石中一定含有二氧化锰
9.下列推理正确的是( )
A.分子可以构成物质,所以物质一定是由分子构成的
B.化学变化伴随有能量变化,则有能量变化的变化一定是化学变化
C.单质只含一种元素,所以含一种元素的物质一定是单质
D.蜡烛在氧气中燃烧生成二氧化碳和水,所以蜡烛中一定含碳、氢元素
10.用如图所示装置及其药品验证质量守恒定律的实验能达到目的的是
A.①②③ B.①③④ C.①③ D.②④
二、判断题
11.2体积的水电解生产氧气和氢气的体积总和为2体积。( )
12.2份质量的水反应生成2份质量的氢气和1份质量的氧气。( )
13.质量守恒定律指质量守恒,不包括其他方面的守恒,如体积等。没有参加反应的物质的质量和非反应生成的物质的质量不能计入“总和”中。( )
14.在探究质量守恒定律实验中,铁和硫酸铜溶液反应,锥形瓶必须要用胶塞塞紧( )
15.化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。( )
三、填空题
16.如图为某化学反应的微观过程,其中“”和“”表示两种不同的原子。
(1)该反应中反应物______(填“可能”或“不可能”)是氧化物,属于______反应(填化学反应的基本类型)。
(2)图中虚线框内应填的微观图示是______(选填A、B、C、D),你推断的依据是:(写两点)______,______。
A、B、C、D、
17.回答下列有关实验的问题:
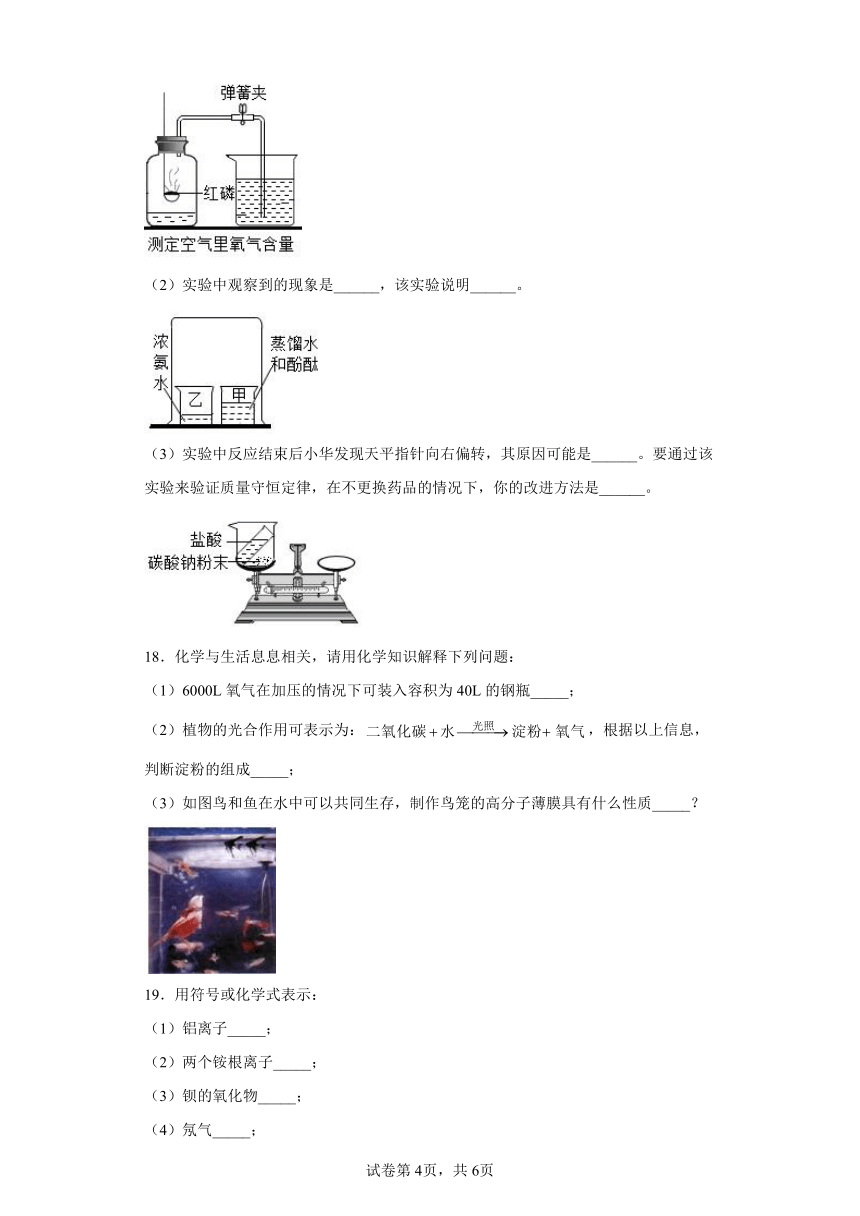
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______。(答一种即可)
(2)实验中观察到的现象是______,该实验说明______。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是______。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______。
18.化学与生活息息相关,请用化学知识解释下列问题:
(1)6000L氧气在加压的情况下可装入容积为40L的钢瓶_____;
(2)植物的光合作用可表示为:,根据以上信息,判断淀粉的组成_____;
(3)如图鸟和鱼在水中可以共同生存,制作鸟笼的高分子薄膜具有什么性质_____?
19.用符号或化学式表示:
(1)铝离子_____;
(2)两个铵根离子_____;
(3)钡的氧化物_____;
(4)氖气_____;
(5)氧化铁中铁元素的化合价为+3价_____;
(6)在空气中燃烧产生白烟的非金属单质_____;
(7)高粱玉米和薯类经发酵蒸馏可得到的绿色燃料是_____。
20.某同学把4g硫放在给定的氧气中充分燃烧,实验数据如下表所示。
第一次 第二次 第三次
O2的质量(g) 3 4 6
生成SO2的质量(g) 6 8 8
回答下列问题:
(1)从以上数据说明,这三次实验中第_______次恰好完全反应;
(2)第_______次实验中硫有剩余,剩余_______g;
(3)第_______次实验中氧气有剩余,剩余_______g;
(4)这三次实验的化学反应过程中,是否有不符合质量守恒定律的?________________。
四、综合应用题
21.某密闭容器中有 X、氧气和二氧化碳三种物质,在一定条件下充分反应,测 得反应前后各物质的质量如表:
物质 x O2 CO2 H2O
反应前质量/g 16 70 1 0
反应后质量/g 0 待测 45 36
表中待测值为_____,X 的化学式为_____; 反应中 X 和氧气的化学计量数 之比为_____。
22.在高温条件下,A、B两种物质可以发生化学反应生成C和D。反应前后分子种类变化的微观示意图如下图所示。
(1)上述图片中,有__________种化合物分子
(2)在该反应中,以下叙述正确的是___________(填字母)。
A.属于置换反应 B.原子种类没有改变
C.分子的个数没有改变 D.A物质中某元素的质量分数为25%
(3)该微观示意图中,为了体现化学变化要遵守质量守恒定律,需在反应后图片中补画____________个D分子
(4)①Fe;②③Fe2+;④Fe3+;⑤Fe3O4是常见的化学用语。下列说法不正确的是( ):
A.表示一个铁原子的是-①; B.表示氧化亚铁中铁元素的化合价的是—②;
C.表示铁离子的是—③; D.表示铁在氧气中燃烧的产物的是—⑤
23.某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过下图所示装置。观察到:①A装置内未见浑浊现象;②D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝):③最终收集到一种不能燃烧的干燥气体(假设每步反应都是完全的)。请回答下列问题:
(1)由①可知原混合气体中肯定不含________;
(2)由②可知原混合气体中一定含有________;
(3)E装置的作用是________;
(4)实验过程中记录的实验数据如下,并依据数据可推知原气体组成。
D装置总质量 E、F装置总质量
反应前 156.6g 356.8g
反应后 158.4g 361.2g
则该气体的成分为________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.D
4.C
5.C
6.B
7.B
8.C
9.D
10.C
11.错误
12.错误
13.√
14.错误
15.错误
16.(1) 可能 分解反应
(2) D 质量守恒定律 每个 由2个 构成
17. 装置漏气(红磷量不足;未完全冷却就打开弹簧夹读数) 烧杯甲中溶液变为红色 分子在不停地运动 生成的CO2气体逸散到空气中,未称量到 将烧杯换成密闭容器(将装置改成密闭装置)
18. 分子间存在间隔,气体受压后,分子间隔变小 一定含有碳元素和氢元素,可能含有氧元素 隔水、透气
19. Al3+; 2NH4+; BaO; Ne; P; C2H5OH。
20. 二 一 1 三 2 三次都符合
21. 6 CH4 1:2
22. 3 BD 2 C
23.(1)二氧化碳##CO2
(2)甲烷##CH4
(3)吸收反应生成的二氧化碳气体
(4)一氧化碳、甲烷和氮气
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.如图所示,下列实验装置不能用来证明质量守恒定律的是( )
A. B. C. D.
2.某化学反应过程的微观示意图如下、下列说法错误的是
A.原子在化学变化中是可以再分的
B.化学反应前后元素的种类、原子的数目不变
C.在化学变化中分子分解为原子,原子又重新组合成新的分子
D.参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和
3.在一定条件下,在一个封闭的容器内发生某反应,测得反应前后各物质的质量如表:
物质 W O2 H2O CO2
反应前质量/g 8 20 1 0
反应后质量/g 0 8 10 a
下列判断正确的是( )A.表中a的值为18 B.W由碳、氢两种元素组成
C.该反应属于分解反应 D.W分子中碳、氢原子个数比为1:4
4.在4A+5B=== 4C+6D反应中,已知34gA与80gB恰好完全反应生成了54gD。若已知C的相对分子质量为30,则A的相对分子质量为( )
A.68 B.34 C.17 D.5
5.香烟的烟气中含有CO和尼古丁(C10H14N2)等有害健康的物质。下列有关尼古丁的说法正确的是
A.完全燃烧只生成CO2和H2O
B.碳、氢、氮元素的质量比为5:7:1
C.162g尼古丁中含氢元素的质量为14g
D.氮元素的质量分数最小
6.某化学反应的微观示意图如下图所示,下列说法正确的是镁原子
A.该反应生成了3种物质
B.反应涉及的物质中,是由原子构成的单质
C.参加反应的和的微粒个数比是4:3
D.反应前后元素的种类及化合价均未发生改变
7.山茶油是一种绿色保健食品,其主要成分是柠檬醛。现从山茶油中提取15.2柠檬醛,使其在氧气中充分燃烧,生成44二氧化碳和14.4水,则柠檬醛中
A.只含碳、氢元素 B.一定含有碳、氢、氧元素
C.一定含碳、氢元素,可能含有氧元素 D.含有的元素种类无法判断
8.近年,科学家找到从月球岩石制取氧气的方法。下列有关叙述正确的是
A.制取过程只发生了物理变化 B.月球岩石中肯定含有高锰酸钾
C.月球岩石中一定含有氧元素 D.月球岩石中一定含有二氧化锰
9.下列推理正确的是( )
A.分子可以构成物质,所以物质一定是由分子构成的
B.化学变化伴随有能量变化,则有能量变化的变化一定是化学变化
C.单质只含一种元素,所以含一种元素的物质一定是单质
D.蜡烛在氧气中燃烧生成二氧化碳和水,所以蜡烛中一定含碳、氢元素
10.用如图所示装置及其药品验证质量守恒定律的实验能达到目的的是
A.①②③ B.①③④ C.①③ D.②④
二、判断题
11.2体积的水电解生产氧气和氢气的体积总和为2体积。( )
12.2份质量的水反应生成2份质量的氢气和1份质量的氧气。( )
13.质量守恒定律指质量守恒,不包括其他方面的守恒,如体积等。没有参加反应的物质的质量和非反应生成的物质的质量不能计入“总和”中。( )
14.在探究质量守恒定律实验中,铁和硫酸铜溶液反应,锥形瓶必须要用胶塞塞紧( )
15.化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。( )
三、填空题
16.如图为某化学反应的微观过程,其中“”和“”表示两种不同的原子。
(1)该反应中反应物______(填“可能”或“不可能”)是氧化物,属于______反应(填化学反应的基本类型)。
(2)图中虚线框内应填的微观图示是______(选填A、B、C、D),你推断的依据是:(写两点)______,______。
A、B、C、D、
17.回答下列有关实验的问题:
(1)实验中,打开弹簧夹进入瓶中的水不足五分之一,其原因可能是______。(答一种即可)
(2)实验中观察到的现象是______,该实验说明______。
(3)实验中反应结束后小华发现天平指针向右偏转,其原因可能是______。要通过该实验来验证质量守恒定律,在不更换药品的情况下,你的改进方法是______。
18.化学与生活息息相关,请用化学知识解释下列问题:
(1)6000L氧气在加压的情况下可装入容积为40L的钢瓶_____;
(2)植物的光合作用可表示为:,根据以上信息,判断淀粉的组成_____;
(3)如图鸟和鱼在水中可以共同生存,制作鸟笼的高分子薄膜具有什么性质_____?
19.用符号或化学式表示:
(1)铝离子_____;
(2)两个铵根离子_____;
(3)钡的氧化物_____;
(4)氖气_____;
(5)氧化铁中铁元素的化合价为+3价_____;
(6)在空气中燃烧产生白烟的非金属单质_____;
(7)高粱玉米和薯类经发酵蒸馏可得到的绿色燃料是_____。
20.某同学把4g硫放在给定的氧气中充分燃烧,实验数据如下表所示。
第一次 第二次 第三次
O2的质量(g) 3 4 6
生成SO2的质量(g) 6 8 8
回答下列问题:
(1)从以上数据说明,这三次实验中第_______次恰好完全反应;
(2)第_______次实验中硫有剩余,剩余_______g;
(3)第_______次实验中氧气有剩余,剩余_______g;
(4)这三次实验的化学反应过程中,是否有不符合质量守恒定律的?________________。
四、综合应用题
21.某密闭容器中有 X、氧气和二氧化碳三种物质,在一定条件下充分反应,测 得反应前后各物质的质量如表:
物质 x O2 CO2 H2O
反应前质量/g 16 70 1 0
反应后质量/g 0 待测 45 36
表中待测值为_____,X 的化学式为_____; 反应中 X 和氧气的化学计量数 之比为_____。
22.在高温条件下,A、B两种物质可以发生化学反应生成C和D。反应前后分子种类变化的微观示意图如下图所示。
(1)上述图片中,有__________种化合物分子
(2)在该反应中,以下叙述正确的是___________(填字母)。
A.属于置换反应 B.原子种类没有改变
C.分子的个数没有改变 D.A物质中某元素的质量分数为25%
(3)该微观示意图中,为了体现化学变化要遵守质量守恒定律,需在反应后图片中补画____________个D分子
(4)①Fe;②③Fe2+;④Fe3+;⑤Fe3O4是常见的化学用语。下列说法不正确的是( ):
A.表示一个铁原子的是-①; B.表示氧化亚铁中铁元素的化合价的是—②;
C.表示铁离子的是—③; D.表示铁在氧气中燃烧的产物的是—⑤
23.某无色气体中可能含有甲烷、一氧化碳、二氧化碳、氮气中的一种或几种,现将该气体依次通过下图所示装置。观察到:①A装置内未见浑浊现象;②D装置内无水硫酸铜变蓝(无水硫酸铜遇水变蓝):③最终收集到一种不能燃烧的干燥气体(假设每步反应都是完全的)。请回答下列问题:
(1)由①可知原混合气体中肯定不含________;
(2)由②可知原混合气体中一定含有________;
(3)E装置的作用是________;
(4)实验过程中记录的实验数据如下,并依据数据可推知原气体组成。
D装置总质量 E、F装置总质量
反应前 156.6g 356.8g
反应后 158.4g 361.2g
则该气体的成分为________。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.A
3.D
4.C
5.C
6.B
7.B
8.C
9.D
10.C
11.错误
12.错误
13.√
14.错误
15.错误
16.(1) 可能 分解反应
(2) D 质量守恒定律 每个 由2个 构成
17. 装置漏气(红磷量不足;未完全冷却就打开弹簧夹读数) 烧杯甲中溶液变为红色 分子在不停地运动 生成的CO2气体逸散到空气中,未称量到 将烧杯换成密闭容器(将装置改成密闭装置)
18. 分子间存在间隔,气体受压后,分子间隔变小 一定含有碳元素和氢元素,可能含有氧元素 隔水、透气
19. Al3+; 2NH4+; BaO; Ne; P; C2H5OH。
20. 二 一 1 三 2 三次都符合
21. 6 CH4 1:2
22. 3 BD 2 C
23.(1)二氧化碳##CO2
(2)甲烷##CH4
(3)吸收反应生成的二氧化碳气体
(4)一氧化碳、甲烷和氮气
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
