生物人教版(2019)必修1 5.1.2降低化学反应活化能的酶课件(共45张ppt)
文档属性
| 名称 | 生物人教版(2019)必修1 5.1.2降低化学反应活化能的酶课件(共45张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 19.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2022-12-25 00:00:00 | ||
图片预览








文档简介
(共45张PPT)
第1节 降低化学反应活化能的酶(第2课时)
第5章 细胞的能量供应和利用
(一)酶具有高效性
一. 酶的特性
3
4
4
3
少量肝脏
研磨液
比较过氧化氢酶和Fe3+的催化效率
酶是活细胞产生的具有催化作用的有机物,一般情况下,酶的催化效率一般是无机催化剂的107 ~1013倍。
保证了细胞内化学反应的顺利进行,也保证了细胞内能量供应的稳定。
意义:
例、下图表示酶高效性的曲线
由曲线可知:___________________的催化效率更高;
酶只能缩短达到________________所需的时间,不改变化学反应的平衡点。因此,酶______(“能”或“不能”)改变最终生成物的量。
酶比无机催化剂
化学平衡
不能
酶只能缩短达到平衡的时间,不能改变平衡点
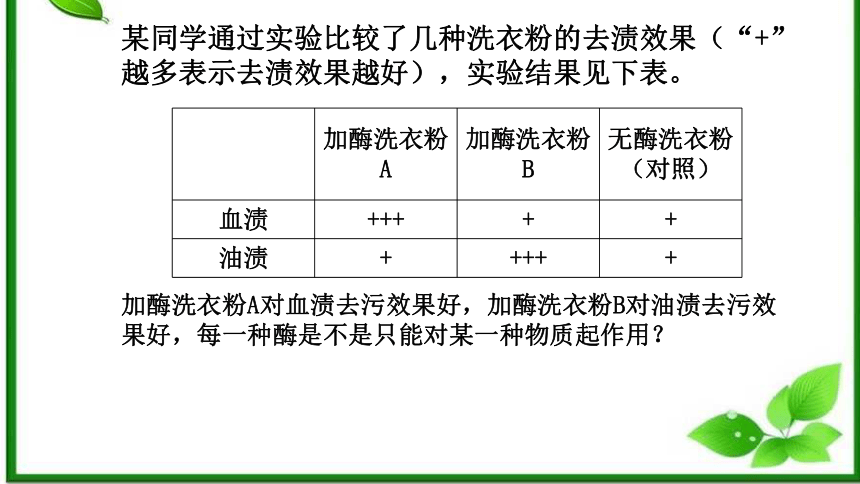
某同学通过实验比较了几种洗衣粉的去渍效果(“+”越多表示去渍效果越好),实验结果见下表。
加酶洗衣粉A 加酶洗衣粉B 无酶洗衣粉(对照)
血渍 +++ + +
油渍 + +++ +
加酶洗衣粉A对血渍去污效果好,加酶洗衣粉B对油渍去污效果好,每一种酶是不是只能对某一种物质起作用?
一、酶的特性
淀粉酶对淀粉和蔗糖的水解作用
实验原理
方法步骤
结果与结论
实验设计
实验探究:
1、实验器材:
质量分数为3%的淀粉溶液、质量分数为2%的新配置的淀粉酶溶液、质量分数为3%的蔗糖溶液、斐林试剂、热水
1. 淀粉和蔗糖都是非还原糖
2. 淀粉在相关酶的催化作用下能水解为麦芽糖
3. 蔗糖在相关酶的催化作用下能水解为葡萄糖和果糖
4. 麦芽糖、葡萄糖、果糖均属还原糖
5. 还原糖能够与斐林试剂发生反应,生成砖红色的沉淀
自变量是什么?
因变量是什么?怎样观察?
无关变量有哪些?
对照组是哪一组?
实验组是哪一组?
等量的淀粉溶液和蔗糖溶液
2、设计思路:
淀粉酶是否只能催化特定的化学反应
通过观察是否出现砖红色沉淀,就可以看出
反应物的浓度、所加物质的体积、反应时间
淀粉溶液和淀粉酶
蔗糖溶液和淀粉酶
各加入淀粉酶2ml,振荡,试管下半部浸入60℃左右的热水中,保温5min
加入2mL淀粉溶液
1号试管 2号试管
实验步骤 一
二
三
实验现象
结论
加入2mL蔗糖溶液
加入2ml斐林试剂
振荡
沸水浴1min
无砖红色沉淀
砖红色沉淀
淀粉酶只能催化淀粉水解,不能催化蔗糖水解
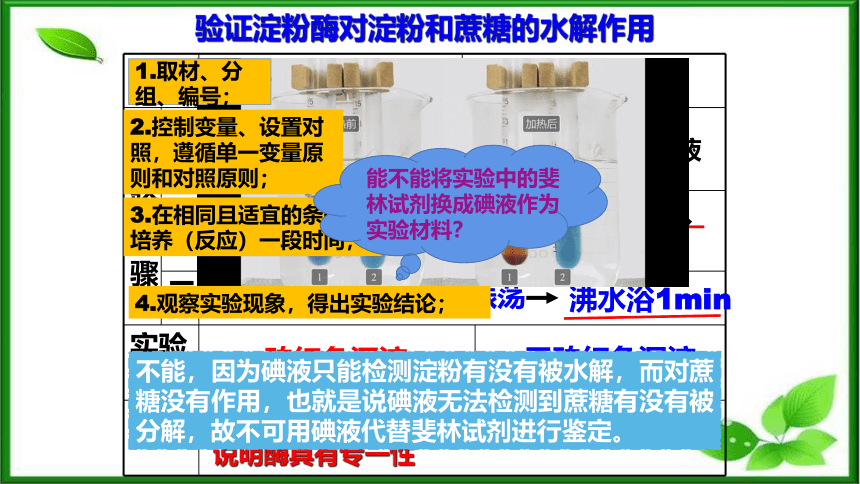
验证淀粉酶对淀粉和蔗糖的水解作用
说明酶具有专一性
1.取材、分组、编号;
2.控制变量、设置对照,遵循单一变量原则和对照原则;
3.在相同且适宜的条件下,培养(反应)一段时间;
4.观察实验现象,得出实验结论;
能不能将实验中的斐林试剂换成碘液作为实验材料?
不能,因为碘液只能检测淀粉有没有被水解,而对蔗糖没有作用,也就是说碘液无法检测到蔗糖有没有被分解,故不可用碘液代替斐林试剂进行鉴定。
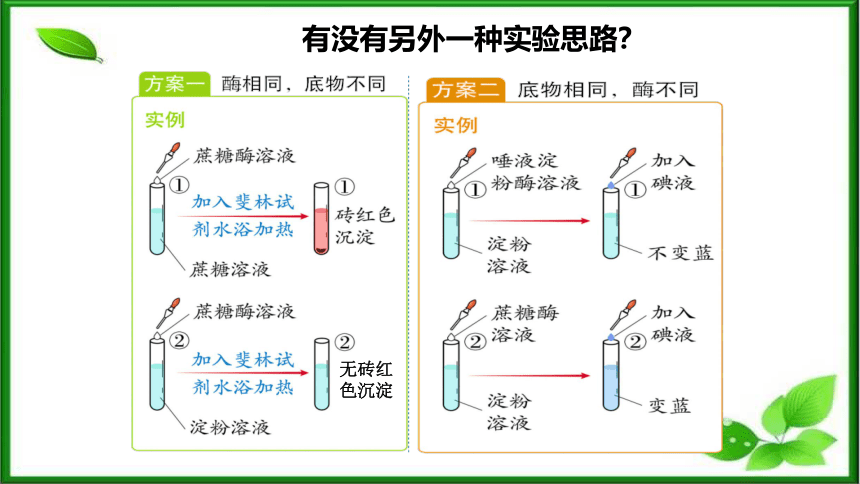
有没有另外一种实验思路?
无砖红
色沉淀
知识小结:
酶具有专一性
含义:
每一种酶只能催化一种或者一类化学反应。
如淀粉酶催化淀粉的水解,二肽酶能催化任意两种氨基酸组成的二肽水解
意义:
保证了细胞代谢能够有条不紊地进行
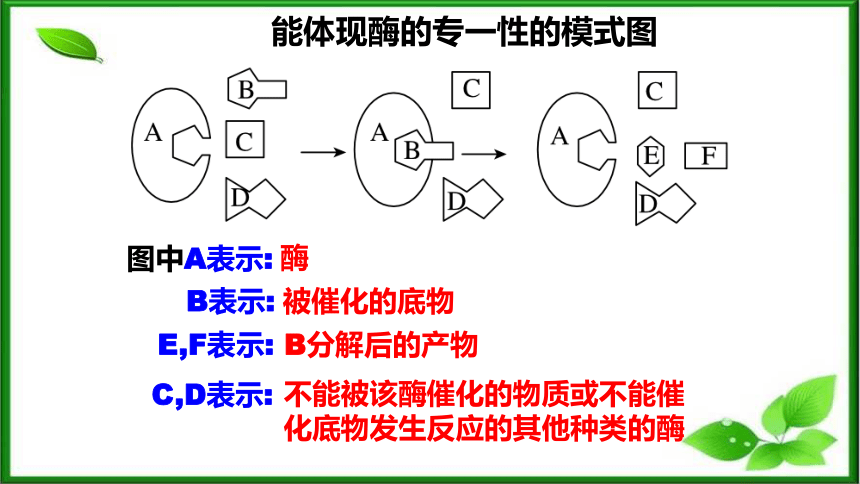
能体现酶的专一性的模式图
酶
被催化的底物
B分解后的产物
不能被该酶催化的物质或不能催化底物发生反应的其他种类的酶
图中A表示:
B表示:
E,F表示:
C,D表示:
②而加入酶A的反应速率随反应物浓度的增大明显加快,说明酶具有专一性
①加入酶B的反应速率和无酶条件下的反应速率相同,说明酶B对此反应无催化作用。
能体现酶的专一性的曲线图
底物
酶
分解反应
产物
酶具有专一性的理论解释:
锁钥学说
酶—底物复合物
在化学反应前后酶的数量和性质不变
在化学反应中酶能重复利用,不会被分解,但酶也会发生自我更新。
知识拓展:
当底物与酶结合时,酶分子上的某些基团常常发生明显的变化。另外,酶常常能够催化同一个生化反应中正逆两个方向的反应。因此,“锁和钥匙学说”把酶的结构看成是固定不变的,这是不符合实际的。
于是,有的科学家又提出,酶并不是事先就以一种与底物互补的形状存在,而是在受到诱导之后才形成互补的形状。
诱导契合学说
当底物与酶结合时,酶分子上的某些基团常常发生明显的变化。另外,酶常常能够催化同一个生化反应中正逆两个方向的反应。因此,“锁和钥匙学说”把酶的结构看成是固定不变的,这是不符合实际的。于是,有的科学家又提出,酶并不是事先就以一种与底物互补的形状存在,而是在受到诱导之后才形成互补的形状。这种方式如同一只手伸进手套之后,才诱导手套的形状发生变化一样。底物一旦结合上去,就能诱导酶蛋白的构像发生相应的变化,从而使酶和底物契合而形成酶-底物络合物。酶分子活性中心的结构原来并非和底物的结构互相吻合,但酶的活性中心是柔软的而非刚性的。当底物与酶相遇时,可诱导酶活性中心的构象发生相应的变化,有关的各个基团达到正确的排列和定向,从而使酶和底物契合而结合成中间络合物,并引起底物发生反应。反应结束当产物从酶上脱落下来后,酶的活性中心又恢复了原来的构象。
酶分子活性中心的结构原来并非和底物的结构互相吻合,但酶的活性中心是柔软的而非刚性的。当底物与酶相遇时,可诱导酶活性中心的构象发生相应的变化,有关的各个基团达到正确的排列和定向,从而使酶和底物契合而结合成中间络合物,并引起底物发生反应。
反应结束当产物从酶上脱落下来后,酶的活性中心又恢复了原来的构象。
知识拓展:
酶具有专一性的理论解释:
诱导契合学说
【检测】图乙表示图甲的反应过程中有关物质浓度随时间变化的曲线,下列叙述正确的是( )
A.图甲中物质a可以是麦芽糖也可以是乳糖
B.图甲中物质b能降低该化学反应的活化能,其化学本质与无机催化剂相同
C.图乙中若曲线①②③表示不同温度下酶促反应速率,则曲线①温度>曲线②>曲线③
D.图乙中若曲线①②③表示不同酶浓度下酶促反应速率,则曲线①酶浓度>曲线②>曲线③
D
根据酶促反应的性质,可把酶分为六大类:
知识拓展:
氧化还原酶类
转移酶类
水解酶类
裂合酶类
异构酶类
连接酶类
是能催化氧化还原反应的酶,分为氧化酶和脱氢酶,反应时需要电子供体或受体。给出电子或脱氢使本身氧化的物质称为电子供体或氢供体,作为还原剂;接受电子或氢使本身被还原的物质称为电子受体或氢受体,作为氧化剂。生物体内众多的氧化还原酶在反应时需要辅酶NAD或NADP来传递电子,如过氧化氢酶、细胞色素氧化酶、琥珀酸脱氢酶
能够催化化合物某些基团的转移,即将一种分子上的某一基团转移到另一种分子上的酶类,如磷酸化酶,以无机酸磷酸作为磷酸基团供体,可添加磷酸基团到受体上,还包括转甲基酶、转氨酶
指催化底物发生水解反应的酶类,如淀粉酶、蛋白酶、磷酸酶等
是指催化从底物除去某个基团而形成双键的反应及其逆反应的酶类,如柠檬酸合成酶
指催化各种同分异构体之间相互转化的酶类,如磷酸丙糖异构酶
催化两分子底物合成为一份子化合物,同时还必须偶联有ATP的磷酸键断裂的酶类,以一种新的化学键结合一起的酶,如氨基酸-tRNA连接酶类
加酶洗衣粉是人们生活中所必需的,但如何使用加酶洗衣粉,尤其是水温多少才算合适?
PH是否影响酶的活性呢?酶起催化作用需要怎样的条件呢?
提出问题
作出假设
设计实验
进行实验,
观察并记录结果
分析结果,得出结论
表达与交流
进一步探究
提出问题
作出假设
设计实验
温度和PH是否影响酶的活性?
温度和PH会影响酶的活性
实验材料:
实验探究:
影响酶活性的条件
新配置的质量分数为2%的淀粉酶溶液,新鲜的质量分数为20%的肝脏眼膜液缓冲液。
质量分数为3%的可溶性淀粉溶液,体积分数为3%的过氧化氢溶液物质的量浓度为0.01摩尔每升的盐酸物质的量浓度为0.01摩尔每升的氢氧化钠溶液、热水、蒸馏水、冰块、碘液,斐林试剂。
选择淀粉酶还是过氧化氢酶做实验?为什么?
自变量是什么?如何控制?
因变量是什么?
鉴定试剂选择碘液还是斐林试剂?观察什么现象?
无关变量有哪些?如何控制?
对照组怎么设置?是否需要重复实验
设计思路一、探究温度对酶活性的影响
不同的温度条件,用冰块降温、水浴加热,用温度计随时测量。
选择淀粉酶,不选用过氧化氢酶,因为加热能促进过氧化氢分解
鉴定试剂选用碘液,不选用斐林试剂,因为斐林试剂需水浴加热,而本实验需严格控制温度,观察的现象是看是否变蓝
淀粉和淀粉酶的浓度和用量、溶液的PH和反应时间等,无关变量需保持一致(相同且适宜)
酶的活性
设置相互对照,都是实验组,不需要需要设置重复实验
酶活性是指酶催化一定化学反应的能力。
酶活力的大小可以用在一定条件下,它所催化的某一化学反应的转化速率来表示,即酶催化的转化速率越快,酶的活力就越高; 反之,速率越慢,酶的活力就越低。
酶转化速率可以用单位时间内单位体积中底物的减少量或产物的增加量来表示
试管 步骤 1 1′ 2 2′ 3 3′
淀粉溶液
淀粉酶溶液
不同温度下 处理5 min
滴加碘液
结果(现象)
探究温度对α淀粉酶活性的影响
0℃
100℃
变蓝
不变蓝
变蓝
将同一温度下的两种物质混合后,保温5分钟
2ml
/
2ml
/
2ml
/
/
1ml
/
1ml
/
1ml
60 ℃
1滴
1滴
1滴
60℃下酶的活性最高,酶的催化作用需在适宜的温度下进行,温度过高或过低都会影响酶的活性
1、本实验能否先将淀粉溶液和淀粉酶混合,再放相应的温度中保温处理?
不能,否则在调节温度的过程中,酶将会催化淀粉分解,导致实验失败。应先将反应物和酶在各自所需的温度下保温一段时间,再混合。
思考与讨论:
2、哪支试管中酶的活性最高?你能得出什么结论?
3、尝试应用酶的化学本质的知识,解释自己的结论
绝大多数酶是蛋白质,每一种蛋白质都有与它所承担功能相适应的独特结构,如果空间结构改变,就可能会影响功能。因此,凡是能破坏酶特定空间结构的因素,如高温、过酸、过碱、加酒精及重金属盐等都会使酶永久失活。
4、如何进一步探究淀粉酶的最适温度?
缩小温度范围,设置一系列温度梯度,重复进行上述实验。
0
最适温度
υ/mmol. s-1
酶活性受温度影响示意图
酶促反应速率(酶活性)与温度的关系
A
C
B
●
●
●
①AB段,随着温度的升高,酶的活性逐渐增强;BC段,随着温度的继续升高,酶的活性逐渐下降,B点酶的活性最高时的温度称为该酶的最适温度;
②温度过高会使酶的空间结构遭到破坏,使酶永久失活,低温只是酶活性降低
每种酶都有自己的最适温度 动物:35--40℃ 植物: 40--50℃ 细菌、真菌 :差别较大
温度
知识小结:
③酶制剂适于在低温(0 ~4℃)下保存。
选择淀粉酶还是或氧化氢酶做实验?为什么?
自变量是什么?如何控制?
因变量是什么?怎样鉴定?
无关变量有哪些?如何控制?
对照组怎么设置?
设计思路二、探究PH对酶活性的影响
酶的活性,可用过氧化氢的分解速度来代表
设置相互对照,都是实验组
选择过氧化氢酶,不选用淀粉酶,因为淀粉在强酸或强碱的条件下会水解
不同的pH条件,可加入强酸或强碱,用pH试纸进行测量
气泡产生的多少或卫生香复然情况
肝脏研磨液的浓度和量,过氧化氢的浓度和量,温度等,保持相同且适宜
试管 步骤 1 2 3
过氧化氢溶液
不同PH下 处理5 min
过氧化氢酶溶液
结果(现象)
课题:探究PH对过氧化氢酶活性的影响
观察气泡的产生情况
少量气泡
几乎无气泡
2ml
1mlHCl
1mlH2O
1mlNaOH
大量气泡
2ml
2ml
1ml
1ml
1ml
思考与讨论:
1、本实验能否在过氧化氢溶液中先加过氧化氢酶溶液,再放相应的PH中处理?
不能,否则在调节PH的过程中,酶会将过氧化氢分解,导致实验失败。应先将反应物和酶在各自所需的PH下保存一段时间,再混合。
酶的催化作用需在适宜的PH下进行,过酸或过碱都会影响酶的活性
2、哪支试管中酶的活性最高?你能得出什么结论?
酶促反应速率(酶活性)与PH的关系
υ/mmol. s-1
最适PH
0
PH
酶活性受pH影响示意图
A
C
B
●
●
●
①AB段,随着pH的升高,酶的活性逐渐增强;BC段,随着pH的继续升高,酶的活性逐渐下降;B点酶的活性最高时的PH成为该酶的最适pH
②过酸、过碱会使酶的空间结构遭到破坏,使酶永久失活
每种酶都有自己的最适pH值,动物:6.5--8.0 (但胃蛋白酶为1.5); 植物: 4.5--6.5
知识小结:
(1)温度和pH对酶促反应的影响
酶促反应:由酶催化的化学反应,生物体内化学反应绝大多数属于
酶促反应。
二、 影响酶促反应的因素曲线分析
从图丙可以看出:
从图丁可以看出:
丁
反应溶液pH的变化不影响酶作用的最适温度。
温度变化不影响酶作用的最适PH
(2)底物浓度和酶浓度对酶促反应的影响
①甲图: 在其他条件适宜、酶量一定的情况下,酶促反应速率随底物浓度增加而加快,但当底物达到一定浓度后,受酶数量限制,酶促反应速率不再增加。
酶的数量有限
P点之后不变的原因:
P
●
②乙图:在底物充足、其他条件适宜的情况下,酶促反应速率与酶浓度成正比
(3)激活剂和抑制剂对酶促反应的影响
酶激活剂是指一些物质可以改变一个无活性酶前体(酶原),使之成为有活性的酶,或加快某种酶反应的速率产生酶激活作用。多种离子是酶的激活剂。
由图实验结果可知Cl-可提高该酶的催化效率,而Cu2+使该酶的催化效率降低,据此可知Cl-可作为该酶的激活剂
(3)激活剂和抑制剂对酶促反应的影响
竞争性抑制剂是与底物竞争酶的共同活性部位,竞争力的大小会受到浓度的影响。
非竞争性抑制剂不与底物竞争酶的共同活性部位,抑制剂和酶结合成功会改变酶的构象,使酶不与底物结合
右图曲线甲代表正常酶的作用,乙代表酶中添加了竞争性抑制剂的效果,丙代表酶中添加了非竞争性抑制剂的效果。
三、酶的应用
果胶酶
加酶洗衣粉
含酶牙膏
多酶片
课堂小结:
一、酶的特性
1、酶具有高效性
2、酶具有专一性:
每一种酶只能催化
一种或者一类化学反应
3、酶的作用条件温和
酶的活性最高时的温度称为该酶的 。
最适温度
酶的活性最高时的PH称为该酶的 。
最适PH
二、影响酶促反应的因素
1、温度和pH对酶促反应的影响
2、底物浓度和酶浓度对酶促反应的影响
3、激活剂和抑制剂对酶促反应的影响
在底物足够,其他条件适宜的情况下,酶促反应的速率与酶浓度成
正比
一定范围内,底物浓度增大反应速度 ,当底物浓度增大到一定限度时,反应速率达到 ,之后不再增大。
加快
最大值
【变式】如图甲是过氧化氢酶活性受pH影响的示意图,图乙表示在最适温度下,pH=b时,H2O2在过氧化氢酶的作用下分解产生O2的量随时间的变化情况。若该酶促反应过程中某一个条件发生变化,下列说法正确的是( )
A. pH=a时,E点下移,D点左移
B. pH=c时,E点为0
C. 温度降低时,E点不变,D点右移
D. H2O2的量增加时,E点下移,D点左移
E点表示O2生成量,只与反应物浓度有关,与PH无关,E点不动,AB错误。 D点右移
H2O2的量增加时,E点上移,D点右移
C
A.减小pH,重复该
实验,A、B点位置
不会改变
B.适当降温,重复
该实验,图示反应
速率可用曲线a表示
C.B点后增加酶量,图示反应速率可用曲线c表示
D.酶量是限制曲线AB段反应速率的主要因素
【检测】下图曲线b表示在其他条件充分适宜时,反应物浓度与酶促反应速率的关系。若改变某一条件,据图分析最准确的是( )
C
适当降温,酶的活性降低,酶促反应速率下降,但酶的数量不会减少, 故达到酶促反应饱和点的反应物浓度不变,依然是乙点,B项错误;
例、某工厂生产了一种加酶洗衣粉,其包装袋上印有如下说明。
成分:含碱性蛋白酶等。
用法:洗涤前先将衣服浸于洗衣粉水内数小时,使用温水效果最佳。
注意:切勿用于丝质及羊毛衣料。用后彻底清洗双手。
请回答下列问题:
(1)质检局针对该洗衣粉设计了如下装置进行实验如图所示。该实验的目的是_______。(2)一学生为探索该洗衣粉中酶催化作用的最适温度,参考上述(1)的实验材料及方法进行了如下实验,并把结果用曲线图A,B表示。
检查该洗衣粉是否含蛋白酶
①由图可知,使用该加酶洗衣粉的最适温度约为_________________。②在0 ℃和75 ℃时,酶的催化效率基本都降为零,但温度再度回到45 ℃,后者的催化作用已不能恢复,这是因为________________________________。③该学生在实验过程中可通过观察____________________________来判断酶的催化效率。(3)大力推广使用加酶洗衣粉代替含磷洗衣粉,有利于生态环境保护,这是因为____________ 。(至少答两点)
45 ℃
在75 ℃时,酶的空间结构已发生不可逆改变(酶已变性),无法恢复。
胶片上的蛋白膜消失所用时间的长短
酶本身无毒,含量少,又能被微生物分解,不会引起富营养化,可减少对环境的污染
【拓展应用】
1.下图表示的是某类酶作用的模型。尝试用文字描述这个模型。这个模型能解释酶的什么特性?
这个模型中 A 代表某类酶,B 代表底物,C 和 D 代表产物。
这个模型的含义是:酶 A与底物 B 专一性结合,催化反应的发生,产生了产物 C 和 D。
这个模型可以类比解释酶的专一性。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(1)请解释在A、B、C三点时该化学反应的状况。
A 点:在一定的范围内,随
着反应底物浓度的增加,
反应速率加快。
B 点:反应速率在此时达到最高 。
C 点:反应速率不再随反应底物浓度的增加而升高,维持在相对稳定的水平。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(2)如果从A点开始温度升高10℃,曲线会发生什么变化 为什么 请画出变化后的曲线。
如果 A 点时温度升高 10℃,曲线上升的幅度变小。
因为图中原曲线表示在最适温度下催化速率随底物浓度的变化。温度高于或低于最适温度,反应速率都会变慢。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(3)如果在B点时向反应混合物中加入少量同样的酶,曲线会发生什么变化 为什么 请画出相应的曲线。
该曲线表明,B 点的反应底物的浓度足够大,是酶的数量限制了反应速率的提高,这时加入少量的酶,会使反应速率加快。
第1节 降低化学反应活化能的酶(第2课时)
第5章 细胞的能量供应和利用
(一)酶具有高效性
一. 酶的特性
3
4
4
3
少量肝脏
研磨液
比较过氧化氢酶和Fe3+的催化效率
酶是活细胞产生的具有催化作用的有机物,一般情况下,酶的催化效率一般是无机催化剂的107 ~1013倍。
保证了细胞内化学反应的顺利进行,也保证了细胞内能量供应的稳定。
意义:
例、下图表示酶高效性的曲线
由曲线可知:___________________的催化效率更高;
酶只能缩短达到________________所需的时间,不改变化学反应的平衡点。因此,酶______(“能”或“不能”)改变最终生成物的量。
酶比无机催化剂
化学平衡
不能
酶只能缩短达到平衡的时间,不能改变平衡点
某同学通过实验比较了几种洗衣粉的去渍效果(“+”越多表示去渍效果越好),实验结果见下表。
加酶洗衣粉A 加酶洗衣粉B 无酶洗衣粉(对照)
血渍 +++ + +
油渍 + +++ +
加酶洗衣粉A对血渍去污效果好,加酶洗衣粉B对油渍去污效果好,每一种酶是不是只能对某一种物质起作用?
一、酶的特性
淀粉酶对淀粉和蔗糖的水解作用
实验原理
方法步骤
结果与结论
实验设计
实验探究:
1、实验器材:
质量分数为3%的淀粉溶液、质量分数为2%的新配置的淀粉酶溶液、质量分数为3%的蔗糖溶液、斐林试剂、热水
1. 淀粉和蔗糖都是非还原糖
2. 淀粉在相关酶的催化作用下能水解为麦芽糖
3. 蔗糖在相关酶的催化作用下能水解为葡萄糖和果糖
4. 麦芽糖、葡萄糖、果糖均属还原糖
5. 还原糖能够与斐林试剂发生反应,生成砖红色的沉淀
自变量是什么?
因变量是什么?怎样观察?
无关变量有哪些?
对照组是哪一组?
实验组是哪一组?
等量的淀粉溶液和蔗糖溶液
2、设计思路:
淀粉酶是否只能催化特定的化学反应
通过观察是否出现砖红色沉淀,就可以看出
反应物的浓度、所加物质的体积、反应时间
淀粉溶液和淀粉酶
蔗糖溶液和淀粉酶
各加入淀粉酶2ml,振荡,试管下半部浸入60℃左右的热水中,保温5min
加入2mL淀粉溶液
1号试管 2号试管
实验步骤 一
二
三
实验现象
结论
加入2mL蔗糖溶液
加入2ml斐林试剂
振荡
沸水浴1min
无砖红色沉淀
砖红色沉淀
淀粉酶只能催化淀粉水解,不能催化蔗糖水解
验证淀粉酶对淀粉和蔗糖的水解作用
说明酶具有专一性
1.取材、分组、编号;
2.控制变量、设置对照,遵循单一变量原则和对照原则;
3.在相同且适宜的条件下,培养(反应)一段时间;
4.观察实验现象,得出实验结论;
能不能将实验中的斐林试剂换成碘液作为实验材料?
不能,因为碘液只能检测淀粉有没有被水解,而对蔗糖没有作用,也就是说碘液无法检测到蔗糖有没有被分解,故不可用碘液代替斐林试剂进行鉴定。
有没有另外一种实验思路?
无砖红
色沉淀
知识小结:
酶具有专一性
含义:
每一种酶只能催化一种或者一类化学反应。
如淀粉酶催化淀粉的水解,二肽酶能催化任意两种氨基酸组成的二肽水解
意义:
保证了细胞代谢能够有条不紊地进行
能体现酶的专一性的模式图
酶
被催化的底物
B分解后的产物
不能被该酶催化的物质或不能催化底物发生反应的其他种类的酶
图中A表示:
B表示:
E,F表示:
C,D表示:
②而加入酶A的反应速率随反应物浓度的增大明显加快,说明酶具有专一性
①加入酶B的反应速率和无酶条件下的反应速率相同,说明酶B对此反应无催化作用。
能体现酶的专一性的曲线图
底物
酶
分解反应
产物
酶具有专一性的理论解释:
锁钥学说
酶—底物复合物
在化学反应前后酶的数量和性质不变
在化学反应中酶能重复利用,不会被分解,但酶也会发生自我更新。
知识拓展:
当底物与酶结合时,酶分子上的某些基团常常发生明显的变化。另外,酶常常能够催化同一个生化反应中正逆两个方向的反应。因此,“锁和钥匙学说”把酶的结构看成是固定不变的,这是不符合实际的。
于是,有的科学家又提出,酶并不是事先就以一种与底物互补的形状存在,而是在受到诱导之后才形成互补的形状。
诱导契合学说
当底物与酶结合时,酶分子上的某些基团常常发生明显的变化。另外,酶常常能够催化同一个生化反应中正逆两个方向的反应。因此,“锁和钥匙学说”把酶的结构看成是固定不变的,这是不符合实际的。于是,有的科学家又提出,酶并不是事先就以一种与底物互补的形状存在,而是在受到诱导之后才形成互补的形状。这种方式如同一只手伸进手套之后,才诱导手套的形状发生变化一样。底物一旦结合上去,就能诱导酶蛋白的构像发生相应的变化,从而使酶和底物契合而形成酶-底物络合物。酶分子活性中心的结构原来并非和底物的结构互相吻合,但酶的活性中心是柔软的而非刚性的。当底物与酶相遇时,可诱导酶活性中心的构象发生相应的变化,有关的各个基团达到正确的排列和定向,从而使酶和底物契合而结合成中间络合物,并引起底物发生反应。反应结束当产物从酶上脱落下来后,酶的活性中心又恢复了原来的构象。
酶分子活性中心的结构原来并非和底物的结构互相吻合,但酶的活性中心是柔软的而非刚性的。当底物与酶相遇时,可诱导酶活性中心的构象发生相应的变化,有关的各个基团达到正确的排列和定向,从而使酶和底物契合而结合成中间络合物,并引起底物发生反应。
反应结束当产物从酶上脱落下来后,酶的活性中心又恢复了原来的构象。
知识拓展:
酶具有专一性的理论解释:
诱导契合学说
【检测】图乙表示图甲的反应过程中有关物质浓度随时间变化的曲线,下列叙述正确的是( )
A.图甲中物质a可以是麦芽糖也可以是乳糖
B.图甲中物质b能降低该化学反应的活化能,其化学本质与无机催化剂相同
C.图乙中若曲线①②③表示不同温度下酶促反应速率,则曲线①温度>曲线②>曲线③
D.图乙中若曲线①②③表示不同酶浓度下酶促反应速率,则曲线①酶浓度>曲线②>曲线③
D
根据酶促反应的性质,可把酶分为六大类:
知识拓展:
氧化还原酶类
转移酶类
水解酶类
裂合酶类
异构酶类
连接酶类
是能催化氧化还原反应的酶,分为氧化酶和脱氢酶,反应时需要电子供体或受体。给出电子或脱氢使本身氧化的物质称为电子供体或氢供体,作为还原剂;接受电子或氢使本身被还原的物质称为电子受体或氢受体,作为氧化剂。生物体内众多的氧化还原酶在反应时需要辅酶NAD或NADP来传递电子,如过氧化氢酶、细胞色素氧化酶、琥珀酸脱氢酶
能够催化化合物某些基团的转移,即将一种分子上的某一基团转移到另一种分子上的酶类,如磷酸化酶,以无机酸磷酸作为磷酸基团供体,可添加磷酸基团到受体上,还包括转甲基酶、转氨酶
指催化底物发生水解反应的酶类,如淀粉酶、蛋白酶、磷酸酶等
是指催化从底物除去某个基团而形成双键的反应及其逆反应的酶类,如柠檬酸合成酶
指催化各种同分异构体之间相互转化的酶类,如磷酸丙糖异构酶
催化两分子底物合成为一份子化合物,同时还必须偶联有ATP的磷酸键断裂的酶类,以一种新的化学键结合一起的酶,如氨基酸-tRNA连接酶类
加酶洗衣粉是人们生活中所必需的,但如何使用加酶洗衣粉,尤其是水温多少才算合适?
PH是否影响酶的活性呢?酶起催化作用需要怎样的条件呢?
提出问题
作出假设
设计实验
进行实验,
观察并记录结果
分析结果,得出结论
表达与交流
进一步探究
提出问题
作出假设
设计实验
温度和PH是否影响酶的活性?
温度和PH会影响酶的活性
实验材料:
实验探究:
影响酶活性的条件
新配置的质量分数为2%的淀粉酶溶液,新鲜的质量分数为20%的肝脏眼膜液缓冲液。
质量分数为3%的可溶性淀粉溶液,体积分数为3%的过氧化氢溶液物质的量浓度为0.01摩尔每升的盐酸物质的量浓度为0.01摩尔每升的氢氧化钠溶液、热水、蒸馏水、冰块、碘液,斐林试剂。
选择淀粉酶还是过氧化氢酶做实验?为什么?
自变量是什么?如何控制?
因变量是什么?
鉴定试剂选择碘液还是斐林试剂?观察什么现象?
无关变量有哪些?如何控制?
对照组怎么设置?是否需要重复实验
设计思路一、探究温度对酶活性的影响
不同的温度条件,用冰块降温、水浴加热,用温度计随时测量。
选择淀粉酶,不选用过氧化氢酶,因为加热能促进过氧化氢分解
鉴定试剂选用碘液,不选用斐林试剂,因为斐林试剂需水浴加热,而本实验需严格控制温度,观察的现象是看是否变蓝
淀粉和淀粉酶的浓度和用量、溶液的PH和反应时间等,无关变量需保持一致(相同且适宜)
酶的活性
设置相互对照,都是实验组,不需要需要设置重复实验
酶活性是指酶催化一定化学反应的能力。
酶活力的大小可以用在一定条件下,它所催化的某一化学反应的转化速率来表示,即酶催化的转化速率越快,酶的活力就越高; 反之,速率越慢,酶的活力就越低。
酶转化速率可以用单位时间内单位体积中底物的减少量或产物的增加量来表示
试管 步骤 1 1′ 2 2′ 3 3′
淀粉溶液
淀粉酶溶液
不同温度下 处理5 min
滴加碘液
结果(现象)
探究温度对α淀粉酶活性的影响
0℃
100℃
变蓝
不变蓝
变蓝
将同一温度下的两种物质混合后,保温5分钟
2ml
/
2ml
/
2ml
/
/
1ml
/
1ml
/
1ml
60 ℃
1滴
1滴
1滴
60℃下酶的活性最高,酶的催化作用需在适宜的温度下进行,温度过高或过低都会影响酶的活性
1、本实验能否先将淀粉溶液和淀粉酶混合,再放相应的温度中保温处理?
不能,否则在调节温度的过程中,酶将会催化淀粉分解,导致实验失败。应先将反应物和酶在各自所需的温度下保温一段时间,再混合。
思考与讨论:
2、哪支试管中酶的活性最高?你能得出什么结论?
3、尝试应用酶的化学本质的知识,解释自己的结论
绝大多数酶是蛋白质,每一种蛋白质都有与它所承担功能相适应的独特结构,如果空间结构改变,就可能会影响功能。因此,凡是能破坏酶特定空间结构的因素,如高温、过酸、过碱、加酒精及重金属盐等都会使酶永久失活。
4、如何进一步探究淀粉酶的最适温度?
缩小温度范围,设置一系列温度梯度,重复进行上述实验。
0
最适温度
υ/mmol. s-1
酶活性受温度影响示意图
酶促反应速率(酶活性)与温度的关系
A
C
B
●
●
●
①AB段,随着温度的升高,酶的活性逐渐增强;BC段,随着温度的继续升高,酶的活性逐渐下降,B点酶的活性最高时的温度称为该酶的最适温度;
②温度过高会使酶的空间结构遭到破坏,使酶永久失活,低温只是酶活性降低
每种酶都有自己的最适温度 动物:35--40℃ 植物: 40--50℃ 细菌、真菌 :差别较大
温度
知识小结:
③酶制剂适于在低温(0 ~4℃)下保存。
选择淀粉酶还是或氧化氢酶做实验?为什么?
自变量是什么?如何控制?
因变量是什么?怎样鉴定?
无关变量有哪些?如何控制?
对照组怎么设置?
设计思路二、探究PH对酶活性的影响
酶的活性,可用过氧化氢的分解速度来代表
设置相互对照,都是实验组
选择过氧化氢酶,不选用淀粉酶,因为淀粉在强酸或强碱的条件下会水解
不同的pH条件,可加入强酸或强碱,用pH试纸进行测量
气泡产生的多少或卫生香复然情况
肝脏研磨液的浓度和量,过氧化氢的浓度和量,温度等,保持相同且适宜
试管 步骤 1 2 3
过氧化氢溶液
不同PH下 处理5 min
过氧化氢酶溶液
结果(现象)
课题:探究PH对过氧化氢酶活性的影响
观察气泡的产生情况
少量气泡
几乎无气泡
2ml
1mlHCl
1mlH2O
1mlNaOH
大量气泡
2ml
2ml
1ml
1ml
1ml
思考与讨论:
1、本实验能否在过氧化氢溶液中先加过氧化氢酶溶液,再放相应的PH中处理?
不能,否则在调节PH的过程中,酶会将过氧化氢分解,导致实验失败。应先将反应物和酶在各自所需的PH下保存一段时间,再混合。
酶的催化作用需在适宜的PH下进行,过酸或过碱都会影响酶的活性
2、哪支试管中酶的活性最高?你能得出什么结论?
酶促反应速率(酶活性)与PH的关系
υ/mmol. s-1
最适PH
0
PH
酶活性受pH影响示意图
A
C
B
●
●
●
①AB段,随着pH的升高,酶的活性逐渐增强;BC段,随着pH的继续升高,酶的活性逐渐下降;B点酶的活性最高时的PH成为该酶的最适pH
②过酸、过碱会使酶的空间结构遭到破坏,使酶永久失活
每种酶都有自己的最适pH值,动物:6.5--8.0 (但胃蛋白酶为1.5); 植物: 4.5--6.5
知识小结:
(1)温度和pH对酶促反应的影响
酶促反应:由酶催化的化学反应,生物体内化学反应绝大多数属于
酶促反应。
二、 影响酶促反应的因素曲线分析
从图丙可以看出:
从图丁可以看出:
丁
反应溶液pH的变化不影响酶作用的最适温度。
温度变化不影响酶作用的最适PH
(2)底物浓度和酶浓度对酶促反应的影响
①甲图: 在其他条件适宜、酶量一定的情况下,酶促反应速率随底物浓度增加而加快,但当底物达到一定浓度后,受酶数量限制,酶促反应速率不再增加。
酶的数量有限
P点之后不变的原因:
P
●
②乙图:在底物充足、其他条件适宜的情况下,酶促反应速率与酶浓度成正比
(3)激活剂和抑制剂对酶促反应的影响
酶激活剂是指一些物质可以改变一个无活性酶前体(酶原),使之成为有活性的酶,或加快某种酶反应的速率产生酶激活作用。多种离子是酶的激活剂。
由图实验结果可知Cl-可提高该酶的催化效率,而Cu2+使该酶的催化效率降低,据此可知Cl-可作为该酶的激活剂
(3)激活剂和抑制剂对酶促反应的影响
竞争性抑制剂是与底物竞争酶的共同活性部位,竞争力的大小会受到浓度的影响。
非竞争性抑制剂不与底物竞争酶的共同活性部位,抑制剂和酶结合成功会改变酶的构象,使酶不与底物结合
右图曲线甲代表正常酶的作用,乙代表酶中添加了竞争性抑制剂的效果,丙代表酶中添加了非竞争性抑制剂的效果。
三、酶的应用
果胶酶
加酶洗衣粉
含酶牙膏
多酶片
课堂小结:
一、酶的特性
1、酶具有高效性
2、酶具有专一性:
每一种酶只能催化
一种或者一类化学反应
3、酶的作用条件温和
酶的活性最高时的温度称为该酶的 。
最适温度
酶的活性最高时的PH称为该酶的 。
最适PH
二、影响酶促反应的因素
1、温度和pH对酶促反应的影响
2、底物浓度和酶浓度对酶促反应的影响
3、激活剂和抑制剂对酶促反应的影响
在底物足够,其他条件适宜的情况下,酶促反应的速率与酶浓度成
正比
一定范围内,底物浓度增大反应速度 ,当底物浓度增大到一定限度时,反应速率达到 ,之后不再增大。
加快
最大值
【变式】如图甲是过氧化氢酶活性受pH影响的示意图,图乙表示在最适温度下,pH=b时,H2O2在过氧化氢酶的作用下分解产生O2的量随时间的变化情况。若该酶促反应过程中某一个条件发生变化,下列说法正确的是( )
A. pH=a时,E点下移,D点左移
B. pH=c时,E点为0
C. 温度降低时,E点不变,D点右移
D. H2O2的量增加时,E点下移,D点左移
E点表示O2生成量,只与反应物浓度有关,与PH无关,E点不动,AB错误。 D点右移
H2O2的量增加时,E点上移,D点右移
C
A.减小pH,重复该
实验,A、B点位置
不会改变
B.适当降温,重复
该实验,图示反应
速率可用曲线a表示
C.B点后增加酶量,图示反应速率可用曲线c表示
D.酶量是限制曲线AB段反应速率的主要因素
【检测】下图曲线b表示在其他条件充分适宜时,反应物浓度与酶促反应速率的关系。若改变某一条件,据图分析最准确的是( )
C
适当降温,酶的活性降低,酶促反应速率下降,但酶的数量不会减少, 故达到酶促反应饱和点的反应物浓度不变,依然是乙点,B项错误;
例、某工厂生产了一种加酶洗衣粉,其包装袋上印有如下说明。
成分:含碱性蛋白酶等。
用法:洗涤前先将衣服浸于洗衣粉水内数小时,使用温水效果最佳。
注意:切勿用于丝质及羊毛衣料。用后彻底清洗双手。
请回答下列问题:
(1)质检局针对该洗衣粉设计了如下装置进行实验如图所示。该实验的目的是_______。(2)一学生为探索该洗衣粉中酶催化作用的最适温度,参考上述(1)的实验材料及方法进行了如下实验,并把结果用曲线图A,B表示。
检查该洗衣粉是否含蛋白酶
①由图可知,使用该加酶洗衣粉的最适温度约为_________________。②在0 ℃和75 ℃时,酶的催化效率基本都降为零,但温度再度回到45 ℃,后者的催化作用已不能恢复,这是因为________________________________。③该学生在实验过程中可通过观察____________________________来判断酶的催化效率。(3)大力推广使用加酶洗衣粉代替含磷洗衣粉,有利于生态环境保护,这是因为____________ 。(至少答两点)
45 ℃
在75 ℃时,酶的空间结构已发生不可逆改变(酶已变性),无法恢复。
胶片上的蛋白膜消失所用时间的长短
酶本身无毒,含量少,又能被微生物分解,不会引起富营养化,可减少对环境的污染
【拓展应用】
1.下图表示的是某类酶作用的模型。尝试用文字描述这个模型。这个模型能解释酶的什么特性?
这个模型中 A 代表某类酶,B 代表底物,C 和 D 代表产物。
这个模型的含义是:酶 A与底物 B 专一性结合,催化反应的发生,产生了产物 C 和 D。
这个模型可以类比解释酶的专一性。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(1)请解释在A、B、C三点时该化学反应的状况。
A 点:在一定的范围内,随
着反应底物浓度的增加,
反应速率加快。
B 点:反应速率在此时达到最高 。
C 点:反应速率不再随反应底物浓度的增加而升高,维持在相对稳定的水平。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(2)如果从A点开始温度升高10℃,曲线会发生什么变化 为什么 请画出变化后的曲线。
如果 A 点时温度升高 10℃,曲线上升的幅度变小。
因为图中原曲线表示在最适温度下催化速率随底物浓度的变化。温度高于或低于最适温度,反应速率都会变慢。
2.下图表示最适温度下反应物浓度对酶所催化的化学反应速率的影响。
(3)如果在B点时向反应混合物中加入少量同样的酶,曲线会发生什么变化 为什么 请画出相应的曲线。
该曲线表明,B 点的反应底物的浓度足够大,是酶的数量限制了反应速率的提高,这时加入少量的酶,会使反应速率加快。
同课章节目录
- 第1章 走近细胞
- 第1节 细胞是生命活动的基本单位
- 第2节 细胞的多样性和统一性
- 第2章 组成细胞的分子
- 第1节 细胞中的元素和化合物
- 第2节 细胞中的无机物
- 第3节 细胞中的糖类和脂质
- 第4节 蛋白质是生命活动的主要承担者
- 第5节 核酸是遗传信息的携带者
- 第3章 细胞的基本结构
- 第1节 细胞膜的结构和功能
- 第2节 细胞器之间的分工合作
- 第3节 细胞核的结构和功能
- 第4章 细胞的物质输入和输出
- 第1节 被动运输
- 第2节 主动运输与胞吞、胞吐
- 第5章 细胞的能量供应和利用
- 第1节 降低化学反应活化能的酶
- 第2节 细胞的能量“货币”ATP
- 第3节 细胞呼吸的原理和应用
- 第4节 光合作用与能量转化
- 第6章 细胞的生命历程
- 第1节 细胞的增殖
- 第2节 细胞的分化
- 第3节 细胞的衰老和死亡
