江苏省2023年1月普通高中学业水平测试练透选择题(四)化学(含答案)
文档属性
| 名称 | 江苏省2023年1月普通高中学业水平测试练透选择题(四)化学(含答案) | 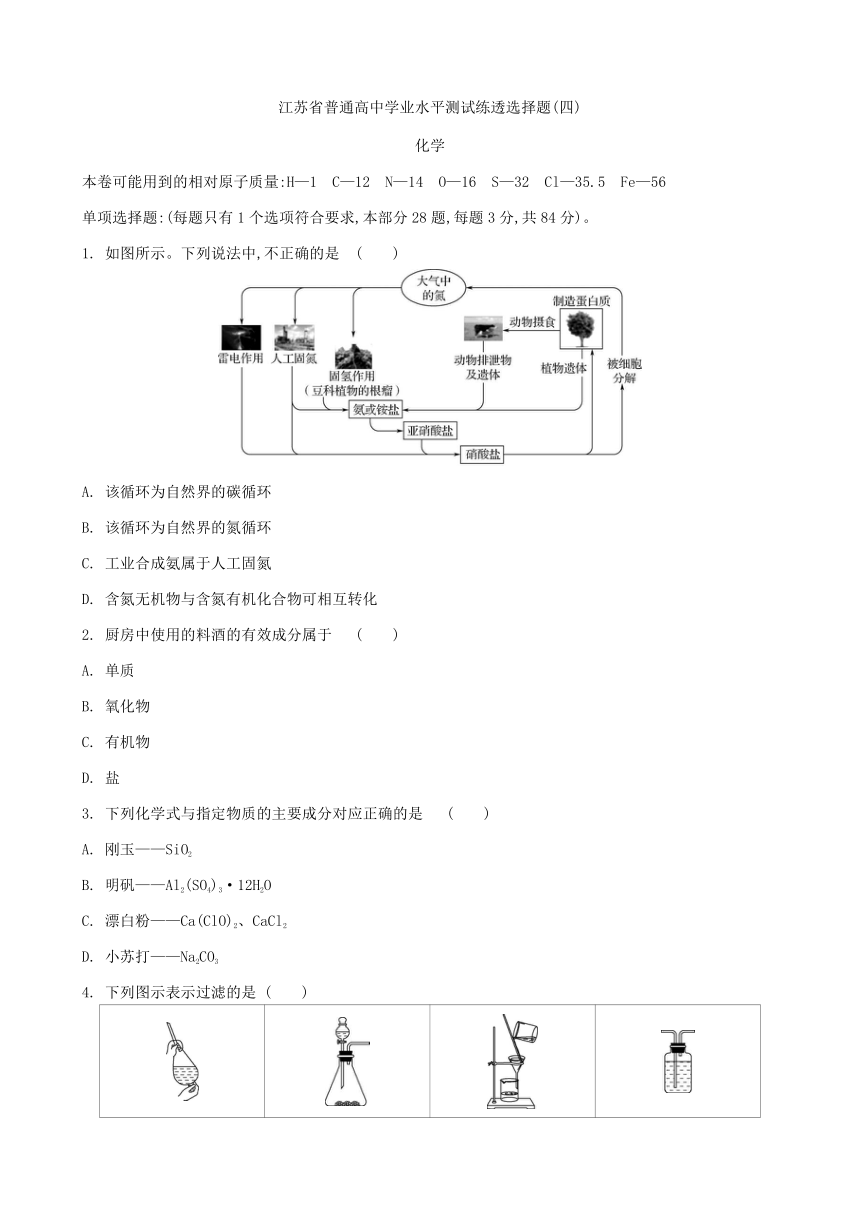 | |
| 格式 | doc | ||
| 文件大小 | 240.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-26 22:07:47 | ||
图片预览




文档简介
江苏省普通高中学业水平测试练透选择题(四)
化学
本卷可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Cl—35.5 Fe—56
单项选择题:(每题只有1个选项符合要求,本部分28题,每题3分,共84分)。
1. 如图所示。下列说法中,不正确的是 ( )
A. 该循环为自然界的碳循环
B. 该循环为自然界的氮循环
C. 工业合成氨属于人工固氮
D. 含氮无机物与含氮有机化合物可相互转化
2. 厨房中使用的料酒的有效成分属于 ( )
A. 单质
B. 氧化物
C. 有机物
D. 盐
3. 下列化学式与指定物质的主要成分对应正确的是 ( )
A. 刚玉——SiO2
B. 明矾——Al2(SO4)3·12H2O
C. 漂白粉——Ca(ClO)2、CaCl2
D. 小苏打——Na2CO3
4. 下列图示表示过滤的是 ( )
A B C D
5. 二氧化硫是造成硫酸型酸雨的主要原因,其摩尔质量为 ( )
A. 32 g
B. 64 g/mol
C. 64 g
D. 32 g/mol
6. 2H2SO3+ O22H2SO4的反应属于 ( )
A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应
7. 下列物质属于高分子的是 ( )
A. 葡萄糖
B. 棉花
C. 油脂
D. 氨基酸
8. 下列变化属于化学变化的是 ( )
A. 冰醋酸溶于水 B. 氨气液化
C. 碘升华 D. 加热NH4Cl固体产生白烟
9. 取某地工厂排出的废液,每千克废液中含有NaCl 5.85 g,CaCl2 11.1 g,KCl 7.45 g,其中物质的量浓度最大的离子是 ( )
A. Na+ B. K+ C. Ca2+ D. Cl-
10. 下列化学用语表示正确的是 ( )
A. 水的电子式:H
B. 乙烯的结构简式:CH2CH2
C. 钠原子的结构示意图:
D. Na2SO4的电离方程式:Na2SO4Na++S
11. CO+2NO24CO2+N2。下列有关该反应的说法正确的是 ( )
A. CO是氧化剂
B. CO2是氧化产物
C. NO2发生氧化反应
D. NO2失去电子
12. 在化学魔术中,一张白纸在用碘溶液喷洒后会呈现出蓝色字迹,其奥秘在于这张白纸曾经一种“隐秘墨水”书写过。这种“隐秘墨水”为 ( )
A. 食盐水 B. 白醋 C. 蔗糖溶液 D. 淀粉溶液
13. 分解水获得H2的能量变化如图所示,下列说法正确的是 ( )
A. 分解水属于吸热反应
B. 断开H-O键放出能量
C. 形成H-H键吸收能量
D. 反应物的总能量大于生成物的总能量
14. 下列方案不能达到实验目的的是 ( )
A. 用闻气味的方法鉴别CO2和CO
B. 用pH试纸鉴别NaCl溶液与HCl溶液
C. 用品红溶液鉴别SO2和CO2
D. 用激光笔照射的方法鉴别溶液和胶体
15. 在含有大量Ca2+、H+、N的溶液中,还可能大量共存的离子是 ( )
A. C B. OH- C. Na+ D. Fe2+
16. 下列离子方程式正确的是 ( )
A. 锌与稀硫酸反应:Zn+H+Zn2++H2↑
B. 铜粉与稀硝酸的反应:Cu+2H+Cu2++H2↑
C. 氢氧化镁与盐酸反应:H++OH-H2O
D. 硝酸银溶液与氯化钠溶液反应:Ag++Cl-AgCl↓
17. 下列物质互为同分异构体的是 ( )
A. 1H和2H
B. O2和O3
C. CH4和C2H6
D. CH3CH2OH和CH3OCH3
18. 下列关于乙烯的说法正确的是 ( )
A. 是天然气的主要成分
B. 能使溴的四氯化碳溶液褪色
C. 不能发生燃烧反应
D. 不能发生加聚反应
19. 下列转化能通过取代反应一步实现的是 ( )
A.
B.
C.
D.
20. 下列过程放出热量的是 ( )
A. 钠与水反应
B. 液氨汽化
C. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
D. 电解水
21. 已知2SO2+ O22SO3为可逆反应,下列有关说法正确的是 ( )
A. 增大O2的浓度能加快反应速率
B. 减小SO3的浓度能加快反应速率
C. 降低温度能加快反应速率
D. 添加催化剂对反应速率无影响
22. 某原电池结构如下图所示,下列有关该原电池的说法正确的是 ( )
A. 电池总反应为Mg+2H+Mg2++H2↑
B. 镁棒发生还原反应
C. 电子从铜棒经外电路流向镁棒
D. 铜棒为负极
请阅读下列材料,回答23~26题。
联合国将2019年定为“国际化学元素周期表年”,纪念门捷列夫的元素周期表发表150周年。他生前科学地预言了11种尚未发现的元素,例如,铝的下方有一个与铝类似的元素“类铝”,所以,镓曾被称为“类铝”。氮化镓(GaN)是第三代半导体材料,四氢铝钠(NaAlH4)是有机合成的重要还原剂。
23. 核素37Cl的中子数为 ( )
A. 37
B. 17
C. 20
D. 54
24. F和O都属于元素周期表第二周期元素,它们原子结构中相同的是 ( )
A. 质子数
B. 电子层数
C. 核外电子数
D. 最外层电子数
25. 判断F的非金属性比C的强,可依据的事实是 ( )
A. HF的热稳定性比CH4的强
B. 常温下氟气能与水反应,碳不与水反应
C. 常温下,氟气呈气态,碳呈固态
D. 氟气为黄绿色,木炭为黑色
26. 硼是第二周期ⅢA族元素,下列有关硼元素性质推测正确的是 ( )
A. 最高化合价为+5
B. 原子半径比铝的小
C. 单质与水剧烈反应
D. 最高价氧化物对应的水化物是强碱
27. 下列有关二氧化硫的说法中,正确的是 ( )
A. 检验SO2气体中是否混有CO2的方法是通入澄清石灰水中
B. SO2气体具有漂白性,能使品红溶液、紫色石蕊试液褪色
C. 在含BaCl2的氨水中通入少量SO2气体会有白色沉淀生成
D. 因为SO2气体具有还原性,所以在实验室不能用浓硫酸干燥SO2
28. 实验室用严重锈蚀的废铁屑为原料制备硫酸亚铁晶体(FeSO4·7H2O),流程如下。下列说法正确的是 ( )
A. 上述流程中涉及的反应均属于氧化还原反应
B. “酸溶”时试剂X可用稀硫酸或稀盐酸
C. “还原”时发生反应的离子方程式为Fe3++Fe2Fe2+
D. “结晶”采用的方式是蒸发浓缩、冷却结晶
江苏省普通高中学业水平测试
练透选择题(四)
1. A 解析:该循环为自然界的氮循环,A错误;B正确;工业合成氨是将N2与H2在一定条件下反应生成NH3,属于人工固氮,C正确;氮循环中铵盐和蛋白质可相互转化,铵盐属于无机物,蛋白质属于有机物,含氮无机物和含氮有机物可相互转化,D正确。
2. C
3. C 解析:刚玉的主要成分为Al2O3,A错误;明矾的主要成分为KAl(SO4)2·12H2O,B错误;漂白粉主要成分为Ca(ClO)2、CaCl2,C正确;小苏打主要成分为NaHCO3,D错误。
4. C 5. B 6 A 7. B 8. D
9. D 解析:废水中含有的三种成分均含有Cl-,Cl-物质的量浓度最大,D正确。
10. B 解析:水的电子式:H,A错误;钠原子的结构示意图:,C错误;Na2SO4的电离方程式:Na2SO42Na++ S,D错误。
11. B
12. D 解析:淀粉遇碘水显蓝色,D正确。
13. A 解析:由图可知,反应物总能量小于生成物总能量,则分解水属于吸热反应,A正确;断开H—O键吸收能量,B错误;形成H—H键放出能量,C错误;由图可知,反应物总能量小于生成物总能量,D错误。
14. A 解析:一氧化碳和二氧化碳都无味,一氧化碳还有毒,不能用闻气味的方法鉴别,A错误;氯化钠溶液显中性,pH=7;稀盐酸显酸性,pH<7,可以用pH试纸鉴别,B正确;SO2可使品红溶液褪色CO2不能使品红溶液褪色,C正确;丁达尔效应可鉴别溶液和胶体,D正确。
15. C 解析:C不能与Ca2+大量共存,A错误;OH-不能与H+大量共存,B错误;Fe2+不能与H+、N大量共存,D错误。
16. D 解析:A电荷总数不等,配平错误;铜与稀硝酸反应生成NO,B原理错误;氢氧化镁为难溶物质,不可以拆分,C错误。
17. D 18. B
19. D 解析:A、B、C为加成反应;D为苯的取代反应,D正确。
20. A 解析:金属与水或酸的反应是放热反应,A正确;其余的都要吸收热量。
21. A 解析:增大O2的浓度能加快反应速率,A正确;减小SO3的浓度、降低温度都使反应速率减慢,B、C错误;添加催化剂会改变反应速率,D错误。
22. A 解析:镁失去电子,生成镁离子,镁作负极,铜棒作正极,氢离子在铜棒上得到电子生成氢气,电子从镁棒流出经外电路流向铜棒,A正确。
23. C 解析:中子数=质量数-质子数=37-17=20,C正确。
24. B 解析:F和O的质子数和核外电子数分别是9、8,A、C错误;电子层数都是2,B正确;F和O的最外层电子数分别为7和6,D错误。
25. A 解析:比较非金属性可根据单质与氢气的化合的难易程度;气态氢化物的稳定性;最高价氧化物所对应水化物的酸性强弱进行比较,A正确。
26. B 解析:硼是第二周期ⅢA族元素,最高化合价是+3,A错误;同主族元素从上到下原子半径逐渐增大,硼的原子半径小于铝的原子半径,B正确;同主族元素的单质从上到下金属性逐渐增强,与水反应剧烈程度增大,最高价氧化物对应的水化物的碱性增强,C、D错误。
27. C 解析:两种气体均可使石灰水变浑浊,不能用澄清石灰水检验检验SO2气体中是否混有CO2,A错误;二氧化硫能使品红褪色,也能使紫色石蕊试液变红,B错误;含BaCl2的氨水中通入少量SO2气体,反应生成亚硫酸钡和氯化铵,观察到白色沉淀生成,C正确;二氧化硫与浓硫酸不反应,在实验室能用浓硫酸干燥SO2,D错误。
28. D 解析:氧化铁与硫酸的反应为非氧化还原反应,A错误;由最终制备晶体的酸根离子可知,“酸溶”时试剂X可用稀硫酸,不能选盐酸,否则易引进杂质,B错误;还原时发生的离子反应为2Fe3++Fe3Fe2+,C错误;由溶液得到含结晶水的晶体,可知“结晶”采用的方式是蒸发浓缩、冷却结晶,D正确。
化学
本卷可能用到的相对原子质量:H—1 C—12 N—14 O—16 S—32 Cl—35.5 Fe—56
单项选择题:(每题只有1个选项符合要求,本部分28题,每题3分,共84分)。
1. 如图所示。下列说法中,不正确的是 ( )
A. 该循环为自然界的碳循环
B. 该循环为自然界的氮循环
C. 工业合成氨属于人工固氮
D. 含氮无机物与含氮有机化合物可相互转化
2. 厨房中使用的料酒的有效成分属于 ( )
A. 单质
B. 氧化物
C. 有机物
D. 盐
3. 下列化学式与指定物质的主要成分对应正确的是 ( )
A. 刚玉——SiO2
B. 明矾——Al2(SO4)3·12H2O
C. 漂白粉——Ca(ClO)2、CaCl2
D. 小苏打——Na2CO3
4. 下列图示表示过滤的是 ( )
A B C D
5. 二氧化硫是造成硫酸型酸雨的主要原因,其摩尔质量为 ( )
A. 32 g
B. 64 g/mol
C. 64 g
D. 32 g/mol
6. 2H2SO3+ O22H2SO4的反应属于 ( )
A. 化合反应
B. 分解反应
C. 置换反应
D. 复分解反应
7. 下列物质属于高分子的是 ( )
A. 葡萄糖
B. 棉花
C. 油脂
D. 氨基酸
8. 下列变化属于化学变化的是 ( )
A. 冰醋酸溶于水 B. 氨气液化
C. 碘升华 D. 加热NH4Cl固体产生白烟
9. 取某地工厂排出的废液,每千克废液中含有NaCl 5.85 g,CaCl2 11.1 g,KCl 7.45 g,其中物质的量浓度最大的离子是 ( )
A. Na+ B. K+ C. Ca2+ D. Cl-
10. 下列化学用语表示正确的是 ( )
A. 水的电子式:H
B. 乙烯的结构简式:CH2CH2
C. 钠原子的结构示意图:
D. Na2SO4的电离方程式:Na2SO4Na++S
11. CO+2NO24CO2+N2。下列有关该反应的说法正确的是 ( )
A. CO是氧化剂
B. CO2是氧化产物
C. NO2发生氧化反应
D. NO2失去电子
12. 在化学魔术中,一张白纸在用碘溶液喷洒后会呈现出蓝色字迹,其奥秘在于这张白纸曾经一种“隐秘墨水”书写过。这种“隐秘墨水”为 ( )
A. 食盐水 B. 白醋 C. 蔗糖溶液 D. 淀粉溶液
13. 分解水获得H2的能量变化如图所示,下列说法正确的是 ( )
A. 分解水属于吸热反应
B. 断开H-O键放出能量
C. 形成H-H键吸收能量
D. 反应物的总能量大于生成物的总能量
14. 下列方案不能达到实验目的的是 ( )
A. 用闻气味的方法鉴别CO2和CO
B. 用pH试纸鉴别NaCl溶液与HCl溶液
C. 用品红溶液鉴别SO2和CO2
D. 用激光笔照射的方法鉴别溶液和胶体
15. 在含有大量Ca2+、H+、N的溶液中,还可能大量共存的离子是 ( )
A. C B. OH- C. Na+ D. Fe2+
16. 下列离子方程式正确的是 ( )
A. 锌与稀硫酸反应:Zn+H+Zn2++H2↑
B. 铜粉与稀硝酸的反应:Cu+2H+Cu2++H2↑
C. 氢氧化镁与盐酸反应:H++OH-H2O
D. 硝酸银溶液与氯化钠溶液反应:Ag++Cl-AgCl↓
17. 下列物质互为同分异构体的是 ( )
A. 1H和2H
B. O2和O3
C. CH4和C2H6
D. CH3CH2OH和CH3OCH3
18. 下列关于乙烯的说法正确的是 ( )
A. 是天然气的主要成分
B. 能使溴的四氯化碳溶液褪色
C. 不能发生燃烧反应
D. 不能发生加聚反应
19. 下列转化能通过取代反应一步实现的是 ( )
A.
B.
C.
D.
20. 下列过程放出热量的是 ( )
A. 钠与水反应
B. 液氨汽化
C. Ba(OH)2·8H2O晶体与NH4Cl晶体反应
D. 电解水
21. 已知2SO2+ O22SO3为可逆反应,下列有关说法正确的是 ( )
A. 增大O2的浓度能加快反应速率
B. 减小SO3的浓度能加快反应速率
C. 降低温度能加快反应速率
D. 添加催化剂对反应速率无影响
22. 某原电池结构如下图所示,下列有关该原电池的说法正确的是 ( )
A. 电池总反应为Mg+2H+Mg2++H2↑
B. 镁棒发生还原反应
C. 电子从铜棒经外电路流向镁棒
D. 铜棒为负极
请阅读下列材料,回答23~26题。
联合国将2019年定为“国际化学元素周期表年”,纪念门捷列夫的元素周期表发表150周年。他生前科学地预言了11种尚未发现的元素,例如,铝的下方有一个与铝类似的元素“类铝”,所以,镓曾被称为“类铝”。氮化镓(GaN)是第三代半导体材料,四氢铝钠(NaAlH4)是有机合成的重要还原剂。
23. 核素37Cl的中子数为 ( )
A. 37
B. 17
C. 20
D. 54
24. F和O都属于元素周期表第二周期元素,它们原子结构中相同的是 ( )
A. 质子数
B. 电子层数
C. 核外电子数
D. 最外层电子数
25. 判断F的非金属性比C的强,可依据的事实是 ( )
A. HF的热稳定性比CH4的强
B. 常温下氟气能与水反应,碳不与水反应
C. 常温下,氟气呈气态,碳呈固态
D. 氟气为黄绿色,木炭为黑色
26. 硼是第二周期ⅢA族元素,下列有关硼元素性质推测正确的是 ( )
A. 最高化合价为+5
B. 原子半径比铝的小
C. 单质与水剧烈反应
D. 最高价氧化物对应的水化物是强碱
27. 下列有关二氧化硫的说法中,正确的是 ( )
A. 检验SO2气体中是否混有CO2的方法是通入澄清石灰水中
B. SO2气体具有漂白性,能使品红溶液、紫色石蕊试液褪色
C. 在含BaCl2的氨水中通入少量SO2气体会有白色沉淀生成
D. 因为SO2气体具有还原性,所以在实验室不能用浓硫酸干燥SO2
28. 实验室用严重锈蚀的废铁屑为原料制备硫酸亚铁晶体(FeSO4·7H2O),流程如下。下列说法正确的是 ( )
A. 上述流程中涉及的反应均属于氧化还原反应
B. “酸溶”时试剂X可用稀硫酸或稀盐酸
C. “还原”时发生反应的离子方程式为Fe3++Fe2Fe2+
D. “结晶”采用的方式是蒸发浓缩、冷却结晶
江苏省普通高中学业水平测试
练透选择题(四)
1. A 解析:该循环为自然界的氮循环,A错误;B正确;工业合成氨是将N2与H2在一定条件下反应生成NH3,属于人工固氮,C正确;氮循环中铵盐和蛋白质可相互转化,铵盐属于无机物,蛋白质属于有机物,含氮无机物和含氮有机物可相互转化,D正确。
2. C
3. C 解析:刚玉的主要成分为Al2O3,A错误;明矾的主要成分为KAl(SO4)2·12H2O,B错误;漂白粉主要成分为Ca(ClO)2、CaCl2,C正确;小苏打主要成分为NaHCO3,D错误。
4. C 5. B 6 A 7. B 8. D
9. D 解析:废水中含有的三种成分均含有Cl-,Cl-物质的量浓度最大,D正确。
10. B 解析:水的电子式:H,A错误;钠原子的结构示意图:,C错误;Na2SO4的电离方程式:Na2SO42Na++ S,D错误。
11. B
12. D 解析:淀粉遇碘水显蓝色,D正确。
13. A 解析:由图可知,反应物总能量小于生成物总能量,则分解水属于吸热反应,A正确;断开H—O键吸收能量,B错误;形成H—H键放出能量,C错误;由图可知,反应物总能量小于生成物总能量,D错误。
14. A 解析:一氧化碳和二氧化碳都无味,一氧化碳还有毒,不能用闻气味的方法鉴别,A错误;氯化钠溶液显中性,pH=7;稀盐酸显酸性,pH<7,可以用pH试纸鉴别,B正确;SO2可使品红溶液褪色CO2不能使品红溶液褪色,C正确;丁达尔效应可鉴别溶液和胶体,D正确。
15. C 解析:C不能与Ca2+大量共存,A错误;OH-不能与H+大量共存,B错误;Fe2+不能与H+、N大量共存,D错误。
16. D 解析:A电荷总数不等,配平错误;铜与稀硝酸反应生成NO,B原理错误;氢氧化镁为难溶物质,不可以拆分,C错误。
17. D 18. B
19. D 解析:A、B、C为加成反应;D为苯的取代反应,D正确。
20. A 解析:金属与水或酸的反应是放热反应,A正确;其余的都要吸收热量。
21. A 解析:增大O2的浓度能加快反应速率,A正确;减小SO3的浓度、降低温度都使反应速率减慢,B、C错误;添加催化剂会改变反应速率,D错误。
22. A 解析:镁失去电子,生成镁离子,镁作负极,铜棒作正极,氢离子在铜棒上得到电子生成氢气,电子从镁棒流出经外电路流向铜棒,A正确。
23. C 解析:中子数=质量数-质子数=37-17=20,C正确。
24. B 解析:F和O的质子数和核外电子数分别是9、8,A、C错误;电子层数都是2,B正确;F和O的最外层电子数分别为7和6,D错误。
25. A 解析:比较非金属性可根据单质与氢气的化合的难易程度;气态氢化物的稳定性;最高价氧化物所对应水化物的酸性强弱进行比较,A正确。
26. B 解析:硼是第二周期ⅢA族元素,最高化合价是+3,A错误;同主族元素从上到下原子半径逐渐增大,硼的原子半径小于铝的原子半径,B正确;同主族元素的单质从上到下金属性逐渐增强,与水反应剧烈程度增大,最高价氧化物对应的水化物的碱性增强,C、D错误。
27. C 解析:两种气体均可使石灰水变浑浊,不能用澄清石灰水检验检验SO2气体中是否混有CO2,A错误;二氧化硫能使品红褪色,也能使紫色石蕊试液变红,B错误;含BaCl2的氨水中通入少量SO2气体,反应生成亚硫酸钡和氯化铵,观察到白色沉淀生成,C正确;二氧化硫与浓硫酸不反应,在实验室能用浓硫酸干燥SO2,D错误。
28. D 解析:氧化铁与硫酸的反应为非氧化还原反应,A错误;由最终制备晶体的酸根离子可知,“酸溶”时试剂X可用稀硫酸,不能选盐酸,否则易引进杂质,B错误;还原时发生的离子反应为2Fe3++Fe3Fe2+,C错误;由溶液得到含结晶水的晶体,可知“结晶”采用的方式是蒸发浓缩、冷却结晶,D正确。
同课章节目录
