第二章《 海水中的重要元素——钠和氯》检测题(Word含答案)2022—2023学年人教版(2019)化学高一上学期必修第一册
文档属性
| 名称 | 第二章《 海水中的重要元素——钠和氯》检测题(Word含答案)2022—2023学年人教版(2019)化学高一上学期必修第一册 |

|
|
| 格式 | docx | ||
| 文件大小 | 404.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-27 00:00:00 | ||
图片预览



文档简介
第二章《 海水中的重要元素——钠和氯》单元检测题
一、单选题
1.下列变化属于化学变化的是
A.车胎爆炸 B.工业制氯气 C.碘的升华 D.海水晒盐
2.设NA表示阿伏伽德罗常数,下列叙述中正确的是
A.常温常压下,11.2 L H2O所含原子数为1.5NA
B.常温常压下,92gNO2 和N2O4混合气体中含有原子总数为6NA
C.标准状况下,22.4 L氦气中所含原子数为2NA
D.常温常压下,18gH2O中含有电子数为3NA
3.下列说法中不正确的是
A.在与金属反应时表现强氧化性
B.任何物质的燃烧必须有参与
C.与反应的离子方程式为
D.漂白粉的主要成分和
4.将钠投入滴有紫色石蕊的水中,下列有关现象的叙述中错误的是
A.钠浮在液面上 B.有沉淀产生
C.溶液变为蓝色 D.钠熔成小球并在水面四处游动
5.用表示阿伏加德罗常数的值,下列说法正确的是
A.11.2 L 含有的分子数为
B.相同质量的与所含氧原子个数比为4:6
C.标准状况下,22.4 L 中含有氢原子的个数为
D.1 mol 和的混合物中含的氧原子数为
6.下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是
A.NaOH溶液与CO2 B.NaHCO3和盐酸
C.Na与O2 D.NaHSO4溶液与Ba(OH)2溶液
7.钙元素在人体血液中以钙离子的形式存在,正常指标参考值为2.13×10-3~2.70 ×10-3 mol·L-1。表示该指标的物理量是
A.溶解度 B.体积分数 C.物质的量浓度 D.质量分数
8.用NA表示阿伏加德罗常数,下列说法正确的是
A.摩尔是一个基本物理量
B.含有2NA个氢原子的水,其物质的量为1 mol
C.0.5 mol氧气所含氧元素为NA
D.2 mol NaCl中含离子数2NA
9.实验室利用NaOH固体配制480mL0.1mol·L-1的NaOH溶液时,以下操作会使溶液的浓度偏高的是
A.用滤纸称量NaOH固体
B.溶解后没有冷却便进行定容
C.定容时仰视刻度线
D.将容量瓶中的溶液转移到试剂瓶的过程中,不慎有少量溶液溅出
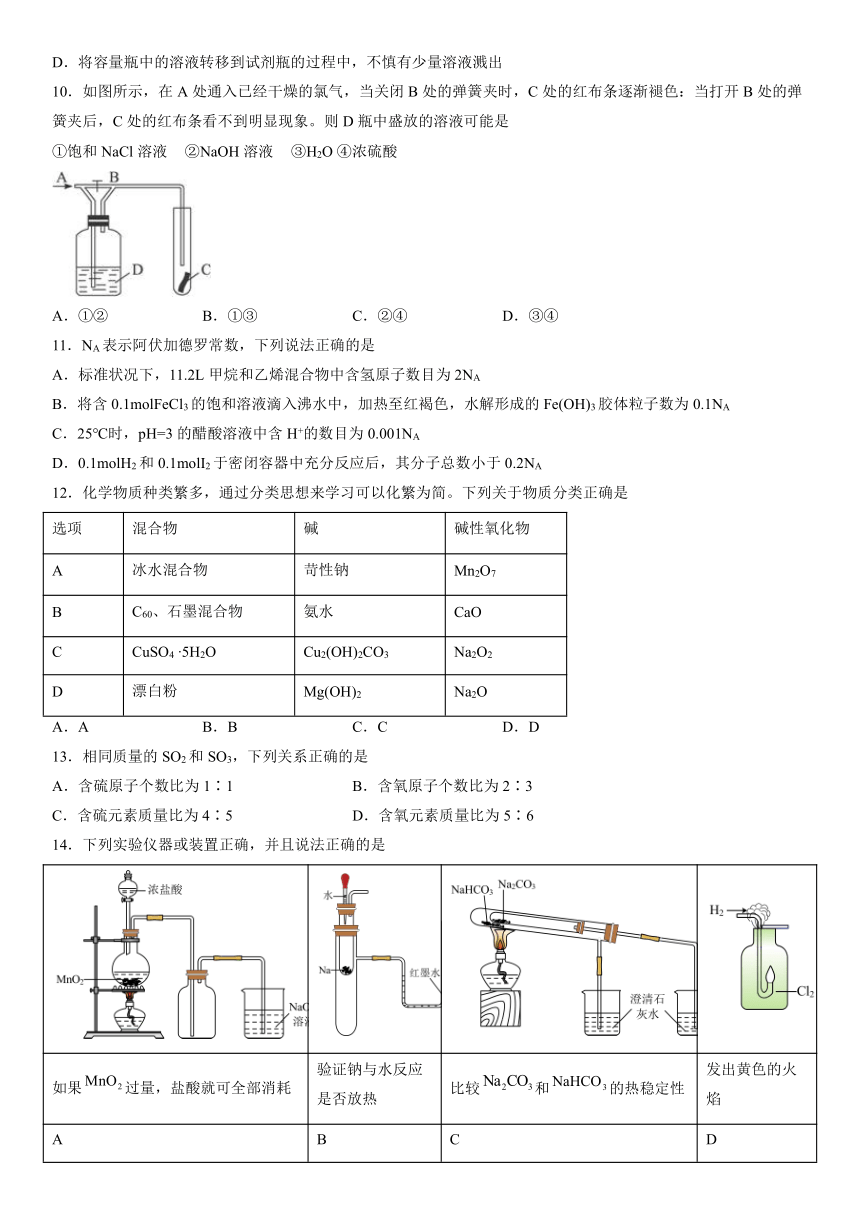
10.如图所示,在A处通入已经干燥的氯气,当关闭B处的弹簧夹时,C处的红布条逐渐褪色:当打开B处的弹簧夹后,C处的红布条看不到明显现象。则D瓶中盛放的溶液可能是
①饱和NaCl溶液 ②NaOH溶液 ③H2O ④浓硫酸
A.①② B.①③ C.②④ D.③④
11.NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
B.将含0.1molFeCl3的饱和溶液滴入沸水中,加热至红褐色,水解形成的Fe(OH)3胶体粒子数为0.1NA
C.25℃时,pH=3的醋酸溶液中含H+的数目为0.001NA
D.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数小于0.2NA
12.化学物质种类繁多,通过分类思想来学习可以化繁为简。下列关于物质分类正确是
选项 混合物 碱 碱性氧化物
A 冰水混合物 苛性钠 Mn2O7
B C60、石墨混合物 氨水 CaO
C CuSO4 5H2O Cu2(OH)2CO3 Na2O2
D 漂白粉 Mg(OH)2 Na2O
A.A B.B C.C D.D
13.相同质量的SO2和SO3,下列关系正确的是
A.含硫原子个数比为1∶1 B.含氧原子个数比为2∶3
C.含硫元素质量比为4∶5 D.含氧元素质量比为5∶6
14.下列实验仪器或装置正确,并且说法正确的是
如果过量,盐酸就可全部消耗 验证钠与水反应是否放热 比较和的热稳定性 发出黄色的火焰
A B C D
A.A B.B C.C D.D
15.下列对陈述I、II的正确性及两者间是否具有因果关系的判断均正确的是
选项 陈述I 陈述II 判断
A 干燥的氯气能使有色鲜花褪色 氯气具有漂白性 I错,II对,有
B 用洁净的铂丝蘸取某溶液进行焰色试验,火焰焰色为黄色 该溶液一定是钠盐的溶液 I对,II对,有
C 向Na2O2与H2O反应后的溶液中滴入酚酞试液,溶液变红 Na2O2与水反应生成氢氧化钠 I对,II对,无
D 氯气可以使湿润的淀粉碘化钾试纸变蓝 Cl2与KI溶液反应生成I2 I对,II对,有
A.A B.B C.C D.D
二、填空题
16.(1)实验室制取氯气反应的化学方程式为:_________;
①在该反应中,氧化剂与还原剂的物质的量之比是_________;
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是________NA。
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目_________;
②浓盐酸在该反应中表现的性质是__________(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是___________(填化学式);
④上述反应产生0.1molCl2时,转移电子的物质的量为___________。
17.氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
(2)c过程中的现象是_____,b过程中的化学方程式为_____。
(3)久置的氯水变为____,用化学反应方程式表示为______。
(4)实验室保存饱和氯水的方法是_____。
18.某同学将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应相同的现象_______,钠在硫酸铜溶液中还可观察到的现象是_______。写出有关的化学方程式_______、_______。
三、计算题
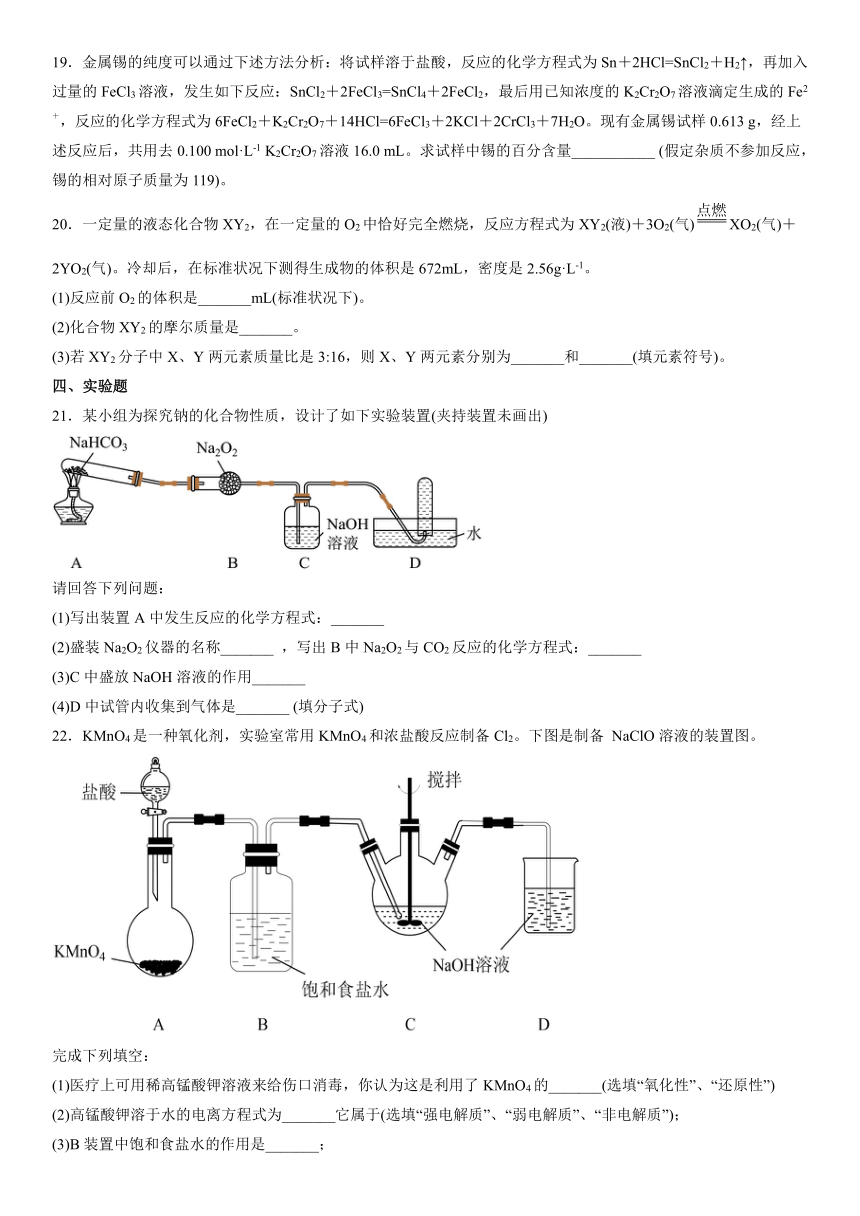
19.金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为Sn+2HCl=SnCl2+H2↑,再加入过量的FeCl3溶液,发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,反应的化学方程式为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。现有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 K2Cr2O7溶液16.0 mL。求试样中锡的百分含量___________ (假定杂质不参加反应,锡的相对原子质量为119)。
20.一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为XY2(液)+3O2(气)XO2(气)+2YO2(气)。冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g·L-1。
(1)反应前O2的体积是_______mL(标准状况下)。
(2)化合物XY2的摩尔质量是_______。
(3)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为_______和_______(填元素符号)。
四、实验题
21.某小组为探究钠的化合物性质,设计了如下实验装置(夹持装置未画出)
请回答下列问题:
(1)写出装置A中发生反应的化学方程式:_______
(2)盛装Na2O2仪器的名称_______ ,写出B中Na2O2与CO2反应的化学方程式:_______
(3)C中盛放NaOH溶液的作用_______
(4)D中试管内收集到气体是_______ (填分子式)
22.KMnO4是一种氧化剂,实验室常用KMnO4和浓盐酸反应制备Cl2。下图是制备 NaClO溶液的装置图。
完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO4的_______(选填“氧化性”、“还原性”)
(2)高锰酸钾溶于水的电离方程式为_______它属于(选填“强电解质”、“弱电解质”、“非电解质”);
(3)B装置中饱和食盐水的作用是_______;
(4)D装置中NaOH的作用是_______(用离子反应方程式表示);
(5)除去Cl2中混有的氯化氢和水蒸气气体,选用的药品及顺序正确的是_______(填序号);
A.水、碱石灰 B.饱和食盐水、浓硫酸
C.无水氯化钙、饱和食盐水 D.烧碱溶液、浓硫酸
参考答案
1.B
【分析】化学变化必须有新物质生成。
【详解】A.轮胎爆炸是气压大引起的,没有生成新物质不属于化学反应,故A错误;
B.工业制氯气是利用MnO2与浓盐酸反应生成氯气,有新物质生成属于化学变化,故B正确;
C.碘的升华是物质状态的改变,碘固体受热转化成气体,没有生成新物质不属于化学反应,故C错误;
D.海水晒盐,是蒸发结晶,没有生成新物质不属于化学反应,故D错误;
故答案为B
2.B
【详解】A.常温常压下,H2O为液态,不能用气体的摩尔体积计算物质的量,选项A错误;
B.二氧化氮和四氧化二氮的最简式相同,都为NO2,则92g NO2中含有的原子个数为×3×NAmol—1=6NA,选项B正确;
C.标准状况下,22.4L氦气的物质的量为1mol,氦气为单原子分子,1mol22.4L氦气含有所含的原子数为NA,选项C错误;
D.18 g H2O的物质的量为=1mol,每个水分子中含有10个电子,所以18 g H2O含有10mol电子,个数为10NA,选项D错误;
答案选B。
3.B
【详解】A.能与大多数金属化合,生成金属氯化物,表现强氧化性,A正确;
B. 燃烧不一定有氧气参加,如氢气在氯气中燃烧,B错误;
C.与反应生成与,离子方程式为,C正确;
D.漂白粉的主要成分为和,有效成分是,D正确;
答案选B。
4.B
【详解】A.钠的密度小于水,所以钠会浮在液面上,A正确;
B.钠和水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和氢气,所以有无色无味的气体产生,没有沉淀产生,B错误;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色, C正确;
D .钠和水反应生成氢氧化钠和氢气,反应放热,且钠熔点低,所以反应过程中钠融成小球在水面四处游动, D正确;
故选B。
5.D
【详解】A.缺标准状况,无法计算11.2 L二氧化碳的物质的量和含有的分子数,A错误;
B.相同质量的SO2和SO3,含氧原子的物质的量之比为,即个数比为5:6,B错误;
C.标准状况下,水不是气态,不能用气体摩尔体积进行计算,C错误;
D.二氧化碳和二氧化氮中含有的氧原子个数都为2,则1 mol 二氧化碳和二氧化氮的混合物中含的氧原子数为1 mol×2×NAmol-1=2NA,D正确;
故选D。
6.B
【详解】A.NaOH溶液与CO2反应,二氧化碳的用量不同,产物不同,少量的二氧化碳生成碳酸钠,过量的二氧化碳生成碳酸氢钠,A不符合题意;
B.NaHCO3和盐酸无论二者的量多少,无论条件如何,反应均生成氯化钠、水和二氧化碳,B符合题意;
C.Na与O2不加热生成Na2O,加热生成Na2O2,条件不同,产物不同,C不符合题意;
D.NaHSO4溶液与Ba(OH)2溶液反应,NaHSO4少量,产物为硫酸钡、水、NaOH,NaHSO4过量,产物为硫酸钡、硫酸钠、水,产物与量有关,D不符合题意;
答案选B。
7.C
【详解】mol·L-1是物质的量浓度的单位,故表示钙离子在血液正常指标数值的单位,其表示的物理量是物质的量浓度,故合理选项是C。
8.B
【详解】A.摩尔是物质的量的单位,不是基本物理量,故A错误;
B.1个水分子中含有2个H原子,含有2NA个氢原子的水分子数是NA,,故B正确;
C.0.5mol氧气所含1mol氧原子,氧原子数是NA,故C错误;
D.根据NaCl= Na++Cl-,2mol NaCl中含离子数4NA,故D错误;
答案选B。
9.B
【详解】A.氢氧化钠易潮解变质,用滤纸称量NaOH固体时,会导致配制的溶液中氢氧化钠的物质的量偏小,配制的溶液浓度偏低,故A错误;
B.NaOH固体溶解时放热,导致溶液温度高,受热膨胀,没有冷却便进行定容会导致溶液体积偏小,浓度偏高,故B正确;
C.定容时仰视刻度线会导致溶液体积偏大,浓度偏低,故C错误;
D.将容量瓶中的溶液转移到试剂瓶的过程中,有少量溶液溅出,会导致所配溶液中溶质的物质的量偏少,浓度偏低,故D错误;
故答案选B。
10.B
【分析】干燥的Cl2没有漂白性,湿润的Cl2具有漂白性;当关闭B处的弹簧夹时,C处的红布条逐渐褪色,说明干燥的Cl2变为湿润的Cl2;当关闭B处的弹簧夹后,C处的红布条看不到明显现象,说明干燥的Cl2无变化。
【详解】①关闭B处的弹簧夹时,干燥的Cl2通入到饱和NaCl溶液中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
②关闭B处的弹簧夹时,干燥的Cl2通入到NaOH溶液中,干燥的Cl2被吸收,C处的红布条看不到明显现象;
③关闭B处的弹簧夹时,干燥的Cl2通入到H2O中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
④关闭B处的弹簧夹时,干燥的Cl2通入到浓硫酸中,干燥的Cl2无变化,C处的红布条看不到明显现象;
综上所述,D瓶中盛放的溶液可能是①③,故选B。
11.A
【详解】A.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为:,A正确;
B.FeCl3水解形成的Fe(OH)3胶体粒子是多个Fe( OH)3的聚集体,所以0.1mol FeCl3水解形成的Fe( OH)3胶体粒子数小于0.1 NA,B不正确;
C.醋酸的体积未知,不能计算出H+的物质的量,C不正确;
D.根据反应H2+I2 2HI可知,反应前后分子数目不变,分子总数仍为0.2NA,D不正确;
故选A。
12.D
【详解】A.冰和水都由水分子构成,冰水混合物属于纯净物,Mn2O7属于酸性氧化物,A不正确;
B.氨水是氨气溶于水形成的混合物,一水合氨才是碱,B不正确;
C.Cu2(OH)2CO3属于碱式盐,Na2O2与酸反应,除生成盐和水外,还有氧气生成,不属于碱性氧化物,C不正确;
D.漂白粉是由氯化钙和次氯酸钙构成的混合物,Mg(OH)2属于难溶性碱,Na2O是氢氧化钠对应的碱性氧化物,D正确;
故选D。
13.D
【详解】SO2和SO3的摩尔质量分别是64g/mol、80g/mol,根据n=m÷M知,相同质量时n与M成反比,所以二者的物质的量之比=80g/mol:64g/mol=5:4,则
A.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,每个分子中都含有一个S原子,所以S原子总数=5:4,故A错误;
B.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以O原子总数=(5×2):(4×3)=5:6,故B错误;
C.二氧化硫和三氧化硫的物质的量之比为5:4,每个分子中都含有一个S原子,所以S元素的物质的量之比为5:4,则根据m=nM知,S元素的质量与n成正比,所以S元素的质量之比=5:4,故C错误;
D.二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以二氧化硫、三氧化硫中O原子的物质的量之比=(5×2):(4×3)=5:6,根据m=nM知,O元素的质量之比等于物质的量之比,所以O元素质量之比=5:6,故D正确;
故选D。
14.B
【详解】A.二氧化锰与稀盐酸不反应,如果过量,盐酸也不可能全部消耗,故A错误;
B.若钠与水反应是放热反应,试管内温度升高,气体膨胀,则“U”形管的右侧液面升高,故B正确;
C.比较和的热稳定性,应把放在温度较低的小试管中,故C错误;
D.氢气在氯气中燃烧,发出苍白色火焰,故D错误;
选B。
15.D
【详解】A.氯气没有漂白性,判断错误,A错误;
B.该溶液可能是氢氧化钠溶液,B错误;
C.因为过氧化钠和水反应生成氢氧化钠,故滴入酚酞试液,溶液变红,两者有因果关系,C错误;
D.Cl2与KI溶液反应生成I2,因此氯气可以使湿润的淀粉碘化钾试纸变蓝,D正确;
故选D。
16. 1:2 0.2NA B ClO2 0.2mol
【详解】(1)实验室用浓盐酸和二氧化锰在加热条件反应制取氯气,化学方程式为:;①在该反应中,锰元素化合价从+4降低到+2、化合价降低2、则二氧化锰是氧化剂,部分浓盐酸氯中元素化合价从-1升高到0、化合价升高了1、为还原剂,得失电子数守恒,则氧化剂与还原剂的物质的量之比是1:2;②从化学方程式知:每生成了1mol氯气、即标况下22.4L氯气,转移电子2mol、即转移的个数为2NA,则在反应中生成了标况下2.24L氯气,则电子转移的个数是0.2NA。
(2)①在反应2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O中,KClO3中氯元素化合价从+5降低到+4、化合价降低1、则KClO3是氧化剂,部分浓盐酸中氯元素化合价从-1升高到0、化合价升高了1、为还原剂,得失电子数守恒,则用双线桥表示上述反应中电子转移的方向和数目为;
②部分浓盐酸中氯元素化合价从-1升高到0、部分化合价不变,则浓盐酸在该反应中表现的性质是还原性和酸性,答案选B;
③KClO3中氯元素化合价从+5降低到+4、则该反应的还原产物是ClO2;
④从化学方程式知:每生成了1mol氯气,转移电子2mol,则上述反应产生0.1molCl2时,转移电子的物质的量为0.2mol。
17. d 有白色沉淀生成 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 稀盐酸 2HClO2HCl+O2↑ 在阴凉处置于棕色试剂瓶中密封保存
【分析】将氯气溶于水,部分氯气与水反应生成盐酸和次氯酸,得到浅黄绿色的氯水,氯水含有H2O、Cl2、HClO、Cl-、H+、OH-(极少量,水微弱电离出来的)多种微粒,其性质取决于其组成的微粒。
【详解】(1)氯水中HClO具有强氧化性,能使有机色质漂白脱色而表现漂白性,故答案为d;
(2)氯水中含有Cl-离子,能与AgNO3溶液反应生成白色的氯化银沉淀;氯水中含有酸性强于碳酸的盐酸,能与Na2CO3溶液发生反应生成氯化钠、二氧化碳和水,故答案为有白色沉淀生成;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)氯水中HClO不稳定,见光易分解生成盐酸和氧气,溶液的颜色由浅绿色变为无色,反应的化学方程式为2HClO2HCl+O2↑,故答案为稀盐酸;2HClO2HCl+O2↑;
(4)为防止氯水中HClO见光易分解,应将新制的饱和氯水在阴凉处置于棕色试剂瓶中密封保存,故答案为在阴凉处置于棕色试剂瓶中密封保存。
【点睛】注意氯水的成分和性质,氯水的性质取决于其组成的微粒,久置氯水(浅黄绿色)会变成稀盐酸(无色)失去漂白性。
18. 钠块浮在水面上,熔成一只闪亮的小球,在水面上不定向地迅速游动,发出“嘶嘶”的响声 产生蓝色沉淀 2Na+2H2O=2NaOH+H2↑ 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【详解】金属钠投入到硫酸铜溶液中,先与水反应:2Na+2H2O=2NaOH+H2↑,因为钠的密度小于水,因此钠块浮在水面,钠与水反应放出热量,又因为钠的熔点较低,观察到钠块熔成小球,钠与水反应产生氢气,观察到钠在水面上此处游动,并发出“嘶嘶”的响声,产生NaOH与Cu2+反应生成Cu(OH)2蓝色沉淀,反应方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;故答案为钠块浮在水面上,熔成一只闪亮的小球,在水面上不定向地迅速游动,发出“嘶嘶”的响声;产生蓝色沉淀;2Na+2H2O=2NaOH+H2↑;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4。
19.93.2%
【详解】根据题给方程式可知,Sn与K2Cr2O7物质的量的关系:3Sn~3SnCl2~6FeCl2~K2Cr2O7;所以存在3×119 g: 1 mol=x:0.100×0.016 mol,解之得到x=0.571 2 g,试样中锡的百分含量w(Sn)= ×100%≈93.2%。
20.(1)672
(2)76
(3) C S
【解析】(1)
由方程式可知,反应前后气体体积不变,则V(O2)=V(XO2)+V(YO2)=672mL;
(2)
依据质量守恒定律,有m(XY2)=0.672L2.56g·L-1-32g/mol≈0.76g,物质的量n(XY2)为n(O2)=0.01mol,所以M(XY2)==76g/mol;
(3)
由及可得,,,则X、Y两元素分别为C、S。
21.(1)2NaHCO3Na2CO3+H2O+CO2↑
(2) 球形干燥管 2Na2O2+2CO2=2Na2CO3+O2
(3)除去未反应的CO2气体
(4)O2
【分析】A中反应为2NaHCO3Na2CO3+H2O+CO2↑,B中Na2O2和H2O、CO2反应生成O2,C中NaOH溶液除去未反应的CO2气体,D中收集生成的O2,据此解答。
(1)
A中发生反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。
(2)
盛装Na2O2仪器的名称为球形干燥管,B中Na2O2与CO2反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2。
(3)
根据分析,C中盛放NaOH溶液的作用为除去未反应的CO2气体。
(4)
根据分析,D中试管内收集到的气体是O2。
22.(1)氧化性
(2)KMnO4=K++MnO;强电解质
(3)除去氯气中的氯化氢
(4)Cl2+2OH-=Cl-+ClO-+H2O
(5)B
【分析】装置A用KMnO4和浓盐酸反应制备Cl2,浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,据此装置B的饱和食盐水除杂,装置C为氯气和NaOH溶液反应制取NaClO,氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应用装置D进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收;
(1)
高锰酸钾与双氧水都具有强的氧化性,能够使蛋白质变性,可用作杀菌消毒,利用其氧化性;
(2)
高锰酸钾属于钾盐,溶于水完全电离,电离方程式为KMnO4=K++MnO,它属于强电解质;
(3)
浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢;
(4)
氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收,离子反应方程式Cl2+2OH-=Cl-+ClO-+H2O;
(5)
除去Cl2中混有的水蒸气和氯化氢气体,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢,用浓硫酸吸收水蒸气,选用的药品及顺序正确的是B。
一、单选题
1.下列变化属于化学变化的是
A.车胎爆炸 B.工业制氯气 C.碘的升华 D.海水晒盐
2.设NA表示阿伏伽德罗常数,下列叙述中正确的是
A.常温常压下,11.2 L H2O所含原子数为1.5NA
B.常温常压下,92gNO2 和N2O4混合气体中含有原子总数为6NA
C.标准状况下,22.4 L氦气中所含原子数为2NA
D.常温常压下,18gH2O中含有电子数为3NA
3.下列说法中不正确的是
A.在与金属反应时表现强氧化性
B.任何物质的燃烧必须有参与
C.与反应的离子方程式为
D.漂白粉的主要成分和
4.将钠投入滴有紫色石蕊的水中,下列有关现象的叙述中错误的是
A.钠浮在液面上 B.有沉淀产生
C.溶液变为蓝色 D.钠熔成小球并在水面四处游动
5.用表示阿伏加德罗常数的值,下列说法正确的是
A.11.2 L 含有的分子数为
B.相同质量的与所含氧原子个数比为4:6
C.标准状况下,22.4 L 中含有氢原子的个数为
D.1 mol 和的混合物中含的氧原子数为
6.下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是
A.NaOH溶液与CO2 B.NaHCO3和盐酸
C.Na与O2 D.NaHSO4溶液与Ba(OH)2溶液
7.钙元素在人体血液中以钙离子的形式存在,正常指标参考值为2.13×10-3~2.70 ×10-3 mol·L-1。表示该指标的物理量是
A.溶解度 B.体积分数 C.物质的量浓度 D.质量分数
8.用NA表示阿伏加德罗常数,下列说法正确的是
A.摩尔是一个基本物理量
B.含有2NA个氢原子的水,其物质的量为1 mol
C.0.5 mol氧气所含氧元素为NA
D.2 mol NaCl中含离子数2NA
9.实验室利用NaOH固体配制480mL0.1mol·L-1的NaOH溶液时,以下操作会使溶液的浓度偏高的是
A.用滤纸称量NaOH固体
B.溶解后没有冷却便进行定容
C.定容时仰视刻度线
D.将容量瓶中的溶液转移到试剂瓶的过程中,不慎有少量溶液溅出
10.如图所示,在A处通入已经干燥的氯气,当关闭B处的弹簧夹时,C处的红布条逐渐褪色:当打开B处的弹簧夹后,C处的红布条看不到明显现象。则D瓶中盛放的溶液可能是
①饱和NaCl溶液 ②NaOH溶液 ③H2O ④浓硫酸
A.①② B.①③ C.②④ D.③④
11.NA表示阿伏加德罗常数,下列说法正确的是
A.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为2NA
B.将含0.1molFeCl3的饱和溶液滴入沸水中,加热至红褐色,水解形成的Fe(OH)3胶体粒子数为0.1NA
C.25℃时,pH=3的醋酸溶液中含H+的数目为0.001NA
D.0.1molH2和0.1molI2于密闭容器中充分反应后,其分子总数小于0.2NA
12.化学物质种类繁多,通过分类思想来学习可以化繁为简。下列关于物质分类正确是
选项 混合物 碱 碱性氧化物
A 冰水混合物 苛性钠 Mn2O7
B C60、石墨混合物 氨水 CaO
C CuSO4 5H2O Cu2(OH)2CO3 Na2O2
D 漂白粉 Mg(OH)2 Na2O
A.A B.B C.C D.D
13.相同质量的SO2和SO3,下列关系正确的是
A.含硫原子个数比为1∶1 B.含氧原子个数比为2∶3
C.含硫元素质量比为4∶5 D.含氧元素质量比为5∶6
14.下列实验仪器或装置正确,并且说法正确的是
如果过量,盐酸就可全部消耗 验证钠与水反应是否放热 比较和的热稳定性 发出黄色的火焰
A B C D
A.A B.B C.C D.D
15.下列对陈述I、II的正确性及两者间是否具有因果关系的判断均正确的是
选项 陈述I 陈述II 判断
A 干燥的氯气能使有色鲜花褪色 氯气具有漂白性 I错,II对,有
B 用洁净的铂丝蘸取某溶液进行焰色试验,火焰焰色为黄色 该溶液一定是钠盐的溶液 I对,II对,有
C 向Na2O2与H2O反应后的溶液中滴入酚酞试液,溶液变红 Na2O2与水反应生成氢氧化钠 I对,II对,无
D 氯气可以使湿润的淀粉碘化钾试纸变蓝 Cl2与KI溶液反应生成I2 I对,II对,有
A.A B.B C.C D.D
二、填空题
16.(1)实验室制取氯气反应的化学方程式为:_________;
①在该反应中,氧化剂与还原剂的物质的量之比是_________;
②若在反应中生成了标况下2.24L氯气,则电子转移的个数是________NA。
(2)氯酸钾和浓盐酸在一定温度下反应会生成黄绿色的易爆物二氧化氯,其化学方程式为:2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
①用双线桥表示上述反应中电子转移的方向和数目_________;
②浓盐酸在该反应中表现的性质是__________(填序号);
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
③该反应的还原产物是___________(填化学式);
④上述反应产生0.1molCl2时,转移电子的物质的量为___________。
17.氯水中含有多种成分,因而具有多种性质,根据氯水分别与如图四种物质发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。
(1)能证明氯水具有漂白性的是______(填“a”“b”“c”或“d”)。
(2)c过程中的现象是_____,b过程中的化学方程式为_____。
(3)久置的氯水变为____,用化学反应方程式表示为______。
(4)实验室保存饱和氯水的方法是_____。
18.某同学将一小块钠投入到硫酸铜溶液中,观察到与钠跟水反应相同的现象_______,钠在硫酸铜溶液中还可观察到的现象是_______。写出有关的化学方程式_______、_______。
三、计算题
19.金属锡的纯度可以通过下述方法分析:将试样溶于盐酸,反应的化学方程式为Sn+2HCl=SnCl2+H2↑,再加入过量的FeCl3溶液,发生如下反应:SnCl2+2FeCl3=SnCl4+2FeCl2,最后用已知浓度的K2Cr2O7溶液滴定生成的Fe2+,反应的化学方程式为6FeCl2+K2Cr2O7+14HCl=6FeCl3+2KCl+2CrCl3+7H2O。现有金属锡试样0.613 g,经上述反应后,共用去0.100 mol·L-1 K2Cr2O7溶液16.0 mL。求试样中锡的百分含量___________ (假定杂质不参加反应,锡的相对原子质量为119)。
20.一定量的液态化合物XY2,在一定量的O2中恰好完全燃烧,反应方程式为XY2(液)+3O2(气)XO2(气)+2YO2(气)。冷却后,在标准状况下测得生成物的体积是672mL,密度是2.56g·L-1。
(1)反应前O2的体积是_______mL(标准状况下)。
(2)化合物XY2的摩尔质量是_______。
(3)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为_______和_______(填元素符号)。
四、实验题
21.某小组为探究钠的化合物性质,设计了如下实验装置(夹持装置未画出)
请回答下列问题:
(1)写出装置A中发生反应的化学方程式:_______
(2)盛装Na2O2仪器的名称_______ ,写出B中Na2O2与CO2反应的化学方程式:_______
(3)C中盛放NaOH溶液的作用_______
(4)D中试管内收集到气体是_______ (填分子式)
22.KMnO4是一种氧化剂,实验室常用KMnO4和浓盐酸反应制备Cl2。下图是制备 NaClO溶液的装置图。
完成下列填空:
(1)医疗上可用稀高锰酸钾溶液来给伤口消毒,你认为这是利用了KMnO4的_______(选填“氧化性”、“还原性”)
(2)高锰酸钾溶于水的电离方程式为_______它属于(选填“强电解质”、“弱电解质”、“非电解质”);
(3)B装置中饱和食盐水的作用是_______;
(4)D装置中NaOH的作用是_______(用离子反应方程式表示);
(5)除去Cl2中混有的氯化氢和水蒸气气体,选用的药品及顺序正确的是_______(填序号);
A.水、碱石灰 B.饱和食盐水、浓硫酸
C.无水氯化钙、饱和食盐水 D.烧碱溶液、浓硫酸
参考答案
1.B
【分析】化学变化必须有新物质生成。
【详解】A.轮胎爆炸是气压大引起的,没有生成新物质不属于化学反应,故A错误;
B.工业制氯气是利用MnO2与浓盐酸反应生成氯气,有新物质生成属于化学变化,故B正确;
C.碘的升华是物质状态的改变,碘固体受热转化成气体,没有生成新物质不属于化学反应,故C错误;
D.海水晒盐,是蒸发结晶,没有生成新物质不属于化学反应,故D错误;
故答案为B
2.B
【详解】A.常温常压下,H2O为液态,不能用气体的摩尔体积计算物质的量,选项A错误;
B.二氧化氮和四氧化二氮的最简式相同,都为NO2,则92g NO2中含有的原子个数为×3×NAmol—1=6NA,选项B正确;
C.标准状况下,22.4L氦气的物质的量为1mol,氦气为单原子分子,1mol22.4L氦气含有所含的原子数为NA,选项C错误;
D.18 g H2O的物质的量为=1mol,每个水分子中含有10个电子,所以18 g H2O含有10mol电子,个数为10NA,选项D错误;
答案选B。
3.B
【详解】A.能与大多数金属化合,生成金属氯化物,表现强氧化性,A正确;
B. 燃烧不一定有氧气参加,如氢气在氯气中燃烧,B错误;
C.与反应生成与,离子方程式为,C正确;
D.漂白粉的主要成分为和,有效成分是,D正确;
答案选B。
4.B
【详解】A.钠的密度小于水,所以钠会浮在液面上,A正确;
B.钠和水反应2Na+2H2O=2NaOH+H2↑,生成氢氧化钠和氢气,所以有无色无味的气体产生,没有沉淀产生,B错误;
C.钠和水反应生成氢氧化钠和氢气,氢氧化钠溶液呈碱性,紫色石蕊试液遇碱变蓝色, C正确;
D .钠和水反应生成氢氧化钠和氢气,反应放热,且钠熔点低,所以反应过程中钠融成小球在水面四处游动, D正确;
故选B。
5.D
【详解】A.缺标准状况,无法计算11.2 L二氧化碳的物质的量和含有的分子数,A错误;
B.相同质量的SO2和SO3,含氧原子的物质的量之比为,即个数比为5:6,B错误;
C.标准状况下,水不是气态,不能用气体摩尔体积进行计算,C错误;
D.二氧化碳和二氧化氮中含有的氧原子个数都为2,则1 mol 二氧化碳和二氧化氮的混合物中含的氧原子数为1 mol×2×NAmol-1=2NA,D正确;
故选D。
6.B
【详解】A.NaOH溶液与CO2反应,二氧化碳的用量不同,产物不同,少量的二氧化碳生成碳酸钠,过量的二氧化碳生成碳酸氢钠,A不符合题意;
B.NaHCO3和盐酸无论二者的量多少,无论条件如何,反应均生成氯化钠、水和二氧化碳,B符合题意;
C.Na与O2不加热生成Na2O,加热生成Na2O2,条件不同,产物不同,C不符合题意;
D.NaHSO4溶液与Ba(OH)2溶液反应,NaHSO4少量,产物为硫酸钡、水、NaOH,NaHSO4过量,产物为硫酸钡、硫酸钠、水,产物与量有关,D不符合题意;
答案选B。
7.C
【详解】mol·L-1是物质的量浓度的单位,故表示钙离子在血液正常指标数值的单位,其表示的物理量是物质的量浓度,故合理选项是C。
8.B
【详解】A.摩尔是物质的量的单位,不是基本物理量,故A错误;
B.1个水分子中含有2个H原子,含有2NA个氢原子的水分子数是NA,,故B正确;
C.0.5mol氧气所含1mol氧原子,氧原子数是NA,故C错误;
D.根据NaCl= Na++Cl-,2mol NaCl中含离子数4NA,故D错误;
答案选B。
9.B
【详解】A.氢氧化钠易潮解变质,用滤纸称量NaOH固体时,会导致配制的溶液中氢氧化钠的物质的量偏小,配制的溶液浓度偏低,故A错误;
B.NaOH固体溶解时放热,导致溶液温度高,受热膨胀,没有冷却便进行定容会导致溶液体积偏小,浓度偏高,故B正确;
C.定容时仰视刻度线会导致溶液体积偏大,浓度偏低,故C错误;
D.将容量瓶中的溶液转移到试剂瓶的过程中,有少量溶液溅出,会导致所配溶液中溶质的物质的量偏少,浓度偏低,故D错误;
故答案选B。
10.B
【分析】干燥的Cl2没有漂白性,湿润的Cl2具有漂白性;当关闭B处的弹簧夹时,C处的红布条逐渐褪色,说明干燥的Cl2变为湿润的Cl2;当关闭B处的弹簧夹后,C处的红布条看不到明显现象,说明干燥的Cl2无变化。
【详解】①关闭B处的弹簧夹时,干燥的Cl2通入到饱和NaCl溶液中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
②关闭B处的弹簧夹时,干燥的Cl2通入到NaOH溶液中,干燥的Cl2被吸收,C处的红布条看不到明显现象;
③关闭B处的弹簧夹时,干燥的Cl2通入到H2O中,干燥的Cl2变为湿润的Cl2,C处的红布条逐渐褪色;
④关闭B处的弹簧夹时,干燥的Cl2通入到浓硫酸中,干燥的Cl2无变化,C处的红布条看不到明显现象;
综上所述,D瓶中盛放的溶液可能是①③,故选B。
11.A
【详解】A.标准状况下,11.2L甲烷和乙烯混合物中含氢原子数目为:,A正确;
B.FeCl3水解形成的Fe(OH)3胶体粒子是多个Fe( OH)3的聚集体,所以0.1mol FeCl3水解形成的Fe( OH)3胶体粒子数小于0.1 NA,B不正确;
C.醋酸的体积未知,不能计算出H+的物质的量,C不正确;
D.根据反应H2+I2 2HI可知,反应前后分子数目不变,分子总数仍为0.2NA,D不正确;
故选A。
12.D
【详解】A.冰和水都由水分子构成,冰水混合物属于纯净物,Mn2O7属于酸性氧化物,A不正确;
B.氨水是氨气溶于水形成的混合物,一水合氨才是碱,B不正确;
C.Cu2(OH)2CO3属于碱式盐,Na2O2与酸反应,除生成盐和水外,还有氧气生成,不属于碱性氧化物,C不正确;
D.漂白粉是由氯化钙和次氯酸钙构成的混合物,Mg(OH)2属于难溶性碱,Na2O是氢氧化钠对应的碱性氧化物,D正确;
故选D。
13.D
【详解】SO2和SO3的摩尔质量分别是64g/mol、80g/mol,根据n=m÷M知,相同质量时n与M成反比,所以二者的物质的量之比=80g/mol:64g/mol=5:4,则
A.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,每个分子中都含有一个S原子,所以S原子总数=5:4,故A错误;
B.根据N=nNA知,其分子数与n成正比,所以分子个数之比=5:4,二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以O原子总数=(5×2):(4×3)=5:6,故B错误;
C.二氧化硫和三氧化硫的物质的量之比为5:4,每个分子中都含有一个S原子,所以S元素的物质的量之比为5:4,则根据m=nM知,S元素的质量与n成正比,所以S元素的质量之比=5:4,故C错误;
D.二氧化硫分子中含有两个O原子、三氧化硫分子中含有3个O原子,所以二氧化硫、三氧化硫中O原子的物质的量之比=(5×2):(4×3)=5:6,根据m=nM知,O元素的质量之比等于物质的量之比,所以O元素质量之比=5:6,故D正确;
故选D。
14.B
【详解】A.二氧化锰与稀盐酸不反应,如果过量,盐酸也不可能全部消耗,故A错误;
B.若钠与水反应是放热反应,试管内温度升高,气体膨胀,则“U”形管的右侧液面升高,故B正确;
C.比较和的热稳定性,应把放在温度较低的小试管中,故C错误;
D.氢气在氯气中燃烧,发出苍白色火焰,故D错误;
选B。
15.D
【详解】A.氯气没有漂白性,判断错误,A错误;
B.该溶液可能是氢氧化钠溶液,B错误;
C.因为过氧化钠和水反应生成氢氧化钠,故滴入酚酞试液,溶液变红,两者有因果关系,C错误;
D.Cl2与KI溶液反应生成I2,因此氯气可以使湿润的淀粉碘化钾试纸变蓝,D正确;
故选D。
16. 1:2 0.2NA B ClO2 0.2mol
【详解】(1)实验室用浓盐酸和二氧化锰在加热条件反应制取氯气,化学方程式为:;①在该反应中,锰元素化合价从+4降低到+2、化合价降低2、则二氧化锰是氧化剂,部分浓盐酸氯中元素化合价从-1升高到0、化合价升高了1、为还原剂,得失电子数守恒,则氧化剂与还原剂的物质的量之比是1:2;②从化学方程式知:每生成了1mol氯气、即标况下22.4L氯气,转移电子2mol、即转移的个数为2NA,则在反应中生成了标况下2.24L氯气,则电子转移的个数是0.2NA。
(2)①在反应2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O中,KClO3中氯元素化合价从+5降低到+4、化合价降低1、则KClO3是氧化剂,部分浓盐酸中氯元素化合价从-1升高到0、化合价升高了1、为还原剂,得失电子数守恒,则用双线桥表示上述反应中电子转移的方向和数目为;
②部分浓盐酸中氯元素化合价从-1升高到0、部分化合价不变,则浓盐酸在该反应中表现的性质是还原性和酸性,答案选B;
③KClO3中氯元素化合价从+5降低到+4、则该反应的还原产物是ClO2;
④从化学方程式知:每生成了1mol氯气,转移电子2mol,则上述反应产生0.1molCl2时,转移电子的物质的量为0.2mol。
17. d 有白色沉淀生成 Na2CO3+2HCl=2NaCl+H2O+CO2↑ 稀盐酸 2HClO2HCl+O2↑ 在阴凉处置于棕色试剂瓶中密封保存
【分析】将氯气溶于水,部分氯气与水反应生成盐酸和次氯酸,得到浅黄绿色的氯水,氯水含有H2O、Cl2、HClO、Cl-、H+、OH-(极少量,水微弱电离出来的)多种微粒,其性质取决于其组成的微粒。
【详解】(1)氯水中HClO具有强氧化性,能使有机色质漂白脱色而表现漂白性,故答案为d;
(2)氯水中含有Cl-离子,能与AgNO3溶液反应生成白色的氯化银沉淀;氯水中含有酸性强于碳酸的盐酸,能与Na2CO3溶液发生反应生成氯化钠、二氧化碳和水,故答案为有白色沉淀生成;Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(3)氯水中HClO不稳定,见光易分解生成盐酸和氧气,溶液的颜色由浅绿色变为无色,反应的化学方程式为2HClO2HCl+O2↑,故答案为稀盐酸;2HClO2HCl+O2↑;
(4)为防止氯水中HClO见光易分解,应将新制的饱和氯水在阴凉处置于棕色试剂瓶中密封保存,故答案为在阴凉处置于棕色试剂瓶中密封保存。
【点睛】注意氯水的成分和性质,氯水的性质取决于其组成的微粒,久置氯水(浅黄绿色)会变成稀盐酸(无色)失去漂白性。
18. 钠块浮在水面上,熔成一只闪亮的小球,在水面上不定向地迅速游动,发出“嘶嘶”的响声 产生蓝色沉淀 2Na+2H2O=2NaOH+H2↑ 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
【详解】金属钠投入到硫酸铜溶液中,先与水反应:2Na+2H2O=2NaOH+H2↑,因为钠的密度小于水,因此钠块浮在水面,钠与水反应放出热量,又因为钠的熔点较低,观察到钠块熔成小球,钠与水反应产生氢气,观察到钠在水面上此处游动,并发出“嘶嘶”的响声,产生NaOH与Cu2+反应生成Cu(OH)2蓝色沉淀,反应方程式2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;故答案为钠块浮在水面上,熔成一只闪亮的小球,在水面上不定向地迅速游动,发出“嘶嘶”的响声;产生蓝色沉淀;2Na+2H2O=2NaOH+H2↑;2NaOH+CuSO4=Cu(OH)2↓+Na2SO4。
19.93.2%
【详解】根据题给方程式可知,Sn与K2Cr2O7物质的量的关系:3Sn~3SnCl2~6FeCl2~K2Cr2O7;所以存在3×119 g: 1 mol=x:0.100×0.016 mol,解之得到x=0.571 2 g,试样中锡的百分含量w(Sn)= ×100%≈93.2%。
20.(1)672
(2)76
(3) C S
【解析】(1)
由方程式可知,反应前后气体体积不变,则V(O2)=V(XO2)+V(YO2)=672mL;
(2)
依据质量守恒定律,有m(XY2)=0.672L2.56g·L-1-32g/mol≈0.76g,物质的量n(XY2)为n(O2)=0.01mol,所以M(XY2)==76g/mol;
(3)
由及可得,,,则X、Y两元素分别为C、S。
21.(1)2NaHCO3Na2CO3+H2O+CO2↑
(2) 球形干燥管 2Na2O2+2CO2=2Na2CO3+O2
(3)除去未反应的CO2气体
(4)O2
【分析】A中反应为2NaHCO3Na2CO3+H2O+CO2↑,B中Na2O2和H2O、CO2反应生成O2,C中NaOH溶液除去未反应的CO2气体,D中收集生成的O2,据此解答。
(1)
A中发生反应的化学方程式为2NaHCO3Na2CO3+H2O+CO2↑。
(2)
盛装Na2O2仪器的名称为球形干燥管,B中Na2O2与CO2反应生成碳酸钠和氧气,反应的化学方程式为2Na2O2+2CO2=2Na2CO3+O2。
(3)
根据分析,C中盛放NaOH溶液的作用为除去未反应的CO2气体。
(4)
根据分析,D中试管内收集到的气体是O2。
22.(1)氧化性
(2)KMnO4=K++MnO;强电解质
(3)除去氯气中的氯化氢
(4)Cl2+2OH-=Cl-+ClO-+H2O
(5)B
【分析】装置A用KMnO4和浓盐酸反应制备Cl2,浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,据此装置B的饱和食盐水除杂,装置C为氯气和NaOH溶液反应制取NaClO,氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应用装置D进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收;
(1)
高锰酸钾与双氧水都具有强的氧化性,能够使蛋白质变性,可用作杀菌消毒,利用其氧化性;
(2)
高锰酸钾属于钾盐,溶于水完全电离,电离方程式为KMnO4=K++MnO,它属于强电解质;
(3)
浓盐酸易挥发,制备的氯气中含有氯化氢,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢;
(4)
氯气有毒,过量的氯气直接排放到空气中能引起空气污染,应进行尾气处理,氯气能够与氢氧化钠反应,被氢氧化钠吸收,离子反应方程式Cl2+2OH-=Cl-+ClO-+H2O;
(5)
除去Cl2中混有的水蒸气和氯化氢气体,氯化氢易溶于水,氯气在饱和食盐水中溶解度不大,所以可以用装有饱和食盐水的洗气瓶除去氯气中的氯化氢,用浓硫酸吸收水蒸气,选用的药品及顺序正确的是B。
