水是常用的溶剂(溶解能力)
图片预览











文档简介
课件36张PPT。3.水是常见的溶剂(第二课时)溶 液:
由一种或一种质以上的物质分散到到另一种液体物质里,形成均一、稳定的混合物。溶液由溶质与溶剂组成。 一般情况下,不同溶质在同一种溶剂里的溶解能力不同;同种溶质在不同溶剂里的溶解能力也是不同的。 可见:一种物质溶解在另一种物质里的能力大小主要是由溶质和溶剂的性质决定的 如何比较两种物质的溶解能力大小?确定温度
确定溶剂的量
确定状态(达到饱和)比较不同物质的溶解能力,应该控制的条件有:溶解性
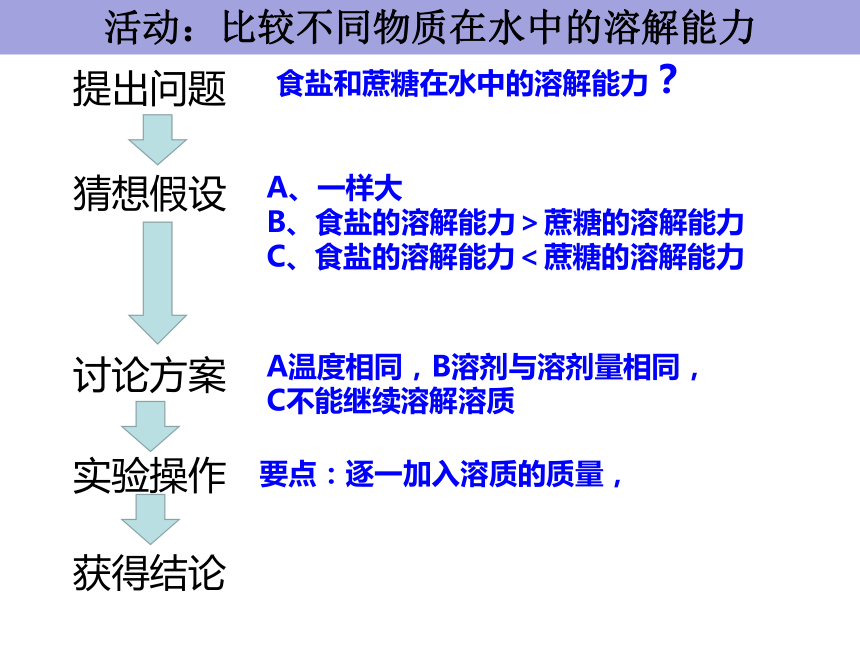
定义:一种物质溶解在另一种物质的能力。提出问题猜想假设讨论方案实验操作获得结论食盐和蔗糖在水中的溶解能力?要点:逐一加入溶质的质量,A、一样大
B、食盐的溶解能力>蔗糖的溶解能力
C、食盐的溶解能力<蔗糖的溶解能力A温度相同,B溶剂与溶剂量相同,
C不能继续溶解溶质活动:比较不同物质在水中的溶解能力 物质的溶解能力主要是由溶质和溶剂的性质以及溶剂的温度决定的。比较不同物质在水中的溶解能力[演示实验一]:
探究蔗糖在水中的溶解能力 从刚才的实验中,我们发现在水中溶解了一定量的蔗糖后,蔗糖不能继续溶解了。【现象】
【实验演示二】硝酸铵在水中的溶解能力
现象: 硝酸铵溶解在水中,得到硝酸铵的溶液,
到一定程度硝酸铵不再溶解。结论:说明在一定的条件下,溶质不能无限地溶解在溶剂里。(一定量的溶剂中,一定的温度下)1、 饱和溶液:
在一定温度下,在一定量的溶剂里,不能继续溶解某种溶质的溶液,称为这种溶质的饱和溶液。 2、 不饱和溶液:
在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。 3、加少量的溶质,不能溶解的是饱和溶液。2、蒸发少量的水,如果溶质就会有析出,表明是饱和溶液;怎样判断一种溶液是不是饱和溶液?1、如果溶液中有少量未溶的溶质,则是饱和溶液;【思考讨论】问题:一定量的水中不能无限的溶解蔗糖,
那它受什么因素的影响?(一定量的溶剂中,一定的温度下)如何使蔗糖,蔗糖全部溶解?活动:饱和溶液与不饱和溶液可以相互转化吗?对蔗糖溶液加热对蔗糖溶液加溶剂蔗糖饱和溶液蔗糖饱和溶液蔗糖不饱和溶液蔗糖不饱和溶液升温降温增加溶剂蒸发溶剂液体不超过试管的1/3
试管夹夹在离管口1/3~1/4处
酒精灯中酒精体积不超过酒精灯的2/3
加热时,试管在酒精灯外焰上预热
试管口与水平面呈45°,不能对人
酒精灯用灯帽盖灭注意事项:[演示实验三] 在各盛有5mL水的两支试管里,分别加入1g食盐和0.5g熟石灰,振荡,观察现象。现象:
分析:
室温下,食盐溶液全部溶解了,但它是浓溶液。
但熟石灰不能再溶解了,是饱和溶液,但它是稀溶液。食盐全部溶解了,但是熟石灰只溶解了一点点,大部分没溶解;结论:
1、浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液。
2、同一种溶质的溶液,在一定温度下,饱和溶液比不饱和溶液要浓。不同溶质在同种溶剂中的溶解能力是不一样。怎样定量比较物质的溶解能力呢? 溶解度注意点:
(1)理解这个概念,抓住四个词:一定的温度、100克溶剂(一般为水)、达到饱和、溶解的质量(单位为克/100克水)。
(2)溶解度值越大,表明该温度下,物质的溶解能力越强。.....硝酸钾....溶解度曲线 以温度为横坐标,溶解度为纵坐标,形象地表示出物质的溶解度随温度变化情况的曲线。不同物质溶解度受温度的影响是不同的。 (1)曲线上每个点表示某温度下某溶质的溶解度(2)曲线表示物质的溶解度受温度变化影响大小的情况(3)两条曲线的交点,表示在该温度下两种物质的溶解度相等(4)曲线上每个点所配制的溶液是该温度下这种溶质的饱和溶液,曲线下方的点表示对应温度下该溶质的不饱和溶液。溶解度曲线的意义 大多数物质的溶解度温度升高而增大;如硝酸钾;
少数物质的溶解度受温度影响变化不大,如氯化钠;0.050.100.150.2090704001020506080100300.050.100.150.29070400102050608010030温度/℃熟石灰的溶解度曲线: 极少数固体物质溶解度随温度升高反而减小,例如熟石灰。生活中我们已经知道,固体、液体、气体能够溶解在水中?有谁能够举出气体溶解在水中的例子吗?二氧化碳溶于水
氧气溶于水各种气体在标准大气压下,纯水中的溶解度(ml/L)结论:一般说来,在一定条件下,气体的溶解度随温度的升高而降低。问题:为什么煮沸后的冷开水不能养鱼吗?常温的冷开水常温的天然泉水活动比较不同物质在溶解过程中的能量变化 实验表明,在溶质溶解于水的过程中都伴随着能量的变化,有些有明显的放热或吸热现象,有些则温度变化不明显。 人们利用某些物质在溶于水的过程中会放出大量的热的性质,为野外工作者设计了方便、安全的自热罐头;反之,人们用硝酸铵制作冰袋。应用——自热罐头和冰袋浊液 黄河水中含有很多泥沙,水的颜色发黄,黄河由此得名。黄河水素有“一碗水,半碗泥”的说法。这是一种典型的悬浊液。二、悬浊液和乳浊液1、悬浊液:固体小颗粒分散于液体里所形
成的混合物2、乳浊液:液体小液滴分散另一种液体里
所形成的混合物溶液、悬浊液、乳浊液的区别:固、液、气体溶解在液体中
固体颗粒悬浮在液体中小液滴颗粒悬浮在液体中
稳定
不稳定
不稳定均一、稳定的
不分层 分层 分层本节小结物质纯净物混合物溶液浊液饱和溶液不饱和溶液悬浊液乳浊液溶解度物质悬浊液乳浊液饱和溶液不饱和溶液1.某物质的溶解度如图所示。在一个大烧杯中装着该物质的饱和溶液,而且杯中还有少量该物质固体存在,现将温度由60℃降到20℃,下列说法正确的是( )
A 杯中固体减少
B 杯中固体增多
C 杯中固体不变
D 以上说法都不对B练习2.下列液体属于溶液的是( )
A.牛奶 B.泥水 C.液氧 D. 碘酒
3.一杯溶液中各部分的性质( )
A.上面和下面不相同 B.完全相同
C.完全不同 C.不一定相同
4.下列各用途与乳化无关的是( )
A.用洗衣粉洗去衣服上的油脂
B.用盐酸洗去铁块表面的锈
C.农药、医药制剂的合成
D.各种日用洗涤剂的配制DBB5.下列小实验不能得到溶液的是( )食盐粉尘植物油蔗糖水水水汽油6.等同条件下,下列物质溶于水后能使水的温度明显降低的是( )
A.食盐 B.硝酸铵 C.浓硫酸 D.氢氧化钠7.现有一杯糖水,取出一部分,测其密度为a g/cm3,则剩余糖水的密度是( )
A.小于 a g/cm3 B.等于 a g/cm3
C.大于a g/cm3 D.无法确定BABCDBB100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃8.固体的溶解度曲线练习:1)A点表示什么意义? 2)40℃时氯化铵的溶解度为
,70℃时氯化铵的溶解度为 。44g/100水A.B.3)B点表示什么意思?该温度下,硝酸钠和硝酸钾的溶解度相等 60g/100水4)在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是___________________________。氯化铵、氯化钾、氯化钠、硼酸气体的溶解度主要受温度和压强的影响,温度升高溶解度减小,压强增大溶解度增大。(2)B点代表的含义是
;(1)T2时,三种物质的溶解度由大到小的顺序是 ,(3)T2时甲的溶解度是___________,该温度下向150g水中加入80g甲物质,所得溶液是 溶液(填“饱和”或“不饱和”),需加入 克甲或蒸发 克水,使其变为饱和溶液。甲>乙>丙甲、丙两种物质的溶解度相等80g/100g水T1℃时,溶解度
(g)9、根据如图所示的溶解度曲线图,回答下列问题:80604020不饱和405010.判断是非:
(1)20℃时,10克食盐溶解在100克水中,所以20℃时食盐的溶解度是10克。
(2)100克水中溶解了36克食盐刚好达到饱和,所以食盐的溶解度是36克。
(3)在20℃时,100克水里最多溶解33.3克氯化铵,则20℃氯化铵的溶解度是33.3。
(4)在20℃时,100克硝酸钾饱和溶液里含硝酸钾24克,则20℃硝酸钾的溶解度是24克。
(5)在30℃时,100克水中加入40克氯化钾后达到饱和溶液,则30℃时氯化钾的溶解度是40克。二、交流与讨论 向右图试管里的水中加入某中物质后,U形管左边支管的红墨水液面下降,右边支管的液面上升的物质可能是:
a.蔗糖 b.生石灰 c.活性炭 d.硝酸铵 e.氢氧化钠 f.浓硫酸红墨水水b e f
由一种或一种质以上的物质分散到到另一种液体物质里,形成均一、稳定的混合物。溶液由溶质与溶剂组成。 一般情况下,不同溶质在同一种溶剂里的溶解能力不同;同种溶质在不同溶剂里的溶解能力也是不同的。 可见:一种物质溶解在另一种物质里的能力大小主要是由溶质和溶剂的性质决定的 如何比较两种物质的溶解能力大小?确定温度
确定溶剂的量
确定状态(达到饱和)比较不同物质的溶解能力,应该控制的条件有:溶解性
定义:一种物质溶解在另一种物质的能力。提出问题猜想假设讨论方案实验操作获得结论食盐和蔗糖在水中的溶解能力?要点:逐一加入溶质的质量,A、一样大
B、食盐的溶解能力>蔗糖的溶解能力
C、食盐的溶解能力<蔗糖的溶解能力A温度相同,B溶剂与溶剂量相同,
C不能继续溶解溶质活动:比较不同物质在水中的溶解能力 物质的溶解能力主要是由溶质和溶剂的性质以及溶剂的温度决定的。比较不同物质在水中的溶解能力[演示实验一]:
探究蔗糖在水中的溶解能力 从刚才的实验中,我们发现在水中溶解了一定量的蔗糖后,蔗糖不能继续溶解了。【现象】
【实验演示二】硝酸铵在水中的溶解能力
现象: 硝酸铵溶解在水中,得到硝酸铵的溶液,
到一定程度硝酸铵不再溶解。结论:说明在一定的条件下,溶质不能无限地溶解在溶剂里。(一定量的溶剂中,一定的温度下)1、 饱和溶液:
在一定温度下,在一定量的溶剂里,不能继续溶解某种溶质的溶液,称为这种溶质的饱和溶液。 2、 不饱和溶液:
在一定温度下,在一定量的溶剂里,还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。 3、加少量的溶质,不能溶解的是饱和溶液。2、蒸发少量的水,如果溶质就会有析出,表明是饱和溶液;怎样判断一种溶液是不是饱和溶液?1、如果溶液中有少量未溶的溶质,则是饱和溶液;【思考讨论】问题:一定量的水中不能无限的溶解蔗糖,
那它受什么因素的影响?(一定量的溶剂中,一定的温度下)如何使蔗糖,蔗糖全部溶解?活动:饱和溶液与不饱和溶液可以相互转化吗?对蔗糖溶液加热对蔗糖溶液加溶剂蔗糖饱和溶液蔗糖饱和溶液蔗糖不饱和溶液蔗糖不饱和溶液升温降温增加溶剂蒸发溶剂液体不超过试管的1/3
试管夹夹在离管口1/3~1/4处
酒精灯中酒精体积不超过酒精灯的2/3
加热时,试管在酒精灯外焰上预热
试管口与水平面呈45°,不能对人
酒精灯用灯帽盖灭注意事项:[演示实验三] 在各盛有5mL水的两支试管里,分别加入1g食盐和0.5g熟石灰,振荡,观察现象。现象:
分析:
室温下,食盐溶液全部溶解了,但它是浓溶液。
但熟石灰不能再溶解了,是饱和溶液,但它是稀溶液。食盐全部溶解了,但是熟石灰只溶解了一点点,大部分没溶解;结论:
1、浓溶液不一定是饱和溶液,稀溶液也不一定是不饱和溶液。
2、同一种溶质的溶液,在一定温度下,饱和溶液比不饱和溶液要浓。不同溶质在同种溶剂中的溶解能力是不一样。怎样定量比较物质的溶解能力呢? 溶解度注意点:
(1)理解这个概念,抓住四个词:一定的温度、100克溶剂(一般为水)、达到饱和、溶解的质量(单位为克/100克水)。
(2)溶解度值越大,表明该温度下,物质的溶解能力越强。.....硝酸钾....溶解度曲线 以温度为横坐标,溶解度为纵坐标,形象地表示出物质的溶解度随温度变化情况的曲线。不同物质溶解度受温度的影响是不同的。 (1)曲线上每个点表示某温度下某溶质的溶解度(2)曲线表示物质的溶解度受温度变化影响大小的情况(3)两条曲线的交点,表示在该温度下两种物质的溶解度相等(4)曲线上每个点所配制的溶液是该温度下这种溶质的饱和溶液,曲线下方的点表示对应温度下该溶质的不饱和溶液。溶解度曲线的意义 大多数物质的溶解度温度升高而增大;如硝酸钾;
少数物质的溶解度受温度影响变化不大,如氯化钠;0.050.100.150.2090704001020506080100300.050.100.150.29070400102050608010030温度/℃熟石灰的溶解度曲线: 极少数固体物质溶解度随温度升高反而减小,例如熟石灰。生活中我们已经知道,固体、液体、气体能够溶解在水中?有谁能够举出气体溶解在水中的例子吗?二氧化碳溶于水
氧气溶于水各种气体在标准大气压下,纯水中的溶解度(ml/L)结论:一般说来,在一定条件下,气体的溶解度随温度的升高而降低。问题:为什么煮沸后的冷开水不能养鱼吗?常温的冷开水常温的天然泉水活动比较不同物质在溶解过程中的能量变化 实验表明,在溶质溶解于水的过程中都伴随着能量的变化,有些有明显的放热或吸热现象,有些则温度变化不明显。 人们利用某些物质在溶于水的过程中会放出大量的热的性质,为野外工作者设计了方便、安全的自热罐头;反之,人们用硝酸铵制作冰袋。应用——自热罐头和冰袋浊液 黄河水中含有很多泥沙,水的颜色发黄,黄河由此得名。黄河水素有“一碗水,半碗泥”的说法。这是一种典型的悬浊液。二、悬浊液和乳浊液1、悬浊液:固体小颗粒分散于液体里所形
成的混合物2、乳浊液:液体小液滴分散另一种液体里
所形成的混合物溶液、悬浊液、乳浊液的区别:固、液、气体溶解在液体中
固体颗粒悬浮在液体中小液滴颗粒悬浮在液体中
稳定
不稳定
不稳定均一、稳定的
不分层 分层 分层本节小结物质纯净物混合物溶液浊液饱和溶液不饱和溶液悬浊液乳浊液溶解度物质悬浊液乳浊液饱和溶液不饱和溶液1.某物质的溶解度如图所示。在一个大烧杯中装着该物质的饱和溶液,而且杯中还有少量该物质固体存在,现将温度由60℃降到20℃,下列说法正确的是( )
A 杯中固体减少
B 杯中固体增多
C 杯中固体不变
D 以上说法都不对B练习2.下列液体属于溶液的是( )
A.牛奶 B.泥水 C.液氧 D. 碘酒
3.一杯溶液中各部分的性质( )
A.上面和下面不相同 B.完全相同
C.完全不同 C.不一定相同
4.下列各用途与乳化无关的是( )
A.用洗衣粉洗去衣服上的油脂
B.用盐酸洗去铁块表面的锈
C.农药、医药制剂的合成
D.各种日用洗涤剂的配制DBB5.下列小实验不能得到溶液的是( )食盐粉尘植物油蔗糖水水水汽油6.等同条件下,下列物质溶于水后能使水的温度明显降低的是( )
A.食盐 B.硝酸铵 C.浓硫酸 D.氢氧化钠7.现有一杯糖水,取出一部分,测其密度为a g/cm3,则剩余糖水的密度是( )
A.小于 a g/cm3 B.等于 a g/cm3
C.大于a g/cm3 D.无法确定BABCDBB100硼酸硝酸铵硝酸钠硝酸钾氯化铵氯化钾氯化钠6070501020304080901001101801701601501401301201902005010203040090607080温度/℃8.固体的溶解度曲线练习:1)A点表示什么意义? 2)40℃时氯化铵的溶解度为
,70℃时氯化铵的溶解度为 。44g/100水A.B.3)B点表示什么意思?该温度下,硝酸钠和硝酸钾的溶解度相等 60g/100水4)在80℃时氯化钠、氯化钾、氯化铵、硼酸的溶解度由大到小的顺序是___________________________。氯化铵、氯化钾、氯化钠、硼酸气体的溶解度主要受温度和压强的影响,温度升高溶解度减小,压强增大溶解度增大。(2)B点代表的含义是
;(1)T2时,三种物质的溶解度由大到小的顺序是 ,(3)T2时甲的溶解度是___________,该温度下向150g水中加入80g甲物质,所得溶液是 溶液(填“饱和”或“不饱和”),需加入 克甲或蒸发 克水,使其变为饱和溶液。甲>乙>丙甲、丙两种物质的溶解度相等80g/100g水T1℃时,溶解度
(g)9、根据如图所示的溶解度曲线图,回答下列问题:80604020不饱和405010.判断是非:
(1)20℃时,10克食盐溶解在100克水中,所以20℃时食盐的溶解度是10克。
(2)100克水中溶解了36克食盐刚好达到饱和,所以食盐的溶解度是36克。
(3)在20℃时,100克水里最多溶解33.3克氯化铵,则20℃氯化铵的溶解度是33.3。
(4)在20℃时,100克硝酸钾饱和溶液里含硝酸钾24克,则20℃硝酸钾的溶解度是24克。
(5)在30℃时,100克水中加入40克氯化钾后达到饱和溶液,则30℃时氯化钾的溶解度是40克。二、交流与讨论 向右图试管里的水中加入某中物质后,U形管左边支管的红墨水液面下降,右边支管的液面上升的物质可能是:
a.蔗糖 b.生石灰 c.活性炭 d.硝酸铵 e.氢氧化钠 f.浓硫酸红墨水水b e f
同课章节目录
- 第1章 水
- 1 地球上的水
- 2 水的三态变化
- 3 水是常用的溶剂
- 4 配制溶液
- 5 水的组成
- 6 水资源的利用和保护
- 第2章 空气
- 1 空气的存在
- 2 空气的成分
- 3 氧气
- 4 二氧化碳
- 5 保护大气圈
- 第3章 阳光
- 1 太阳辐射能
- 2 阳光的传播
- 3 阳光的组成
- 第4章 土壤
- 1 土壤的组成和性状
- 2 土壤与植物
- 3 人类活动与土壤
- 第5章 生态系统
- 1 种群和群落
- 2 生态系统
- 3 生物圈
- 第6章 动物和人的生殖与发育
- 1 动物的生殖与发育
- 2 人的生殖与发育
- 第7章 植物和微生物的生殖与发育
- 1 绿色开花植物的有性生殖和发育
- 2 种子的萌发和幼苗形成
- 3 植物的无性生殖
- 4 细菌和真菌的繁殖
