2022—2023学年化学人教版九年级下册第八单元:金属和金属材料 分层练习(含答案)
文档属性
| 名称 | 2022—2023学年化学人教版九年级下册第八单元:金属和金属材料 分层练习(含答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 489.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-27 00:00:00 | ||
图片预览



文档简介
2022—2023学年化学人教版九年级下册第八单元:金属和金属材料 分层练习含答案
人教第八单元:金属和金属材料
一、选择题。
1、铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的 ( )
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
2、将少量的生铁放入足量的稀盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳 B.氯化铁 C.氯化亚铁 D.单质铁
3、除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质 杂质 除杂所用的试剂和方法
A KCl KClO3 加入MnO2再加热
B CO2气体 CO气体 点燃
C FeCl2溶液 CuCl2 加入过量铁粉,再过滤
D CuO C 隔绝空气加强热
A.A B.B C.C D.D
4、下列四种矿石中主要成分属于单质的是( )
A.铝土矿 B.金矿 C.白钨矿 D.辉铜矿
5、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
6、下列关于金属的说法正确的是( )
A.铜质插头利用了铜的导电性
B.硬铝的硬度比铝小
C.在金属表面喷涂油漆是防止其锈蚀的唯一方法
D.Ag能将硝酸铜溶液中的铜置换出来
7、某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,产生电信号,与金属线相连的警报系统就会立刻报警,这是利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
8、人类历史上大量使用铝、钛、铁、铜四种金属的时间先后顺序是 ( )
A.铜、铁、铝、钛 B.铁、铝、铜、钛
C.铜、铁、钛、铝 D.铁、铜、铝、钛
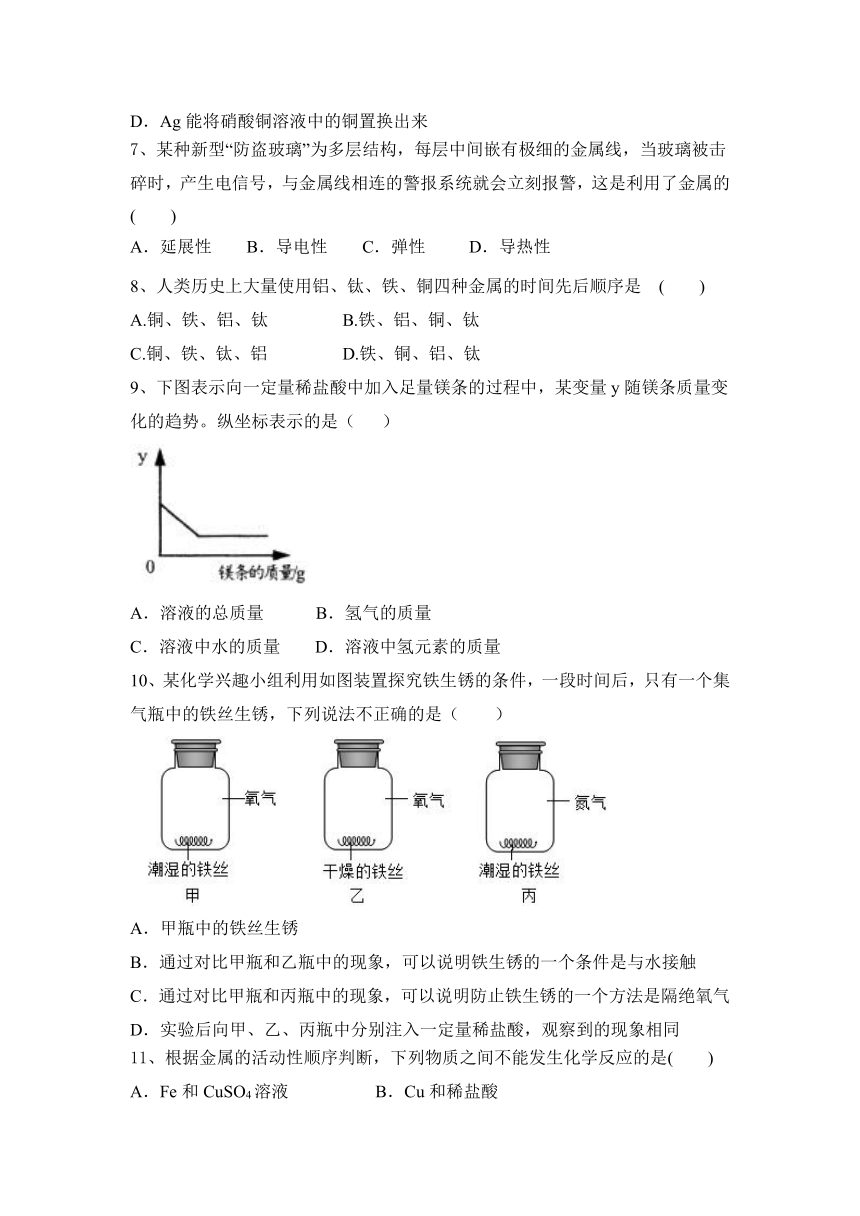
9、下图表示向一定量稀盐酸中加入足量镁条的过程中,某变量y随镁条质量变化的趋势。纵坐标表示的是( )
A.溶液的总质量 B.氢气的质量
C.溶液中水的质量 D.溶液中氢元素的质量
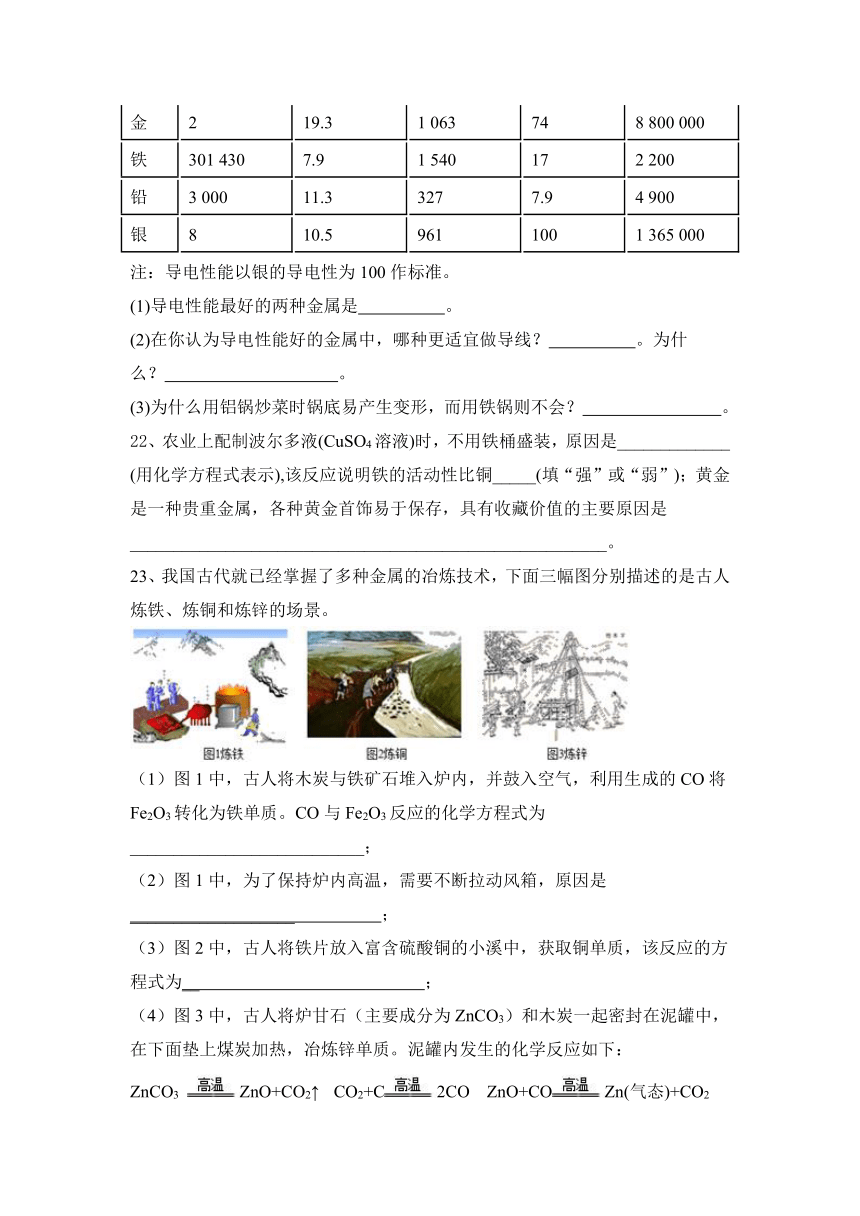
10、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
11、根据金属的活动性顺序判断,下列物质之间不能发生化学反应的是( )
A.Fe和CuSO4溶液 B.Cu和稀盐酸
C.Zn和Hg(NO3)2溶液 D.Mg和稀硫酸
12、物质的性质决定物质的用途,下列金属制品的用途与其性质不存在决定关系的是 ( )
13、除去下表物质中含有的杂质,所选试剂错误的是( )
选 项 物 质 杂 质 除去杂质所选试剂
A 碳酸钙 氧化钙 盐酸
B 氯化钠溶液 碳酸氢钠 盐酸
C 一氧化碳 二氧化碳 氢氧化钠溶液
D 硝酸铜溶液 硝酸银 铜
A.A B.B C.C D.D
*14、下列推理或归纳合理的是( )
A.点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
B.一氧化碳能从氧化铁中还原出铁,所以冶炼金属一定要用一氧化碳
C.单质只含一种元素,由一种元素组成的物质一定是单质
D.置换反应中一定有元素化合价发生变化,则有元素化合价发生变化的反应一定是置换反应
15、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
16、下列物质中,不能在氧气中燃烧的是( )
A.金箔 B.铁丝 C.木炭 D.氢气
二、填空题。
17、“轻轨电车”(如图)是近年来新兴的城市高架交通工具,具有污染小的优点.当轻轨电车开动时,轻轨电车上裸露的“电刷”沿架空电线滑动.电刷材料中含有石墨.选择石墨作电刷材料是因为其具有下列性质:
① ;
② .
18、铝在空气中与氧气反应,其表面生成一层致密的______薄膜,请写出反应的化学方程式______ 。金属材料包括纯金属和______。
19、铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___________组成;从微观看,铁由___________构成。
(2)生活中:下图是常用的铁锅。把铁制成铁锅利用了铁的延展性和___________性。 为防止铁制品锈蚀,可采用的一种防锈方法是___________。
(3)实验室:细铁丝在氧气中燃烧的现象是________________,放热。该反应的化学方程式是_________________________________。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__________,该反应利用了一氧化碳的哪种化学性质:______________________。
20、用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,可看到铜片表面变 ,反应的化学方程式为 。
21、阅读表格,综合考虑表中各方面的因素,回答以下问题:
金属 全球产量(104吨) 密度(g·cm-3) 熔点(℃) 导电性能 市场价格(元/吨)
铝 15 000 2.7 660 61 16 000
铜 8 000 8.9 1 083 99 17 700
金 2 19.3 1 063 74 8 800 000
铁 301 430 7.9 1 540 17 2 200
铅 3 000 11.3 327 7.9 4 900
银 8 10.5 961 100 1 365 000
注:导电性能以银的导电性为100作标准。
(1)导电性能最好的两种金属是 。
(2)在你认为导电性能好的金属中,哪种更适宜做导线? 。为什么? 。
(3)为什么用铝锅炒菜时锅底易产生变形,而用铁锅则不会? 。
22、农业上配制波尔多液(CuSO4溶液)时,不用铁桶盛装,原因是_____________
(用化学方程式表示),该反应说明铁的活动性比铜_____(填“强”或“弱”);黄金是一种贵重金属,各种黄金首饰易于保存,具有收藏价值的主要原因是_______________________________________________________。
23、我国古代就已经掌握了多种金属的冶炼技术,下面三幅图分别描述的是古人炼铁、炼铜和炼锌的场景。
(1)图1中,古人将木炭与铁矿石堆入炉内,并鼓入空气,利用生成的CO将Fe2O3转化为铁单质。CO与Fe2O3反应的化学方程式为___________________________;
(2)图1中,为了保持炉内高温,需要不断拉动风箱,原因是___________________ ;
(3)图2中,古人将铁片放入富含硫酸铜的小溪中,获取铜单质,该反应的方程式为__ ;
(4)图3中,古人将炉甘石(主要成分为ZnCO3)和木炭一起密封在泥罐中,在下面垫上煤炭加热,冶炼锌单质。泥罐内发生的化学反应如下:
ZnCO3 ZnO+CO2↑ CO2+C2CO ZnO+COZn(气态)+CO2
其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因_________。
24、镁条与稀硫酸反应,产生大量 ,反应的化学方程式为 。
三、综合题。
25、如图是与铁的性质有关的部分实验。请回答。
(1)A中铁丝燃烧的化学方程式为 ,集气瓶中预先放少量水的目的是 。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可如铁钉生锈需要与 接触。通过对比①与 试管中的现象,可知铁钉生锈还需要与 接触。这两步运用了实验中常用的 研究方法。
(3)写出一种日常生活中防止铁制品锈蚀的方法 。
(4)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的试剂组是 (填字母)。
A.Mn、FeSO4溶液
B.Mn、Fe、MgSO4溶液
C.Mn、Fe、ZnSO4溶液
(5)在我国,用金属制造硬币已有几千年的历史。为了延长硬币的使用寿命,请分别从物理性质、化学性质的角度分析,用于铸造硬币的金属材料应具有的性质。
①从物理性质的角度分析,应具有的性质是 。
②从化学性质的角度分析,应具有的性质是 。
四、计算题。
26、欲测定某锌—铜合金中铜的质量分数,进行如下实验:取合金样品10 g放入烧杯中,将60 g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
2022—2023学年化学人教版九年级下册第八单元:金属和金属材料 分层练习含答案
人教第八单元:金属和金属材料
一、选择题。
1、铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的 ( )
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
【答案】B。
2、将少量的生铁放入足量的稀盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳 B.氯化铁 C.氯化亚铁 D.单质铁
【答案】A
3、除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质 杂质 除杂所用的试剂和方法
A KCl KClO3 加入MnO2再加热
B CO2气体 CO气体 点燃
C FeCl2溶液 CuCl2 加入过量铁粉,再过滤
D CuO C 隔绝空气加强热
A.A B.B C.C D.D
【答案】C
4、下列四种矿石中主要成分属于单质的是( )
A.铝土矿 B.金矿 C.白钨矿 D.辉铜矿
【答案】B
5、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
【答案】A
6、下列关于金属的说法正确的是( )
A.铜质插头利用了铜的导电性
B.硬铝的硬度比铝小
C.在金属表面喷涂油漆是防止其锈蚀的唯一方法
D.Ag能将硝酸铜溶液中的铜置换出来
【答案】A
7、某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,产生电信号,与金属线相连的警报系统就会立刻报警,这是利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
【答案】B
8、人类历史上大量使用铝、钛、铁、铜四种金属的时间先后顺序是 ( )
A.铜、铁、铝、钛 B.铁、铝、铜、钛
C.铜、铁、钛、铝 D.铁、铜、铝、钛
【答案】A。
9、下图表示向一定量稀盐酸中加入足量镁条的过程中,某变量y随镁条质量变化的趋势。纵坐标表示的是( )
A.溶液的总质量 B.氢气的质量
C.溶液中水的质量 D.溶液中氢元素的质量
【答案】D
10、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
【答案】D
11、根据金属的活动性顺序判断,下列物质之间不能发生化学反应的是( )
A.Fe和CuSO4溶液 B.Cu和稀盐酸
C.Zn和Hg(NO3)2溶液 D.Mg和稀硫酸
【答案】B
12、物质的性质决定物质的用途,下列金属制品的用途与其性质不存在决定关系的是 ( )
【答案】A。
13、除去下表物质中含有的杂质,所选试剂错误的是( )
选 项 物 质 杂 质 除去杂质所选试剂
A 碳酸钙 氧化钙 盐酸
B 氯化钠溶液 碳酸氢钠 盐酸
C 一氧化碳 二氧化碳 氢氧化钠溶液
D 硝酸铜溶液 硝酸银 铜
A.A B.B C.C D.D
【答案】A
*14、下列推理或归纳合理的是( )
A.点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
B.一氧化碳能从氧化铁中还原出铁,所以冶炼金属一定要用一氧化碳
C.单质只含一种元素,由一种元素组成的物质一定是单质
D.置换反应中一定有元素化合价发生变化,则有元素化合价发生变化的反应一定是置换反应
【答案】A
15、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
【答案】C
16、下列物质中,不能在氧气中燃烧的是( )
A.金箔 B.铁丝 C.木炭 D.氢气
【答案】A
二、填空题。
17、“轻轨电车”(如图)是近年来新兴的城市高架交通工具,具有污染小的优点.当轻轨电车开动时,轻轨电车上裸露的“电刷”沿架空电线滑动.电刷材料中含有石墨.选择石墨作电刷材料是因为其具有下列性质:
① ;
② .
【答案】①导电 性; ②润滑性.
18、铝在空气中与氧气反应,其表面生成一层致密的______薄膜,请写出反应的化学方程式______ 。金属材料包括纯金属和______。
【答案】Al2O3 4Al+3O2=2Al2O3 合金
19、铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___________组成;从微观看,铁由___________构成。
(2)生活中:下图是常用的铁锅。把铁制成铁锅利用了铁的延展性和___________性。 为防止铁制品锈蚀,可采用的一种防锈方法是___________。
(3)实验室:细铁丝在氧气中燃烧的现象是________________,放热。该反应的化学方程式是_________________________________。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__________,该反应利用了一氧化碳的哪种化学性质:______________________。
【答案】 铁元素 铁原子 导热 保持铁制品表面洁净干燥(合理即可) 剧烈燃烧,火星四射,生成黑色固体 3Fe+2O2Fe3O4 3CO+Fe2O32Fe+3CO2 还原性
20、用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,可看到铜片表面变 ,反应的化学方程式为 。
【答案】黑 2Cu+O22CuO
21、阅读表格,综合考虑表中各方面的因素,回答以下问题:
金属 全球产量(104吨) 密度(g·cm-3) 熔点(℃) 导电性能 市场价格(元/吨)
铝 15 000 2.7 660 61 16 000
铜 8 000 8.9 1 083 99 17 700
金 2 19.3 1 063 74 8 800 000
铁 301 430 7.9 1 540 17 2 200
铅 3 000 11.3 327 7.9 4 900
银 8 10.5 961 100 1 365 000
注:导电性能以银的导电性为100作标准。
(1)导电性能最好的两种金属是 。
(2)在你认为导电性能好的金属中,哪种更适宜做导线? 。为什么? 。
(3)为什么用铝锅炒菜时锅底易产生变形,而用铁锅则不会? 。
【答案】银、铜_
铜_价格便宜__ 铝的熔点较低,而铁的熔点较高
22、农业上配制波尔多液(CuSO4溶液)时,不用铁桶盛装,原因是_____________
(用化学方程式表示),该反应说明铁的活动性比铜_____(填“强”或“弱”);黄金是一种贵重金属,各种黄金首饰易于保存,具有收藏价值的主要原因是_______________________________________________________。
【答案】Fe+CuSO4 ==== Cu+FeSO4 强
金属活动性弱(或化学性质不活泼或性质稳定或难与其他物质反应等)
23、我国古代就已经掌握了多种金属的冶炼技术,下面三幅图分别描述的是古人炼铁、炼铜和炼锌的场景。
(1)图1中,古人将木炭与铁矿石堆入炉内,并鼓入空气,利用生成的CO将Fe2O3转化为铁单质。CO与Fe2O3反应的化学方程式为___________________________;
(2)图1中,为了保持炉内高温,需要不断拉动风箱,原因是___________________ ;
(3)图2中,古人将铁片放入富含硫酸铜的小溪中,获取铜单质,该反应的方程式为__ ;
(4)图3中,古人将炉甘石(主要成分为ZnCO3)和木炭一起密封在泥罐中,在下面垫上煤炭加热,冶炼锌单质。泥罐内发生的化学反应如下:
ZnCO3 ZnO+CO2↑ CO2+C2CO ZnO+COZn(气态)+CO2
其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因_________。
【答案】 Fe2O3+3CO高温2Fe+3CO2 带来更多新鲜空气,使木炭充分燃烧 Fe+CuSO4═Cu+FeSO4 防止Zn、CO与氧气发生反应
24、镁条与稀硫酸反应,产生大量 ,反应的化学方程式为 。
【答案】气泡 Mg+H2SO4===MgSO4+H2↑
三、综合题。
25、如图是与铁的性质有关的部分实验。请回答。
(1)A中铁丝燃烧的化学方程式为 ,集气瓶中预先放少量水的目的是 。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可如铁钉生锈需要与 接触。通过对比①与 试管中的现象,可知铁钉生锈还需要与 接触。这两步运用了实验中常用的 研究方法。
(3)写出一种日常生活中防止铁制品锈蚀的方法 。
(4)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的试剂组是 (填字母)。
A.Mn、FeSO4溶液
B.Mn、Fe、MgSO4溶液
C.Mn、Fe、ZnSO4溶液
(5)在我国,用金属制造硬币已有几千年的历史。为了延长硬币的使用寿命,请分别从物理性质、化学性质的角度分析,用于铸造硬币的金属材料应具有的性质。
①从物理性质的角度分析,应具有的性质是 。
②从化学性质的角度分析,应具有的性质是 。
【答案】(1)3Fe+2O2Fe3O4;防止铁的熔化物溅落而炸裂集气瓶;
(2)水;②;空气(氧气);对照; (3)在铁制品表面喷漆或涂油等;
(4)AC。 (5)①硬度大、有光泽等;②不易锈蚀、化学性质不活泼等;
四、计算题。
26、欲测定某锌—铜合金中铜的质量分数,进行如下实验:取合金样品10 g放入烧杯中,将60 g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
【答案】0.08
解:设该合金样品中锌的质量为x。
Zn+H2SO4===ZnSO4+H2↑
65 2
x 0.2 g
= x=6.5 g
铜的质量为10 g-6.5 g=3.5 g
该合金样品中铜的质量分数为×100%=35%
答:铜的质量分数为35%。
人教第八单元:金属和金属材料
一、选择题。
1、铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的 ( )
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
2、将少量的生铁放入足量的稀盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳 B.氯化铁 C.氯化亚铁 D.单质铁
3、除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质 杂质 除杂所用的试剂和方法
A KCl KClO3 加入MnO2再加热
B CO2气体 CO气体 点燃
C FeCl2溶液 CuCl2 加入过量铁粉,再过滤
D CuO C 隔绝空气加强热
A.A B.B C.C D.D
4、下列四种矿石中主要成分属于单质的是( )
A.铝土矿 B.金矿 C.白钨矿 D.辉铜矿
5、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
6、下列关于金属的说法正确的是( )
A.铜质插头利用了铜的导电性
B.硬铝的硬度比铝小
C.在金属表面喷涂油漆是防止其锈蚀的唯一方法
D.Ag能将硝酸铜溶液中的铜置换出来
7、某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,产生电信号,与金属线相连的警报系统就会立刻报警,这是利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
8、人类历史上大量使用铝、钛、铁、铜四种金属的时间先后顺序是 ( )
A.铜、铁、铝、钛 B.铁、铝、铜、钛
C.铜、铁、钛、铝 D.铁、铜、铝、钛
9、下图表示向一定量稀盐酸中加入足量镁条的过程中,某变量y随镁条质量变化的趋势。纵坐标表示的是( )
A.溶液的总质量 B.氢气的质量
C.溶液中水的质量 D.溶液中氢元素的质量
10、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
11、根据金属的活动性顺序判断,下列物质之间不能发生化学反应的是( )
A.Fe和CuSO4溶液 B.Cu和稀盐酸
C.Zn和Hg(NO3)2溶液 D.Mg和稀硫酸
12、物质的性质决定物质的用途,下列金属制品的用途与其性质不存在决定关系的是 ( )
13、除去下表物质中含有的杂质,所选试剂错误的是( )
选 项 物 质 杂 质 除去杂质所选试剂
A 碳酸钙 氧化钙 盐酸
B 氯化钠溶液 碳酸氢钠 盐酸
C 一氧化碳 二氧化碳 氢氧化钠溶液
D 硝酸铜溶液 硝酸银 铜
A.A B.B C.C D.D
*14、下列推理或归纳合理的是( )
A.点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
B.一氧化碳能从氧化铁中还原出铁,所以冶炼金属一定要用一氧化碳
C.单质只含一种元素,由一种元素组成的物质一定是单质
D.置换反应中一定有元素化合价发生变化,则有元素化合价发生变化的反应一定是置换反应
15、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
16、下列物质中,不能在氧气中燃烧的是( )
A.金箔 B.铁丝 C.木炭 D.氢气
二、填空题。
17、“轻轨电车”(如图)是近年来新兴的城市高架交通工具,具有污染小的优点.当轻轨电车开动时,轻轨电车上裸露的“电刷”沿架空电线滑动.电刷材料中含有石墨.选择石墨作电刷材料是因为其具有下列性质:
① ;
② .
18、铝在空气中与氧气反应,其表面生成一层致密的______薄膜,请写出反应的化学方程式______ 。金属材料包括纯金属和______。
19、铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___________组成;从微观看,铁由___________构成。
(2)生活中:下图是常用的铁锅。把铁制成铁锅利用了铁的延展性和___________性。 为防止铁制品锈蚀,可采用的一种防锈方法是___________。
(3)实验室:细铁丝在氧气中燃烧的现象是________________,放热。该反应的化学方程式是_________________________________。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__________,该反应利用了一氧化碳的哪种化学性质:______________________。
20、用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,可看到铜片表面变 ,反应的化学方程式为 。
21、阅读表格,综合考虑表中各方面的因素,回答以下问题:
金属 全球产量(104吨) 密度(g·cm-3) 熔点(℃) 导电性能 市场价格(元/吨)
铝 15 000 2.7 660 61 16 000
铜 8 000 8.9 1 083 99 17 700
金 2 19.3 1 063 74 8 800 000
铁 301 430 7.9 1 540 17 2 200
铅 3 000 11.3 327 7.9 4 900
银 8 10.5 961 100 1 365 000
注:导电性能以银的导电性为100作标准。
(1)导电性能最好的两种金属是 。
(2)在你认为导电性能好的金属中,哪种更适宜做导线? 。为什么? 。
(3)为什么用铝锅炒菜时锅底易产生变形,而用铁锅则不会? 。
22、农业上配制波尔多液(CuSO4溶液)时,不用铁桶盛装,原因是_____________
(用化学方程式表示),该反应说明铁的活动性比铜_____(填“强”或“弱”);黄金是一种贵重金属,各种黄金首饰易于保存,具有收藏价值的主要原因是_______________________________________________________。
23、我国古代就已经掌握了多种金属的冶炼技术,下面三幅图分别描述的是古人炼铁、炼铜和炼锌的场景。
(1)图1中,古人将木炭与铁矿石堆入炉内,并鼓入空气,利用生成的CO将Fe2O3转化为铁单质。CO与Fe2O3反应的化学方程式为___________________________;
(2)图1中,为了保持炉内高温,需要不断拉动风箱,原因是___________________ ;
(3)图2中,古人将铁片放入富含硫酸铜的小溪中,获取铜单质,该反应的方程式为__ ;
(4)图3中,古人将炉甘石(主要成分为ZnCO3)和木炭一起密封在泥罐中,在下面垫上煤炭加热,冶炼锌单质。泥罐内发生的化学反应如下:
ZnCO3 ZnO+CO2↑ CO2+C2CO ZnO+COZn(气态)+CO2
其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因_________。
24、镁条与稀硫酸反应,产生大量 ,反应的化学方程式为 。
三、综合题。
25、如图是与铁的性质有关的部分实验。请回答。
(1)A中铁丝燃烧的化学方程式为 ,集气瓶中预先放少量水的目的是 。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可如铁钉生锈需要与 接触。通过对比①与 试管中的现象,可知铁钉生锈还需要与 接触。这两步运用了实验中常用的 研究方法。
(3)写出一种日常生活中防止铁制品锈蚀的方法 。
(4)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的试剂组是 (填字母)。
A.Mn、FeSO4溶液
B.Mn、Fe、MgSO4溶液
C.Mn、Fe、ZnSO4溶液
(5)在我国,用金属制造硬币已有几千年的历史。为了延长硬币的使用寿命,请分别从物理性质、化学性质的角度分析,用于铸造硬币的金属材料应具有的性质。
①从物理性质的角度分析,应具有的性质是 。
②从化学性质的角度分析,应具有的性质是 。
四、计算题。
26、欲测定某锌—铜合金中铜的质量分数,进行如下实验:取合金样品10 g放入烧杯中,将60 g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
2022—2023学年化学人教版九年级下册第八单元:金属和金属材料 分层练习含答案
人教第八单元:金属和金属材料
一、选择题。
1、铜能被加工成厚度仅为7微米的超薄铜箔,说明铜具有良好的 ( )
A.导电性 B.延展性 C.导热性 D.抗腐蚀性
【答案】B。
2、将少量的生铁放入足量的稀盐酸中充分反应,有黑色的残渣剩余,该残渣主要是( )
A.单质碳 B.氯化铁 C.氯化亚铁 D.单质铁
【答案】A
3、除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
物质 杂质 除杂所用的试剂和方法
A KCl KClO3 加入MnO2再加热
B CO2气体 CO气体 点燃
C FeCl2溶液 CuCl2 加入过量铁粉,再过滤
D CuO C 隔绝空气加强热
A.A B.B C.C D.D
【答案】C
4、下列四种矿石中主要成分属于单质的是( )
A.铝土矿 B.金矿 C.白钨矿 D.辉铜矿
【答案】B
5、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
【答案】A
6、下列关于金属的说法正确的是( )
A.铜质插头利用了铜的导电性
B.硬铝的硬度比铝小
C.在金属表面喷涂油漆是防止其锈蚀的唯一方法
D.Ag能将硝酸铜溶液中的铜置换出来
【答案】A
7、某种新型“防盗玻璃”为多层结构,每层中间嵌有极细的金属线,当玻璃被击碎时,产生电信号,与金属线相连的警报系统就会立刻报警,这是利用了金属的( )
A.延展性 B.导电性 C.弹性 D.导热性
【答案】B
8、人类历史上大量使用铝、钛、铁、铜四种金属的时间先后顺序是 ( )
A.铜、铁、铝、钛 B.铁、铝、铜、钛
C.铜、铁、钛、铝 D.铁、铜、铝、钛
【答案】A。
9、下图表示向一定量稀盐酸中加入足量镁条的过程中,某变量y随镁条质量变化的趋势。纵坐标表示的是( )
A.溶液的总质量 B.氢气的质量
C.溶液中水的质量 D.溶液中氢元素的质量
【答案】D
10、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
【答案】D
11、根据金属的活动性顺序判断,下列物质之间不能发生化学反应的是( )
A.Fe和CuSO4溶液 B.Cu和稀盐酸
C.Zn和Hg(NO3)2溶液 D.Mg和稀硫酸
【答案】B
12、物质的性质决定物质的用途,下列金属制品的用途与其性质不存在决定关系的是 ( )
【答案】A。
13、除去下表物质中含有的杂质,所选试剂错误的是( )
选 项 物 质 杂 质 除去杂质所选试剂
A 碳酸钙 氧化钙 盐酸
B 氯化钠溶液 碳酸氢钠 盐酸
C 一氧化碳 二氧化碳 氢氧化钠溶液
D 硝酸铜溶液 硝酸银 铜
A.A B.B C.C D.D
【答案】A
*14、下列推理或归纳合理的是( )
A.点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
B.一氧化碳能从氧化铁中还原出铁,所以冶炼金属一定要用一氧化碳
C.单质只含一种元素,由一种元素组成的物质一定是单质
D.置换反应中一定有元素化合价发生变化,则有元素化合价发生变化的反应一定是置换反应
【答案】A
15、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
【答案】C
16、下列物质中,不能在氧气中燃烧的是( )
A.金箔 B.铁丝 C.木炭 D.氢气
【答案】A
二、填空题。
17、“轻轨电车”(如图)是近年来新兴的城市高架交通工具,具有污染小的优点.当轻轨电车开动时,轻轨电车上裸露的“电刷”沿架空电线滑动.电刷材料中含有石墨.选择石墨作电刷材料是因为其具有下列性质:
① ;
② .
【答案】①导电 性; ②润滑性.
18、铝在空气中与氧气反应,其表面生成一层致密的______薄膜,请写出反应的化学方程式______ 。金属材料包括纯金属和______。
【答案】Al2O3 4Al+3O2=2Al2O3 合金
19、铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由___________组成;从微观看,铁由___________构成。
(2)生活中:下图是常用的铁锅。把铁制成铁锅利用了铁的延展性和___________性。 为防止铁制品锈蚀,可采用的一种防锈方法是___________。
(3)实验室:细铁丝在氧气中燃烧的现象是________________,放热。该反应的化学方程式是_________________________________。
(4)工业上:用一氧化碳和赤铁矿(主要成分是Fe2O3 )炼铁的化学方程式是__________,该反应利用了一氧化碳的哪种化学性质:______________________。
【答案】 铁元素 铁原子 导热 保持铁制品表面洁净干燥(合理即可) 剧烈燃烧,火星四射,生成黑色固体 3Fe+2O2Fe3O4 3CO+Fe2O32Fe+3CO2 还原性
20、用坩埚钳夹取一块铜片,放在酒精灯火焰上加热,可看到铜片表面变 ,反应的化学方程式为 。
【答案】黑 2Cu+O22CuO
21、阅读表格,综合考虑表中各方面的因素,回答以下问题:
金属 全球产量(104吨) 密度(g·cm-3) 熔点(℃) 导电性能 市场价格(元/吨)
铝 15 000 2.7 660 61 16 000
铜 8 000 8.9 1 083 99 17 700
金 2 19.3 1 063 74 8 800 000
铁 301 430 7.9 1 540 17 2 200
铅 3 000 11.3 327 7.9 4 900
银 8 10.5 961 100 1 365 000
注:导电性能以银的导电性为100作标准。
(1)导电性能最好的两种金属是 。
(2)在你认为导电性能好的金属中,哪种更适宜做导线? 。为什么? 。
(3)为什么用铝锅炒菜时锅底易产生变形,而用铁锅则不会? 。
【答案】银、铜_
铜_价格便宜__ 铝的熔点较低,而铁的熔点较高
22、农业上配制波尔多液(CuSO4溶液)时,不用铁桶盛装,原因是_____________
(用化学方程式表示),该反应说明铁的活动性比铜_____(填“强”或“弱”);黄金是一种贵重金属,各种黄金首饰易于保存,具有收藏价值的主要原因是_______________________________________________________。
【答案】Fe+CuSO4 ==== Cu+FeSO4 强
金属活动性弱(或化学性质不活泼或性质稳定或难与其他物质反应等)
23、我国古代就已经掌握了多种金属的冶炼技术,下面三幅图分别描述的是古人炼铁、炼铜和炼锌的场景。
(1)图1中,古人将木炭与铁矿石堆入炉内,并鼓入空气,利用生成的CO将Fe2O3转化为铁单质。CO与Fe2O3反应的化学方程式为___________________________;
(2)图1中,为了保持炉内高温,需要不断拉动风箱,原因是___________________ ;
(3)图2中,古人将铁片放入富含硫酸铜的小溪中,获取铜单质,该反应的方程式为__ ;
(4)图3中,古人将炉甘石(主要成分为ZnCO3)和木炭一起密封在泥罐中,在下面垫上煤炭加热,冶炼锌单质。泥罐内发生的化学反应如下:
ZnCO3 ZnO+CO2↑ CO2+C2CO ZnO+COZn(气态)+CO2
其中,用泥罐密封是炼锌的关键,请结合物质的化学性质解释其原因_________。
【答案】 Fe2O3+3CO高温2Fe+3CO2 带来更多新鲜空气,使木炭充分燃烧 Fe+CuSO4═Cu+FeSO4 防止Zn、CO与氧气发生反应
24、镁条与稀硫酸反应,产生大量 ,反应的化学方程式为 。
【答案】气泡 Mg+H2SO4===MgSO4+H2↑
三、综合题。
25、如图是与铁的性质有关的部分实验。请回答。
(1)A中铁丝燃烧的化学方程式为 ,集气瓶中预先放少量水的目的是 。
(2)B是探究铁钉锈蚀条件的实验。通过对比①③试管中的现象,可如铁钉生锈需要与 接触。通过对比①与 试管中的现象,可知铁钉生锈还需要与 接触。这两步运用了实验中常用的 研究方法。
(3)写出一种日常生活中防止铁制品锈蚀的方法 。
(4)已知锰(Mn)的金属活动性介于镁和锌之间,如果通过实验验证铁和锰的金属活动性强弱,能达到实验目的试剂组是 (填字母)。
A.Mn、FeSO4溶液
B.Mn、Fe、MgSO4溶液
C.Mn、Fe、ZnSO4溶液
(5)在我国,用金属制造硬币已有几千年的历史。为了延长硬币的使用寿命,请分别从物理性质、化学性质的角度分析,用于铸造硬币的金属材料应具有的性质。
①从物理性质的角度分析,应具有的性质是 。
②从化学性质的角度分析,应具有的性质是 。
【答案】(1)3Fe+2O2Fe3O4;防止铁的熔化物溅落而炸裂集气瓶;
(2)水;②;空气(氧气);对照; (3)在铁制品表面喷漆或涂油等;
(4)AC。 (5)①硬度大、有光泽等;②不易锈蚀、化学性质不活泼等;
四、计算题。
26、欲测定某锌—铜合金中铜的质量分数,进行如下实验:取合金样品10 g放入烧杯中,将60 g稀硫酸分三次加入,充分反应后,测得生成气体的质量如下:
实验次数 第一次 第二次 第三次
加入稀硫酸质量/g 20 20 20
生成气体质量/g 0.08 m 0.04
请回答下列问题并计算:
(1)第二次实验时生成气体质量m= g;
(2)计算该合金样品中铜的质量分数。
【答案】0.08
解:设该合金样品中锌的质量为x。
Zn+H2SO4===ZnSO4+H2↑
65 2
x 0.2 g
= x=6.5 g
铜的质量为10 g-6.5 g=3.5 g
该合金样品中铜的质量分数为×100%=35%
答:铜的质量分数为35%。
同课章节目录
