10.1常见的酸和碱(第3课时)课件(共24张PPT 内嵌视频)-2022-2023学年九年级化学下册同步课件(人教版)
文档属性
| 名称 | 10.1常见的酸和碱(第3课时)课件(共24张PPT 内嵌视频)-2022-2023学年九年级化学下册同步课件(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 36.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-12-28 00:00:00 | ||
图片预览






文档简介
(共24张PPT)
第3课时 酸的化学性质
常见的酸和碱
了解酸的通性及其原理,能写出有关的化学方程式。
01
运用比较概括的方法对获取的信息进行加工。
02
体会化学与人类密切关系,培养学生学习化学的兴趣。
03
学习目标
导入新课
某路段,由于路面湿滑,一辆满载浓硫酸的罐车下坡转弯时操作不当致使车辆侧翻,车内31吨浓硫酸不断向外泄漏。浓硫酸遇到水会产生大量“白雾”,“白雾”会使树叶逐渐枯萎。为什么会发生这种现象呢?为了揭开浓硫酸的神秘面纱,我们一起来学习常见的酸。
PART ONE
酸的化学性质
01
酸与指示剂的作用
用点滴板进行实验可以节约药品,也便于对比实验现象。
在白色点滴板上进行实验,并观察现象。
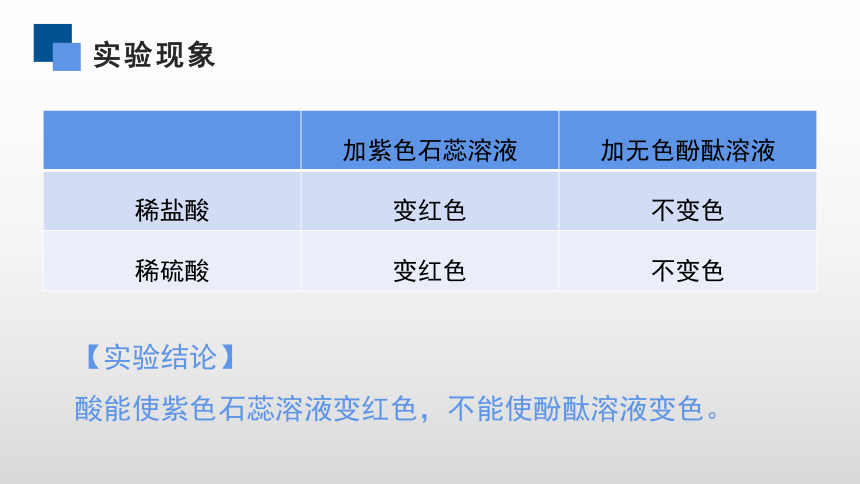
实验现象
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸 变红色 不变色
稀硫酸 变红色 不变色
【实验结论】
酸能使紫色石蕊溶液变红色,不能使酚酞溶液变色。
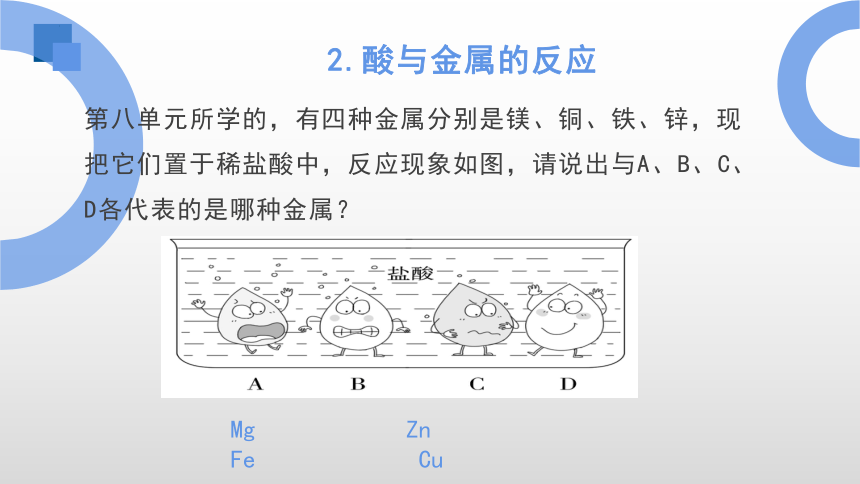
2.酸与金属的反应
第八单元所学的,有四种金属分别是镁、铜、铁、锌,现把它们置于稀盐酸中,反应现象如图,请说出与A、B、C、D各代表的是哪种金属?
Mg Zn Fe Cu
【实验操作】
在三支试管中分别加入少量镁条、锌粒、铁片,向三支试管中分别加入5 mL稀盐酸(稀硫酸),观察现象。
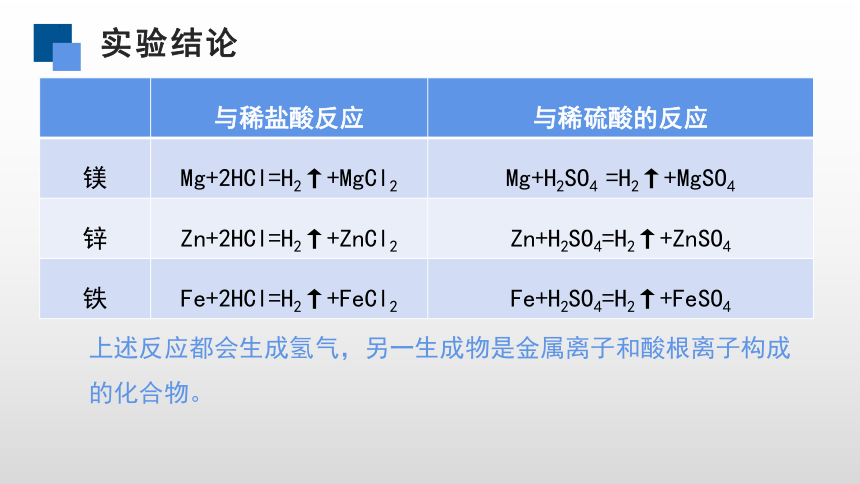
实验结论
与稀盐酸反应 与稀硫酸的反应
镁 Mg+2HCl=H2↑+MgCl2 Mg+H2SO4 =H2↑+MgSO4
锌 Zn+2HCl=H2↑+ZnCl2 Zn+H2SO4=H2↑+ZnSO4
铁 Fe+2HCl=H2↑+FeCl2 Fe+H2SO4=H2↑+FeSO4
上述反应都会生成氢气,另一生成物是金属离子和酸根离子构成的化合物。
特别提醒
3
铁与盐酸、稀硫酸反应,生成物中铁元素的化合价为+2价,溶液为浅绿色。
2
1
从反应的基本类型看:它们都属于置换反应。
浓硫酸与硝酸有强氧化性,不能与金属发生置换反应生成氢气。
3.酸与金属氧化物反应
在盛有稀盐酸和稀硫酸的试管里分别放入一根生锈的铁钉,过一会儿取出铁钉,用水清洗干净,铁钉表面和溶液颜色有什么变化?
实验现象
现象 化学方程式
铁锈+稀盐酸 铁锈溶解,溶液由无色变成黄色 Fe2O3+6HCl=2FeCl3+3H2O
铁锈+稀硫酸 铁锈溶解,溶液由无色变成黄色 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
特别提醒
铁锈的主要成分是Fe2O3,铁元素的化合价为+3价。
与盐酸、稀硫酸反应,生成物为FeCl3、Fe2(SO4)3,溶液为黄色。
稀盐酸、稀硫酸具有一定的腐蚀性,使用时要十分小心,防止沾到皮肤上;如果不说明用量,液体取1~2 mL为宜。
小组讨论
利用上面的反应可以清除金属制品表面的锈,除锈时能否将金属制品长时间浸在酸中?为什么?
不能长时间浸入酸中,因为酸会与金属继续反应,造成金属制品腐蚀。
PART TWO
酸的通性
02
根据以上实验和讨论,你能归纳出盐酸、硫酸等酸有哪些相似的化学性质吗?
酸的化学性质
酸能使紫色石蕊溶液变红色,无色酚酞溶液遇酸不变色。
酸能与活泼金属反应生成该金属的化合物和氢气。
酸能与某些金属氧化物反应生成该金属的化合物和水。
1
酸的通性
通过比较盐酸和硫酸的水溶液中阴、阳离子的种类可知:
此类化合物在水溶液中解离出的阳离子全部是H+,这类化合物称为酸。
不同的酸在水溶液中都能解离出自由移动的H+,所以酸具有相似的化学性质。酸的这些相似化学性质称作酸的通性。
01
浓硫酸、硝酸有很强的氧化性,与金属反应不能生成 H2,而是生成水。所以酸的通性通常指的是盐酸和稀硫酸的性质。
02
酸中一定含有氢元素,但含有氢元素的物质不一定是酸,如 H2O、NaHCO3 等。
03
盐是组成中含有金属离子(或 NH4+)和酸根离子的一类化合物。如 FeCl2、NH4Cl 等。
04
不同的酸溶液中都含有H+,所以酸有一些相似的性质;由于酸根离子不同,不同的酸也有各自的特性。
酸的化学性质
与金属反应
与指示剂反应
与活泼金属反应生成盐和氢气
酸能使石蕊溶液变红色
酸不能使酚酞溶液变色
与某些金属氧化物反应生成盐和水
与金属氧化物反应
课堂小结
酸的通性
随堂练习
1.下列物质中,不能用金属跟稀酸反应直接制得的是( )
A.硫酸锌 B.氯化镁 C.氯化铜 D.硫酸铝
2.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( )
A.汽油 B.食盐水 C.白醋 D.米酒
C
C
随堂练习
3.下列物质与稀盐酸反应的化学方程式正确的是( )
A.CaCO3+2HCl=CaCl2+H2O+CO2↑
B.2Fe+6HCl=2FeCl3+3H2↑
C.Cu+2HCl=CuCl2+H2↑
D.Fe2O3+4HCl=2FeCl2+3H2O
A
随堂练习
4.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,下列物品不会被蚁酸腐蚀的是( )
A.镀锌水管 B.铜制塑像
C.大理石栏杆 D.铝合金门窗
B
随堂练习
5.对某无色溶液进行下列实验,根据实验现象得出的结论中,不正确的是( )
A.滴入紫色石蕊溶液,颜色变红,则该溶液显酸性
B.滴入酚酞溶液,溶液保持无色,则该溶液显酸性
C.加入Mg 粉,有气泡产生,则该溶液显酸性
D.加入 CaCO 固体,有气泡产生,则该溶液显酸性
B
第3课时 酸的化学性质
常见的酸和碱
了解酸的通性及其原理,能写出有关的化学方程式。
01
运用比较概括的方法对获取的信息进行加工。
02
体会化学与人类密切关系,培养学生学习化学的兴趣。
03
学习目标
导入新课
某路段,由于路面湿滑,一辆满载浓硫酸的罐车下坡转弯时操作不当致使车辆侧翻,车内31吨浓硫酸不断向外泄漏。浓硫酸遇到水会产生大量“白雾”,“白雾”会使树叶逐渐枯萎。为什么会发生这种现象呢?为了揭开浓硫酸的神秘面纱,我们一起来学习常见的酸。
PART ONE
酸的化学性质
01
酸与指示剂的作用
用点滴板进行实验可以节约药品,也便于对比实验现象。
在白色点滴板上进行实验,并观察现象。
实验现象
加紫色石蕊溶液 加无色酚酞溶液
稀盐酸 变红色 不变色
稀硫酸 变红色 不变色
【实验结论】
酸能使紫色石蕊溶液变红色,不能使酚酞溶液变色。
2.酸与金属的反应
第八单元所学的,有四种金属分别是镁、铜、铁、锌,现把它们置于稀盐酸中,反应现象如图,请说出与A、B、C、D各代表的是哪种金属?
Mg Zn Fe Cu
【实验操作】
在三支试管中分别加入少量镁条、锌粒、铁片,向三支试管中分别加入5 mL稀盐酸(稀硫酸),观察现象。
实验结论
与稀盐酸反应 与稀硫酸的反应
镁 Mg+2HCl=H2↑+MgCl2 Mg+H2SO4 =H2↑+MgSO4
锌 Zn+2HCl=H2↑+ZnCl2 Zn+H2SO4=H2↑+ZnSO4
铁 Fe+2HCl=H2↑+FeCl2 Fe+H2SO4=H2↑+FeSO4
上述反应都会生成氢气,另一生成物是金属离子和酸根离子构成的化合物。
特别提醒
3
铁与盐酸、稀硫酸反应,生成物中铁元素的化合价为+2价,溶液为浅绿色。
2
1
从反应的基本类型看:它们都属于置换反应。
浓硫酸与硝酸有强氧化性,不能与金属发生置换反应生成氢气。
3.酸与金属氧化物反应
在盛有稀盐酸和稀硫酸的试管里分别放入一根生锈的铁钉,过一会儿取出铁钉,用水清洗干净,铁钉表面和溶液颜色有什么变化?
实验现象
现象 化学方程式
铁锈+稀盐酸 铁锈溶解,溶液由无色变成黄色 Fe2O3+6HCl=2FeCl3+3H2O
铁锈+稀硫酸 铁锈溶解,溶液由无色变成黄色 Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
特别提醒
铁锈的主要成分是Fe2O3,铁元素的化合价为+3价。
与盐酸、稀硫酸反应,生成物为FeCl3、Fe2(SO4)3,溶液为黄色。
稀盐酸、稀硫酸具有一定的腐蚀性,使用时要十分小心,防止沾到皮肤上;如果不说明用量,液体取1~2 mL为宜。
小组讨论
利用上面的反应可以清除金属制品表面的锈,除锈时能否将金属制品长时间浸在酸中?为什么?
不能长时间浸入酸中,因为酸会与金属继续反应,造成金属制品腐蚀。
PART TWO
酸的通性
02
根据以上实验和讨论,你能归纳出盐酸、硫酸等酸有哪些相似的化学性质吗?
酸的化学性质
酸能使紫色石蕊溶液变红色,无色酚酞溶液遇酸不变色。
酸能与活泼金属反应生成该金属的化合物和氢气。
酸能与某些金属氧化物反应生成该金属的化合物和水。
1
酸的通性
通过比较盐酸和硫酸的水溶液中阴、阳离子的种类可知:
此类化合物在水溶液中解离出的阳离子全部是H+,这类化合物称为酸。
不同的酸在水溶液中都能解离出自由移动的H+,所以酸具有相似的化学性质。酸的这些相似化学性质称作酸的通性。
01
浓硫酸、硝酸有很强的氧化性,与金属反应不能生成 H2,而是生成水。所以酸的通性通常指的是盐酸和稀硫酸的性质。
02
酸中一定含有氢元素,但含有氢元素的物质不一定是酸,如 H2O、NaHCO3 等。
03
盐是组成中含有金属离子(或 NH4+)和酸根离子的一类化合物。如 FeCl2、NH4Cl 等。
04
不同的酸溶液中都含有H+,所以酸有一些相似的性质;由于酸根离子不同,不同的酸也有各自的特性。
酸的化学性质
与金属反应
与指示剂反应
与活泼金属反应生成盐和氢气
酸能使石蕊溶液变红色
酸不能使酚酞溶液变色
与某些金属氧化物反应生成盐和水
与金属氧化物反应
课堂小结
酸的通性
随堂练习
1.下列物质中,不能用金属跟稀酸反应直接制得的是( )
A.硫酸锌 B.氯化镁 C.氯化铜 D.硫酸铝
2.小明想除去卫生间瓷砖上的铁锈痕迹,在用清水洗涤之前,他从家中选择了一种最合适的物质对铁锈进行处理,这种物质是( )
A.汽油 B.食盐水 C.白醋 D.米酒
C
C
随堂练习
3.下列物质与稀盐酸反应的化学方程式正确的是( )
A.CaCO3+2HCl=CaCl2+H2O+CO2↑
B.2Fe+6HCl=2FeCl3+3H2↑
C.Cu+2HCl=CuCl2+H2↑
D.Fe2O3+4HCl=2FeCl2+3H2O
A
随堂练习
4.白蚁能分泌出蚁酸。蚁酸的化学性质与盐酸相似,下列物品不会被蚁酸腐蚀的是( )
A.镀锌水管 B.铜制塑像
C.大理石栏杆 D.铝合金门窗
B
随堂练习
5.对某无色溶液进行下列实验,根据实验现象得出的结论中,不正确的是( )
A.滴入紫色石蕊溶液,颜色变红,则该溶液显酸性
B.滴入酚酞溶液,溶液保持无色,则该溶液显酸性
C.加入Mg 粉,有气泡产生,则该溶液显酸性
D.加入 CaCO 固体,有气泡产生,则该溶液显酸性
B
同课章节目录
